激光腔内消融术联合硬化治疗下肢静脉曲张患者的效果
刘岳,肖强
广州医科大学附属第六医院·清远市人民医院普通外科 (广东清远 511500)
既往临床常采用介入下顺行硬化治疗方法治疗下肢静脉曲张(varicose veins of lower extremity,VVLE)患者,其作用机制为通过隐静脉顺行插入导管,经静脉造影明确深静脉通畅后,注入血管硬化剂,使其与静脉血管壁接触,引起化学性炎症反应,使血管内皮受损,导致人工血栓的形成、血管闭合,进而达到治疗VVLE的效果[1]。但单纯注射硬化剂难以充分阻断静脉主干,复发率往往较高,且相关并发症的发生率较高,严重影响患者的预后。近年来,激光腔内消融术(endogenous laser ablation,EVLA)逐渐被应用于治疗VVLE,其是微创、腔内外科技术在血管外科应用的典范。EVLT虽可有效阻断大隐静脉主干,但对呈扭曲、块状的静脉穿刺置管较为困难,且易引起局部并发症[2]。有研究指出,将EVLA与硬化治疗联合用于下肢慢性静脉功能不全患者的治疗中可发挥各自的优势,具有较好的治疗效果[3]。基于此,本研究旨在比较EVLA联合硬化治疗与介入下顺行硬化治疗VVLE患者的效果,现报道如下。
1 资料与方法
1.1 一般资料
回顾性分析2017年1月至2018年12月于医院治疗的80例VVLE患者的临床资料,按照治疗方法的不同将其分为对照组(40例)和试验组(40例)。对照组男15例,女25例;年龄28~67岁,平均(47.36±5.19)岁;病程3~10年,平均(6.72±1.28)年;国际静脉联盟临床-病因-解剖-病理生理(Clinical-Etiological-Anatomical-Pathophysiological,CEAP)分期,C2期9例,C3期16例,C4期13例,C5期2例。试验组男14例,女26例;年龄29~63岁,平均(48.26±5.33)岁;病程3~11年,平均(6.65±1.31)年;CEAP分期,C2期8例,C3期18例,C4期12例,C5期2例。两组一般资料比较,差异无统计学意义(P>0.05),具有可比性。纳入标准:患者存在1项或多项典型的VVLE临床表现,即患肢有色素沉着、久站或行走后酸胀不适、水肿、瘙痒,可见迂曲扩张的静脉;患者术前行常规检查无手术禁忌证;患者在术前完善彩色多普勒超声检查;临床资料完整。排除标准:下肢深静脉血栓等其他并发症者;合并呼吸、循环、肾脏、造血系统疾病者;既往罹患深静脉血栓者;凝血功能异常者。
1.2 方法
所有患者在治疗时取平卧位,于患肢大腿上常规扎上止血带后消毒、铺巾。对照组实施介入下顺行硬化治疗:取患肢小腿静脉曲张明显处用头皮针穿刺,共选择2个穿刺点,见回血后松开止血带,经静脉行顺行穿刺插管,行静脉造影见大隐静脉曲张明显,深静脉未见明显显影;将泡沫硬化剂聚桂醇注射液(陕西天宇制药有限公司,国药准字H20080445,规格100 mg∶10 ml)与空气,按照1∶4的比例配置,混合后从2个穿刺点注入,并根据患者的静脉曲张严重程度调整注射硬化剂的剂量,见原造影剂填充处被泡沫硬化剂填充后,结束手术,常规采用绷带加压包扎。
试验组实施EVLA联合硬化治疗:于腹股沟韧带足侧2~3 cm处做一3~4 cm长的横行或斜行手术切口,暴露卵圆窝,游离大隐静脉主干及其主要属支,分别结扎离断分支血管,在距离大隐静脉汇入股静脉处下方0.5 cm处,用7号丝线双重结扎大隐静脉主干;用穿刺针穿刺大隐静脉近结扎处,于回血后置入导丝,并逆行置入导管至内踝处;顺导丝放入血管造影导管,拔出导丝,置入光纤,连接静脉曲张半导体激光治疗仪(武汉博激世纪科技有限公司,VELAS-980nm),光纤顶端伸出导管外2 cm;激光治疗仪的参数为,发射功率为10~12 W,每次发射时间为1 s,间隔1 s;一边发射激光一边缓慢撤回激光光纤及导管,注意保持光纤和导管同步回撤,速度为5~8 mm/s,助手用0.9%氯化钠注射液浸湿的敷料沿大隐静脉行程压迫,注意按压时避免太过用力,以免引起皮肤灼伤的情况;用头皮针行多点穿刺注射泡沫硬化剂(配制方法同对照组),每个穿刺点注射1~2 ml,在完成注射后,轻轻按摩,并结扎置入光纤处,逐层缝合关闭切口,术毕,最后以绷带加压包扎患肢。
两组术后当日均需去枕平卧6~8 h,并抬高患肢;术后第2天以卧床休息、抬高患肢为主,开始逐渐适量下床活动;在卧床休息时,指导患者进行足踝背伸运动,预防形成深静脉血栓;鼓励患者多饮水,术后1周内用弹力绷带加压包扎患肢,腹股沟部位切口于1周左右拆线,术后3个月内患肢需穿戴预防型弹力袜。
1.3 临床评价
(1)记录两组术中硬化剂使用总量。 (2)分别于术前、术后1个月采用静脉临床严重程度评分表 (venous clinical severity score,VCSS)[5]评估患者的病情改善情况,该量表共10个项目,每项按0~3分计分,总分0~30分,评分越低表明患者的病情越轻。(3)统计术后3个月内两组肺栓塞、静脉炎、皮下瘀斑硬结、隐神经损伤及术后下肢疼痛等并发症发生情况。
1.4 统计学处理
采用SPSS23.0统计软件进行数据分析。计量资料均行正态分布检验,符合正态分布的数据以±s表示,组间比较采用t检验,组内比较采用配对样本t检验;计数资料以率表示,组间比较采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组硬化剂使用总量比较
试验组硬化剂使用总量为(21.13±12.47)ml,低于对照组的(24.35±15.47)ml,差异有统计学意义(t=10.220,P<0.05)。
2.2 两组手术前后VCSS评分比较
术前,两组VCSS评分比较,差异无统计学意义(P>0.05);术后1个月,两组VCSS评分均较术前降低,且试验组低于对照组,差异有统计学意义(P<0.05),见表1。
表1 两组手术前后VCSS评分比较(分,±s)

表1 两组手术前后VCSS评分比较(分,±s)
注:VCSS为静脉临床严重程度评分表
组别例数术前术后1个月t P试验组40 13.36±5.24 3.84±1.03 14.302 <0.001对照组40 12.18±4.87 5.02±1.53 13.558 <0.001 t 1.043 4.046 P 0.300<0.001
2.3 两组并发症发生情况比较
试验组并发症发生率低于对照组,差异有统计学意义(P<0.05),见表2。
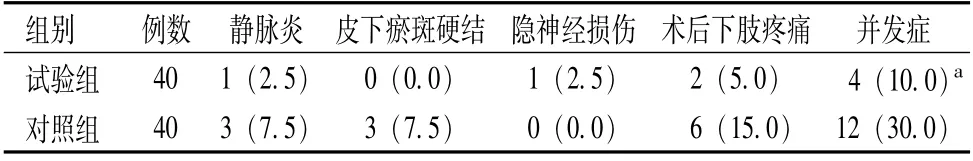
表2 两组并发症发生情况比较[例(%)]
3 讨论
VVLE为常见的一种外周血管疾病,以下肢浅表静脉扩张、迂曲为主要临床表现。随着病情的发展,可出现下肢营养性障碍性病变,严重者可引起溃疡、下肢水胀、静脉血栓等并发症,影响患者的正常生活。泡沫硬化剂血管内注射疗法具有操作简单、价格低廉的优点,在临床上被广泛应用于VVLE患者的治疗中;其作用机制是使含有空气的泡沫硬化剂与血管壁接触,刺激血管内膜发生无菌性炎症,引起血管内皮受损,促进血栓形成,血栓纤维化后导致血管永久性闭塞,从而达到治疗VVLE的效果[6]。介入下顺行硬化疗法是单纯泡沫硬化剂注射的改良治疗方式,通过在静脉顺行插入导管,经静脉造影明确下肢深静脉曲张程度,浅表静脉被造影剂填充,然后注入泡沫硬化剂;相比单纯注射泡沫硬化剂,介入下顺行硬化疗法可实时观察患肢浅静脉被硬化剂填充的情况,有助于医师根据填充效果调整硬化剂的注射剂量。然而单纯采用硬化疗法治疗时,硬化剂与血管内壁的接触往往有限,难以完全阻断静脉主干,复发率极高,且易引起静脉炎、术后下肢疼痛等并发症,影响患者术后的恢复速度。
本研究结果显示,试验组血管硬化药物使用总量少于对照组,差异有统计学意义(P<0.05);术后1个月,两组VCSS评分均低于术前,且试验组低于对照组,差异有统计学意义(P<0.05);术后3个月,试验组并发症发生率明显低于对照组,差异有统计学意义(P<0.05)。这一结果表明,与介入下顺行硬化治疗相比,EVLA联合硬化治疗可较好地改善患者的病情,减少硬化剂使用总量,降低相关并发症的发生率。其原因为,EVLA可通过激光效应损毁静脉内膜,使血管壁纤维化,刺激血管收缩,诱发血液凝固,促进血栓形成,达到促使血管腔闭合,消除反流的目的,对大隐静脉主干有较好的阻断效果,可有效治疗VVLE[7];由于主干静脉已由激光操作闭合,只需在穿刺困难部位注射硬化剂,因此使用的硬化剂总量较少;但EVLA对管径较细的静脉和扭曲、块状的静脉穿刺置管困难,激光光纤所使用的5F导管直径为2.8 mm,直径小于此数值的静脉光纤无法达到;激光在腔内激发时光纤位置的温度达到300℃,可瞬间损伤血管内膜,术中随着光纤向膝盖以下部位细小静脉移动,激发位置越来越接近皮肤表层,易引起操作部位皮肤烧伤、隐神经损伤和术后下肢疼痛等并发症,因此,在激发时需由助手用冷生理盐水浸湿的纱布对光纤头部施加压力,以分散吸收激光发射的过高热量。EVLA联合硬化治疗先利用EVLA有效闭合大隐静脉主干,之后再利用泡沫硬化剂治疗细小、扭曲、块状的静脉,不仅可有效减少皮肤灼伤、隐神经损伤及术后下肢疼痛等并发症的发生,还能减少泡沫硬化剂的使用剂量,进而减少泡沫硬化剂使用引起的并发症。术后患者下肢予物理加压同样重要。术后患肢即刻用弹力绷带包扎,应遵循从远端到近端、压力逐渐减小的原则。术后1周将弹力绷带更换为更方便脱换的弹力袜,嘱患者下地活动时穿戴,卧床休息时脱掉。包扎弹力绷带及穿戴弹力袜时需注意松紧适宜,通常以绷带或弹力袜内轻松容纳1个手指为标准。
综上所述,与介入下顺行硬化治疗相比,EVLA联合硬化治疗可较显著改善VVLE患者的病情,减少硬化剂使用总量及术后并发症的发生。

