肠溶缓释型替米考星固体分散体的制备、鉴定及体外释放度评价
伍涛,唐达
(重庆市畜牧科学院,重庆 荣昌 402460)
合理规避替米考星(tilmicosin,TMC)水溶性差、适口性差、毒副作用大和胃刺激性大等缺点[1],利用缓控释技术有效掩盖其苦味和降低毒副作用,是该药剂型发展的新方向[2].本试验综合考虑替米考星的物理化学性质以及操作简单便于工业化生产等因素,将肠溶性缓释材料羧甲基乙基纤维素(CMEC)、丙烯酸树脂(Eudragit L100)和羟丙基甲基纤维素邻苯二甲酸酯(HPMCP hp55s)作为载体,采用溶剂法制备肠溶缓释型替米考星固体分散体,对于控制替米考星在胃肠液中的溶出度,提高替米考星的生物利用度具有重要意义,也为替米考星剂型开发和临床应用提供理论参考,同时为该类兽药的科学合理使用创造更好条件.
1 材料与方法
1.1 药品与试剂
替米考星原料(含量94.01%,批号TMCZ1901011,宁夏泰瑞制药股份有限公司);替米考星对照品(含量93.9%,批号k0311407,中国兽医药品监察所);市售替米考星肠溶颗粒(含量20%,批号T1909011,湖北某动物药业有限公司);CMEC(广州锦骅化工科技有限公司);Eudragit L100(批号B181103223,德国EVONIK公司);HPMCP(浙江德清维康生物科技有限公司);无水乙醇、盐酸、磷酸、氢氧化钠、二丁胺、甲醇、乙腈等(色谱纯,重庆川东化工有限公司).
1.2 仪器设备
高效液相色谱仪(型号agilent1260,安捷伦);旋转蒸发仪(型号OSB-2200,东京理化EYELA公司);真空干燥箱(型号DZF-6050型,巩义市予华仪器有限责任公司);冰箱(型号BCD-212YM/T,海信容声冰箱有限公司);智能溶出试验仪(型号ZRS-8G,上海圣科仪器设备有限公司);多功能X射线衍射仪(型号XRD-7000S/L型,日本岛津);傅里叶变换红外光谱仪(型号IRTracer-100,日本岛津);集热式恒温加热磁力搅拌器(型号DF-101S,郑州长城);高速万能粉碎机(型号DFY-400C,无锡沃信).
1.3 肠溶缓释型替米考星固体分散体的制备
参考固体分散体的常用制备方法[3],本研究采用溶剂法制备3种肠溶缓释型替米考星固体分散体.
1.3.1 替米考星CMEC固体分散体(TMC+CMEC SD)的制备 精确称量8 g CMEC到90 mL 90%乙醇-水(v/v)溶液中,50 ℃水浴条件下搅拌至澄明使完全溶解后,缓慢加入2 g替米考星继续搅拌45 min,得TMC+CMEC乙醇-水混合溶液.
1.3.2 替米考星Eudragit固体分散体(TMC+Eudragit SD)的制备 精确称量2 g替米考星和8 g Eudragit L100到80 mL 95%乙醇-水(v/v)溶液中,50 ℃水浴条件下搅拌至澄明使完全溶解后,继续搅拌30 min,得TMC+Eudragit乙醇-水混合溶液.
1.3.3 替米考星HPMCP固体分散体(TMC+HPMCP SD)的制备 精确称量2 g替米考星和8 g HPMCP hp55s到100 mL 80%乙醇-水(v/v)溶液中,50 ℃水浴条件下搅拌至澄明使完全溶解后,继续搅拌30 min,得TMC+HPMCP乙醇-水混合溶液.
将上述所得混合溶液分别转移至旋转蒸发仪减压蒸发至粘稠状态或形成干燥粉末层(水浴温度50 ℃,转速40 r/min),然后迅速倒入预冷的金属托盘中,在-20 ℃冰箱中固化24 h,取出置于40 ℃真空干燥箱中干燥18~36 h,彻底除去溶剂.取出粉碎,过80目筛,放置干燥器避光保存.
1.4 替米考星含量的测定方法
1.4.1 溶液的配制 磷酸盐缓冲液:取0.1 mol/L的盐酸溶液和0.2 mo1/L磷酸钠溶液,按3∶1混合均匀,必要时用2 mol/L的盐酸或2 mol/L氢氧化钠溶液调节pH值至6.8.磷酸溶液:取磷酸5.71 g,加水900 mL用12.5 mol/L氢氧化钠溶液调节pH值至(2.5±0.1),加水至1 000 mL.供试品溶液:取适量替米考星肠溶性固体分散体粉末(以替米考星计约0.2 g),精密称定,置50 mL量瓶中,加提取液磷酸盐缓冲液10 mL,超声处理15 min,放冷后加乙腈10 mL,再加磷酸溶液稀释至刻度,摇匀后即得.对照品溶液的配制:取替米考星对照品适量,精密称定,加乙腈制成每毫升中含0.25 mg的溶液,精密量取5 mL,置25 mL量瓶中,用上述磷酸溶液稀释至刻度,摇匀后即得.
1.4.2 色谱条件 用十八烷基硅烷键合硅胶(250 mm×4.6 mm,5 μm)为填充剂;以水-磷酸二丁胺缓冲液[取二丁胺16.8 mL,加磷酸溶液(1→10)70 mL,边加边搅拌,放冷后,用磷酸调节pH值至(2.5±0.1),加水至100 mL](975∶25)为流动相A,以乙腈为流动相B.检测波长为280 nm;流速为每分钟1.1 mL.
1.4.3 线性关系考察 精确称取替米考星对照品50 mg,置50 mL容量瓶中,加入乙腈5 mL溶解,加流动相至刻度,摇匀备用.分别量取对照品溶液1.0、2.0、3.0、5.0及10.0 mL至25 mL容量瓶中,加流动相稀释至刻度,摇匀,制备浓度分别为0.04、0.08、0.12、0.20、0.40 mg/mL的标准样品作为对照品.将上述各浓度的对照品溶液,分别进样20 μL,记录峰面积,以替米考星溶液的浓度对峰面积作线性回归,绘制替米考星标准曲线.
1.4.4 精密度、稳定性和回收率试验 精密度试验:精密吸取120 μg/mL对照品溶液20 μL,重复进样6次,测量峰面积,计算峰面积的RSD值.稳定性试验:分别精密吸120 μg/mL对照品溶液20 μL于0、2、4、8、10、12及24 h进样,测量峰面积,计算峰面积的RSD值.回收率试验:取替米考星对照品约0.005、0.010及0.015 g,精密称定,分别置于50 mL的容量瓶中,加乙腈5 mL溶解,然后加入已知含量的样品溶液(300 μg/mL)5 mL,加流动相至刻度,摇匀,进样,测定替米考星的含量,除去样品本底,计算回收率及RSD值.
1.5 物象鉴定
参照固体分散体表征手段[4],将替米考星原料药和制得的3种肠溶缓释型替米考星固体分散体分别进行X射线粉末衍射(XRPD)和傅里叶变换红外光谱法(FTIR)试验.
1.5.1 X射线粉末衍射法 检测依据为JY/T009-1996转靶多晶体X射线衍射方法通则.测试条件:Cu靶,PIXceIID探测器,Ni滤波片,电压40 kV,电流40 mA,角度范围30°~60°,扫描速度12°/min,取适量样品填充样品槽,压实刮平,使用正装法进样,分别进行X射线衍射分析.
1.5.2 傅里叶变换红外光谱法 在红外光灯照射下,将KBr置入玛瑙研钵中研磨,直到KBr粉末中呈现出均匀的粉末状.为了确保红外图谱的质量,将供试品和KBr以1∶50~100的比例混合均匀,再放入研钵中进行研磨.取适量粉末放入压片机进行压片,在4 000~400 cm-1的范围内进行红外扫描.
1.6 体外溶出度的测定
1.6.1 酸中溶出量 分别取替米考星原料、市售替米考星肠溶颗粒和制得的3种肠溶缓释型替米考星固体分散体(以替米考星计约0.5 g),按照释放度测定法[5],用溶出度测定法第二法(浆法)装置,以0.1 mol/L盐酸溶液750 mL为溶出介质,溶出介质(37±0.5)℃,转速75 r/min,依法操作,经120 min时,取样10 mL,滤过待检.
1.6.2 缓冲液中的累计溶出度 在上述市售替米考星肠溶颗粒和制得的3种肠溶缓释型替米考星固体分散体的酸液中加入温度为(37±0.5)℃的0.2 mol/L磷酸钠溶液250 mL(必要时用2 mol/L盐酸溶液或2 mol/L氢氧化钠溶液调节pH至6.8),继续运转60 min.于2、5、8、10、15、22、30、45、60 min取样10 mL,滤过待检.每次取样后补充相同释放介质10 mL.采用高效液相色谱法分别测定峰面积,计算出不同时间样品液的浓度,求算药物的累积溶出百分率,计算累积溶出度,绘制溶出曲线.
2 结果与分析
2.1 含量测定方法研究结果
2.1.1 线性关系考察 线性关系考察结果见图1,线性回归方程为y=3 604.83x+19 756.99(r2=0.999 5),替米考星浓度在40~400 μg/mL范围内,与峰面积呈良好线性关系.

图1 替米考星标准曲线
2.1.2 精密度、稳定性和回收率试验结果 结果显示,精密度RSD0.64%,稳定性RSD0.61%;平均回收率100.12%,RSD1.58%.说明本方法测定精密度和稳定性良好,回收率高,可满足肠溶缓释型替米考星固体分散体含量测定要求.
2.2 物象鉴定结果
2.2.1 X射线粉末衍射分析 检测结果用软件Origin进行绘制,见图2.经X射线衍射表征后发现,替米考星是一种无定型物质,没有特征衍射峰出现,只是在低角度处具有一些叠状衍射峰,这与其他文献报道一致[6-7].使用不同肠溶性载体制备的替米考星固体分散体分别在9°、17°和23°左右处具有特征衍射峰.说明替米考星以无定形态分散在载体中,制备的肠溶缓释型替米考星固体分散体为晶体结构.
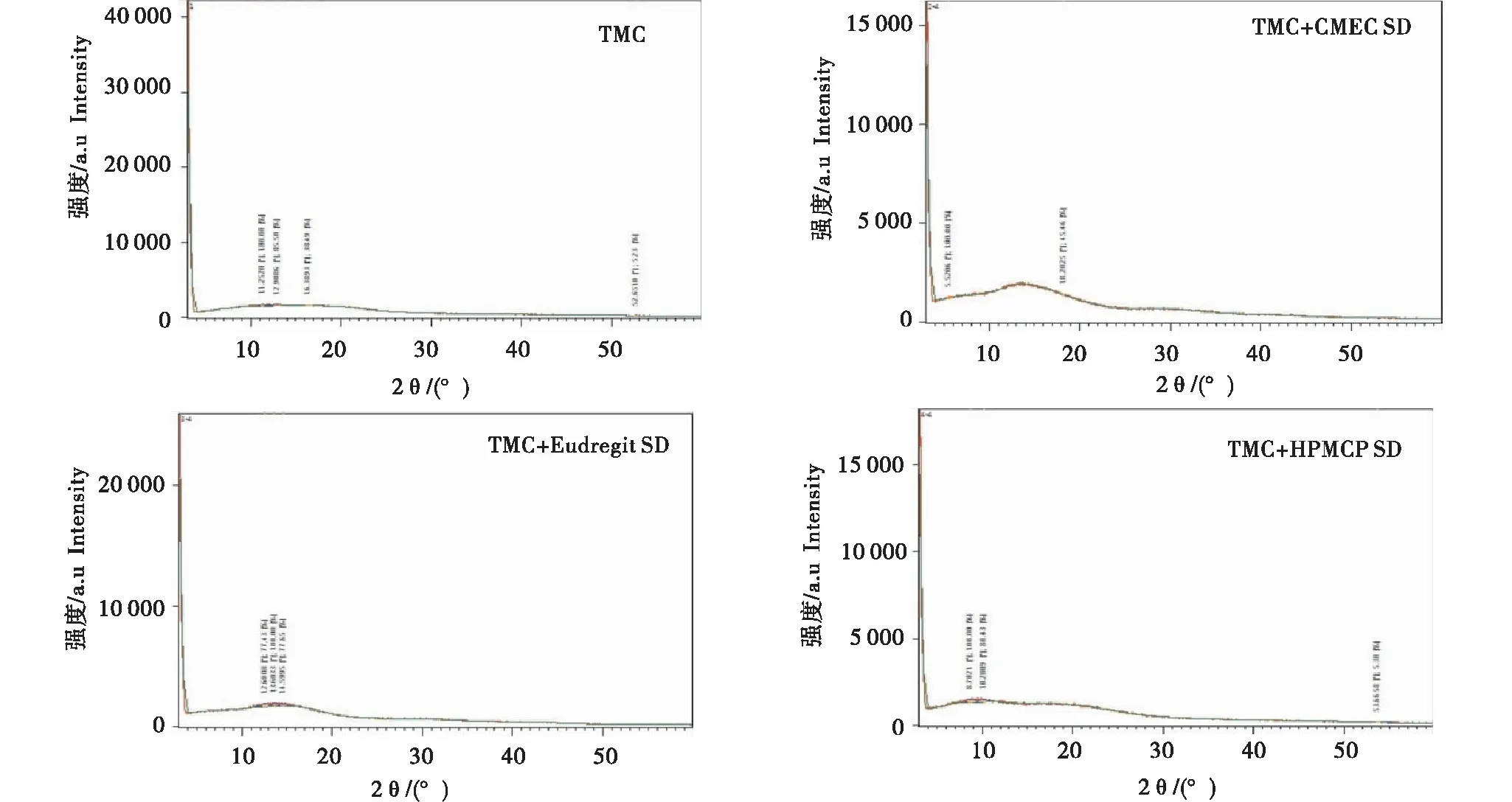
图2 肠溶缓释型替米考星固体分散体XRPD检测结果
2.2.2 傅里叶变换红外光谱法分析 如图3~6所示,替米考星在1 592 cm-1和1 456 cm-1处有中等强度的吸收峰,分别为N-H弯曲振动和C-H的不对称弯曲振动吸收峰.在2 966 cm-1和2 933 cm-1处具有尖锐的吸收峰,分别为-CH2和-CH3的不对称伸缩振动峰.在1 168 cm-1和1 082 cm-1处具有强烈吸收峰,分别为C-O和C-O-C的伸缩振动.分析发现,1 592 cm-1和1 456 cm-1的中等吸收峰相对减弱,2 966 cm-1和2 933 cm-1处的尖锐吸收峰以及在1 168 cm-1和1 082 cm-1处的强烈吸收峰均消失,这说明替米考星原料药已分散于不同载体中.
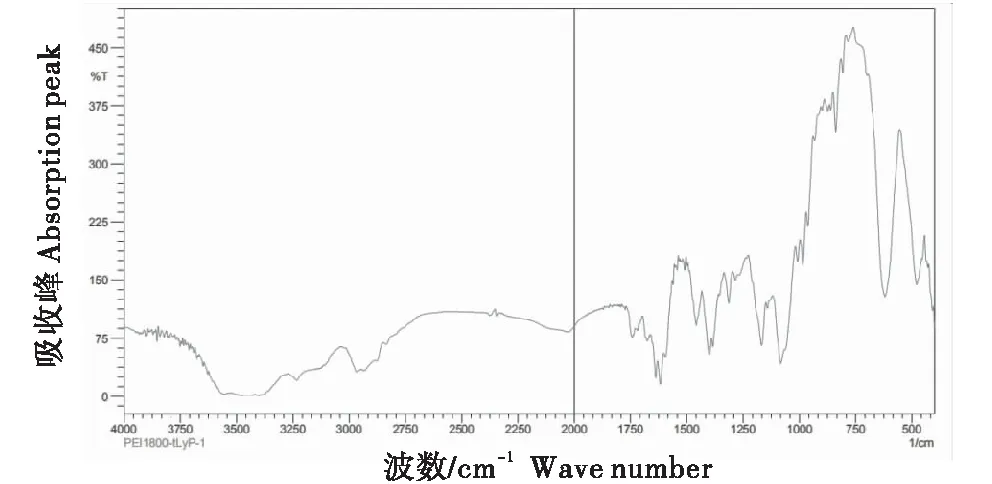
图3 替米考星原料FTIR检测结果
2.3 体外溶出度测定结果
2.3.1 酸中溶出量 替米考星原料、市售替米考星肠溶颗粒和肠溶缓释型替米考星固体分散体在120 min时的酸中溶出量见表1.结果显示,替米考星原料几乎全部溶出(97.46%),市售替米考星肠溶颗粒溶出量为16.07%,而试验制得的3种固体分散体溶出量分别为8.91%、6.57%和7.04%.因此本试验制得的3种肠溶缓释型替米考星固体分散体均符合兽药典对肠溶制剂在酸中溶出量小于10%的规定.

图4 TMC+CMEC SD的FTIR检测结果

图5 TMC+Eudragit SD的FTIR检测结果

图6 TMC+HPMCP SD的FTIR检测结果

表1 肠溶缓释型替米考星固体分散体的酸中溶出量
2.3.2 缓冲液中累计溶出度 市售替米考星肠溶颗粒和肠溶缓释型替米考星固体分散体在2、5、8、10、15、22、30、45、60 min时的累计溶出度见表2和图7.结果显示,市售替米考星肠溶颗粒溶出较慢,60 min时最终累计溶出度43.31%,有效成分释放不完全.而试验制备的3种固体分散体在缓冲液中的释放效果较理想,45 min时累计溶出度均达70%以上,60 min时最终累计溶出度分别为71.67%、77.04%和73.87%,有效成分释放迅速且完全.因此本试验制得的3种肠溶缓释型替米考星固体分散体均符合兽药典对肠溶制剂在缓冲液中累计溶出度不低于70%的规定.

图7 缓冲液累计溶出曲线

表2 缓冲液累计溶出度试验结果
3 讨论
3.1 替米考星口服制剂的胃刺激性问题
替米考星对胸膜肺炎放线菌、巴氏杆菌引起的畜禽呼吸疾病有较理想的治疗效果[8-9],是目前治疗该类呼吸道感染用量最大、最常用的药物之一,该药的不良反应主要是在肠道外给药时对心脏肾脏的毒性作用[10],因此替米考星口服给药更安全有效.但替米考星味苦,动物拒食情况非常普遍,同时替米考星口服时在胃中溶解释放与胃黏膜接触,刺激胃黏膜分泌过多胃液,引起胃出血、胃溃疡[11].据文献报道,替米考星在胃中溶解释放同时也会大大降低其生物利用度[12],这显著增加了用药成本.目前,一些研究人员将替米考星制作成盐[13],或者做成微囊[14]、纳米乳[15]、包合物[16]等新型制剂,甚至用水溶性载体制备成水溶性替米考星固体分散体[17-18],虽能不同程度地掩盖苦味、提高溶解度和生物利用度,但依然没有真正解决口服替米考星对胃的刺激性问题.
3.2 载体材料的选择
固体分散体技术(solid dispersion,SD)是指通过一定方法使药物以分子、微晶或无定形态高度分散在适宜载体材料中的固态分散技术[19].不同载体制备的固体分散体,可表现出不同的溶出特性,亲水性载体可增加难溶性药物的溶出速度和溶解度,并提高药物的生物利用度;难溶性载体可延缓或控制药物释放,使药物长效化;而肠溶性载体可控制药物于小肠中靶向释放[20].随着药剂学的发展及新辅料的不断出现,结合动物生理生化特征和用药特点,选择CMEC、Eudragit L100和HPMCP hp55s 3种肠溶性缓释材料[21-23]作为载体制备肠溶缓释型替米考星固体分散体,既可掩盖替米考星苦味,又可靶向在动物肠道前端位置定位释放,有效解决替米考星的胃刺激性问题,同时制得的成品呈粉末状,可拌料给药,便于群防群控.
3.3 制备方法的选择
由于替米考星熔点较高,因此本试验采用溶剂法制备替米考星固体分散体,相对于流化床包衣法、溶剂-喷雾(冷冻)干燥法等制备固体分散体的新工艺[24-25],本法具有收率高、步骤简易和成本较低的特点,同时通过安装溶剂自动回收装置,可以有效对溶剂进行回收和循环再利用,进一步节约成本,避免环境污染.
3.4 体外溶出度测定的选择
体外溶出度测定是筛选缓控释制剂处方和质量控制的重要手段[26],目前以转篮法和桨法应用最广泛,且均符合2015年版《兽药典》附录0931的相关规定.桨法搅拌速度虽然与转篮法篮子的转动速度一致,但桨法中搅拌桨的摆动强度大,搅拌范围宽,强有力的搅拌更有利于样品的溶出释放,因此本研究采用桨法对替米考星原料、市售替米考星肠溶颗粒和肠溶缓释型替米考星固体分散体进行了体外溶出度的测定.
4 结论
本试验制得的TMC+CMEC SD、TMC+Eudragit SD和TMC+HPMCP SD 3种肠溶缓释型替米考星固体分散体,通过XRPD和FTIR物象鉴别试验,验证了替米考星以无定形态分散于3种不同肠溶性缓释载体材料中.3种固体分散体的体外溶出度结果较为理想,均符合兽药典中对肠溶制剂在酸中溶出量小于10%、在缓冲液中累计溶出度不低于70%的规定,为替米考星口服新剂型的开发应用提供了理论参考.3种肠溶液缓释型替米考星固体分散体操作简单,具有良好的开发前景.

