妊娠中晚期替诺福韦治疗乙肝高病毒血症孕妇的效果观察
熊华刚,王 梅,杨智刚,谭 丽,马 菁,王 静
(贵阳市公共卫生救治中心肝病科 贵州 贵阳 550004)
在我国乙型肝炎表面阳性的乙型肝炎病毒(HBV)携带人员较高,这部分人群身体里面有乙肝病毒,具有传染性,如果在孕期会因为母婴直接传播而造成感染,而且宫腔感染的患儿90%以上概率会发展成为慢性感染[1],终身携带肝脏疾病,发生肝硬化,甚至出现肝癌,因此需要在孕期对HBV 感染进行阻断,控制疾病蔓延。研究显示如果孕妇机体内的HBV-DNA、HBsAg 为阳性,而胎儿感染的概率较高,需要对其进行阻断[2]。替诺福韦对于HBV 阻断效果较好,而且安全性高。本文对妊娠中晚期孕妇应用替诺福韦治疗乙肝高病毒血症孕妇的效果进行研究,现分析如下。
1.资料与方法
1.1 一般资料
选取2018 年1 月—2020 年3 月自本院肝病科和妇产科抽取60 例乙肝高病毒血症HBV 产妇展开回顾性分析。其中,初产妇36 例,经产妇24 例,年龄21 ~38 岁,平均年龄(29.76±2.34)岁,产次1 ~3 次,平均(2.03±0.54)次。纳入标准:(1)均在孕前发生感染,全程接受产检[3];(2)进行HBsAg、HBV-DNA检验为阳性,HBV-DNA ≥2×10E5IU/mL;(3)自身肝功能正常,未接受药物治疗;(4)签署知情同意书。排除指标:(1)合并其他妊娠疾病(高血压、高血糖等);(2)严重脑部、肾脏以及肝脏疾病;(3)胎盘早剥、前置胎盘、甲状腺史、精神疾病史[10];(4)胎儿畸形。
1.2 方法
实验组产妇在孕期接受健康指导,全程关注饮食和生活等变化,自孕周的第24 ~28 周开始口服替诺福韦,1 次/d,每次300 mg,持续至妊娠结束。而新生儿在出生之后的6 h 内注射乙型肝炎免疫球蛋白注射,并在出生的24 h、1 个月和6 个月注射乙型肝炎疫苗。
1.3 观察指标
(1)治疗有效率评估,在治疗前、治疗4 周、分娩前、分娩后4 周,检测HBV-DNA、HBsAg、HBeAg、ALT(谷丙转氨酶)、AST(谷草转氨酶)指标的变化情况。
(2)治疗后的孕期安全性评估,新生儿在出生7 个月之后通过实时荧光定量聚合酶链式反应对HBV-DNA 进行测试。同时统计孕期和分娩过程中的各项并发症(包括胎膜早破、羊水污染、产后出血和新生儿窒息)。
(3)治疗不良反应评估,对产妇治疗前后肾功能(血肌酐、血尿素氮)、心肌酶(乳酸脱氢酶、谷草转氨酶)、电解质(钙、磷)、乳酸、骨密度进行检查,获取各项指标。
1.4 统计学方法
数据采用SPSS 23.0 统计软件处理,计数资料以率[n(%)]表示,采用χ2检验;计量资料用均数±标准差(± s)表示,应用t检验。以P<0.05 为差异有统计学意义。
2.结果
2.1 治疗疗效评估
治疗前HBV-DNA、HBsAg、ALT、AST 指标与治疗后4 周、分娩前、分娩后4 周对比降低显著,数据两两对比差异有统计学意义(P<0.05),见表1。
表1 治疗疗效评估( ± s)
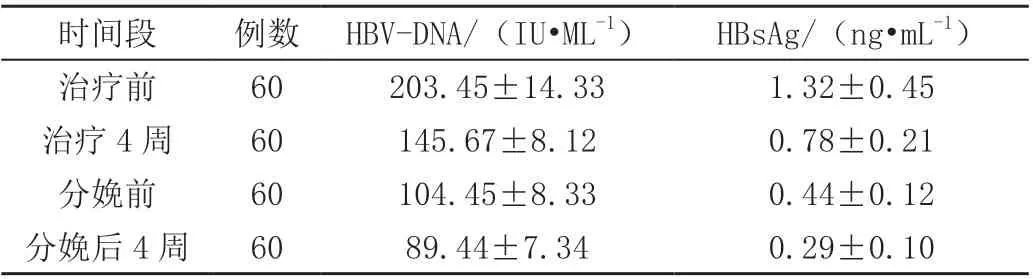
表1 治疗疗效评估( ± s)
时间段 例数 HBV-DNA/(IU·ML-1) HBsAg/(ng·mL-1)治疗前 60 203.45±14.33 1.32±0.45治疗4 周 60 145.67±8.12 0.78±0.21分娩前 60 104.45±8.33 0.44±0.12分娩后4 周 60 89.44±7.34 0.29±0.10

表1(续)
2.2 治疗后的孕期安全性评估
60 例产妇中新生儿HBV-DNA 阳性0 例,胎膜早破2 例、羊水污染1 例、新生儿窒息1 例,感染率为0.00%,分娩并发症发生率为6.67%,安全性较高。
2.3 治疗不良反应评估
治疗后血肌酐、血尿素氮、钙、骨密度与治疗前对比差异无统计学意义(P>0.05);治疗后虽然乳酸脱氢酶、谷草转氨酶、磷、乳酸较治疗前升高,差异显著(P<0.05),但是均在正常范围内,见表2。
表2 治疗不良反应评估( ± s)
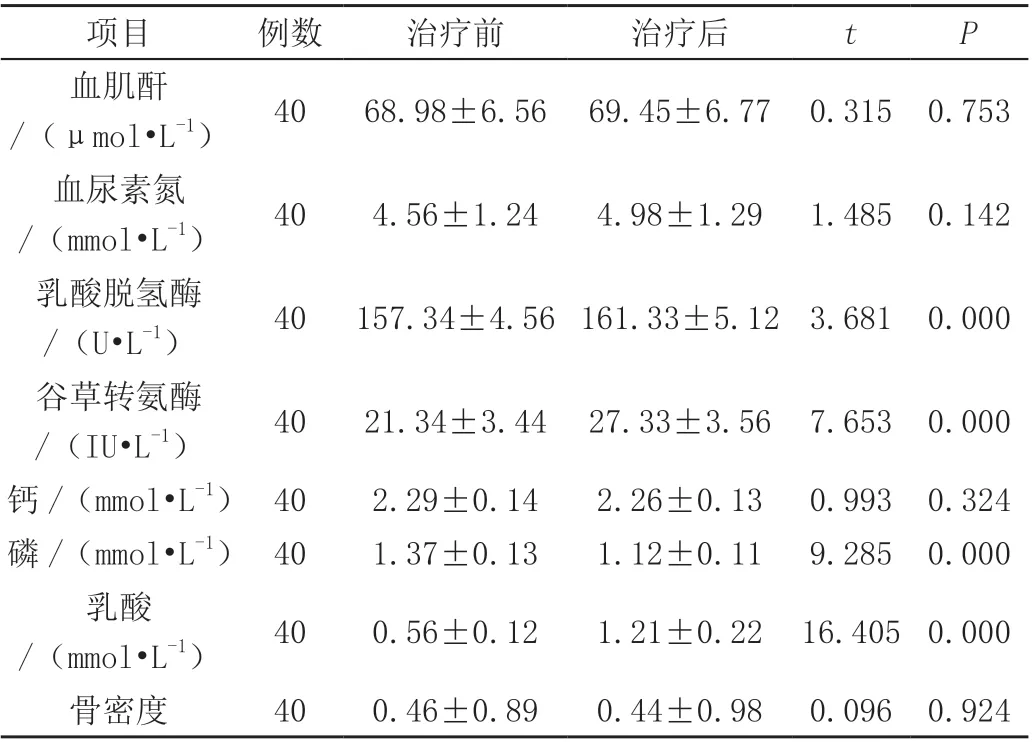
表2 治疗不良反应评估( ± s)
项目 例数 治疗前 治疗后 t P血肌酐/(μmol·L-1) 40 68.98±6.56 69.45±6.77 0.315 0.753血尿素氮/(mmol·L-1) 40 4.56±1.24 4.98±1.29 1.485 0.142乳酸脱氢酶/(U·L-1) 40 157.34±4.56 161.33±5.12 3.681 0.000谷草转氨酶/(IU·L-1) 40 21.34±3.44 27.33±3.56 7.653 0.000钙/(mmol·L-1) 40 2.29±0.14 2.26±0.13 0.993 0.324磷/(mmol·L-1) 40 1.37±0.13 1.12±0.11 9.285 0.000乳酸/(mmol·L-1) 40 0.56±0.12 1.21±0.22 16.405 0.000骨密度 40 0.46±0.89 0.44±0.98 0.096 0.924
3.讨论
相关研究显示围生期、围产期是导致新生儿慢性乙型肝炎感染的重要原因,而婴幼儿期HBV 感染也占据感染的25%~30%。以往对于HBV 感染的阻断主要依靠乙肝免疫球蛋白疫苗,但是存在阻断失败的问题,因此对于乙肝高病毒血症乙型肝炎病毒患者需要在孕期就考虑进行病毒阻断,降低母体血液中HBV 病毒量,以控制新生儿在宫腔内的感染[4]。
替诺福韦属于核苷酸逆转录酶抑制剂的一种类型,在使用之后可以对病毒的控制进行控制,可以在妊娠期使用,药物地安全性较高[5],因此该药物使用之后患者肝功功能各指标均得到改善,前HBV-DNA、HBsAg、ALT、AST 指标下降显著。
研究显示妊娠期、产褥期女性身体会发生变化,导致肝脏的负担增加,自身的免疫功能降低,血液中的HBV病毒会增加[6],导致感染的概率增加。而且分娩期间会因为出血等问题,导致肝脏负担增加,而替诺福韦可以抑制病毒的复制,使血液中HBV 病毒数量降低[7],以减少新生儿感染的概率,因此实验组新生儿HBV-DNA 阳性率显著低于对照组,感染率得到显著的降低。
乙肝高病毒血症的出现与产前出血、妊娠期糖尿病之间存在非常密切的联系,一旦发生乙肝高病毒血症,产妇机体没内病毒量增加,对血液流动、脏器等造成损伤,而替诺福韦的加入则对病毒进行控制,抑制机体内的毒性和炎症反应[8],因此感染率较为0.00%,分娩并发症发生率为6.67%。
从不良反应分析,替诺福韦属于替诺福韦脂的前体药,具有更高的抗病毒活性以及更好的淋巴组织分散度,大大降低了肾毒性和骨质疏松风险,但是可能增加心脏负荷,因此需要遵医嘱使用药物,并定期进行各项检查。
综上所述,乙肝高病毒血症乙型肝炎病毒携带患者在妊娠中晚期进行替诺福韦治疗干预,可以使孕产妇肝功能各项指标基本恢复正常,能有效阻断HBV-DNA 的母婴传播,降低孕产妇分娩期间的并发症发生率,提升分娩安全。

