肝移植术后人细小病毒B19 感染致纯红细胞再生障碍性贫血1 例并文献复习
封立魁,杜国盛,周林,郑永根(中国人民解放军总医院第八医学中心肝胆外科,北京100091)
纯红细胞再生障碍性贫血(pure red cell aplasia,PRCA)表现为正细胞正色素性贫血,以外周血红细胞、网织红细胞计数严重减少,骨髓象有核红细胞减少或缺如为特征的一种典型的贫血综合征[1]。随着器官移植数量的增多,术后人细小病毒B19(human parvovirus B19,HPV-B19)感染导致的PRCA 逐渐引起移植医生的重视。回顾我院1 例肝移植术后HPV-B19 感染导致PRCA 的病例,现随访近2 年并结合文献复习对此病的临床表现及诊治特点进行总结。
1 临床资料
患者男性,48 岁。因“酒精性肝硬化,食管胃底静脉曲张出血,2 型糖尿病”就诊我院于2018 年4 月6 日行同种异体肝移植术。术前给予巴利昔单抗(20 mg)及甲泼尼龙(500 mg)免疫诱导,术后口服醋酸泼尼松+他克莫司(tacrolimus,FK506)+ 吗替麦考酚酯(mycophenolate mofetil,MMF)抗排斥反应治疗,胰岛素控制血糖良好,肝功能顺利恢复。术后3 周患者出现乏力伴有一过性高热(39.3℃),随后出现血红蛋白进行性下降,其下降程度比慢性失血更为严重,且输血难以纠正。患者的叶酸、维生素B12水平正常,化验血清铁34.2 μmol/L,铁蛋白981.4 ng/ml,网织红细胞百分比0.25%,绝对值0.006×1012/L,尿便隐血均阴性。排除临床相关的出血事件并停用吗替麦考酚酯后患者贫血仍无改善。
患者2018 年5 月15 日于中国医学科学院血液病院行骨髓穿刺提示骨髓增生活跃,粒系比例增高,红系比例减低,以早阶段有核红细胞为主,符合PRCA骨髓象。化验促红细胞生成素(Erythropoietin,EPO)>762 U/L (正常参考2.59 ~ 18.5 U/L),叶酸、维生素B12均正常。2018 年5 月18 日实时荧光PCR 定 量 检 测HPV-B19 DNA >1×108copies/ml,IgM(+), 排 除 药 物、 巨 细 胞 病 毒 及EB 病毒感染, 确诊为HPV-B19 急性感染所致PRCA。患者于2018 年5 月25 日开始静脉注射免 疫 球 蛋 白(intravenous immunoglobulin,IVIG)400 mg/(kg·d)连用5 d,6 月5 日复查HPV-B19 DNA >1×108copies/ml,IgM 呈弱(+),6 月11 日复查HPV-B19 DNA >1×108copies/ml,此时IgM已转为阴性。患者第一次IVIG 冲击治疗期间血红蛋白持续下降,平均每日输注悬浮红细胞2 U,在冲击结束后复查血红蛋白最低仅22 g/L。首次冲击治疗后复查HPV-B19 DNA 未见下降趋势,考虑与此时的他克莫司药物浓度较高相关(图1),随后他克莫司予以减量在维持较低的他克莫司浓度情况下于6 月24 日再次给予IVIG〔400 mg/(kg·d)〕连续冲击5 d,6 月29 日患者HPV-B19 DNA 定量检测为6×105copies/ml,同时伴随网织红细胞迅速回升(图2),1 周后不依赖输血情况下患者血红蛋白稳定在70 g/L 以上(图1)并呈上升趋势。随访至投稿日患者血红蛋白稳定在100 g/L 以上。
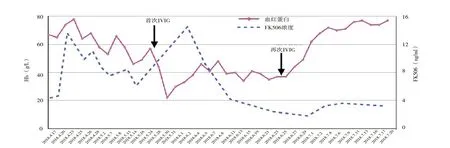
图1 血红蛋白及FK506 血药浓度变化趋势

图2 细小病毒B19 DNA 及网织红细胞计数变化趋势
2 讨 论
HPV-B19 是一种小型(25 nm)、无包膜单链DNA 病毒,1975 年澳大利亚病毒学家Cossart 在筛查乙肝表面抗原时在微量滴定板B 组19 号标本中发现并命名[2]。HPV-B19 主要经呼吸道传播,也可经母婴垂直传播,输血和血制品或器官移植传播[3-4]。HPV-B19 对人红系祖细胞具有趋向性,细胞受体为红细胞糖苷酯(又称红细胞P 抗原),该抗原存在于胎盘、胎儿心肌、胎儿肝脏,红细胞、红细胞前体细胞,以及一些巨核细胞和内皮细胞上。少数人可能缺乏血型P 抗原而对HPV-B19 感染具有天然抵抗力[5]。
HPV-B19 感染的临床表现多种多样[6],与宿主的年龄及免疫状态有关,免疫功能正常者感染后呈自限性,多表现为发热、头痛等类似感冒的症状。特殊人群感染会导致严重疾病,儿童感染后的典型表现是急性传染性红斑(第5 病),孕妇感染后可导致自然流产,胎儿积水,胎儿死亡[7]。少数人HPV-B19 感染还可引起急性肾小球肾炎、暴发性肝衰竭[8-10]。实体器官移植患者感染后通常表现为持久的纯红细胞再生障碍性贫血,大多在移植术后3 个月内发病,其中99%的患者存在贫血,白细胞减少、血小板减少、发热分别占37%、21%和25%[11]。有报道心脏移植术后HPV-B19 感染所致贫血其血红蛋白均低于80 g/L[12]。
HPV-B19 公认有3 种基因型,我国主要流行1 型,冬春季节是感染的高发期,约3 ~4 年会出现一次爆发流行[13-14]。由于HPV-B19 体积小、无包膜,对热不敏感等特点,用于血液制品的病毒灭活程序包括溶剂/去污剂(S/D)和巴氏杀菌很难将其灭活。Zhang 等[15]对我国2009 — 2011 年间142 个原料血浆池进行HPV-B19 检测,54.2%(77/142)的血浆池检测到病毒污染,血浆制品的污染率约21%,其中凝血因子Ⅷ、凝血酶原复合物、纤维蛋白原的污染率超过50%,静注人免疫球蛋白污染率也达39%。Jia 等[16]对我国2008 — 2013 年3 家血制品企业的原料血浆进行HPV-B19 核酸检测显示污染率达72%(169/235),且49%的病毒量>104U/ml。重症肝病受者肝移植围术期大量应用血浆、凝血酶原复合物、纤维蛋白原等血制品,加上术后免疫抑制治疗,使其感染HPV-B19的风险增大。此患者围术期大量输注血制品,术后1 个月内出现HPV-B19 感染,不能排除经输血或血制品传播的可能,且追踪来自同一供体的两例肾移植患者未出现相关症状。为保障血制品的安全性,美国食品药品监督管理局(Food and Drug Administration,FDA)建议混合原料血浆中HPV-B19 的病毒含量不应超过104U/ml。
美国移植会感染病实践委员会建议当患者出现以下表现时应怀疑HPV-B19 感染:① 网织红细胞减少或促红细胞生成素抵抗性贫血,伴或不伴发热、关节痛或皮疹;② 器官功能障碍如肝炎、心肌炎、肺炎、肾小球肾炎、神经系统疾病或血管炎;③ 全血细胞减少。初步检查应包括血清学(IgG 和IgM)和HPV-B19 PCR 定量检测,血清学和PCR检测阴性时应进一步行骨髓活检[17]。总结国内肝移植术后HPV-B19 相关PRCA 的病例报道,其发病时间多在术后2 个月内,且大多数经调整免疫方案及IVIG 治疗后2 周时病情开始好转,复发率约10%,复发后再次冲击治疗效果良好(表1)[18-23]。
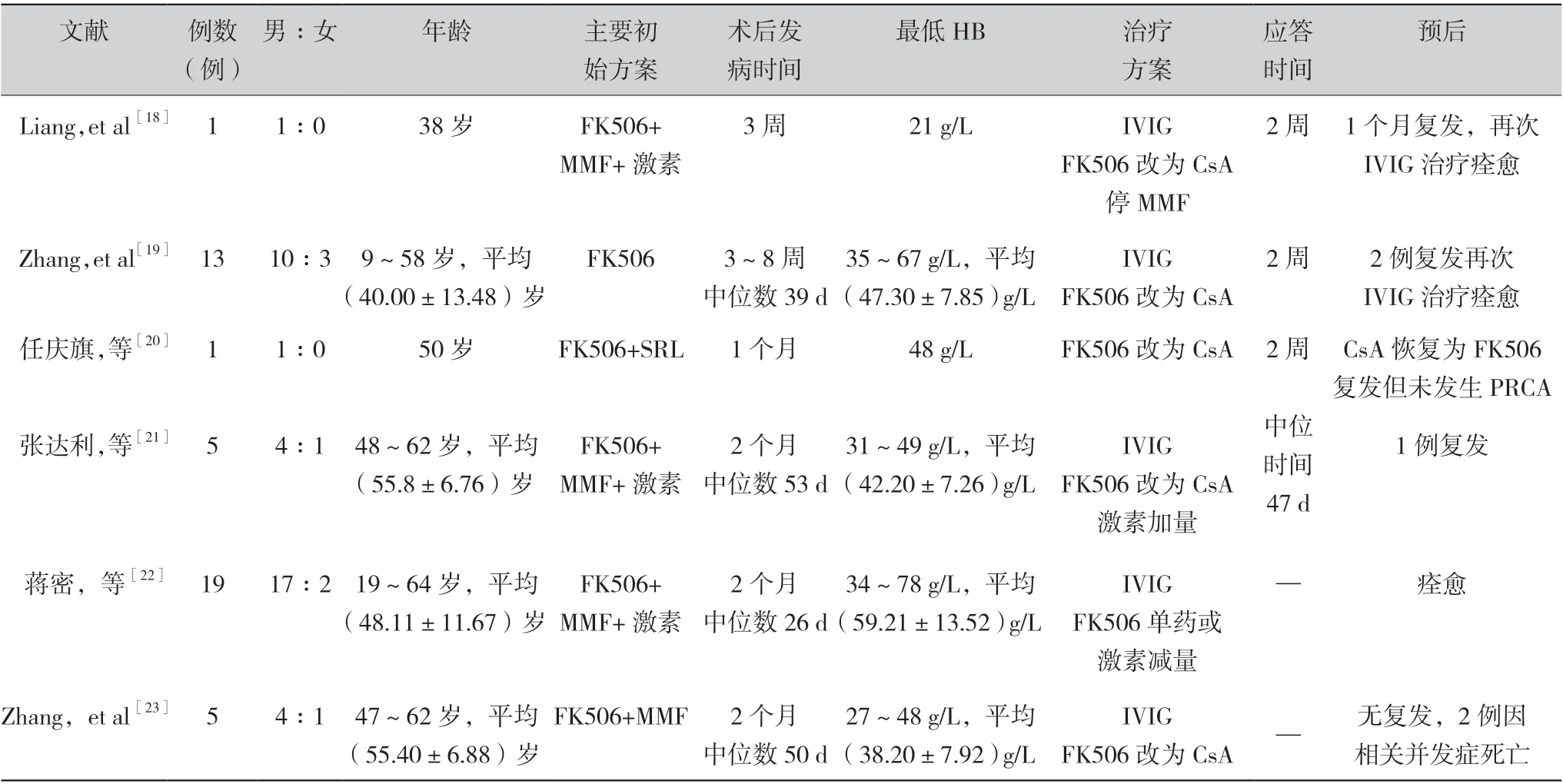
表1 我国肝移植术后HPV-B19 感染所致PRCA 的病例特点
目前还没有治疗HPV-B19 的抗病毒药物,美国移植会感染病实践委员会建议通过减少免疫抑制剂和输注IVIG 补充外源性抗体治疗,并建议IVIG剂量为400 mg/(kg·d)连用5 d。IVIG 每日剂量≥1 g/kg 时肾毒性和其他不良反应的发生率升高,用蔗糖做稳定剂的IVIG 有导致可逆性渗透性肾损伤的风险[24]。该患者首次IVIG 冲击治疗后贫血未见好转迹象,随后在维持较低的他克莫司浓度下再次给予IVIG冲击治疗, 1周后贫血迅速改善而不再依赖输血。
另外本例患者诊治期间两次化验EPO 浓度均远高于正常值,因此未使用重组人促红细胞生成素(recombinant human erythropoietin,r-HuEPO)治疗。有文献报道EPO 可能促使病毒复制[25],EPO 与骨髓红系祖细胞表面的EPO 受体结合促进红系集落形成单位扩增分化,HPV-B19 有嗜红系祖细胞的特性,通过结合红细胞P 抗原感染红系祖细胞,随后病毒复制导致细胞溶解下调EPO 受体表达,因此对EPO 治疗无反应[26]。Liang 等[18]报告1 例确诊时化验EPO 为200 U/L(正常参考4 ~ 21 U/L),随后停用r-HuEPO 并输注IVIG 治疗后病情迅速缓解。我们推测HPV-B19 导致的PRCA 在确诊时EPO 已处于较高水平,因此无需补充r-HuEPO 治疗,因该病例较少见需要临床工作中进一步总结验证。
本例患者在肝移植术后1 个月时出现输血治疗无效的顽固贫血,经骨髓穿刺及荧光PCR 定量确诊为HPV-B19 感染导致的PRCA,经减少免疫抑制剂用量、IVIG 冲击及输血治疗痊愈至今未见复发。因此对于肝移植术后出现纯红细胞再生障碍性贫血的患者应排除HPV-B19 感染,及早确诊后经减少免疫抑制剂剂量和输注IVIG 治疗预后良好。

