二黄膏外敷联合西医常规疗法治疗 急性痛风性关节炎临床研究
段连香,陈杰,刘子洋,廖琳,郭玥,路建饶
1.上海中医药大学附属第七人民医院,上海 200137;2.叶景华全国名老中医传承工作室,上海 200137
痛风性关节炎是由于尿酸盐沉积在关节囊、滑囊、软骨、骨质和其他组织中而引起的病损及炎性反应[1],起病急,以关节红、肿、热、痛及活动受限为主要表现,多夜间发作,属中医学“痹证”范畴。目前强调需在治疗早期(24 h内)抗炎止痛,以达到快速缓解疼痛的首要目的[2],非甾体消炎药、秋水仙碱及糖皮质激素等虽可在一定程度上缓解病情,但可能伴随消化道不良事件及肝肾损伤,甚至出现心脑血管不良事件。目前,中西医结合治疗急性痛风的方法众多,但缺乏规范化标准。二黄膏是上海市名老中医叶景华经验方,主要用于痛风病急性发作的局部外敷及其他局部关节炎症导致的红肿热痛。本研究采用二黄膏外敷联合西药常规疗法治疗急性痛风性关节炎,观察其临床疗效,现报道如下。
1 资料与方法
1.1 一般资料
选择2019年10月1日-2020年10月1日上海中医药大学附属第七人民医院肾病科门诊或住院痛风性关节炎急性发作患者80例,采用随机数字表法分为治疗组和对照组各40例。治疗组男性33例,女性7例;年龄25~59岁,平均(46.1±9.7)岁;病程1.0~8.0年,平均(3.77±1.86)年;急性发作病程12~46 h,平均(28.50±9.22)h;累及关节1~3个,平均(1.63±0.63)个。对照组男性32例,女性8例;年龄26~58岁,平均(45.8±9.2)岁;病程0.8~7.5年,平均(3.40±1.81)年;急性发作病程12~45 h,平均(28.35±8.39)h;累及关节1~3个,平均(1.53±0.51)个。2组一般资料比较差异无统计学意义(P>0.05),具有可比性。本研究经上海中医药大学附属第七人民医院伦理委员会审查批准(2019-IRBQYYS-022)。
1.2 诊断标准
参照《2015年美国风湿病学会/欧洲抗风湿病联盟痛风分类标准》[3]制定急性痛风性关节炎诊断标准:①急性关节炎发作>1次;②第一跖趾关节痛、肿;③单关节炎发作;④关节色红;⑤第一跖趾关节受累;⑥高尿酸血症;⑦可疑痛风石;⑧炎症反应7 d内达高峰;⑨单侧跗骨关节受累;⑩X线证实关节内肿胀。具有上述症状中的6项即可确诊。
1.3 纳入标准
①符合上述急性痛风性关节炎诊断标准;②急性起病,本次发作48 h内;③年龄18~60岁;④意识清晰,无明显障碍,无心、肝、肾、血液系统或免疫系统等严重疾病;⑤患者依从性良好,自愿签署知情同意书。
1.4 排除标准
①合并其他风湿病;②合并心、肝、肾功能和造血系统严重原发疾病;③妊娠及哺乳期妇女;④精神疾病患者;⑤药物过敏者或不能够按要求用药,后续资料统计不全;⑥皮肤破溃者或对本方药过敏。
1.5 脱落与剔除标准
脱落标准:①治疗过程中,受访者依从性差,影响诊治信息真实、完整记录;②观察过程中自行退出;③资料不全,影响有效性和安全性判断。
剔除标准:因不符合纳入标准而纳入的病例或事后发现应予排除的病例,包括误诊、误纳、无任何检测记录。
1.6 治疗方法
2组均进行生活干预,包括健康教育,卧床休息,抬高患肢,保护患侧关节,限制活动,调整生活方式;低嘌呤饮食,禁止饮酒;饮水>2 L/d。
对照组在生活干预基础上加用秋水仙碱片(昆药集团股份有限公司,0.5 mg/片,批号190705)0.5~1 mg,24 h总量不超过6 mg,疼痛症状明显改善后减量,疗程1周。
治疗组在对照组治疗基础上予二黄膏(专利号ZL201810920600.8)外敷,将栀子、大黄、红花、丁香、肉桂、芒硝按4∶5∶2∶1∶1∶5打粉,以甘油调成糊状,上海中医药大学附属第七人民医院中药房制备。敷药前温水清洗患处,均匀外敷并覆盖患者关节的红肿热痛点,厚度约2 mm,以纱布覆盖后用绷带固定,4 h/次,2次/d,疗程1周。
1.7 观察指标
1.7.1 临床体征评分
于治疗前后参考《22个专业95个病种中医诊疗方案》[4]对关节肿胀按4级计分。0分:关节无肿胀或肿胀消失;1分:关节肿胀、皮色红;2分:关节显著肿胀、皮色发红;3分:关节高度肿胀、皮色黯红。
1.7.2 疼痛视觉模拟法评分
于治疗前后采用疼痛视觉模拟法(VAS)[5]评估患者主观表述的疼痛强度。10 cm标尺上选择可代表当前疼痛强度的点,0分表示无痛,10分表示最大强度疼痛,患者所选分数为VAS评分。记录疼痛缓解时间。
1.7.3 实验室指标
于治疗前后采集2组患者空腹肘静脉血10 mL,由上海中医药大学附属第七人民医院检验科采用全自动生化分析仪检测白细胞计数(WBC)、血尿酸(UA)、C反应蛋白(CRP)、红细胞沉降率(ESR)、白细胞介素(IL)-1β、IL-6、肿瘤坏死因子-α(TNF-α)水平。
1.7.4 超声声像图
由上海中医药大学附属第七人民医院超声科采用Siemens Acuson Oxana 2型彩色多普勒超声诊断仪,于治疗前后清晨检测2组患者双肘及双膝、双踝及双足第1跖趾关节,记录超声声像图双轨征、痛风石、骨侵蚀、积液、滑膜增生、最大痛风石直径及软骨厚度。
1.7.5 不良反应及安全性
观察并记录2组治疗期间不良反应,检测2组血常规、尿常规、肝功能、肾功能。
1.7.6 随访
主要采用门诊、住院及电话随访,直至入组治疗后1周,观察截止日期2020年10月1日(首例入组2019年12月15日,末位入组2020年9月22日),后续随访3个月至2020年12月31日,记录再次因痛风性关节急性发作入院患者情况。
1.8 疗效标准
参照《中药新药临床研究指导原则(试行)》[6]评价临床疗效。治愈:症状消失或基本消失,临床体征评分降低率≥95%,生化指标正常;显效:症状明显改善或消失1项,60%≤临床体征评分降低率<95%,生化指标基本恢复正常;有效:症状有所好转,30%≤临床体征评分降低率<60%,生化指标明显好转;无效:症状缓解不明显或无缓解,甚或加重,临床体征评分降低率<30%,生化指标未见改变或加重。总有效率(%)=(治愈例数+显效例数+有效例数)÷总例数×100%。
1.9 统计学方法
采用SPSS20.0统计软件进行分析。计量资料以±s表示,采用t检验;计数资料采用卡方检验。P<0.05表示差异有统计学意义。
2 结果
2.1 2组治疗前后临床体征评分及视觉模拟评分法评分比较
与本组治疗前比较,2组治疗后临床体征评分及VAS评分明显降低(P<0.05);2组治疗后比较,治疗组临床体征评分及VAS评分明显低于对照组(P<0.05)。见表1。
表1 2组急性痛风性关节炎患者临床体征评分及VAS评分比较(±s,分)
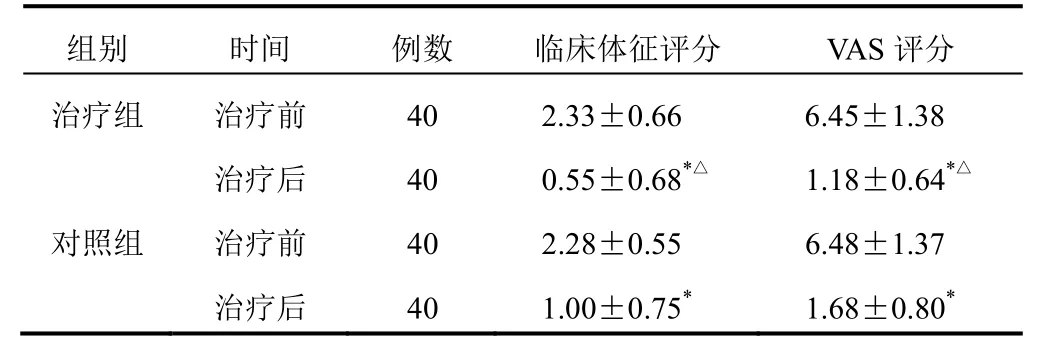
表1 2组急性痛风性关节炎患者临床体征评分及VAS评分比较(±s,分)
注:与本组治疗前比较,*P<0.05;与对照组治疗后比较,△P<0.05
组别 时间 例数 临床体征评分 VAS评分 治疗组 治疗前 40 2.33±0.66 6.45±1.38 治疗后 40 0.55±0.68*△ 1.18±0.64*△ 对照组 治疗前 40 2.28±0.55 6.48±1.37 治疗后 40 1.00±0.75* 1.68±0.80*
2.2 2组治疗前后白细胞计数、血尿酸、C反应蛋白、红细胞沉降率比较
与本组治疗前比较,2组治疗后WBC、UA、CRP、ESR水平明显降低(P<0.05);2组治疗后比较,治疗组上述实验室指标明显低于对照组(P<0.05)。见表2。
表2 2组急性痛风性关节炎患者治疗前后WBC、UA、CRP、ESR水平比较(±s)

表2 2组急性痛风性关节炎患者治疗前后WBC、UA、CRP、ESR水平比较(±s)
注:与本组治疗前比较,*P<0.05;与对照组治疗后比较,△P<0.05
组别 时间 例数 WBC(×109/L) UA/(μmol/L) CRP/(mg/L) ESR/(mm/h) 治疗组 治疗前 40 14.71±2.59 488.90±60.28 40.44±10.07 30.73±5.13 治疗后 40 6.93±1.29*△ 334.50±25.14*△ 7.19± 1.25*△ 12.28±3.45*△ 对照组 治疗前 40 14.92±2.61 486.09±48.79 39.76± 9.83 30.55±4.58 治疗后 40 7.88±1.20* 397.08±27.10* 8.02± 1.04* 13.95±3.69*
2.3 2组治疗前后炎症因子水平比较
与本组治疗前比较,2组治疗后IL-1β、IL-6、TNF-α水平明显降低(P<0.05);2组治疗后比较,治疗组上述炎症因子水平明显低于对照组(P<0.05)。见表3。
表3 2组急性痛风性关节炎患者治疗前后炎症因子水平比较(±s,pg/mL)

表3 2组急性痛风性关节炎患者治疗前后炎症因子水平比较(±s,pg/mL)
注:与本组治疗前比较,*P<0.05;与对照组治疗后比较,△P<0.05
组别 时间 例数 IL-1β IL-6 TNF-α 治疗组 治疗前 40 20.34±1.13 15.42±2.58 4.51±0.73 治疗后 40 9.25±0.98*△ 5.11±1.10*△ 2.06±0.32*△对照组 治疗前 40 20.19±1.04 15.78±2.26 4.60±0.51 治疗后 40 11.33±0.69* 8.53±1.21* 3.28±0.39*
2.4 2组治疗前后超声声像图比较
与本组治疗前比较,治疗组积液、滑膜增生明显改善(P<0.05),见表4。2组治疗前后最大痛风石直径比较差异无统计学意义(P>0.05),治疗组治疗后软骨厚度变薄明显减轻(P<0.05),见表5。

表4 2组急性痛风性关节炎患者治疗前后超声声像图比较(例)
表5 2组急性痛风性关节炎患者最大痛风石直径及软骨厚度 治疗前后比较(±s,mm)

表5 2组急性痛风性关节炎患者最大痛风石直径及软骨厚度 治疗前后比较(±s,mm)
注:与对照组治疗后比较,△P<0.05
组别 例数 最大痛风石直径 软骨厚度 治疗前 治疗后 治疗前 治疗后 治疗组 40 8.12±4.15 8.10±3.70 2.20±0.37 2.17±0.28△对照组 40 7.95±5.24 7.92±5.13 2.19±0.35 2.10±0.22
2.5 2组临床疗效比较
治疗组总有效率为95.0%(38/40),对照组为87.5%(35/40),治疗组临床疗效优于对照组(P<0.05),见表6。

表6 2组急性痛风性关节炎患者临床疗效比较(例)
2.6 2组不良反应比较
对照组出现恶心、食欲不振等胃肠道反应2例,服用质子泵抑制剂后改善,治疗组未见明显不良反应,2组均无因不良反应放弃治疗,无脱落。2组治疗前后肝功能、肾功能、血常规、尿常规未见明显异常。治疗组不良反应低于对照组(P<0.05)。
2.7 2组随访情况比较
随访3个月,治疗组最长缓解时间为6 d,对照组最长缓解时间为11 d。3个月内对照组再次出现痛风急性发作1例。
3 讨论
痛风性关节炎的发病与环境、饮食、代谢紊乱、遗传等因素密切相关。由于近年来生活水平提高,海产品、肉类、酒等高嘌呤饮食的摄入增加,以及运动减少、作息不规律、肥胖等导致代谢异常的因素增多,痛风性关节炎发病率逐年上升,且有年轻化趋势[7]。
急性痛风性关节炎属中医学“痹证”范畴,主要病机为脾肾失调,痰浊内聚,又外感风寒湿热之邪、劳倦过度、七情所伤,或饮食不节,或关节外伤等,加重并促使痰浊流注关节、肌肉、骨骼,气血不畅而致病。中医治疗痛风采用中药汤剂、外敷、针灸、熏洗等,其中药物外敷因不良反应小,患者适应性好,有广泛临床基础[8]。中药外敷存在药物透皮吸收机理及神经-内分泌-免疫网络机理,中药外用通过局部微作用、微刺激、微吸收,即“三微调平衡”[9],调整神经-内分泌-免疫网络紊乱,外敷后游离的药物与皮肤角蛋白发生结合或吸附,有促进炎症吸收、改善微循环等维护机体稳态的作用。
二黄膏以大黄、栀子为君,大黄泻火通便、破积行瘀,栀子凉血解毒、清热利湿,两者联合有清热解毒、消肿止痛的作用;芒硝助君药清热解毒、消肿散结为臣;红花活血化瘀为佐;丁香、肉桂性温,既助活血消肿,更助局部外敷药物的透散之力,是为佐使。大黄酸是大黄的有效化学成分之一,大黄酸通过抑制靶向蛋白P38、PI3Kγ、JAK2,进而阻碍炎症信号传递,影响下游蛋白表达,发挥抗炎作用[10]。栀子主要成分栀子苷通过使A549细胞中黄嘌呤氧化酶的活性下降,从而降低尿酸水平[11]。研究表明,含有栀子的中药组方外敷痛风患部,可有效改善局部红肿热痛[12]。芒硝外敷可加快淋巴循环,增强网状内皮细胞吞噬功能,减少局部白细胞浸润,减轻炎性反应[13]。热板实验显示,丁香的甲醇提取物在200 mg/kg给药剂量时具有较好的镇痛作用,并在给药后45 min药效达到高峰[14]。桂皮醛可通过调控固有免疫应答进程进而抑制滑膜炎性反应[15]。红花具有较好的抗炎作用,对于致炎物质组织胺引起的毛细血管通透性增高有明显抑制作用[16]。
本研究显示,二黄膏外敷能快速有效地缓解痛风性关节炎红肿热痛,降低UA、WBC、CRP、ESR,总有效率优于对照组,且不良反应少,与相关研究[17-18]结果相符。炎性因子与急性痛风性关节炎发生、发展密切相关,血清及关节液IL-1β、IL-6、TNF-α在急性痛风性关节炎中明显升高[19-21]。故推测二黄膏治疗急性痛风性关节炎可能与介导炎症因子下调有关。
本研究依据2015年类风湿关节炎临床试验结果测量组(OMERACT)超声痛风组发布的痛风患者基本病变的国际共识[22],分析2组治疗前后局部超声声像图特征,发现治疗前2组均有双轨征、痛风石、骨侵蚀、积液及滑膜增生表现。在西医常规治疗基础上,联合二黄膏外敷能明显改善关节局部积液及滑膜增生,减轻软骨厚度变薄的程度,表明二黄膏可通过减轻局部积液,减轻尿酸结晶对软骨的破坏,从而改善急性痛风性关节炎红肿热痛。有研究显示,痛风石与关节骨质破坏密切相关[23]。本研究暂未发现对痛风石的改变,考虑可能与观察周期短有关。
综上所述,在西医常规治疗基础上联合二黄膏外敷,可明显改善急性痛风性关节炎患者临床症状和炎症性指标,减轻关节积液、滑膜增生。结合炎症因子及超声声像图,考虑二黄膏可能通过抑制炎症因子以减轻局部积液,减轻尿酸结晶对软骨的破坏,从而改善急性痛风性关节炎红肿热痛。但本研究观察周期短,还需进一步观察远期效应,探讨其分子机制。

