基于气相色谱的饮用水中挥发性有机物测定方法
王 文
(河南省豫北水利勘测设计院有限公司,河南 安阳 455000)
在我国各领域不断发展与进步的同时,因各种原因导致部分有机溶剂、化合物、工业废水等没有得到有效的处理便进行了定点排放,而这一行为也造成了目前挥发性有机物在我国饮用水以及地表水中普遍存在的问题[1]。挥发性有机物往往具有浓度低、危害性强的特点,其中具有代表性的挥发性有机物如苯系物、卤代烃等,它们不仅具有挥发性的特点,而且能够麻痹人体的中枢神经,因此,需要研究能够有效测定这些挥发性有机物的方法[2]。而在环境不断恶化,水中有机物逐渐增多的背景下,现有方法无法满足准确检测水中挥发性有机物的需求,因此,本文提出一种基于气相色谱的饮用水中挥发性有机物的测定方法。
1 材料与方法
1.1 材料与仪器
1.1.1 实验样本试剂 为保证测定的准确性,本文需要提前准备以下试剂标准品:二氯甲烷、苯、甲苯、1,2-二氯乙烷、乙苯、对二甲苯、间二甲苯、氯苯、苯乙烯、氯乙烯、四氯乙烯溴苯、丙苯、1,1,2-三氯乙烷。
1.1.2 实验仪器 本文所研究的测定方法集合了吹扫捕集与顶空挥发两种富集方式,因此,需要Agilent G1888B型顶空自动进样系统装置,Vocarb300捕集井与Tekmar-8800吹扫捕集装置等,而对饮用水中挥发性有机物的测定则应用了配备挥发性有机物识别器的Agilent 5976B型气相色谱质谱仪器来进行测定。
1.2 测定方法的确定
目前,常见的测定方法通常先运用固相萃取法、吹扫富集法、顶空挥发法等对饮用水中的挥发性有机物进行富集,再通过气相色谱仪等对这些有机物进行测定[3]。而本文则采取吹扫富集与顶空挥发联合使用的方式对饮用水中的挥发性有机物进行富集,并采用气相色谱质谱联用的方法对饮用水中的挥发性有机物进行测定,该测定方法是目前最为高效、精确和灵敏的一种测定手段,它不但可以直接对挥发性有机物进行相关测定,还可以提供相关挥发性有机物的结构信息与预估量,为饮用水中挥发性有机物的定性和定量处理打下了基础[4]。
1.2.1 基于气相色谱的饮用水中挥发性有机物的提取 针对饮用水中的挥发性有机物提取,首先,应用吹扫捕集装置与Agilent G1888B型顶空自动进样系统装置提取饮用水样本,然后,将饮用水样本置于0.4μm的滤膜中进行过滤[5-7]。本文所应用的Tekmar-8800吹扫捕集装置平面结构图见图1。
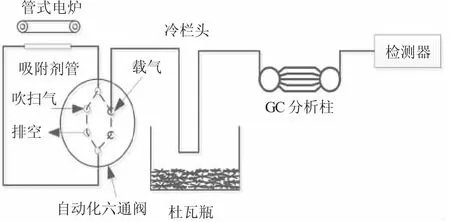
图1 Tekmar-8800吹扫捕集装置平面结构图Fig.1 Tekmar-8800 purge and trap device plan structure diagram
该装置是目前较为先进化的全自动吹扫捕集装置,应用该装置可以提高对饮用水中挥发性有机物的整体提取效率,而本文所应用的Agilent G1888B型顶空自动进样系统装置的核心平面结构则见图2。
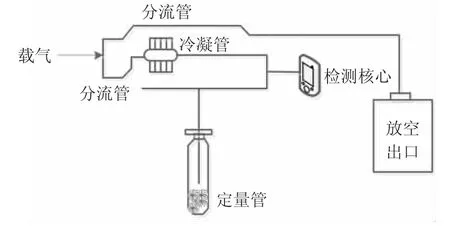
图2 AgilentG1888B型顶空自动进样系统装置核心平面结构图Fig.2 Core structure diagram of Agilent G1888B type headspace automatic sampling system device
与本文选取吹扫捕集装置的理念相同,本文所选取的Agilent G1888B型顶空自动进样系统装置也是当前较为先进的全自动进样装置,它与本文所选取吹扫捕集装置都具有自动化、高效率、高精度的特点。
本文对滤膜网的选取并没有选用目前较为常见的传统滤膜网,而是对它的结构进行了重新的设计,传统的滤膜网只有一层结构,而本文应用的滤膜网分为3层,每一层滤膜网的组装结构都有所不同,分别为活性炭膜、活性棉膜和生物膜[8]。该滤膜的结构图见图3。
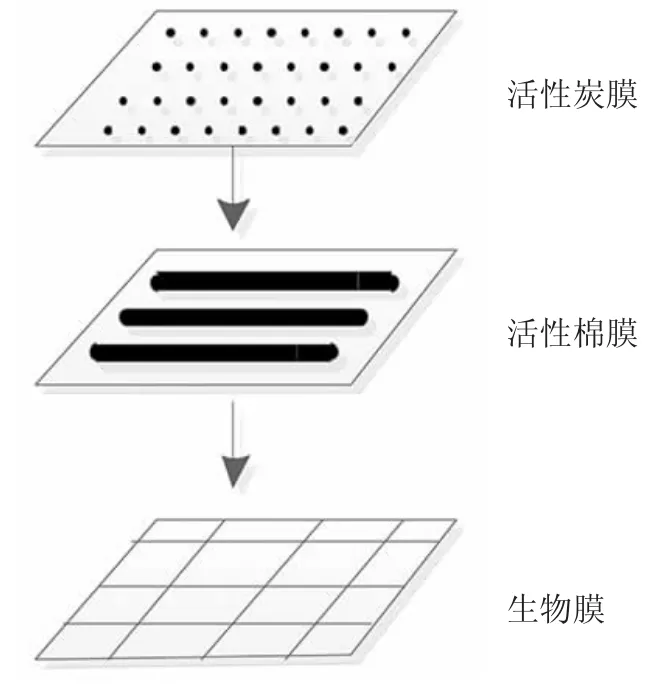
图3 滤膜网结构Fig.3 Filter net structure
该滤膜网中的活性炭膜与活性棉膜会对饮用水中的杂质进行充分过滤,同时,不会对饮用水中的有机物造成破坏,而生物膜作为当前最新的应用设计,可以将饮用水中的无害物质进行保留,将饮用水中的挥发性有机物进行最大程度的过滤,降低了后续操作的难度[9]。表1为过膜前后饮用水中有机物过滤效果对比结果。
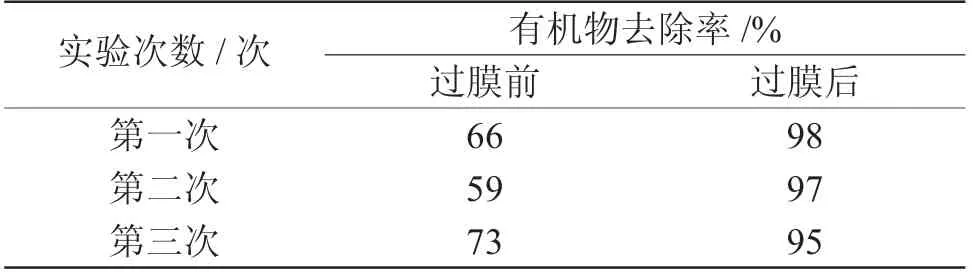
表1 过膜前后饮用水中有机物过滤效果Tab.1 Filtration effect of organic matter in drinking water before and after membrane filtration
分析表1中数据可知,采用本文设计的滤膜网对饮用水中的有机物进行过滤后,有机物的去除率得到了明显提高,说明该滤膜网的过滤效果较好。
将过滤后的液体振荡均匀后分别装入样本瓶A和样本瓶B中,在此步骤中,为了防止液体溢出,影响回收率,采用振荡器对液体进行混匀,将液体倒入容器内,液体容量占容器的1/3,将振荡器置于工作台上即可实现对液体的均匀振荡,达到防止液体溢出的目的。应用Tekmar-8800吹扫捕集装置先将振荡均匀的样本的初始温度调至45℃,保持10min后,以5℃·min-1的速率对样本中的液体进行升温,直到温度达到100℃。升温至100℃后对样本瓶中的液体进行吹扫处理,处理时间为10min,吹扫处理后,以10℃·min-1的速率进行降温,降温到60℃后进行解吸,用时为5min,最后用浓度99.99%的H2以2mL·min-1的速率进行载气分流,分流比为100∶1,进而完成样本A的提取[10]。
将第二瓶样本放入到Vocarb300捕集井当中,应用Agilent G1888B型顶空自动进样系统装置先将样本温度的初始温度调为50℃,之后以15℃·min-1的速率对样本中的液体进行升温,直到温度达到100℃,当温度达到后,用浓度99.99%的N2与90%的H2以1mL·min-1的速率对其进行载气分流,分流比为1∶1,再将处理后的样本降温到60℃,施以80kPa的压力维持10min,进而完成第二样本的提取,进而完成样本B的提取[11]。
在将过滤后的样本液体分为相同的两组后分别进行提取的这一过程中,饮用水中的挥发性有机物可能因为振荡波动较大而造成结构发生改变,因此,本文分别对A组与B组的振荡频率进行了整体实时检测,检测结果见图4。
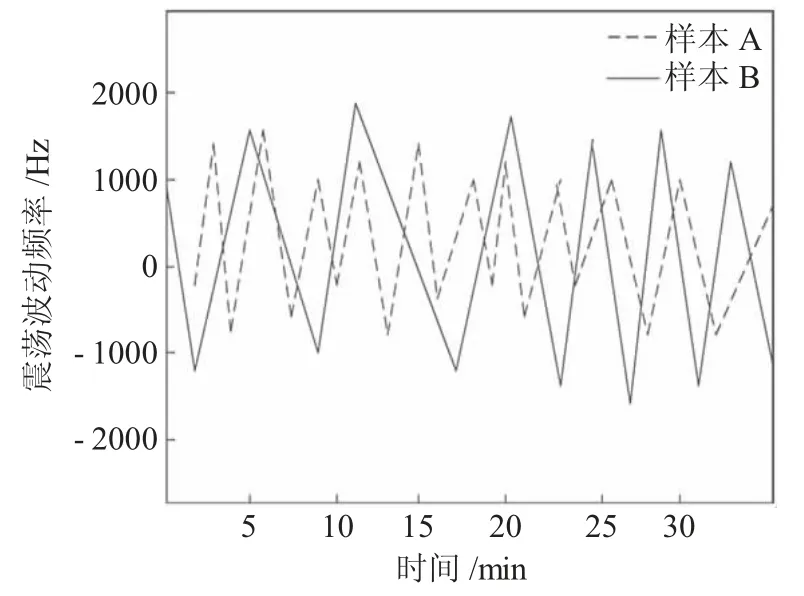
图4 挥发性有机物整体振荡频率检测图Fig.4 Detection diagram of the overall oscillation frequency of volatile organic compounds
分析图4可知,不论是样本A还是样本B中挥发性有机物的整体振荡频率均不高于2000Hz,说明挥发性有机物的结构不易发生改变,因此,本文设计的方法对饮用水中挥发性有机物进行提取是可行的[12]。
1.2.2 基于气相色谱的饮用水中挥发性有机物的测定 饮用水中的有机物普遍以化合物的形式存在,首先对样本A中的挥发性有机物进行测定,然后应用气质联用仪对水中的挥发性有机物进行定性定量检测,得到样本A中挥发性有机物的浓度值见表2。
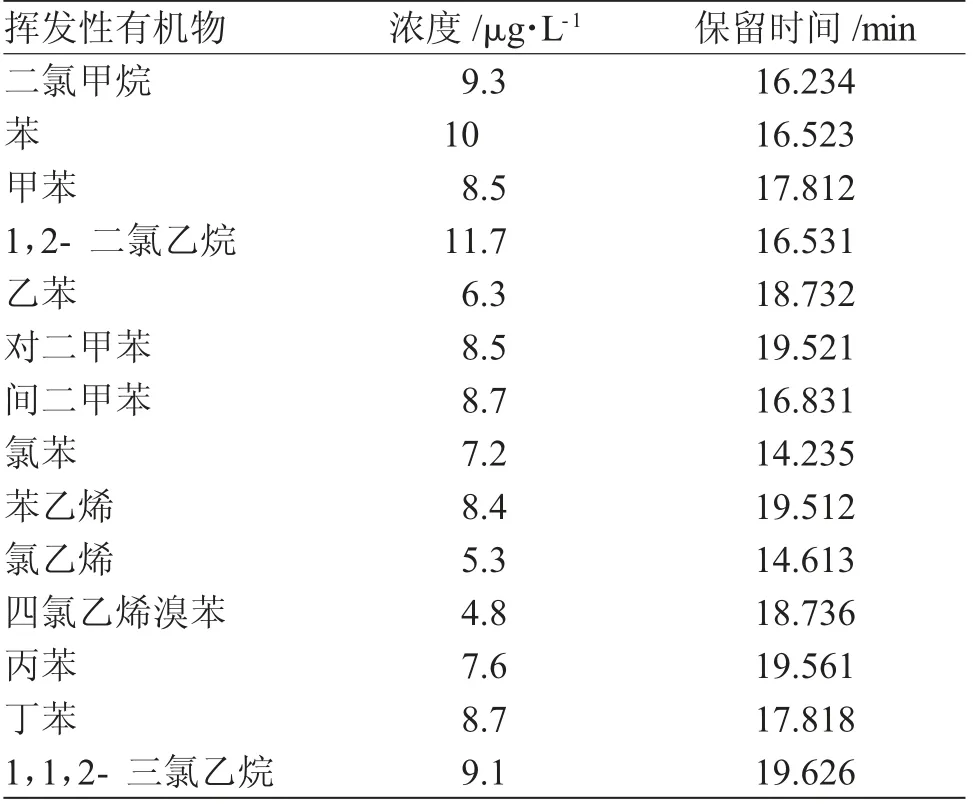
表2 样本A中挥发性有机物的浓度值Tab.2 Concentration value of volatile organic compounds in sample A
表2中数据,为通过配备挥发性有机物识别器的Agilent5976B型气相色谱质谱仪器来对样本A中的挥发性有机物进行测定,得到的14种饮用水挥发性有机物的测定数据,通过公式(1)来进行计算:

式中 n:表2中各种挥发性有机物的浓度;t:相对应的挥发性有机物所保留的时间,将表2中计算所得到的结果归纳为数据组A,数据组A中包含了14个小数据组即(a1,a2,a3……a14),得到数据组A后,完成对样本A的测定[13,14]。
在对样本B进行测定时,首先需要对样本B进行冷却,使其重新变为液态,将液态样本加入到15mL的顶空瓶当中进行振荡,再将2.3g的NaCl与8mL的纯净水(玻璃瓶采集获得)加入其中进行搅拌,待生成物完全静止后,通过配备挥发性有机物识别器的Agilent 5976B型气相色谱质谱仪器对样本B中的挥发性有机物进行测定,得到样本B中挥发性有机物的浓度所占比例见表3。
表3中数据,为本文通过配备挥发性有机物识别器的Agilent 5976B型气相色谱质谱仪器来对样本B中的挥发性有机物进行测定得到的14种饮用水挥发性有机物的测定数据,通过公式(2)来进行计算:
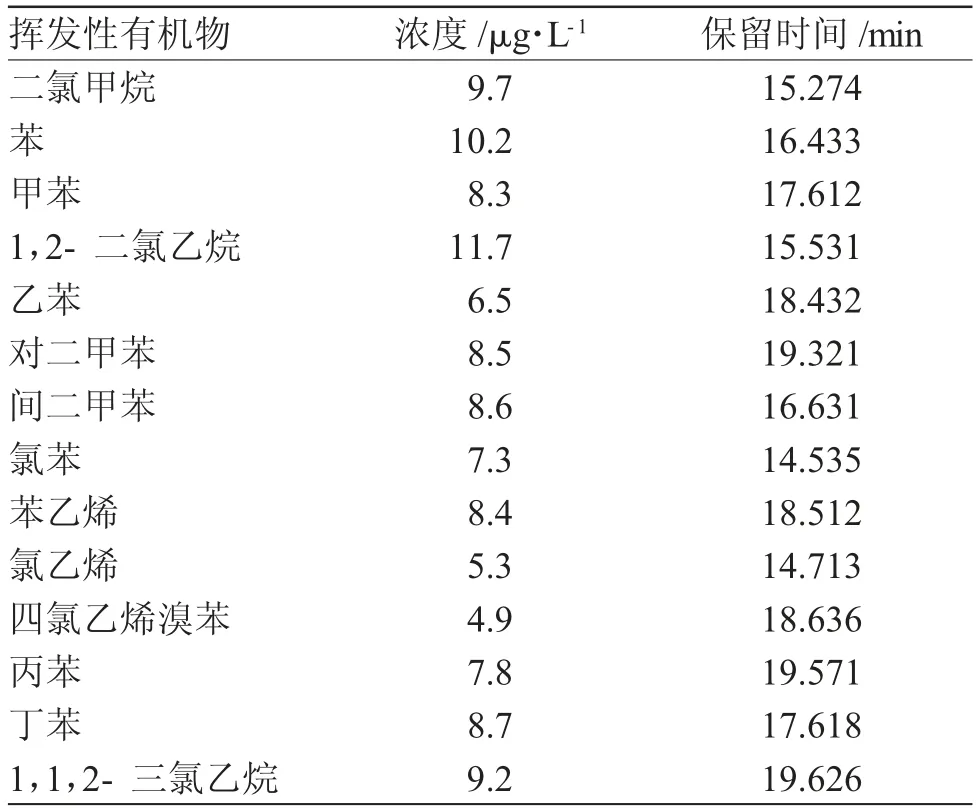
表3 样本B中挥发性有机物的浓度所占比例Tab.3 Proportion of concentration of volatile organic compounds in sample B

式中 C:NaCl的反应量。将计算所得到的结果归纳为数据组B,数据组B中包含了14个小数据组即(b1,b2,b3……b14)[15]。通过公式(3)对数据组A与数据组B进行计算:

通过上述分析,得出了14种饮用水挥发性有机物的测定数据。
2 结果与分析
2.1 获取气相色谱图
根据1.2节中的公式计算结果,得到样本A与样本B的整合测定气相色谱图见图5。
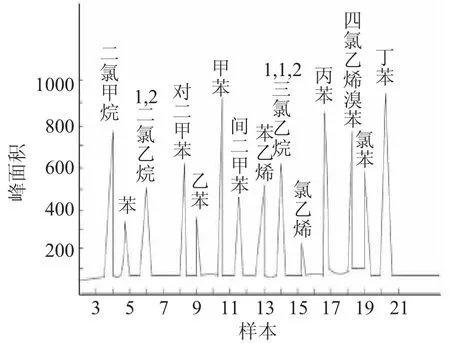
图5 样本A与样本B的整合测定气相色谱图Fig.5 Gas chromatogram of the integrated determination of sample A and sample B
2.2 标准曲线线性对比
对14种挥发性有机物进行测定,并对不同的方法进行线性回归处理,得出线性回归相关系数R的取值,结果见表4。其中,R值越接近1,表明相关性越高。
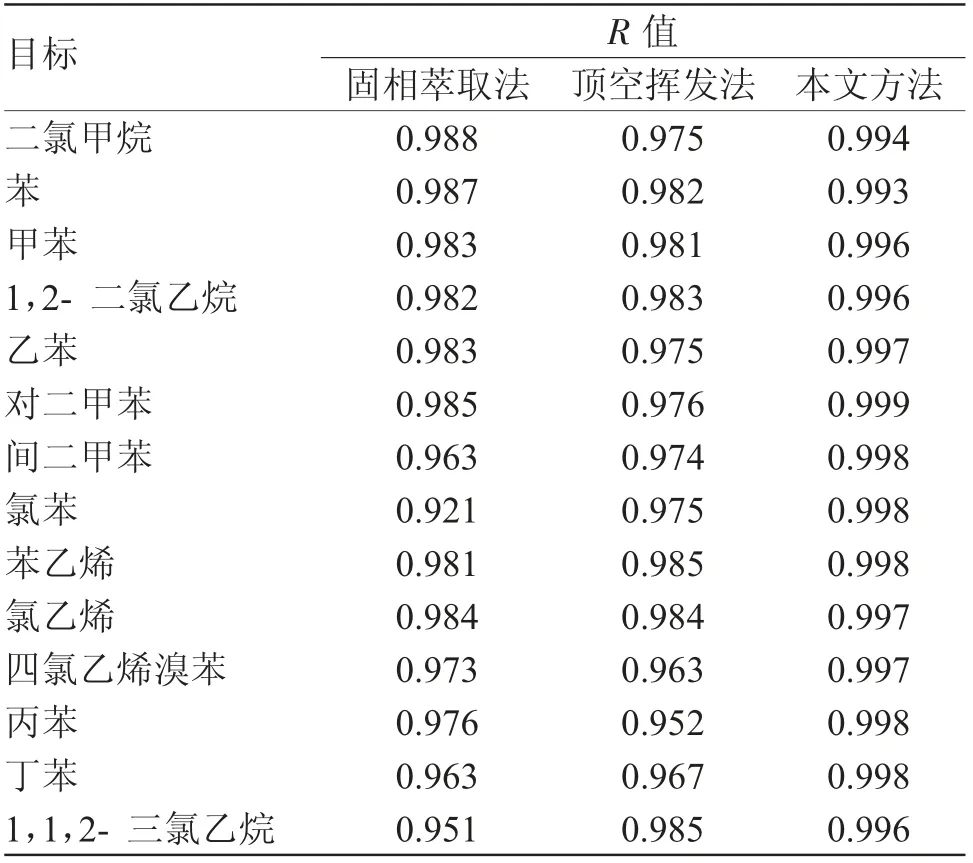
表4 不同方法的R值比较结果Tab.4 Comparison results of R values of different methods
由表4可知,本文方法的R值取值范围在0.993~0.999之间,整体水平高于固相萃取法和顶空挥发法,说明本文方法得出的测定结果与标准曲线相关性更高。
2.3 应用效果分析
为了验证本文方法的应用性,将本文研究的基于气相色谱的饮用水中挥发性有机物测定方法与传统固相萃取法和顶空挥发法的测定效果进行对比,首先将测定对象分为14组进行测定,得到不同测定方法的测定精确率对比结果见图6。
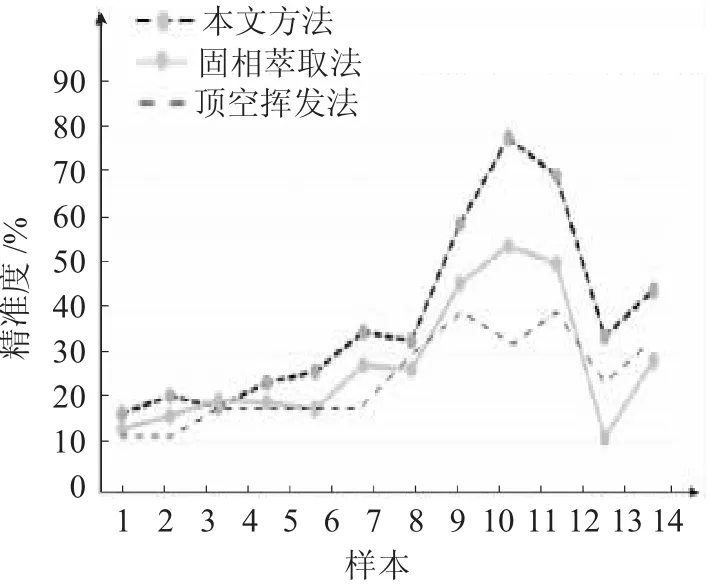
图6 测定精确率对比图(14组)Fig.6 Comparison chart of determination accuracy(14 groups)
由图6可知,在对14组测定对象进行测定的过程中,本文研究的基于气相色谱的饮用水中挥发性有机物测定方法的测定结果精确率较高,而传统固相萃取法和顶空挥发法测定精确率较低,但由于测定对象较少,因此,该对比结果可能存在局部差异的可能性,为了增强应用效果的说服力,本文增加了测定对象数量达到280组,得到了测定精确率对比图见图7。
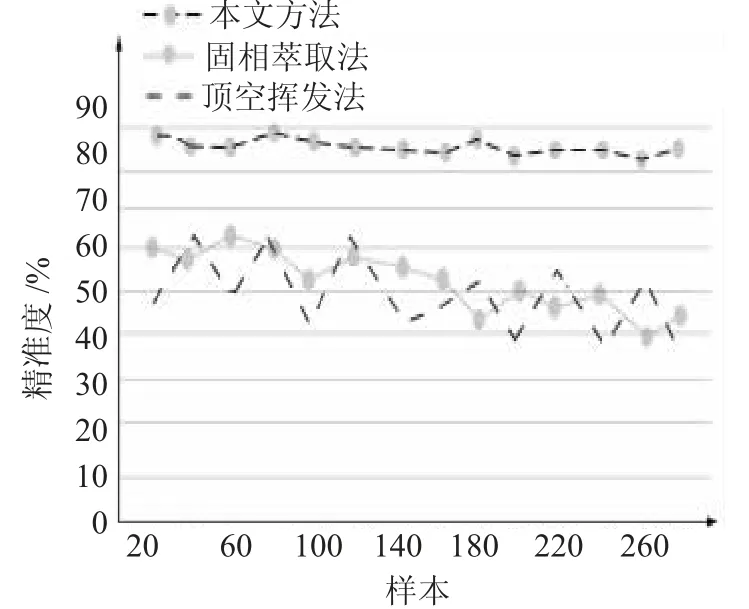
图7 测定精确率对比图(280组)Fig.7 Comparison chart of determination accuracy(280 groups)
由图7可以看出,在测定对象数量增加的情况下,本文所研究的测定方法测定的精确率仍然高于传统固相萃取法和顶空挥发法,产生测定精确率差异明显的主要原因是,本文测定方法采用技术相对成熟的挥发性有机物富集法,该方法不仅可以减少有机物挥发,而且能够最大限度的保证测定饮用水中的有机物含量不会缺失。此外,本文研究的测定方法所采用的测定试剂均为无污染试剂,且试剂本身不含挥发性有机物成分,不会对测定结果造成干扰。而传统的测定方法在测定过程中,由于采用的富集法不够成熟,造成挥发性有机物的大量挥发,使得检测结果不够精确,因而产生测定误差。
综上,由于本文测定方法采用的滤膜网具有多重过滤性,可以对饮用水中的物质进行过滤,排除其他杂质,有效地提取饮用水中挥发性有机物,从而提升测定结果的精准性。
3 结语
本文研究的基于气相色谱的饮用水中挥发性有机物测定方法摒弃了传统测定方法的单一性,将吹扫富集法与顶空挥发法进行充分结合,使用的同时达到了彼此相互验证与监督的目的,使得最终得到的测定数据更加准确。对于未来饮用水中挥发性有机物的测定来说,需要测定的数据只会越来越多,得到准确数据的过程只会越来越困难,因此,在充分利用当前测定方法的同时还需要不断地创新与进步,为保障未来饮用水的安全不断贡献力量。

