他达拉非纳米晶体干混悬剂的制备与质量评价
李 永,蔡文婷
(1.武汉市红十字会医院药剂科,武汉 430015;2.武汉市红十字会医院老年病科,武汉 430015)
他达拉非是一种环状鸟苷单磷酸(cGMP)特异性5型磷酸二酯酶(PDE5)抑制剂,主治男性勃起功能障碍[1],该药为生物药剂学分类系统(BCS)中的Ⅳ型,极低的溶解度(约为2 μg·mL-1)以及较差的生物膜渗透性严重影响了药物口服生物利用度[2-3]。他达拉非片(希爱力®)通过微粉化技术减小原料药的粒径,并在处方中加入十二烷基硫酸钠(SDS)提高药物的溶解度和生物利用度[4]。SDS被认为是一种有毒物质,能够引起皮肤和黏膜刺激性[5]。因此,本研究将他达拉非制备成纳米晶体干混悬剂,以提高药物的溶出度及生物利用度,为他达拉非的临床应用提供参考。
1 仪器与试药
1.1仪器 F-P2000E型高能全方位行星式球磨仪(湖南弗卡斯实验仪器有限公司);Malvern Zetasizer动态激光粒度测定仪(英国Malvern公司);FEI Nova 400型场发射扫描电子显微镜(美国FEI公司);安捷伦1100高效液相色谱仪(安捷伦科技有限公司);RC810型药物溶出试验仪(宁波新芝生物科技股份有限公司);B-290型实验室小型喷雾干燥机(瑞士Buchi公司)。
1.2试药 他达拉非原料药(常州制药厂有限公司,批号20190216);聚维酮K30(PVP K30,巴斯夫中国有限公司);山梨醇和黄原胶,均购于湖北葛店人福药用辅料有限责任公司;甘露醇(石家庄华旭药业有限责任公司);蔗糖(江西汉江药业有限公司);乳糖(江苏道宁药业有限公司);微晶纤维素、羧甲基纤维素钠(CMC-Na)和羟丙甲基纤维素(HPMC)均购于安徽山河药用辅料股份有限公司;十二烷基硫酸钠(SDS,国药集团化学试剂有限公司);吐温80(南京威尔药业股份有限公司);盐酸(湖南尔康制药股份有限公司);醋酸(南京化学试剂股份有限公司);磷酸二氢钾(湖南九典制药股份有限公司);pH4.5醋酸缓冲液和pH6.8磷酸盐(PBS)缓冲液,均为实验自制;水为实验室自制纯化水。
2 方法与结果
2.1他达拉非平衡溶解度的测定 考察他达拉非原料药在不同介质中的平衡溶解度[6]。取多只具塞试管,分别加入纯化水、pH值1.2盐酸溶液、pH值4.5醋酸缓冲液、pH值6.8 PBS以及含有不同浓度的SDS的对应溶液,再加入足量的他达拉非原料药,水浴超声使原料药充分分散,置于恒温振荡器中,在37 ℃水浴中持续振荡72 h,取出药物悬浊液,离心,取上清液,经0.45 μm微孔滤膜过滤,经适当稀释,检测药物含量,计算平衡溶解度,结果见表1。
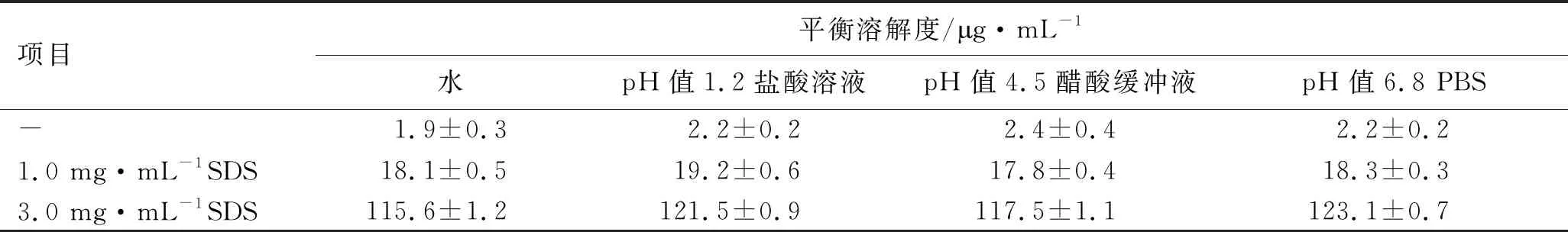
表1 他达拉非在不同介质中的平衡溶解度 (n=3,37 ℃)
由表1可知,他达拉非在不同pH溶液中的平衡溶解度均较低,约为2 μg·mL-1,溶解度不具有pH值依赖性;溶液中加入SDS后可提高药物溶解度,且随着表面活性剂的增加溶解度显著增大。
2.2他达拉非纳米晶体的制备 采用介质研磨法制备他达拉非纳米晶体[7-8],配制含有质量浓度为10 mg·mL-1PVP K30和质量浓度为1 mg·mL-1吐温80的混合溶液,取经气流粉碎的他达拉非原料药10 g[粒径分布为D90(表示“累计粒度分布数达到90%时所对应的粒径”)为10.4 μm,D50(表示“累计粒度分布数达到50%时所对应的粒径”)为5.3 μm,D10(表示“累计粒度分布数达到10%时所对应的粒径”)为1.0 μm]分散到200 mL上述混合溶液中,加入载有直径为0.6 mm氧化锆球珠的介质研磨机中进行研磨,研磨速度为500 r·min-1,温度为15~20 ℃,在不同时间点取样测定粒径分布及多聚分散系数(PDI),结果见表2。

表2 不同时间点粒径分布及PDI (n=3)
研磨时间对减小他达拉非纳米晶体粒径极其重要,研磨时间太短,难以获得粒径细小且均匀的纳米晶体,研磨时间过长,不仅不能再继续减小纳米晶体粒径,还可能导致粒径分布不均匀[9],因此在研磨过程中要监控粒径及PDI,确定最佳的研磨时间。由表2可知,随着研磨时间的延长,他达拉非纳米晶体的粒径逐渐减小,在研磨开始阶段粒径减小较为明显,研磨2 h后粒径由最初的5.3 μm减小至(857.4±25.7) nm,而研磨时间延长至4 h时粒径减小至(726.8±24.8) nm,PDI为0.197±0.008,继续研磨至6 h,粒径不再减小,而PDI为0.241±0.010,呈现增加趋势。因此,确定他达拉非纳米晶体的研磨时间为4 h。
2.3他达拉非纳米晶体的固化 取他达拉非纳米晶体溶液100 mL,加入甘露醇20 g,搅拌溶解,在喷雾干燥过程中纳米晶体溶液需持续搅拌,避免沉降,喷雾干燥工艺参数如下:进气温度为120 ℃,出气温度为68~70 ℃,进气量为0.1 m3·min-1,进料流速为3 mL·min-1。收集喷雾干燥得到的他达拉非纳米晶体粉末,密闭保存。取他达拉非纳米晶体粉末加水复溶后,测定喷雾干燥前后纳米晶体的性质。见表3。
由表3可知,他达拉非纳米晶体在喷雾干燥前粒径为(732.5±32.1) nm,复溶后粒径为(779.4±26.7) nm,略有增大,可能是由于在喷雾干燥过程中导致部分纳米晶体发生了聚集,形成较大的粒子所致;而喷雾干燥前PDI为0.197±0.009,复溶后的PDI为0.219±0.011,二者较为接近;复溶后纳米晶体的Zeta电位为(-19.2±0.8) mV,与喷雾干燥前的(-18.2±0.9) mV相近。他达拉非纳米晶体经喷雾干燥固化成颗粒状粉末,能够保持其粒径大小、PDI以及Zeta电位与喷雾干燥之前性质基本不变。

表3 他达拉非纳米晶体性质检测结果 (n=3)
2.4他达拉非纳米晶体干混悬剂的制备 取他达拉非纳米晶体粉末及其他辅料,依次过60目筛整粒,依照处方筛选设计,称取处方量的主药及辅料,采用等量递加法将主药与辅料预混,过20目筛网,混匀,即得他达拉非纳米晶体干混悬剂,称量分装至铝箔袋中,密封保存[10]。
2.5干混悬剂质量评价
2.5.1沉降体积比(F值) 取他达拉非纳米晶体干混悬剂,置于50 mL具塞量筒中,加水至50 mL,密塞,用力振摇,分散形成均匀的混悬剂,测量混悬物初始高度(H0),静置3 h后再次测量混悬物高度(H),按照公式计算F值,F=H÷H0,F值越大表示混悬剂越稳定[11]。
2.5.2分散性及再分散性 取他达拉非纳米晶体干混悬剂,置于50 mL具塞量筒中,加水至50 mL,密塞,置于温振荡器中振荡分散,频率为100次·min-1,记录分散时间,分散时间越短分散性越好;另将分散形成均匀的混悬剂静置3 d,取具塞量筒用力均匀旋转180°,计为分散1次,重复该操作直至混悬剂完全重新分散,记录所需分散次数,旋转次数越少表示再分散性越好[12]。
2.6处方筛选
2.6.1填充剂筛选 干混悬剂中需要加入填充剂以提高其流动性以及分散性等性质。分别选择山梨醇、甘露醇、蔗糖、乳糖和微晶纤维素作为填充剂(用量为40%),以黄原胶作为助悬剂(用量为25%),与他达拉非纳米晶体粉末及其他辅料(矫味剂、助流剂)混合,其他各组分用量均相同,按照2.3项下工艺制备他达拉非纳米晶体干混悬剂,以干混悬剂的流动性、分散性、F值和再分散性作为评价指标,结果见表4。
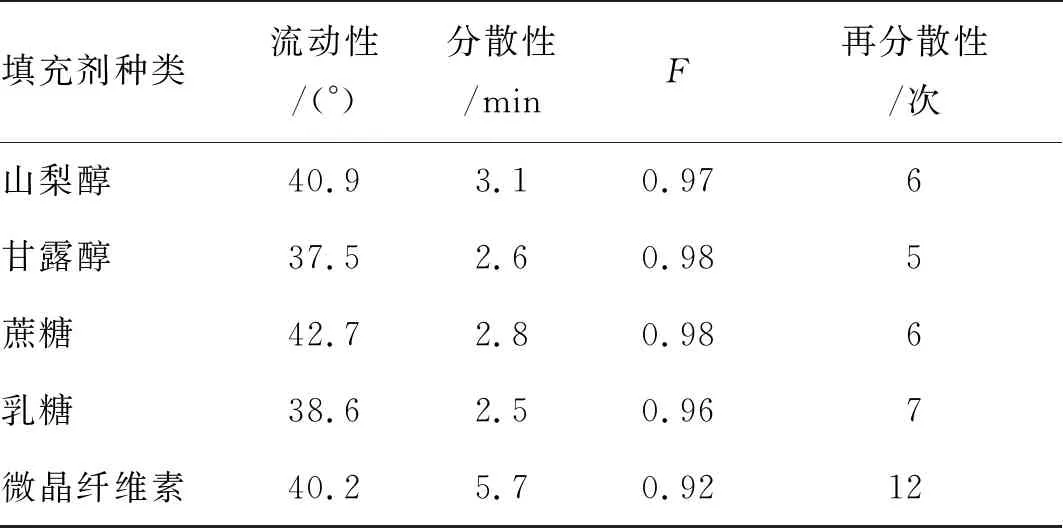
表4 填充剂筛选结果
由表4可知,以甘露醇作为填充剂制备的干混悬剂的流动性较好,易于分装,且分散时间较短,易分散,F值及再分散性均较好,因此本研究选择甘露醇作为他达拉非纳米晶体干混悬剂处方中的填充剂,用量为40%。
2.6.2助悬剂筛选 干混悬剂中加入助悬剂能够防止药物沉降,保持体系的稳定性。分别选择CMC-Na、HPMC以及黄原胶作为助悬剂(用量为25%),以甘露醇作为填充剂(用量为40%),与他达拉非纳米晶体粉末及其他辅料(矫味剂、助流剂)混合,其他各组分用量均相同,按照2.3项下工艺制备他达拉非纳米晶体干混悬剂,以干混悬剂的流动性、分散性、F值和再分散性作为评价指标,结果见表5。
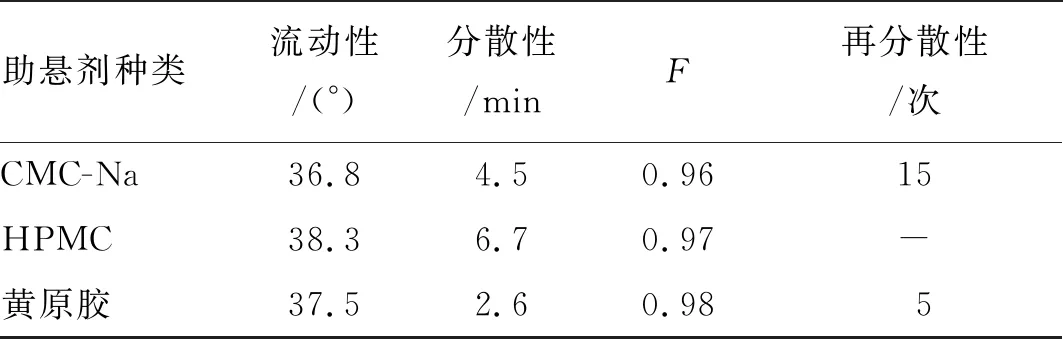
表5 助悬剂筛选结果
由表5可知,3种助悬剂均能使混悬剂放置3 d后稳定,F值均较好;以HPMC作为助悬剂的处方,混悬液放置3 d后在量筒底部可观察到有一部分药物沉淀,振摇多次无法分散,以CMC-Na作为助悬剂的处方,放置3 d后在量筒下部能观察到有少量絮凝物质出现,但经旋转量筒后絮凝物消失;使用黄原胶作为助悬剂的处方,混悬液的再分散性较好,这是由于黄原胶具有触变性,静止状态下黏度增加,能够有效避免药物出现絮凝、沉降现象。因此本研究选择黄原胶作为助悬剂,用量为25%。
2.7扫描电镜观察 通过扫描电镜观察他达拉非原料药、他达拉非纳米晶体、他达拉非纳米晶体喷雾干燥颗粒以及他达拉非纳米晶体干混悬剂的微观形态。分别取上述样品黏附至电胶布上,喷金,在扫描电镜下观察,并拍摄电镜照片,见图1。

图1 他达拉非原料药(A)、他达拉非纳米晶体(B)、他达拉非纳米晶体喷雾干燥颗粒(C)和他达拉非纳米晶体干混悬剂(D)的扫描电镜图
在扫描电镜图中可观察到他达拉非原料药呈片状或柱状(图1-A);他达拉非纳米晶体呈不规则块状(图1-B),分布较均匀,粒径大约在500~1 000 nm范围内;他达拉非纳米晶体经喷雾干燥后呈疏松粉末状,粒径分布不均匀(图1-C);他达拉非纳米晶体干混悬剂中纳米晶体颗粒均匀散落在辅料之中(图1-D)。
2.8体外溶出度比较 采用《中国药典》2015年版四部0931项下第Ⅱ法(桨法)比较自制他达拉非纳米晶体干混悬剂与市售他达拉非片(希爱力®)的体外溶出度,溶出介质为含有3.0 mg·mL-1SDS的水溶液,体积为900 mL,温度为(37±0.5) ℃,转速为(50±1) r·min-1,分别取自制他达拉非纳米晶体干混悬剂(规格:5 mg·袋-1)以及市售他达拉非片(规格:5 mg·片-1),加入溶出仪中,在设定的时间间隔吸取5 mL溶出介质(补加等温等体积空白介质),经0.45 μm微孔滤膜过滤,经适当稀释,检测药物含量,计算溶出度,绘制溶出度-时间曲线。见图2。
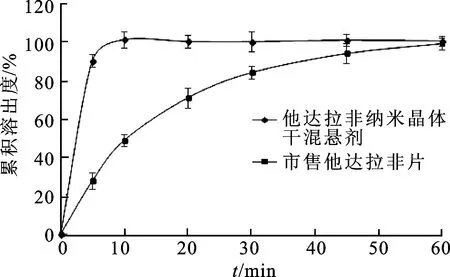
图2 他达拉非纳米晶体干混悬剂与市售他达拉非片的体外溶出曲线 (n=6)
由图2可知,他达拉非纳米晶体干混悬剂中药物溶出速度非常快,在10 min内药物可完全溶出,而市售他达拉非片溶出速度相对较慢,说明将他达拉非制备成纳米晶体后,加速了药物的溶出,虽然市售制剂中的原料药进行了微粉化处理,处方中加入了SDS,仍未达到药物快速溶出的效果。本研究制备的他达拉非纳米晶体干混悬剂体外药物溶出速度较快,有望提高药物的口服生物利用度。
3 讨论
原研制剂厂家通过在处方中加入SDS以提高他达拉非的溶解度和生物利用度,但SDS对人体具有一定的不良反应,因此,有必要开发一种既不含有阴离子表面活性剂又能提高药物口服生物利用度的给药系统[13-14]。
近年来,将难溶性药物制成纳米晶体已成为提高药物溶解度和生物利用度的有效策略[15],且可以通过喷雾干燥和冷冻干燥等固化技术来解决纳米晶体存在的不稳定性问题[16]。介质研磨法是将药物混悬液与研磨介质置于封闭的研磨腔内进行研磨,在介质研磨过程中,药物粒子之间、药物粒子与研磨介质及腔体壁之间持续发生强烈碰撞,药物粒子发生破裂、溶解和重结晶,同时稳定剂会吸附到药物粒子表面,形成稳定的药物纳米结晶体[17]。介质研磨工艺简单,粒径可控,重复性好,易于扩大生产,因此本研究采用介质研磨法制备他达拉非纳米晶体,并通过喷雾干燥将其固化成固体颗粒,以提高纳米晶体的稳定性。
纳米晶体属于热力学不稳定系统,需要加入稳定剂以防止药物粒子之间的聚集和沉降,通常在处方中加入表面活性剂和高分子物质是提高纳米晶体稳定性的有效方式,表面活性剂能够降低液-固界面张力,润湿药物粒子表面,降低粒子之间的吸附性,而高分子物质能够吸附在药物粒子表面,形成一种空间膜屏障,有效避免粒子间的相互聚集[18-20]。本研究以PVP K30和吐温80作为稳定剂制备的他达拉非纳米晶体稳定性良好,在喷雾干燥后纳米晶体性质未发生改变。

