经后腹腔入路腹腔镜肾部分切除术治疗肾癌患者的临床效果
冯洪周
(尉氏县人民医院 泌尿外科,河南 开封 475500)
肾癌为常见泌尿外科肿瘤,多发于50~70岁人群,统计显示,泌尿系统肿瘤中肾癌发生率仅低于膀胱癌,在全部实体瘤中占比为3%~4%,严重危害患者生命安全[1]。肾部分切除术为治疗早期肾癌的有效方法,可清除病灶,控制病情进展,降低病死率。但随着微创外科技术不断进步,腹腔镜下肾部分切除术可缩小切口,减轻手术创伤,促进术后恢复,逐渐取代传统开放式手术,成为现阶段治疗早期肾癌主要术式[2]。经腹入路、经后腹腔入路为腹腔镜肾部分切除术常见入路方式,但各入路优劣不一,各有不足之处[3]。本研究选取73例肾癌患者作为研究对象,探讨经后腹腔入路腹腔镜肾部分切除术治疗肾癌患者的效果。
1 资料与方法
1.1 一般资料选取2017年8月至2019年10月尉氏县人民医院收治的73例肾癌患者作为研究对象,按手术方法分为经腹组(n=36)与经后腹腔组(n=37)。经腹组男22例,女14例;年龄42~64岁,平均(53.28±5.24)岁;肿瘤部位20例右侧,16例左侧。肿瘤直径1.5~3.6 cm,平均(2.46±0.37)cm。经后腹腔组男24例,女13例;年龄43~62岁,平均(52.65±4.59)岁;肿瘤部位18例右侧,19例左侧。肿瘤直径1.6~3.4 cm,平均(2.52±0.35)cm。两组性别、年龄、肿瘤部位、肿瘤直径比较,差异均无统计学意义(P>0.05),具有可比性。本研究经尉氏县人民医院医学伦理委员会审核通过。
1.2 选取标准(1)纳入标准:①经病理学诊断确诊为肾癌,MRI、CT、B超检查无远处转移、无腔静脉及肾静脉癌栓;②符合手术指征,术前血肌酐、尿素氮正常;③自愿签署同意书。(2)排除标准:①合并心脑血管病、糖尿病、凝血功能障碍;②合并恶性肿瘤;③合并严重感染;④既往有腹腔手术史、外伤史;⑤对侧肾功能异常;⑥精神疾病。
1.3 手术方法
1.3.1经腹组 接受经腹入路腹腔镜肾部分切除术。患者取侧卧位,接受全身麻醉,脐旁行约1 cm的穿刺孔,置入气腹针,创建气腹。置入腹腔镜,分别于腋前线平脐、平髂嵴水平及腹直肌外缘肋缘下2 cm位置进行穿刺,置入5、10 mm套管针,结肠旁沟切开后,内下方游离结肠、结肠系膜,超声分离粘连,暴露肾肿瘤、肾实质,以超声刀行肾门脂肪组织钝性分离,打开血管鞘,以直角钳行肾动脉游离并以血管夹夹闭,肿瘤边缘约0.5 cm处以超声刀进行切割,止血,用2-0可吸收线缝合肾实质,恢复肾血供,降低气腹压,明确无出血后取出器械,置管引流,闭合切口。
1.3.2经后腹腔组 接受经后腹腔入路腹腔镜肾部分切除术。患者取侧卧位,接受全身麻醉,腋后线12肋缘下行约2 cm的穿刺孔,以血管钳行腰背筋膜分离,置入水囊,行腹膜间隙扩张,于腋前线平髂嵴、腋前线肋缘下2 cm、腋中线髂嵴上2 cm位置穿刺并置入套管针,分离腰大肌,切开肾脂肪囊、肾周筋膜。分离肾周脂肪、肾实质,超声分离粘连,暴露肾实质、肾肿瘤,以超声刀行肾门脂肪组织分离,打开血管鞘,游离并夹闭肾动脉,于肿瘤边缘0.5 cm位置以超声刀切割,止血,用2-0可吸收线缝合肾实质,恢复肾血供,明确无出血后放置引流管,闭合切口。
1.4 观察指标(1)手术指标。包括术中出血量、手术时间、术后进食时间、住院时间。(2)术后1、2 d疼痛程度。通过视觉模拟量表(visual analogue scale,VAS)评估,总分0~10分,分数越高,疼痛程度越严重。(3)生活质量。通过Spitzer生活质量指数(Spitzer quality of life index,SQOL)评估,总分0~10分,得分越高,生活质量越高。(4)并发症发生情况。如应激性溃疡、切口感染、肠梗阻、肋腹部神经痛等。

2 结果
2.1 手术指标两组术中出血量、手术时间比较,差异无统计学意义(P>0.05);经后腹腔组进食时间、住院时间短于经腹组,差异有统计学意义(P<0.05)。见表1。
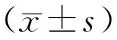
表1 两组手术指标比较
2.2 术后疼痛程度和生活质量术后1、2 d,经后腹腔组VAS评分均低于经腹组,SQOL评分均高于经腹组,差异有统计学意义(P<0.05);且术后2 d,两组VAS评分低于术后1 d,SQOL评分高于术后1 d,差异有统计学意义(P<0.05)。见表2。
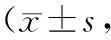
表2 术后两组VAS、SQOL评分比较分)
2.3 并发症发生情况经后腹腔组并发症发生率与经腹组比较,差异无统计学意义(P>0.05)。见表3。

表3 两组并发症发生情况比较[n(%)]
3 讨论
肾癌为一种常见的恶性肿瘤,严重损害肾功能,发生恶性转移时,严重威胁患者的生命安全。手术为治疗中早期肾癌的有效手段,有研究指出,肾癌Ⅰ、Ⅱ、Ⅲ期患者经有效手术治疗,其5 a生存率分别为92%、86%、64%[4]。因此,临床应及时选择合理手术方案,以控制患者病情,降低病死率,改善预后。
肾部分切除术为治疗肾癌的主要手段,可有效延缓肿瘤进展,延长患者生存期[5]。近年来,随着微创医学不断进步,腹腔镜技术在肾部分切除术中得到广泛应用,其可缩小手术切口,减轻手术创伤。同时,腹腔镜直视下可充分探查患者腹腔,清晰呈现肾肿瘤位置及其和周围组织的解剖关系,便于实现微创性操作[6]。经腹入路腹腔镜肾部分切除术作为目前肾癌常用治疗术式,可有效清除病灶,控制病情,具有操作范围广、可操作性强等优势,但由于其动脉分离、阻断时不直接,易误伤肠管、腹腔器官,引发腹膜炎、肠梗阻、肠麻痹等并发症,不利于术后恢复[7]。而经后腹腔入路可直接到达肾门,能较大程度避免误伤其他器官,且无需切开患者腹膜,通过腹膜后间隙扩张即可创建工作通道,能在封闭腹腔环境中实施手术,故可进一步降低手术对腹腔内环境的刺激,减轻腹腔损伤[8]。与经腹入路手术比较,经后腹腔入路进入术区难度较小、分离组织少,降低了对器官的干扰,减轻手术创伤,且由于操作环境封闭,引流物仅限于后腹腔,降低了腹腔污染概率,有助于患者术后恢复[9]。梁博等[10]研究指出,肾癌患者接受经后腹腔入路腹腔镜手术后其疾病控制率可达93.3%,且术后疼痛明显减轻。本研究结果显示,经后腹腔组住院时间、进食时间短于经腹组,术后1、2 d VAS评分低于经腹组,SQOL评分高于经腹组,说明经后腹腔入路腹腔镜肾部分切除术治疗肾癌能减轻患者术后疼痛程度,促进恢复。但是行经后腹腔入路腹腔镜肾部分切除术时需注意:肾游离时尽可能减轻腰肌表面肌膜损伤,有助于预防腰神经受损。
综上所述,后腹腔入路腹腔镜肾部分切除术可减轻肾癌患者的术后疼痛程度,缩短康复进程,提升术后生活质量,且安全性可。

