金矿非氰化浸金研究进展
彭科波,高利坤,饶 兵,龚志辉,沈海榕,高广言,何 飞,张 明
昆明理工大学国土资源工程学院,昆明 650093
金是地壳中十种最稀有元素之一[1],并且金具有十分稳定的化学性质和特殊的物理性能[2-3],在国际贸易和国防工业中发挥着重要作用,广泛应用于珠宝首饰、金融(作为交换媒介)、医学、航空航天设备和电子设备制造等领域[4],是一个国家重要的战略储备资源.据世界黄金协会数据显示,截至2020年9月底,中国官方黄金储备为1948.31 t,位列全球第7位;2019年中国黄金产量为383.2 t,约占全球总产量的11%,中国是2019年全球最大的生产国.随着科学技术的进步,对黄金的需求正在稳定增长.
目前,许多国家易处理的金矿石资源日益减少,难处理金矿石的比例增加[5].难处理金矿石是指不能使用常规氰化浸出工艺提取金或者直接采用氰化法浸金浸出率低于80%的金矿石[6-8].这类矿石工艺矿物学的特性以及难处理的原因可分为以下五类:
(1)伴生多金属复杂金矿石.在浸出时,金属元素(如:铜、铅、铁、银、锑)会与金争夺浸出剂,不仅会增加浸出剂的用量,而且也降低了金的浸出率[9].
(2)碳质金矿石.矿石中含有无定型碳、石墨和有机碳时,会在浸出时产生“劫金”作用,降低金的浸出率[10].
(3)含有大量黏土矿物的金矿石.黏土矿物具有吸附性,部分溶解的金被吸附,导致不能有效浸出金.
(4)高硫、高砷类金矿石.金以微细粒或显微形态被包裹或嵌存于毒砂、锑硫化物、黄铁矿和黄铜矿中,甚至浸染在金属硫化矿物的晶体中,通过细磨也难以解离出金.
(5)硅酸盐包裹金矿石.金以微细粒、显微或者次显微的形态被包裹于硅酸盐类脉石矿物中,以至于通过常规磨矿工艺也不能把金暴露在氰化物溶液中.
我国作为主要的黄金生产国,近年来,随着金矿资源的持续开发利用,易处理的金矿资源减少,难处理金矿成为未来开采的主要资源.其中,含砷、含碳、高硫、被硅酸盐包裹的微细颗粒金矿石已成为金矿开采的重点,这些矿石应用氰化法浸出效果差,氰化物具有剧毒,在实际生产中对环境和人体健康构成潜在威胁.为实现难处理金矿中高效、环保的回收金,非氰化法浸金逐渐成为研究热点.当前,国内外学者提出了多种非氰化浸金方法,主要有硫代硫酸盐法、甘氨酸法、卤素法、石硫合剂法以及其他工艺与方法(碘化焙烧工艺、硫脲浸出法和非水溶液浸金等).本文介绍了这些方法的浸金原理及其在难处理金矿方面的最新研究进展,讨论了这些方法存在的浸金试剂昂贵、浸出液中金难回收、浸出体系复杂、浸出剂性质不稳定及消耗量大等问题,并对非氰浸金技术的发展方向进行了展望.
1 硫代硫酸盐法浸金
硫代硫酸盐法由于其低毒、环保、浸出速率快、效率高等特点,成为目前最有可能取代氰化法提金的方法[11-14].
硫代硫酸盐法浸金是指在硫代硫酸盐浸金体系中金与硫代硫酸根离子形成可溶性配合物.若浸出溶液中不加任何催化剂,纯的硫代硫酸盐浸金速率缓慢.通过添加铜和氨形成铜氨络合物,从而催化金的溶解.但也会导致硫代硫酸盐分解,从而增加了试剂消耗.硫代硫酸盐的消耗主要是由于Cu2+与离子之间的反应,导致浸出液中的Cu2+浓度降低,从而降低金的浸出率,如方程式(1)所示[14].

Nie等[15]研究了Cu2+对铜-氨-硫代硫酸盐浸金体系中金的钝化和金溶解的影响.在Cu2+的存在下添加乙二胺(EN)和乙二胺四乙酸(EDTA)会增加金的溶解度,添加剂通过与Cu2+络合而削弱了Cu2+与硫代硫酸盐之间的相互作用,从而稳定了硫代硫酸盐并防止了金表面上钝化物质在形成.
Xu等[16]采用加氧、加压的碱性硫代硫酸盐体系浸金,研究表明硫代硫酸盐在氨水中是一种亚稳态阴离子,可以氧化成亚稳态或稳定的含硫物质,如(连多硫酸盐,x=3、4、5、6、···)、、S.生成的连四硫酸盐被进一步氧化为S;的简化分解路线如图1所示,相关反应如式(2)~(6)所示(ΔG⊖:同一温度、标准压强下的吉布斯自由能).铜氨催化金溶解的机理如图2所示[14].金的氧化反应发生在阳极区,如式(7)~(9)所示.另外,铜配合物的还原反应发生在阴极区域,如式(10)所示.

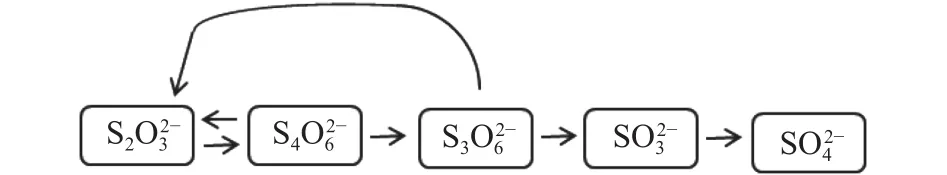
图 1 硫代硫酸盐分解的简化路线[16]Fig.1 Simplified route for thiosulfate decomposition[16]
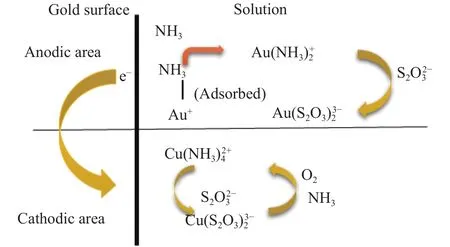
图 2 铜氨催化金溶解的机理[14]Fig.2 Mechanism of copper ammonia catalyzed gold dissolution[14]
Jeffrey等[17]使用表面加强拉曼光谱(SERS)鉴定抑制和钝化硫代硫酸盐浸金中金的表面物质.SERS表明,由于硫代硫酸盐的氧化,金表面形成硫.Baron等[18]在硫代硫酸盐浸出条件下通过SERS和电化学研究金-电解质界面,发现硫酸盐和三硫酸盐是硫代硫酸盐的最终产物,扫描电子显微镜(SEM)和拉曼光谱表明,在金表面形成硫化铜和多硫化物.Xu等[19]使用硫代硫酸盐浸出伴生硫化物金矿.通过X射线电子能谱(XPS)分析推断得出相同的结论.


为了解决上述问题,Yu等[20]用其他催化剂取代铜氨催化.添加增效剂(十六烷基三甲基溴化铵),用铜乙二胺催化从伴生褐铁矿的金矿中浸出金,金的浸出率为94.3%,而硫代硫酸盐的消耗量仅1.12 kg·t-1.然而,乙二胺的毒性限制了这种新型催化剂的应用.
在硫代硫酸盐浸金体系中,用铁-乙二胺四乙酸和草酸铁取代铜氨催化浸金,铁-乙二胺四乙酸和草酸铁络合物是硫代硫酸盐溶液中有氧和厌氧浸金的有效氧化剂,但铁配合物与硫代硫酸盐反应非常缓慢.虽然硫代硫酸盐消耗量可忽略不计,但若不添加硫脲,金的浸出率非常低.在浸出液中存在黄铁矿和磁黄铁矿时,金的浸出明显受阻,可能是由于硫化矿物催化Fe3+氧化硫代硫酸盐,导致缺乏Fe3+氧化剂[21-22].有学者还提出使用铁、镍和钴取代Cu2+氧化剂.Xu等[23]使用镍氨催化硫代硫酸铵浸出焙烧金精矿中的金,发现镍是有效的催化剂,可实现与Cu2+做催化剂时金的浸出率相当.镍氨催化硫代硫酸盐浸出金的机理模型如图3所示[23].

图 3 镍氨催化硫代硫酸盐浸出金的机理模型[23]Fig.3 Mechanism model of thiosulfate leaching of gold with nickelammonia catalysis[23]
Xu等[24]针对伴生铜、铅、锌多金属的复杂金矿,经硫酸氧压浸出铜、锌,氟硅酸浸出铅后,采用两步逆流镍催化的硫代硫酸盐法回收残留渣中的金,金的浸出率为95%,而硫代硫酸盐的消耗量仅1.2 kg·t-1.研究发现,镍氨在硫代硫酸盐浸出多金属复杂金矿石时具有催化作用.另外,浸出溶液中的金采用树脂回收,且镍不会负载在树脂表面,因此负载的金可通过简单的解吸进行回收.
然而,镍氨催化硫代硫酸盐浸金体系中,金表面形成的Ni3O4和溶液中以胶体溶胶形式存在的Ni3O4颗粒可能导致金浸出率降低,这是一个难以克服的问题.关于如何消除Ni3O4对镍氨催化硫代硫酸盐浸金体系影响的研究未见报道.
Xu等[25]利用钴-氨络合物作氧化剂代替传统的铜氨催化剂,金的浸出效率更高,钴氨催化硫代硫酸盐浸金机理的电化学模型如图4所示[26],反应如式(11)~(14)所示.


图 4 钴氨催化硫代硫酸盐浸金机理的电化学模型[26]Fig.4 Electrochemical model for cobalt-catalytic mechanism of ammoniacal thiosulfate leaching of gold[26]
Liu等[26]对不同pH、不同电极电势(Eh)条件下的氨性硫代硫酸钴溶液进行了一系列热力学计算.在pH值为8.8~9.7时,可形成Eh为0.05~0.35 V的,而不产生钴沉淀(即Co3O4),且的氧化还原电位高于.因此,热力学上,Co3+氧化为Co2+能催化金在氨性硫代硫酸盐溶液中的溶解.Co3+/Co2+的氧化还原电位低于Cu2+/Cu+,Co3+/Co2+的氧化还原催化机理与Cu2+/Cu+的氧化还原反应机理相似,即在金表面的阳极区氨催化金的氧化,而在阴极区氧的还原则由Co3+/Co2+的氧化还原反应催化.并且八面体的结构稳定性远高于,Co3+与硫代硫酸盐的反应活性低于Cu+与硫代硫酸盐的反应活性.因此,在Co3+体系中硫代硫酸盐分解显著减少.
Nie等[27]研究钴表面改性提高铜氨硫代硫酸盐溶液中金的溶解性.钴加入到铜氨硫代硫酸盐溶液中,会降低金表面的功函数和金浸出反应的表观活化能,使金浸出速率明显高于没有加入钴之前的浸出速率.8 h内金浸出率提高了40%.在溶液中Co生成Co(OH)2的过程中可能会生成Co3O4,Co3O4的高氧化性提高了金的浸出率.实验中仅向100 g金矿石中添加50 mg钴便有利于金的浸出,研究结果在工业上有应用的可能性.
综上,用钴氨替代传统的铜氨催化不仅可以减少硫代硫酸盐的消耗,且有利于降低从其母液中回收金的成本.因为树脂对络离子的亲和力较弱,所以钴氨络离子对树脂吸附金的回收几乎没有干扰.
2 甘氨酸法浸金
甘氨酸是一种无毒、不挥发且生产成本较低的试剂[28].在较宽的pH、Eh和温度范围内,甘氨酸与铜和贵金属均可形成稳定的络合物[29].另外,在甘氨酸浸金体系中,除了少部分甘氨酸会损失在浸渣中,其余甘氨酸还可以被回收并循环利用[30].
Feng等[31]通过向硫代硫酸盐浸金溶液中添加氨基酸(L-缬氨酸,甘氨酸,DL-丙氨酸和L-组氨酸),提升了金的浸出率.Groudev等[32]在研究生物浸出金的过程中,发现金的溶解是通过金氧化(过氧化物)和细菌分泌的物质混合来实现的.经过对细菌分泌的物质鉴定,发现这些细菌分泌的物质是天冬酰胺、甘氨酸、天冬氨酸、组胺酸、丝氨酸、苯丙氨酸和丙氨酸.Oraby等[33]研究了碱性甘氨酸过氧化物溶液中金的浸出,在碱性pH条件下,甘氨酸溶液中金的化学反应为式(15).氨基酸(如甘氨酸,丙氨酸,缬氨酸和苯丙氨酸)与金形成络合物,有利于后续从浸出液中回收金.
甘氨酸与Au+形成一种强络合物,如,在pH为9时的稳定常数为18.0,高于和.在碱性甘氨酸溶液中通入氧气,甘氨酸与金的反应如式(16)所示,在碱性甘氨酸溶液中添加过氧化氢,甘氨酸与金的反应如式(17)所示[28].
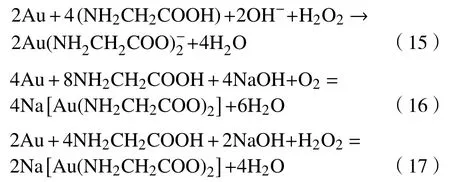
Wu等[34]研究了甘氨酸在硫氰酸铵浸液中的作用,研究发现由于氨基酸基团的脱质子作用,氨基酸具有络合金属离子的能力.铁离子对甘氨酸的络合能力强于硫氰酸铵,当甘氨酸加入硫氰酸盐浸出液中时,甘氨酸将与铁离子结合形成比硫氰酸铁更稳定的络合物,如式(18)所示(logK为稳定常数).溶液中形成的甘氨酸-铁络合物离子阻碍了硫氰酸盐与铁离子的氧化反应.
当添加甘氨酸时,金与甘氨酸形成络合物,反应如式(19)所示,降低了硫氰酸铵的消耗,提高了金的浸出率.在甘氨酸溶液中除了氧、过氧化氢可作为浸金氧化剂外,Fe3+也可作为甘氨酸溶液浸金的氧化剂,其反应式如(20)所示.Perea等[35]在甘氨酸溶液中添加高锰酸钾,金浸出效果优于加入过氧化氢时的效果.

为了进一步证明碱性条件下,甘氨酸能作浸金试剂.Oraby等[33]在碱性条件下,采用过氧化氢-甘氨酸溶液浸出金银合金,金的浸出率高于硫代硫酸盐-乙二胺四乙酸体系或硫代硫酸盐-草酸盐体系,并且过氧化氢-甘氨酸溶液中添加OH-离子可以提高金的浸出率,浸出液中金与甘氨酸形成的络合物可用活性炭吸附.Altinkaya等[28]在碱性甘氨酸溶液中,采用搅拌反应器浸出难处理金矿石.浸出条件如下:甘氨酸浓度为 1.25 mol·L-1、pH值为12、溶液温度为60 ℃、浸出时间为24 h,金的浸出率达到90%.Wu等[34]采用甘氨酸-硫氰酸盐溶液浸出浮选金精矿,金的浸出率达到93.15%.硫氰酸盐可通过氰化物生物解毒作用而形成,虽然毒性比氰化物小,但对水生生物和人类仍是有害的.
Oraby等[36]对澳大利亚的古河矿区金矿进行原地浸出(ISL).结果表明,在pH 值为12.5、c(NH2CH2COOH)=0.5 mol·L-1及浸出时间为336 h的条件下,金浸出率达到85%以上.在甘氨酸浸金溶液中,高pH值有利于金的浸出,原因是由于溶液中形成了氢氧化二乙酸乙酯和稳定性高的甘氨酸乙酯,加速了金浸出速率.
综上,学者对甘氨酸的浸金机理和协同浸出作用做了广泛研究.当使用氨基酸与硫代硫酸盐的混合试剂进行金的浸出时,氨基酸与Cu2+形成的络合物比氨水更稳定,这有助于降低混合溶液的电势,从而降低硫代硫酸盐的消耗.由于甘氨酸具有溶解金的作用,在硫代硫酸盐浸金过程中甘氨酸可作为额外的金浸出剂,提高了金浸出率,且甘氨酸浸金过程中杂质的溶解非常少,具有高选择性.
3 卤素法浸金
卤族元素的化学性质非常活泼,卤族元素原子的最外电子层上都有7个电子,容易获得1个电子而形成稳定结构,属于强氧化剂,可直接与金属化合成盐类.卤素离子CI-、Br-、I-均可与金离子形成稳定的配合物,利用这一性质,常将它们与适当的氧化剂相结合,组成金的浸出剂.除了氟和砹,其他卤素都曾尝试或用来浸金[37].
3.1 氯化法浸金
利用Au3+与CI-形成配合物这一性质,构成了现代从阳极泥中湿法提金的基础.氯化法适于处理含碳金矿、酸洗金矿和砷精矿[38].
氯化法的浸金工艺主要分为盐酸介质浸出、氯盐(次氯酸盐、氯酸盐等)浸出、电氯化浸出和氯气浸出等.在氯化法浸出过程中,氯既是浸金的氧化剂,又是金的络合剂[39].
金与氯离子能否形成离子络合物,取决于浸出液中氯离子的浓度和电极电位的高低[40].Seisko等[41]研究了氧化还原电位和开路电位(OCP)对氯化铁和氯化铜浸出金的影响,研究发现氧化还原电位可用于估算金的溶解速率,氧化还原电位与OCP和金溶解速率的对数呈正相关.
Seisko等[42]研究了氯化铜浸金的影响因素,研究表明大多数金以的形式溶解,而不是的形式溶解,金在氯化铜溶液中的溶解反应如式(21)所示.另外,可通过吹入氧气将亚铜物质再生成铜离子,反应式如(22)所示,且铜离子是氧化反应的催化剂.氯化铜浸金工艺的主要优点是氧化剂能再生、再利用.由于在氧气和酸的存在下,反应中不断生成亚铜离子,综合反应如式(23)和(24).

然而,上述方程是简化的,因为在氯化物溶液中,铜通常以复杂形式存在,能否形成络合物取决于温度和氯化物浓度.Zhang 等[43]指出,当c(Cu2+)=0.0005 mol·L-1,溶液温度为 25 ℃ 时,随着氯离子浓度从0增加到5.57 mol·L-1,溶液中可形成铜络合物(如CuCl+、CuCl2、和等).当络合物中含有较高的氯化物时,络合物的浓度相对增加量较小.当c(Cl-)= 3 mol·L-1时,铜离子最有可能以CuCl+的形式存在.
研究发现,金在氯化物溶液中的溶解会受到诸多工艺变量的影响,包括温度、氧化剂种类、氯化物浓度以及pH值[41].
Ahtiainen等[38]研究氯化物溶液浸出金时,发现来自金矿石中的铁和铜可成为浸出金时所需的氧化剂,在c(CaCl2)= 2.8 mol·L-1的溶液中,金的浸出率为87%.金浸出率随温度的降低而降低,在90 ℃时金浸出率为95%,60 ℃时金浸出率为73%,在25 ℃时金浸出率为67%.但在90 ℃和 98 ℃的温度之间,金浸出率差异不明显,温度的降低只是显著降低了溶液的氧化能力.研究中添加的氯离子浓度(0.6 mol·L-1)与海水中氯化物浓度相当,表明未来海水也可作为氯化物浸金过程中的浸出剂,降低浸出成本.
Seisko等[44]研究了铜离子浓度、温度和氯化物浓度对氯化铜介质中纯金溶解速率的影响,发现金溶解速率的增加与温度和较高浓度(>0.5 mol·L-1)铜离子的浓度成正比,溶解速率随着铜离子浓度由 0.75 mol·L-1升到 1.0 mol·L-1而降低,溶解速率降低的原因尚不清楚.为促进金溶解,温度应至少设置为65 ℃.研究发现无论氯化物浓度高低,金都以金离子形式溶解为,与Lampinen等[45]的研究结果一致.计算得出的氧化为的理论平衡电势表明,在所研究的条件下,金离子与氯离子不会生成.在氧化还原电势上检查了pH的影响,发现pH与氯化铁和氯化铜溶液中的金溶解速率不相关.Bonsdorff等[46]采用固定金电极进行电化学研究,发现介质移动对金溶解速率的影响大于温度、铜和氯化物浓度以及pH值对金溶解速率的影响,通过泵调节溶液的流速由0到300 mL·min-1,金溶解速率增加.为最大限度地提高金溶解速率,Lampinen等[45]将电极(旋转圆盘电极)的转速调到大于1000 r·min-1时,金溶解速率几乎是恒定的.
Baghalha等[47]用氯化物-次氯酸盐溶液浸出氧化物金矿.研究发现浸出液中加入次氯酸钠(NaOCl),金的浸出率大于加入Ca(OCl)2时金的浸出率.在氯化物浸金过程中,HOCl是生成[AuCl4]-络合物所需的氧化剂.对于包裹于硫化矿物(尤其是黄铁矿)中的金,次氯酸能够氧化硫化物和浸出金,反应式如(25)和(26)所示.

Nam等[48]使用NaCl-NaOCl溶液处理浮选后的含金尾矿,金浸出率为80%.Hasab等[49]采用NaCl-Ca(OCl)2溶液处理含硫化物的浮选金精矿,金浸出率达到82%.Hasab等[50]采用氯化物-次氯酸盐溶液处理含金的黄铁矿精矿,先用盐酸除去黄铁矿颗粒上的氢氧化铁层,再经过三个阶段的氯化物-次氯酸盐浸出、盐酸洗涤后,金的浸出率达到96%.Yanuar等[51]研究氯化物-次氯酸盐浸出(印度尼西亚)拉佩-苏姆巴瓦岩石中的金时,得出的最佳浸金条件是:体积分数为37%的盐酸溶液、体积分数为12% NaOCl溶液、液固比为20,金的浸出率约为89%.Pak等[52]采用加压氧化预处理和氯化法相结合的工艺处理高硫难熔金精矿,先对金精矿预处理,预处理后的金精矿在pH值为4、氧化还原电势高于 1.0 V、c(NaCl)= 1.28 mol·L-1、反应温度为40 ℃、液固比为3、浸出2 h的条件下,金浸出率为96.54%.
综上,氯化法作为一种卤素浸金方法,能浸出含硫、难熔的金矿,甚至无需进行压力氧化或焙烧的预处理.然而氯化物溶液具有腐蚀性和氧化性,这在工业规模运用上增加了设备与建筑方面的成本.
3.2 溴化物浸金
自19世纪以来,就有学者发现溴是一种极好的黄金浸出试剂,但有关其作为替代氰化物浸金的研究却相对较少,主要是由于溴元素具有危险性,且很难安全地存储或运输[53].
溴酸根离子具有很高的氧化电位,溴比全八面体少一个电子,因此是一种能与许多元素发生反应的强氧化剂[54].金在溴化物溶液中的溶解是一种电化学过程[53],金与溴离子的反应如式(27)(E⊖:标准电极电位).影响溴化物溶解金的主要因素是溴化物和金的浓度、阳极和阴极的pH值与电化学电位.
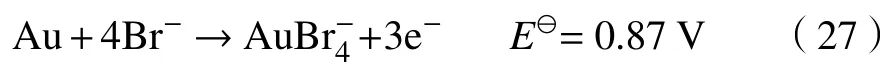

金被溴离子(Br-)络合,并被溴(Br2)氧化,溴可水解形成次溴酸,金被次溴酸氧化并溶解.该现象由反应(29)和(30)表示.

王强等[39]以微细粒包裹型的碳质金矿为实验研究对象,分别采用传统的氰化法和硫代硫酸盐法直接浸出实际矿石中的金,金浸出率仅为5.9%和4.3%.溴酸盐法在c(KBrO3) = 0.25 mol·L-1、c(FeCl3)= 0.08 mol·L-1、c(HCl)= 0.4 mol·L-1,溴酸盐搅拌速度为 250 r·min-1,液固比为 5,浸出时间为5 min的条件下,金的浸出率为94.5%.研究发现溴酸盐浸出法同样适用于处理浮选金精矿,且金的浸出率可达到91.8%.
Sousa等[53]对葡萄牙卡斯特罗米未开发矿的金矿石进行溴化物浸出实验.在c(NaBr)= 1.53 mol·L-1、c(NaOCl)= 0.4 mol·L-1、c(HCl)= 1 mol·L-1,浸出温度为 95 ℃,固液比为 1,搅拌速度为 450 r·min-1,浸出时间为4,pH值为4的条件下,金浸出率为73%.研究者在溴化物溶液中添加H2O2、Fe3+、氯化物等氧化剂,金的浸出率为80%.优化操作条件的同时,也提高了金回收率,降低了溴的消耗.与其他方法的比较表明,溴浸出法中金浸出率与氰化物法相近,且高于硫酸氢钠法;溴浸出过程中金浸出速度快,仅需4 h金浸出率即可达到80%,而氰化物浸出则需要24 h才能获得同样的金浸出效果.溴化物浸金工艺的优点主要表现为:①溶液中氯和溴都能浸出金,加速了金的浸出速度;②氯和溴循环再生,试剂消耗低.
综上,溴相比于其他卤族素元素,在酸性环境和碱性环境中都可作为金的浸出试剂,且浸出速率快;将溴化物添加到含氯和次氯酸盐的浸出溶液中便可产生溴,从而达到浸出金的目的;溴化物浸金过程中使用的溴酸盐比溴更好储存,而且它不会挥发到大气中.溴酸盐还可降解,零价铝(ZVA1)[54]、金属有机骨架 HKUST-1([Cu3(BTC)2(H2O)3]n,BTC为苯-1,3,5-三羧酸盐)都能有效降解废液中的溴酸盐[55-56].溴化物浸出金过程中,可通过电化学氧化循环生成溴酸盐[57],为避免选矿废液的排放、浸出液的回收以及生产成本的降低提供了理论依据.
3.3 碘化物浸金
碘与金形成的络合物比溴和氯与金形成的络合物更稳定,这是碘化物浸金的优势.Davis等[58]对碘-碘化物混合溶液中金的溶解做了基础研究.碘在碘化物的存在下溶解形成三碘化物离子,三碘化物离子是将金元素氧化成碘化物络合物的氧化剂.金与二价碘离子形成AuI、AuI3,也可形成复合化合物(M代表金属或有机阳离子).AuI和AuI3在水中的溶度积常数分别为 1.6×10-23和 1×10-46.将碘化钾(碘离子)加入溶液后,形成复合离子,使AuI的溶解度增加.相关反应及其热力学数据如式(31)~(33)所示,(其中aq表示水溶液;K是溶度积常数;φ是相对于标准氢电极的电势).

宫丽媛等[59]采用碘化法处理含银氧化金矿.研究中探究了液固比对金浸出率的影响,液固比从2提高到5时,金浸出率逐渐提高.徐渠等[60]采用碘化法从废印刷线路板(PCB)中提取金.浸出实验中也探究了液固比对金浸出率的影响,当固液比例较高时,金浸出率较低,液固比为10时,金浸出率90%.不断降低固液比时金浸出率下降,原因是溶液中过量的I-会与废PCB中的其他金属结合在一起.因此,碘化法浸金过程中合适的液固比有利于金的浸出.Konyratbekova等[61]研究了碘-碘化物浸出金的热力学和动力学.在温度为25 ℃,pH值为0~12.1时,碘以I-的形式存在,当pH值高于12.1时,IO3-离子稳定存在于浸出液中.选择碘化物浸出含金物料时,通常,酸性条件更适合于金的浸出,因为存在多种络合离子可以与金形成络合物.徐渠等[60]采用碘化法从废印刷线路板中提取金,探究了浸出溶液pH对金浸出率的影响.当溶液中pH值为碱性区间时,I-被氧化,且浸出溶液中其他金属产生沉淀,从而导致金浸出率降低.考虑到在工程应用中浸出液酸性高会腐蚀设备,因此,浸出过程中溶液pH值通常控制在中性或微酸性范围内,此时浸出液中大多数金属元素不会被浸出,有利于后续从浸出液回收金.
宫丽媛等[59]的研究还发现,用碘化法处理含银氧化金矿的浸出过程中金浸出率随时间的增加而增加,在前3 h内,特别是在1~2 h内,金浸出率显著增加,之后浸出率趋于稳定.Baghalha等[62]研究了氧化金矿石在碘-碘化物溶液中的浸出动力学.研究发现,浸出时间为6 h,金的浸出率为77%;浸出时间为24 h,金浸出率89%;但随浸出时间增加,溶液中的碘与氧化金矿中的硫化物、铁反应,增加了浸出试剂的消耗.Altansukh等[63]从预处理的废旧印刷线路板中浸金.在c(I2)=0.008 mol·L-1、c(KI)= 0.07 mol·L-1、溶液温度为 40 ℃、浸出2 h的条件下,金的浸出率大于99%.
碘-碘化物体系浸金过程.最为重要的是氧化剂与碘-碘化物的质量比,控制好该比值不仅可确保金的浸出率,还可节省成本;pH值低于11时,碘是一种很好的金浸出试剂,此时金的浸出率高;添加辅助氧化剂,如次氯酸钠和氨水可提高金浸出率,并减少碘的消耗.与其他卤化物体系相比,碘-碘化物体系具有较低的电势和较高的浸出速率,对贵金属浸出有很好的选择性.在当量的氧化剂和相同的络合剂浓度下,碘-碘化物对金矿的浸出速率不仅大于氰化物和硫脲对金矿的浸出速率,而且碘溶液无毒.
制约碘-碘化物浸金体系发展的主要原因是浸出成本高,其工业化的关键是如何降低浸出成本以及如何从浸出液中回收金和碘.研究人员正在努力通过尝试多次重用浸出液来降低浸出成本;同时向浸出液中添加电解质来提高金的浸出率,减少碘的消耗,这是碘化法浸金的研究方向之一.
4 其他工艺与方法
4.1 石硫合剂法
金精矿氧化焙烧过程产生的烟气中含有大量的有毒氧化物,限制了该预处理方法在工业上的广泛应用.Zhang等[64]使用石硫合剂法从含金硫化物中提取了金,首先将含金的硫化矿样放置于微波炉中焙烧,焙烧中产生的硫是制备石灰硫合成液(LSSS)的主要成分,可用于从含金硫化物中提取金,避免了有毒的气体对环境的污染.此外,当在惰性气氛中通过微波加热分解含金硫化物时,可有效释放包裹于硫化物矿物中的细粒金.石硫合剂法从含金硫精矿,特别是微细粒浸染型金精矿中提取金的方法如下:在样品质量为5 g,微波功率为4 kW、辐照时间为600 s的最佳工艺参数下,用质量分数为15%的LSSS碱性溶液浸金,金的提取率为91.98%.
4.2 碘化焙烧工艺
Guo等[65]研究了一种碘化焙烧工艺,实现了从难选金尾矿中有选择性且有效地回收金、银.在20 g的矿样中加入1.6 g的KI,混匀后在1100 ℃温度下通入空气焙烧1 h,金回收率达99.92%,银回收率达87.78%.碘化焙烧的反应机理为:碘分解为碘气,通过分子扩散与金尾矿中的金、银发生反应.此外,通过电子显微镜(SEM)和X射线衍射(XRD)分析表明,在碘化焙烧过程中,金尾矿表面只发生了表面改性,保持了金尾矿主要的相.研究者正在研究焙烧气体的分离和回收,目的是处理焙烧气体,降低处理成本.
4.3 硫脲浸出法
硫脲有望替代氰化物浸金的无毒浸金试剂.硫脲浸金可分为酸性硫脲浸金体系与碱性硫脲浸金体系,其中对酸性硫脲浸金体系研究较多.硫脲试剂的高消耗量和额外的氧化剂阻碍了其商业化应用.
4.3.1 酸性硫脲浸出法
硫脲在酸性体系中可被氧化为二硫甲脒[66],如反应式(34).

硫脲在有O2的酸性溶液中与金发生络合反应,如反应式(35).

硫脲在Fe3+氧化剂存在的酸性溶液中也能与金形成络合物,其反应为(36):

硫脲浸金过程中,H2O2、Na2O、O2、Fe3+、O2和MnO2等可作为氧化剂.其中,Fe3+氧化效果最佳;缺点是Fe3+或硫脲过量时,会形成不利于金浸出的铁-硫脲络合物,从而增加了硫脲的消耗.
Örgül等[67]对土耳其Kaymaz的一种精细分散的含金矿石进行硫脲浸出实验.将矿样磨至粒度小于53 μm,在室温、pH 值1.35、硫脲用量16.04 kg·t-1、浸出时间6 h的条件下,金浸出率为85.8%.硫脲浸液中不添加氧化剂(Fe2(SO4)3)时,金浸出率非常低.由于硫脲易被氧化,因此浸出系统的控制非常困难.为稳定硫脲浸出剂,研究人员进行了许多研究,利用硫酸根、六偏磷酸钠(SHMP)、木质素磺酸钠(CMN)和氨基酸可有效减少硫脲的消耗[68].
Guo等[3]对高硫高砷金精矿氧化焙烧后进行硫脲浸出实验,浸出液除硫脲外不添加其他试剂时,金的浸出率为84.42%.通过添加CMN、尿素和Fe3+,金浸出率可达到88.71%.这归因于添加剂可以抑制硫脲分解,防止矿样表面上形成钝化层.
4.3.2 碱性硫脲浸出法
为解决酸性体系中硫脲浸金存在的弊端,研究者尝试在碱性体系中硫脲浸金.在碱性体系中,硫脲也会分解[69],方程式为(37)~(38).


在碱性体系中硫脲会与银、铜、镉、铅、铁等的金属阳离子生成硫化物沉淀,降低金浸出率.白安平[69]在微孔材料充气条件下以埃塞俄比亚的金矿石为试验样品做了碱性硫脲浸金实验.在浸出液中,硫脲用量为1.5 kg·t-1、六偏磷酸钠用量为1.5 kg·t-1、液固比为 3∶1、矿浆初始pH值为11.5、浸出时间为8 h、空气充气量为0.8 L·min-1、搅拌桨转速为300 r·min-1的条件下,金浸出率54.27%.虽然六偏磷酸钠增强了硫脲的稳定性,但效果十分有限,浸出体系中增加六偏磷酸钠用量会导致浸出液黏度增大,使后续固液分离困难.需要进一步研究寻找效果更好的稳定剂.
4.3.3 生物氧化硫脲浸出法
生物氧化硫脲浸出是一种比氰化法更环保、更有效的从难浸含金矿石(精矿)中回收金的方法.
Guo等[71]采用生物氧化和两步硫脲浸出工艺处理难浸金精矿.通过生物氧化对矿样处理6 h.硫脲浸出前对生物残渣预洗,以减少可溶性杂质.在硫脲用量为 4.47 kg·t-1、浸出液温度为 35 ℃、浸出时间为6 h的硫脲浸出条件下,金的浸出率95.0%.研究结果表明两步浸出法是处理金精矿的有效工艺.微生物利用堆浸过程中的生物效应,使Fe3+成为氧化剂,维持酸性环境,降低药剂消耗.考虑到中和无需额外成本,且环境友好,这种生物氧化法与硫脲浸出法相结合是一种值得进一步研究甚至应用于工业的方法.
4.4 非水溶液浸金
Yoshimura等[72]提出了一种从二次资源中回收金的新方法,用含CuBr2的二甲基亚砜(DMSO)非水溶液浸金,金经过水沉淀后回收.金在温度为333~348 K的DMSO溶液中溶解,溶液中c(CuBr2)=0.2 mol·L-1、c(KBr2)=0.2 mol·L-1,金浸出率达到99%.采用水沉淀法沉淀溶液中的金,金的回收率为87%.DMSO溶液浸金工艺的优点有:毒性低、常温下蒸气压低、抗氧化性强、浸出液能够重复使用、工艺中不产生化学污泥;中小型企业可采用此工艺从二次资源中回收金.
5 结语与展望
本文综述了硫代硫酸盐法、甘氨酸法、卤素法(氯化物法、溴化物法,碘化物法)、石硫合剂法、碘化焙烧工艺、硫脲浸出法、非水溶液浸金7种非氰浸金方法的浸金机理及国内外研究进展.与氰化浸金法相比,以上7种非氰浸金法更加环保,浸金速度快,省去了预先处理工序,对难处理金矿石浸金效果显著,应用前景广泛;但是非氰浸金试剂消耗量大,性质不稳定,药剂种类多,浸出体系复杂,浸出液中的金难回收,设备腐蚀严重,工艺成本高,限制其大规模工业应用,针对这些问题,最近的研究显示:
(1)硫代硫酸盐浸金过程中,若浸出溶液中不加任何添加剂,纯的硫代硫酸盐浸金速率缓慢.通过添加铜氨催化剂可加速金的溶解.但催化剂也会分解硫代硫酸盐,导致试剂消耗高,分解产物在金表面形成钝化膜,阻碍金的浸出.当用钴氨替代铜氨催化硫代硫酸盐浸金时,硫代硫酸盐消耗减少,金的浸出效率更高,并降低了从浸出液中回收金的成本.但钴氨催化硫代硫酸盐浸金法仍难以浸出包裹在硫化矿物、硅酸盐矿物中的金.
(2)甘氨酸法浸金由于浸金速度慢,可作为原地浸出的浸金试剂.由于甘氨酸浸金过程中杂质的溶解少,且具有高选择性、工艺简单、络合物稳定性好等优点.除此之外,甘氨酸与其他浸金试剂有协同浸金的作用,不仅提高了金的浸出效率,还可以减少其他试剂的消耗.因此利用协同效应,探索新的浸金试剂组合方式,也是浸金发展方向之一.
(3)卤素法浸金中:氯化法能浸出含硫、砷、难熔金矿中的金,且矿样无需进行预处理,然而氯化物溶液具有腐蚀性和氧化性,阻碍了氯化法浸金的大规模工业运用;溴相比于其他卤族素元素,在酸性环境和碱性环境中都可作为金的浸出试剂,且浸出速率快;将溴化物添加到含氯和次氯酸盐的浸出溶液中便可产生溴,从而达到浸出金的目的.溴化法浸金中使用的溴具有危险性,溴很难安全地存储或运输,可通过将溴制备成溴酸盐来解决储运问题;溴化法浸金工艺中,找到了溴循环利用的方法,为降低生产成本提供了理论依据,但关于其替代氰化物浸金的研究却相对较少;碘化法浸金体系中,由于浸出成本高,可通过向浸出液中添加电解质,减少碘的消耗,另外,可进一步研究如何从浸出液中回收金和碘,从而降低浸出成本.
(4)硫脲虽然是有望替代氰化物浸金的无毒浸金试剂,但无论是在酸性还是碱性体系中,硫脲都不太稳定;在pH值大于2的酸性体系或温度大于25 ℃时易分解,导致硫脲消耗高,需要进一步研究硫脲的稳定性,防止二硫甲脒的分解,控制氧化还原电位值,防止硫脲的过度氧化.生物氧化和两步硫脲浸出工艺药剂消耗低,浸出液中和无需额外成本,且环境友好,因此,将两步硫脲法与生物氧化法相结合是一种值得进一步研究甚至应用于工业的方法.
(5)二甲基亚砜是一种非质子极性溶剂,用含CuBr2的二甲基亚砜溶液浸金,浸出液可重复使用且浸金过程中不产生化学污泥.因此,中小型企业可采用此工艺从二次资源中回收金.

