天南星炮制成胆南星的“减毒改性”作用
单丽倩,刘晓峰,崔亚晨,刘 悦,高 慧
(辽宁中医药大学药学院,辽宁 大连 116600)
天南星是天南星科植物天南星Arisaema erubescens(Wall.)Schott.、异叶天南星Arisaema heterophyllum Blume.或东北天南星Arisaema amurense Maxim.的干燥块茎,有温化寒痰、祛风止痉之功效。胆南星为制天南星细粉与牛、羊或猪胆汁经加工而成,或为生天南星细粉与牛、羊或猪胆汁经发酵加工而成[1],长于清热化痰、息风定惊,多用于痰热咳嗽、急惊风、癫痫等症。天南星经发酵后制成胆南星,是炮制对改变药性最典型的例子,性由温转凉,味由辛转苦,功效由温化寒痰转为清化热痰,且毒性降低。
关于胆南星的炮制作用,历代本草学著作中多有记载,如“天南星为燥痰之品,制以牛胆以杀其毒。得牛胆则燥性减,且胆有益肝胆之功”[2]、“胆南星……降痰因火动如神,治小儿急惊必用……较之南星味苦性凉,故善解风痰热滞……”[3]等。在现代研究中,有人基于小鼠生理生化指标对天南星、胆南星的药性变化进行探讨[4],另有实验证明天南星具有显著毒性[5],但未见对天南星、胆南星传统药效和毒性的系统对比研究。本课题组前期对胆南星中化学成分进行了对比研究[6],并对发酵前后的胆酸类成分含有量进行了比较,证明了发酵后结合型胆酸转化为游离型胆酸,确立了胆南星的发酵工艺,并建立了用3 种游离型胆酸含有量评价胆南星质量的标准[7]。本实验围绕胆南星的传统功效,分别从抗高热惊厥、清热以及毒性三个方面,对天南星发酵前后的药效、毒性进行对比研究,以从传统药效学方面验证天南星发酵“减毒改性”的炮制理论,为进一步研究天南星的炮制原理提供基础。
1 材料
1.1 仪器 恒温恒湿培养箱(HWS-080 型,上海精宏实验设备有限公司);HZ-A6002 型电子天平(HZ-A6002 型,瑞安市金讯贸易有限公司监制);酶标仪(MuLtiskan Mk3型,上海赛默飞世尔仪器有限公司);医用离心机(湖南湘仪实验室仪器开发有限公司)。
1.2 药物及试剂 东北天南星采自辽宁省本溪市,经辽宁省药品检验检测院王维宁教授鉴定为天南星科植物东北天南星Arisaema amurense Maxim.的干燥块茎,采后净制,洗去泥沙并切制成2~3 mm 厚片,晾干,即得。猪胆汁购于大连础明集团有限公司。大鼠前列腺素E2(PGE2)试剂盒(生产批号 BPE35446)、大鼠钠钾ATP酶(Na+/K+ATPase)试剂盒(批号BPE30580)、大鼠琥珀酸脱氢酶(SDH)试剂盒(批号 BPE30230)、大鼠肝糖原(Glycogen)试剂盒(批号20171116HE)、大鼠白细胞介素-1 β(IL-1β)试剂盒(批号BPE30419)、大鼠白细胞介素-6(IL-6)试剂盒(批号BPE30666)购自上海朗顿生物科技有限公司;干酵母粉(产品标准代号GB/T20886,湖北安琪酵母股份有限公司);PBS(批号P1020-500,北京索莱宝科技有限公司)。
1.3 动物 SPF 级21 日龄雄性SD 大鼠48 只(体质量60~80 g);SPF 级雄性SD 大鼠32 只(体质量180~220 g);SPF 级KM 小鼠80 只,雌雄各半(体质量18~22 g),均购自辽宁长生生物科技有限公司,实验动物生产许可证号SCXK(辽)2017-0001,饲养于辽宁中医药大学SPF 级动物房。本实验所进行的所有相关操作均在辽宁中医药大学动物伦理委员会的批准下进行,批准号2018YS(DW)-043-01。
1.4 样品制备 天南星鲜品:取天南星块茎,洗去泥沙,即得。天南星:取天南星块茎,洗去泥沙,切制成2~3 mm厚片,晾干,即得。胆南星:取天南星细粉过五号筛,加入净胆汁(经绢布滤过),经1∶1 比例混合,置32 ℃、80%的恒温恒湿培养箱中发酵15 d 取出,至蒸制容器中蒸1 h 至透,趁热切成1.5~2 cm 的小块,晒至黑褐色,即得[7]。
2 方法
2.1 样品水煎液制备 抗惊厥实验用药:取适量天南星、胆南星,用10 倍量水回流提取3 次,浓缩制成中剂量(0.14 g 生药/mL)、高剂量(0.28 g 生药/mL)水煎液。解热实验用药:取适量天南星、胆南星,用10 倍量水回流提取3 次,浓缩制成0.28 g 生药/mL 水煎液。毒性实验用药:取适量天南星捣碎,加水制成低剂量(0.18 g 生药/mL)、中剂量(0.25 g 生药/mL)、高剂量(0.32 g 生药/mL)溶液;天南星、胆南星用10 倍量水回流提取3 次,浓缩制成低剂量(0.18 g 生药/mL)、中剂量(0.25 g 生药/mL)、高剂量(0.32 g 生药/mL)水煎液。
2.2 抗惊厥实验 取48 只21 日龄SD 大鼠适应性饲养1周,随机分为6 组,每组8 只,分别为空白组、模型组以及天南星中、高剂量组和胆南星中、高剂量组。给药组大鼠按1.4、2.8 g 生药/kg 剂量灌胃给药,空白组、模型组给予等容量生理盐水,连续7 d。于第7 天灌胃给药后1 h后测肛温,参照周国平等[8]建立的45 ℃热水浴诱发的大鼠惊厥模型,将除空白组外其余各组大鼠置于(45±2)℃热水浴中,诱发惊厥发作,惊厥发生后立即从水中捞出大鼠。观察各组大鼠惊厥发生数、惊厥死亡数、惊厥潜伏期(从进入热水浴至惊厥发作的时间)、惊厥持续时间和惊厥诱发结束时肛温并计算惊厥发生率、惊厥致死率和肛温上升速度,肛温上升速度=(惊厥诱发结束时肛温-惊厥诱发开始时肛温)/惊厥潜伏期,规定惊厥最大观察时间为5 min[9]。
2.3 解热实验 取32 只SD 大鼠适应性饲养1 周,于正式实验前3 天在每日上午9 时测定大鼠体温,选取体温在36.6~38.3 ℃之间、正常波动小于0.2 ℃的大鼠作为正常实验大鼠,末次测量体温之后随机将大鼠随机分为4 组,每组8 只,分别为空白组、模型组、天南星组、胆南星组。给药组大鼠按2.8 g 生药/kg 剂量灌胃给药,空白组、模型组给予等体积生理盐水,连续7 d。于给药第7 天,分别测量晨起肛温,空白组皮下注射生理盐水,其余组均按10 mL/kg剂量皮下注射20% 干酵母混悬液造模[10]。造模30 min后,各组灌胃相应药物,空白组和模型组给予生理盐水,测量给药后0、1、2、3、4、5、6 h 的肛温,并于末次测量后,用乙醚麻醉大鼠,断头处死,随后立即在冰浴中取脑,切取下丘脑组织并加PBS 溶剂匀浆置冷冻室内保存,测定各给药组下丘脑组织中前列腺素E2(PGE2)的水平;取肝组织并称重,切取部分肝组织加PBS 溶剂匀浆后置冷冻室内保存,测定各给药组肝脏组织中钠钾ATP 酶(Na+/K+ATPase)、琥珀酸脱氢酶(SDH)以及肝糖原(Glycogen)的水平;腹主动脉取血,置于EP 管中,3 800 r/min离心20 min,吸取血清上清液,测定各给药组血清中炎症因子白胞介素-6(IL-6)、白细胞介素-1 β(IL-1 β)的水平。
2.4 毒性实验 SPF 级KM 小鼠80 只,体质量(20±2)g,雌雄各半,按体质量和性别随机分为10 组,每组8 只,分别为空白组,天南星鲜品高、中、低剂量组及天南星高、中、低剂量组和胆南星高、中、低剂量组,受试动物实验前禁食不禁水12 h,空白组灌胃等体积生理盐水,给药组按1.8、2.5、3.2 g 生药/kg 剂量灌胃给药2 次,时间间隔为12 h。灌胃后各组小鼠自由摄取标准鼠粮,自由饮水,密切观察小鼠的行为活动、精神状态、摄食饮水、皮毛光泽、粪便尿液、呼吸情况、鼻、眼、口腔有无异常分泌物等情况,并记录小鼠死亡情况。
2.5 统计学分析 通过SPSS 23.0 软件进行分析,数据以()表示,各组数据采用单因素方差分析与组间t 检验。P<0.05 表示差异具有统计学意义。
3 结果
3.1 天南星发酵前后抗高热惊厥作用结果 与模型组相比,除天南星高剂量组外,各给药组均能够降低幼龄SD大鼠由高热引起的惊厥发生率,且天南星高剂量组具有一定的致死率,可能与天南星具有毒性有关;与天南星组相比,高剂量胆南星组能显著降低惊厥发生率,在同样发生惊厥的中剂量组中,胆南星组能够明显降低惊厥发生率,缩短惊厥持续时间,降低肛温上升速度,说明天南星经发酵炮制后可明显增强抗高热惊厥作用。见表1。
表1 各组药物对幼龄SD 大鼠惊厥发生率、惊厥致死率、惊厥潜伏期、惊厥持续时间以及肛温上升速度的影响(,n=8)
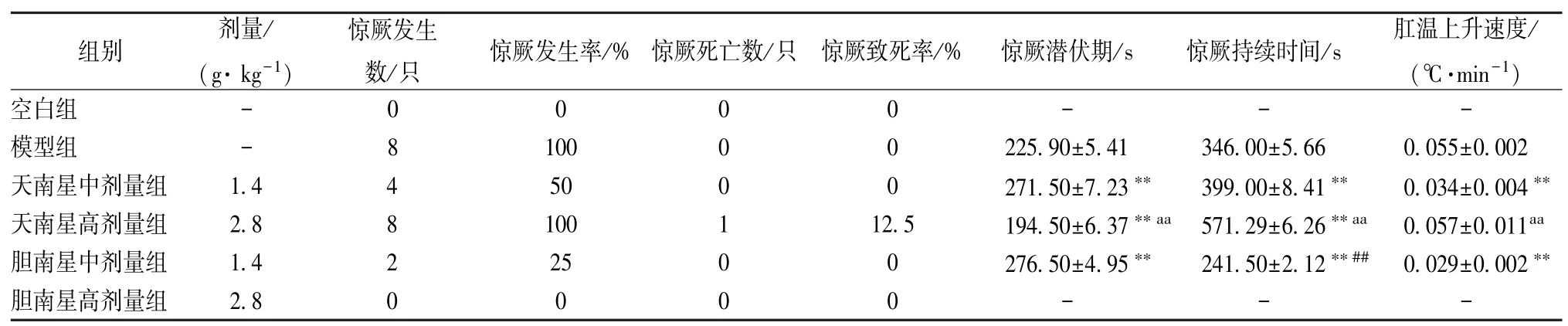
表1 各组药物对幼龄SD 大鼠惊厥发生率、惊厥致死率、惊厥潜伏期、惊厥持续时间以及肛温上升速度的影响(,n=8)
注:-代表未惊厥。与模型组比较,*P<0.05,**P<0.01;中剂量天南星发酵前后比较,##P<0.01;天南星中、高剂量组比较,aaP<0.01。
3.2 天南星发酵前后解热作用结果
3.2.1 天南星发酵前后肛温变化 给药0~6 h 期间,与空白组比较,模型组肛温持续增加,3 h 之后体温升高(P<0.01),说明造模成功;与模型组相比,天南星组与模型组无显著性差异,说明天南星并没有解热作用,符合天南星作为热性药的性质,胆南星组肛温降低(P <0.05,P<0.01),说明胆南星有良好的解热作用;天南星组与胆南星组相比,于给药2 h 后胆南星组肛温低于天南星组(P<0.05,P<0.01),证明经加胆汁发酵炮制后,胆南星有良好的解热作用,说明了胆汁以寒制热的作用。见表2。
表2 各组药物对各组SD 大鼠肛温变化情况(,n=8)

表2 各组药物对各组SD 大鼠肛温变化情况(,n=8)
注:与空白组比较,*P<0.05,**P<0.01;与模型组比较,#P<0.05,##P<0.01;天南星发酵前后比较,aP<0.05,aaP<0.01。
3.2.2 天南星发酵前后对大鼠下丘脑组织中前列腺素E2(PGE2)的影响 与空白组相比,模型组大鼠下丘脑组织中PGE2水平增加(P<0.05,P<0.01);与模型组相比,天南星组水平相差不大,胆南星组水平降低(P<0.05,P<0.01);天南星组与胆南星组相比,胆南星组低于天南星组(P<0.05,P<0.01)。见表3。
3.2.3 天南星发酵前后各给药组血清中炎症因子白胞介素-6(IL-6)、白细胞介素-1 β(IL-1 β)的表达 与空白组相比,模型组IL-6、IL-1 β 水平显著增加(P<0.05,P<0.01);与模型组相比,天南星组IL-6、IL-1 β 水平相差不大,胆南星组IL-6、IL-1 β 水平降低(P<0.05,P<0.01);天南星组与胆南星组相比,胆南星组IL-6、IL-1 β 水平低于天南星组(P<0.05,P<0.01)。见表3。
表3 药物对SD 大鼠下丘脑组织PGE2 及血清IL-6、IL-1β 的影响(,n=8)

表3 药物对SD 大鼠下丘脑组织PGE2 及血清IL-6、IL-1β 的影响(,n=8)
注:与空白组比较,**P<0.01;与模型组比较,##P<0.01;天南星发酵前后比较,aP<0.05,aaP<0.01。
3.2.4 天南星发酵前后各给药组肝脏组织中钠钾ATP 酶(Na+/K+ATPase)、琥珀酸脱氢酶(SDH)以及肝糖原(Glycogen)的代谢 与空白组相比,模型组大鼠肝脏组织中Na+/K+ATPase、SDH 水平增加,Glycogen 水平降低(P<0.05,P <0.01);与模型组相比,天南星组Na+/K+ATPase、SDH 以及Glycogen 水平相差不大,胆南星组Na+/K+ATPase、SDH 水平降低(P<0.05,P<0.01),Glycogen水平增加(P<0.05,P<0.01);天南星组与胆南星组相比,胆南星组Na+/K+ATPase、SDH 水平降低,Glycogen 水平高于天南星组(P<0.05,P<0.01)。见表4。
表4 药物对大鼠肝脏组织中Na+/K+ATPase、SDH、Glycogen 代谢的影响(,n=8)
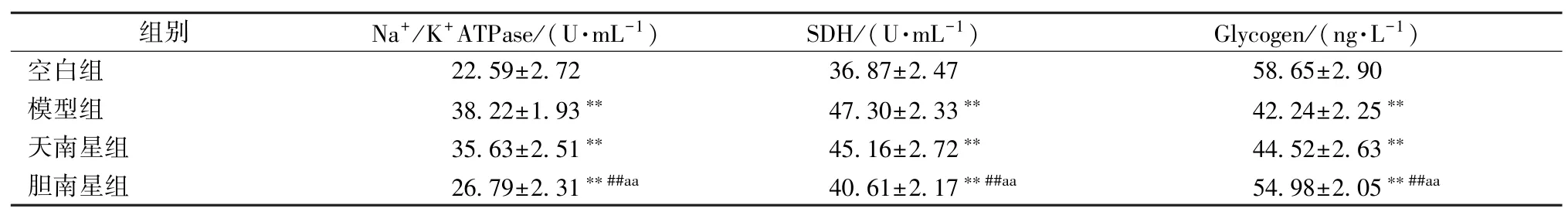
表4 药物对大鼠肝脏组织中Na+/K+ATPase、SDH、Glycogen 代谢的影响(,n=8)
注:与空白组比较,**P<0.01;与模型组比较,##P<0.01;天南星发酵前后比较,aaP<0.01。
由以上肛温变化情况、下丘脑体温调节中枢、肝脏组织能量代谢以及血清中炎性因子的对比,能够发现天南星组与模型组相比无显著性差异,说明天南星是热性药,无解热作用。胆南星与模型组有显著性差异,且向空白组接近,说明胆南星具有良好的解热作用。
3.3 天南星发酵前后毒性作用结果 各组动物在第二次灌胃后6 h 内均出现不同程度的怠动、竖毛、聚堆、静止俯卧、呼吸急促或呼吸困难、身体震颤、抽搐至死亡。对死亡动物立即解剖,可见小鼠胃肠均有大量尚未吸收的药液,个别小鼠胃底部有充血现象,其余脏器未见有明显异常。第二次灌胃6 h 后大部分存活动物开始逐渐进食饮水,第三天开始各组小鼠饮食进水恢复正常。天南星本身具有毒性,可致小鼠死亡,且天南星鲜品组死亡率高于天南星组,说明天南星经发酵炮制后,可有效降低死亡率,使毒性降低。见表5。
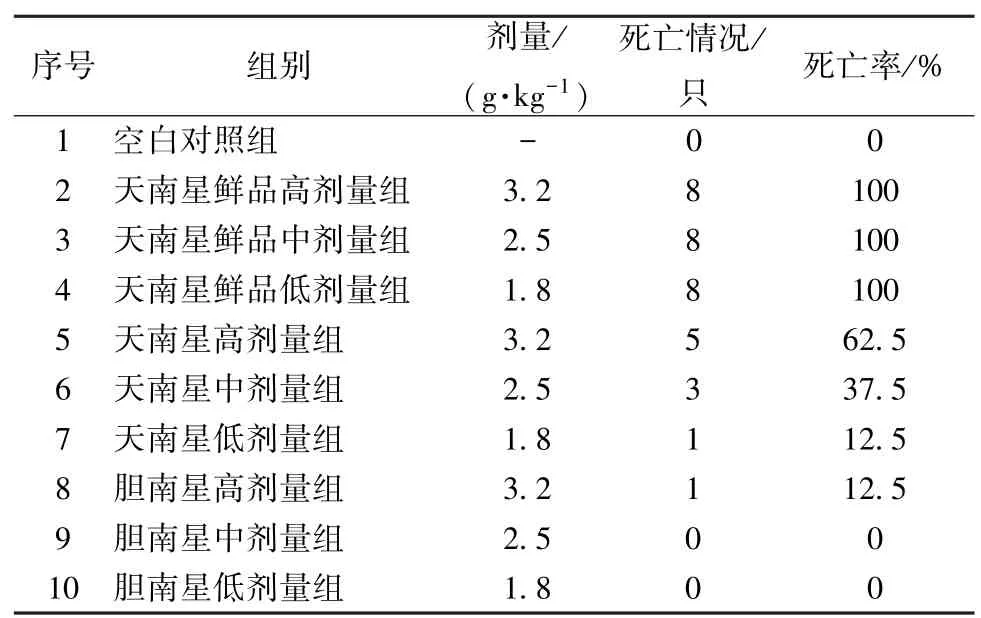
表5 药物对动物死亡情况的影响
4 讨论
天南星经发酵制成胆南星后,药性由温转凉,毒性降低。这一炮制作用在古代各大医书中均有大量记载,但在现代研究中,欠缺炮制前后药效及毒性对比研究,无法解释其炮制原理。抗高热惊厥和清热作为胆南星典型的药理作用,能够直观的对比出两者在传统药效方面的区别,比较贴合胆南星实际应用情况;毒性实验则能直观的对比出两者毒性强弱。所以本实验从药效和毒性两方面系统阐述了天南星炮制前后的变化,从而验证天南星发酵“减毒改性”的炮制原理。
胆南星临床上常用于治疗小儿高热惊厥[11],故本实验模拟小儿高热致惊厥的模型,选用幼龄的SD 大鼠,并用热水浴诱发惊厥,以最大程度的还原胆南星在临床中的应用情况[12]。将惊厥发生率作为最直接的观察指标用以评价抗惊厥作用强弱。胆南星抗高热惊厥作用明显强于天南星,胆南星不仅在抗惊厥作用上强于天南星,还可降低肛温上升速度,从侧面辅助证明了胆南星的解热作用。
解热作用机理之一是使下丘脑体温调节中枢的PGE2水平降低[13],或使大鼠肝组织Na+/K+ATPase 的水平降低、SDH 活力降低、升高肝糖原水平,而IL-6、IL-1 β 作为重要的抗炎症细胞因子[14-16],发热会导致其水平增加,故解热实验中选定上述指标进行比较。对于干酵母所引起的发热,胆南星组可有效降低大鼠体温,降低发热大鼠的PGE2、Na+/K+ATPase、IL-6、IL-1 β 和SDH 水平,增加肝糖原含量,而天南星则未表现出解热作用。说明天南星在加入胆汁进行发酵制成胆南星后,具备了胆汁中寒凉的药性,产生了解热作用,体现了热性药向寒性药的转变,证明了炮制改性的原理。
因为在产地采收、加工天南星鲜品时,天南星鲜品表现出极明显的对皮肤的刺痛作用,我们在对比天南星、胆南星毒性时增加了天南星鲜品组。预实验表明,天南星鲜品有明显的毒性,而天南星、胆南星组均受给药体积和浓度的限制,给到最大浓度仍然无法致全部死亡,无法得到Dm、Dn、LD50等数据,故正式实验对不同样品对小鼠致死率进行了比较。结果表明,天南星鲜品具有明显的毒性,经干燥后毒性有所降低,进一步发酵制成胆南星后毒性大大降低,体现了天南星的“炮制减毒”。
本实验通过对天南星发酵前后的传统药效及毒性比较,证明了天南星发酵炮制后药性由热转凉,增强抗高热惊厥作用,产生显著的解热作用,并使毒性降低,验证了炮制“减毒改性”的原理。

