优化角度分组对宫颈癌容积旋转调强计划剂量分布的影响
王 成, 陈维军, 李玉成, 贾勇士, 詹文明, 李 强, 杨 帆, 赵桂芝*
(1.南华大学核科学技术学院, 衡阳 421001; 2.浙江省人民医院放疗科/杭州医学院附属人民医院, 杭州 310014)
宫颈癌在临床上是一种常见的妇科肿瘤,其发病率和致死率均处于女性肿瘤疾病的第四位[1]。随着科学技术的进步,放疗成为治疗宫颈癌的一种重要手段,而容积旋转调强放射治疗(volumetric-modulated arc therapy, VMAT)作为当代放疗技术中一种先进手段,它相较于传统调强技术在减少治疗时间的同时,能使靶区保持更均匀的剂量分布[2-3],因而成为目前一种主流放疗技术。
在Monaco计划系统对病人进行VMAT计划设计时,第一阶段中,系统将光子束分成多个扇形,使用理想的光子束注量分布优化,用来满足给定光束组的定义处方。在第二阶段,系统在优化过程中使用蒙特卡洛模拟,根据优化限制函数完成分割,包括分割形状和权重,并在此之间进行优化平衡,以获得优化结果。已有大量文献报道[4-7]:最小子野面积、优化模式的选择、剂量计算网格、优化角度分组(increment,Inc)等参数的不当设置,会严重影响VMAT剂量计算结果。针对优化角度分组这一参数,尚没有标准的量化指标,需要物理师根据经验手动输入参数,如果参数设置不合理,可能会延长计划的优化时间,甚至导致优化结果失败,会严重影响临床的工作效率。中外已有文献报道Inc参数会影响鼻咽癌、食管癌、前列腺癌剂量计算的准确性和影响剂量分布[7-9],从而影响治疗效率及疗效。宫颈癌作为女性腹部常见的癌症疾病,相较于食管癌病例其危及器官体积相对较小,数量更多且相互邻近。相较于前列腺癌主要针对男性患者,宫颈癌作为女性腹部常见的肿瘤疾病,病灶位置与邻近危及器官与之具有部分差异。相较于宫颈癌,鼻咽癌危及器官通常体积较小,串行器官较多,而宫颈癌危及器官多为并行器官,器官体积偏大。由于这些差异的存在,所以对宫颈癌患者的优化角度分组参数影响研究仍具有一定临床意义。在保证计划靶区(planning target volume, PTV)剂量充足的条件下,为减少危及器官的剂量受量,减少临床放射性副反应的发生,得到更优的剂量分布结果,从宫颈癌患者的VMAT技术出发,定量分析常用Inc参数对宫颈癌患者靶区和危及器官中剂量分布的影响,从而指导临床应用选择合适的Inc参数。
1 材料与方法
1.1 病例资料
随机选取浙江省人民医院2020年1月—2020年7月收治的15例宫颈癌术后放疗的病人,病理类型均为鳞癌,年龄31~72岁,中位年龄53岁。所有患者此前均未接受过宫颈癌放疗,且均无放疗禁忌证。
1.2 模拟定位
患者取仰卧位,使用热塑体膜(8例)或真空负压垫(7例)进行体位固定,采用双手交叉抱肘置于额头,采用美国通用电气公司(General Electric Company, GE)生产的Discovery CT590 RT型号的大孔径CT机扫描,扫描范围从第一腰椎至坐骨结节下缘水平,层厚5 mm,平扫加增强扫描。然后导入Monaco计划系统中。
1.3 靶区勾画及处方剂量
根据国际辐射单位和测量委员(International Commission Radiological Units,ICRU)62 号和83 号报告[10-11],由其临床主治医师勾画临床靶区(clinical target volume,CTV)及危及器官,然后PTV由临床靶区头脚方向外扩0.7 cm,腹背及其他方向外扩0.5 cm形成。再由物理师进行计划设计。处方剂量给予PTV95%达到4 500 cGy的处方剂量,25×180 cGy的分次剂量。针对部分宫颈癌患者存在需要更高剂量的PTV-boost,为了进行定量的剂量分析,本文暂且忽略PTV-boost所需达到的目标剂量体积,同时使用系统自带的Rescale dose技术将PTV调整到95%的目标剂量体积,这样可以定量对比分析其他危及器官的受量。
1.4 计划设计
由于宫颈癌病人的靶区通常均处于体内居中的位置,常使用360°全弧的方式进行计划设计,由于Monaco自身条件的限制,不能由179°顺时针旋转到181°,所以令所有全弧的设计为178°逆时针旋转350°。其余参数选择为:剂量网格0.3 cm,计算不确定度为1%,平滑度选择中等medium,选择单弧VMAT计划(机架转向为单向,逆时针178°~188°),单弧的控制点数选择180。并在Inc为30°的条件下对计划进行优化设计,如图1所示,此时CT图被分为12个优化区间进行同时优化。然后另外对Inc分别赋值10°、20°、40°,同时将Inc=10°、20°、30°、40°时的计划分别命名为Inc10°、Inc20°、Inc30°、Inc40°。在约束条件相同的情况下,分析各Inc下VMAT计划的剂量分布。
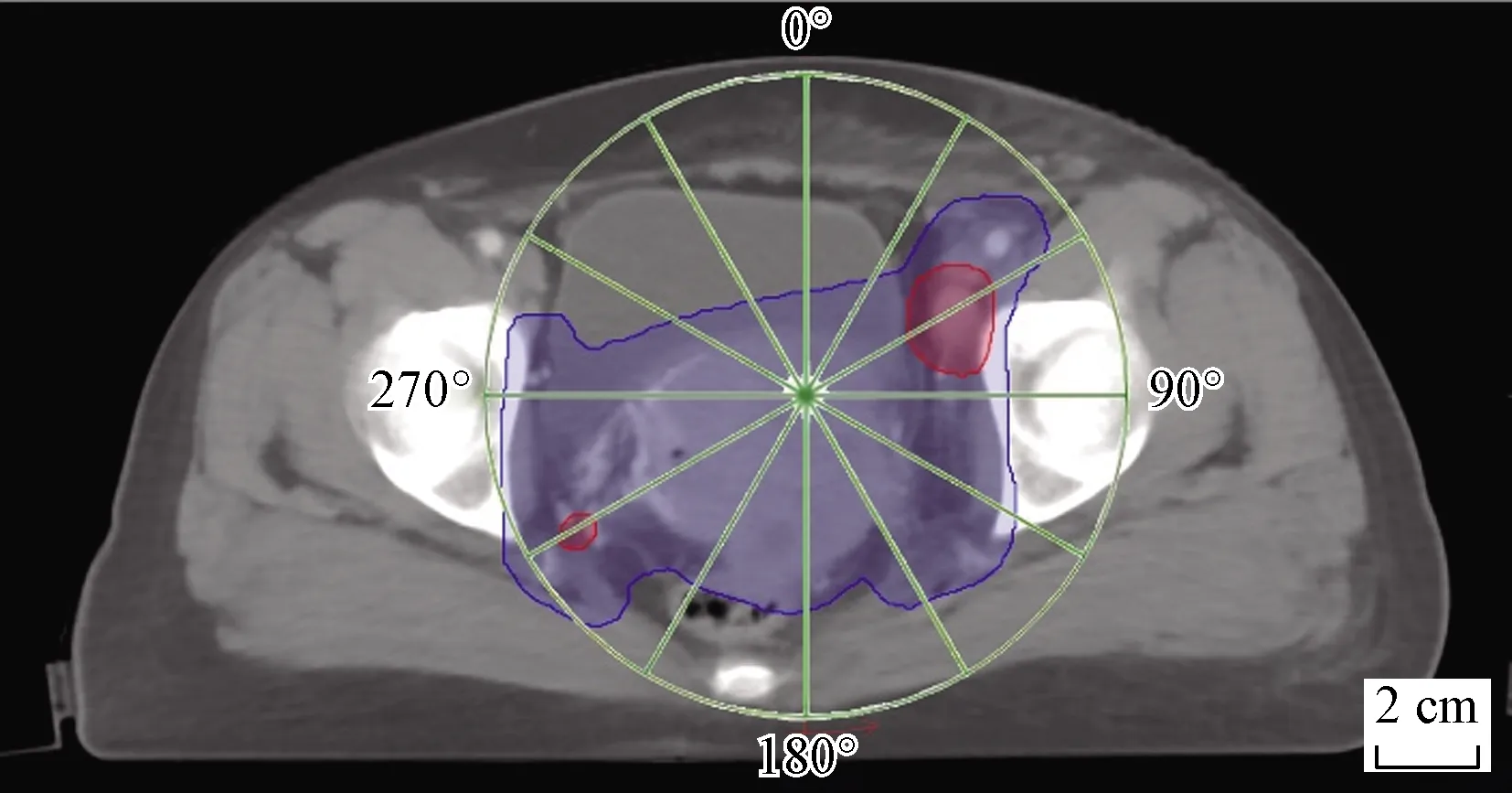
图1 360°的弧长其扇区数被分为12个Fig.1 The number of sectors for 360° arc length is 12
1.5 计划评估指标
根据国际辐射单位和测量委员会(International Commission on Radiation Units and Measurements,ICRU)发布的83号报告的要求对靶区和危及器官进行分析[11]。针对靶区,靶区使用D2、D50(Dx为器官中x%的体积包含的剂量),靶区适形度指数(homogeneity index,CI)和靶区均匀性指数(homogeneity index,HI)进行分析,CI、HI的计算公式为
CI=(VT,ref/VT)(VT,ref/Vref)
(1)
式(1)中:VT,ref为参考等剂量线面所包围的靶区体积;VT为总的靶区体积;Vref为参考等剂量线面包围的所有区域体积。CI越接近1表示适形度越好[12]。HI的计算公式为
HI=(D2-D98)/D50
(2)
式(2)中:HI越接近1表示均匀性越好。针对宫颈癌的病灶所处的特殊位置,其危及器官的评价参数选择左右股骨头的平均剂量Dmean,盆骨V10、V20及Dmean,膀胱、直肠、小肠的D2及V45,乙状结肠的D2及Dmean,和脊髓的D2来进行分析。其中Vx代表xGy的剂量线所包含的器官体积百分比。
1.6 统计学方法

2 结果
2.1 靶区剂量参数比较
与对照组Inc=30°相比较,10°、20°、40°的优化角度分组计算得到PTV的HI均不具有统计学意义(P>0.05),D2除40°组以外,D50及CI除10°组以外,均不具有统计学意义(P>0.05)。与对照组Inc=40°相比较,实验组10°、20°中的D2、D50、HI、CI除10°组中的CI具有统计学意义(P<0.05)以外,其余均不具有统计学意义(P>0.05)。与对照组Inc=20°相比较,实验组Inc10°中均有统计学意义(P<0.05),且D2、D50,HI明显增加,CI明显减小。四组对照组在CT上的剂量分布差异如图2所示。

图2 4组计划下的靶区横切面的剂量分布Fig.2 The dose distribution of target region transverse of section among four groups
2.2 危及器官剂量参数比较
(1)与对照组Inc=20°时的计划相比较,实验组10°时的盆骨V20、Dmean和膀胱、直肠及乙状结肠的D2与对照组相比具有统计学意义,且盆骨V20、Dmean减小,膀胱、直肠及乙状结肠的D2增加,其余参数不具有统计学意义。
(2)与对照组Inc=30°时的计划相比较,实验组10°其危及器官中的盆骨V10、V20、Dmean低于30°组,且具有统计学意义(P<0.05),膀胱D2,直肠D2均高于30°组,且具有统计学意义(P<0.05),10°时的其余危及器官参数不具有统计学意义(P>0.05)。实验组20°的所有危及器官参数与对照组相比,均不具有统计学差异(P>0.05)。实验组40°的左股骨头Dmean与盆骨Dmean均高于30°组,且具有统计学意义(P<0.05),其余危及器官参数与对照组相比不具有统计学意义(P>0.05)。

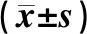
表1 4组计划靶区和危及器官剂量参数Table 1 Comparison of dosimetric parameters of targets and OARs among four groups
3 讨论
VMAT技术相较于传统固定野调强技术,其有着良好的肿瘤控制率和危及器官受量,短治疗时间的优势[13],在选择Inc参数时,系统提示可以在3°~60°选择,而在使用全弧计划且使用单弧的条件下,Inc>45°时系统将进行报错参数选择过大,可能是在选择45°时,VMAT的优化角度的8个分组相较于常规固定野调强为8个射野,此时不能体现VMAT的技术优势,所以系统在Inc选择大于45°时系统将进行报错[14]。
从整体来看,Inc10°、Inc20°、Inc30°、Inc40°时的所用的平均计划时间分别为55.4、36.27、26.2、25.07 min,而计划时间的减少对于优化过程较复杂的Monaco来说,可以较为显著地提高计划效率。Inc10°、Inc20°、Inc30°、Inc40°的平均机器跳数(monitor unit,MU) 分别为949.28、812.57、786.16、773.08 MU,由于MU是指在标定下1 MU=1 cGy,则出束剂量率一定时,跳数越少时治疗时间就越短,不仅可以提高治疗效率,也可以减少由于较长的治疗时间引起的分次内器官体积变化,提高治疗精确度。并且机器跳数明显减少时,还可以降低加速器机头附近的射线散射,理论上也可以降低二次致癌的概率[15]。
从文章数据中得出,当随着Inc的增大,其计划运算时间会随之减小,这是由于Inc=10°时,其射野需要在36个弧内进行相互优化,而当Inc=40°时,计划只需在9个弧段内进行优化,其计划运算效率提升显著。但在部分病人身上,当其Inc越大,用的时间却越多,可能是由于Inc增大时,优化结果较差,靶区剂量和危及器官剂量不能达到目标,进行了反复的优化调整,从而导致计划时间的增加。本文在对照组Inc10°中,发现较小的Inc在危及器官的优化结果上较好,但此时容易导致靶区的目标剂量体积不足,在使用剂量提升Rescale Dose功能进行靶区提量到95%的目标剂量体积后,此时危及器官的剂量优化结果相较于Inc30°的对照组,危及器官受量提高,其优化结果相对较差。在Inc20°时发现,大部分剂量优化结果较好,但大部分器官所受剂量,相较于Inc30°对照组,会呈现下降的趋势。实验组Inc40°中,由于其优化精度相对较低,因此在靶区和危及器官剂量上的优化结果也相对较差。Nithya等[7]对比了食管癌病人使用的4种不同角度优化分组(15°、20°、30°、40°)的靶区及器官剂量学差异,得出越小的Inc优化结果越好,其结论在本文宫颈癌全弧的计划Inc20°、Inc30°、Inc40°三组中成立,这一点与本文结果相似。而本文Inc10°的对照组由于靶区目标剂量的欠缺而优化结果较差,但Nithya等在食管癌患者使用的最小的Inc值为15°,可能是15°与20°的优化角度分组分区数目差异较小,从而其得出Inc越小优化结果越好的结论,因而与本文的部分结果不一致。
在实验组Inc10°中,发现有两组病例靶区剂量D2较高,导致其PTV及危及器官剂量严重偏大。经分析其中一组为乙状结肠部分被PTV所覆盖,而PTV作为靶区,其剂量值较高,乙状结肠剂量此时无法得到有效限制,导致优化结果较差。另一组为部分乙状结肠被当作小肠进行了勾画,乙状结肠离靶区较近,通常被PTV环绕,其D2、Dmean较高,小肠相对于乙状结肠而言位置离靶区稍远,剂量限值通常较小,在包含了乙状结肠作为其体积后,其靶区剂量D2会偏大,当使用小肠的剂量函数再进行限制时,靶区无法进行一个较大的剂量跌落,难以进行限制,导致PTV剂量不足,PTV靶区提量后随之靶区D2较高,其余危及器官受量也随之上升。而Inc20°、Inc30°、Inc40°组中受到勾画错误的影响相较于Inc10°并不大,由此可猜测,Inc越小时,对危及器官优化精度较好,但容易降低部分靶区的目标剂量体积,Inc越小影响越显著。而靶区HI和CI指数在不同角度分组优化下,其值均无统计学差异,证明当Inc变化时,由于靶区是固定的,其剂量线在PTV达到95%的时候,靶区覆盖率较好,其剂量梯度差异较小,所以HI和CI指数没有统计学差异。Inc20°实验组中的D2、D50、CI、HI与对照组相比均不具有统计学意义,但其D2、D50的均值都有减少的趋势,而在部分病人的计划中,会出现D2及D50会出现随着Inc的增大反而略微减小的情况,经分析,这部分异常的病人身体相对瘦小,靶区体积相对较小,此时受Inc的影响也会较小。冯丽娜[14]也对比多种不同类型的病例也指出:靶区越简单,体积越小,受Inc影响越小,相反则受Inc影响越大。
由于宫颈癌病人靶区附近危及器官较多,在计划设计时需要根据病人实际情况选择最重要的器官优先保护,减少临床不良反应。针对宫颈癌术后的病人,其小肠会落入盆腔,且肠道会受粘连,此时小肠是盆腔放疗的主要限制性器官[16]。单从小肠剂量上来看,在考虑宫颈癌术后的病人时,可以选择Inc30°小肠可以得到较低的剂量体积。王利华等[17]指出,满膀胱状态下的小肠V45会比空膀胱状态下的小肠V45的体积减小26%,文献[18-19]也指出,膀胱充盈时能减少小肠受照体积,同时也能降低小肠受到的最大剂量。因此可以通过增加膀胱尿液量,来避免小肠由于高剂量受照体积引起的放射性损伤,同时使用膀胱容量测定,以保证定位和治疗时膀胱尿液充盈程度的一致性[20],提升治疗精度,同时减少小肠的放射性损伤。放射性直肠及膀胱黏膜损伤也是宫颈癌放疗常见的不良反应[21],严重程度与直肠及膀胱接受的高剂量照射体积有关,由文中数据可知,选用Inc30°能得到相对较低的直肠膀胱照射量。另外在Inc20°下,乙状结肠及脊髓受量较低,可以减少乙状结肠放射性肠道损伤及放射性脊髓炎的随机性发生效应,文献[22-23]研究显示,骨盆V20、Dmean可能是宫颈癌放疗患者血液学毒性发生的主要影响因素。由本文数据,骨盆剂量会随着Inc的增大而增加,则骨盆剂量可以在Inc10°下进行计算,观察靶区及危及器官的剂量分布,如骨盆不能得到理想的剂量分布,可以考虑将Inc的数值由10°进行小幅度提升,在保证靶区剂量充足的情况下,以最优的方式将骨盆剂量降低。
因此,笔者在平衡计划设计效率和优化结果下,认为针对常规病人,使用Inc=30°时能得到较好的剂量分布,既能得到临床要求的靶区剂量和危及器官限制,又能提高治疗效率。而针对部分身体状况较差或者靶区体积较大的病人,需要更好的优化精度时,可以选择Inc为20°,以得到更好的剂量分布。

