同种异体骨板联合ETO 在全髋关节翻修中的早期疗效分析*
刘益宏 李杨洋 孔令超 唐魁韩 卢小龙 孙立
在全髋关节翻修中,对股骨假体固定牢靠、股骨髓腔内骨水泥难以取出、术区视野显露困难、股骨近端畸形等难题[1],应用大粗隆延长截骨术(extended trochanteric osteotomy,ETO)可以取得出色的临床疗效。
截骨块的固定方式主要有钢丝、钛缆、大粗隆钢板、记忆合金环抱器等,但以上方法均无法处理较大面积骨缺损,且存在应力遮挡导致局部骨量丢失或应力集中造成继发性股骨骨折等问题。而同种异体骨板具备更接近宿主骨的弹性模量,在填补骨缺损的同时,还可以避免应力集中,降低股骨骨折的发生率。但目前对于使用同种异体骨板固定截骨块的报道较少[2],因此,本研究回顾性收集贵州省人民医院2014年2 月至2019 年2 月行全髋关节翻修,术中应用ETO 技术,并使用同种异体骨板固定截骨块的患者共31 例,对其相关临床资料进行分析报道。
1 资料与方法
1.1 一般资料
本组患者共31 例,其中男17 例,女14 例,年龄37~83 岁,平均63.5 岁。所有患者均为初次全髋关节置换术后,初次置换股骨侧假体类型均为生物型假体。观察组为使用同种异体骨板与钛缆固定截骨块,对照组为仅使用钛缆固定截骨块。
1.2 纳入与排除标准
纳入标准:①行全髋关节翻修术;②翻修原因为假体无菌性松动;③术中应用ETO 技术;④固定方式为同种异体骨板结合钛缆或仅使用钛缆。排除标准:①术中考虑假体周围感染可能;②采用其他固定方式;③随访资料不全;④失随访。
1.3 术前准备
术前常规检查骨盆平片、患侧髋关节正侧位平片、髋关节CT、骨密度,必要时行髋关节3D 模型打印以明确骨缺损类型及程度,行双下肢全长片测量双下肢长度差等;常规检查白细胞、血沉、C 反应蛋白等炎症指标排除感染。
1.4 手术方法
全麻成功后,术区常规消毒铺巾,患者健侧卧位,采用后外侧入路,切开皮肤、皮下、筋膜层,显露并切开关节囊,常规取关节液及假体周围组织送术中冰冻排除感染。内收内旋患侧下肢,脱位髋关节,取下股骨头,清理髋臼及股骨侧增生疤痕及骨组织。股骨侧行大粗隆延长截骨术,截骨起始处位于股骨大粗隆上缘,斜向下方截骨,截骨远端根据术前X 线片规划决定,截骨块宽度约为股骨干周径的1/3,保持后内侧骨膜连续,用拔出器取出股骨柄。髋臼侧以电钻钻孔取出内衬,完整取出臼杯,打磨髋臼,1 g 万古霉素粉末撒至髋臼处,安装臼杯及内衬。股骨髓腔扩髓并试模后,以1 g 万古霉素混合生理盐水稀释至10 mL 注入股骨髓腔内,安装股骨柄,复位截骨块,观察组以同种异体骨板置于股骨干外侧和(或)前侧,骨板远端应超过截骨远端,以钛缆依次从小转子水平捆扎至截骨远端稍远处。对照组以钛缆自小转子水平依次捆扎至截骨终点近端。安装陶瓷球头,复位髋关节,髋关节张力适中,屈髋90°、内旋40°无脱位,截骨块无松动、移位。术区远端放置引流管1 根,逐层缝合。术后即刻C 臂机透视见假体位置良好,压配满意,截骨块无移位,骨板及钛缆固定在位。
1.5 围手术期处理
手术开始前30 min 预防性使用抗生素1 次,若手术时间超过3 h,术中追加使用抗生素1 次,术后常规应用抗生素3 d,必要时可延长至1 周;术后2 d 开始常规使用低分子肝素钙抗凝,配合使用下肢气压静脉泵,预防下肢深静脉血栓形成。术后3 d 内拔除引流管。术后拔除引流管后可扶助行器部分负重,定期复查,视复查情况决定完全负重时间。术后1 个月、3 个月、6 个月、1 年及之后每年定期门诊复查。
1.6 观察指标
所有患者均常规术后即刻复查床旁X 线片,随访定期复查双下肢全长片、骨盆正位及患侧髋关节正侧位X 线片,并与术后床旁X 线片进行比较,同时行Harris 评分、髋关节功能检查,了解髋关节功能、截骨块愈合情况及假体稳定性。X 线片显示截骨处出现桥接骨小梁为截骨块愈合标准。
1.7 统计学方法
采用SPSS 23.0 软件进行统计学处理。计量资料以均数±标准差表示,组间数据对比采用独立样本t 检验,组内数据对比采用配对样本t 检验。P<0.05 为差异有统计学意义。
2 结果
2.1 手术资料
两组患者术中关节液及假体周围组织冰冻检查:中性粒细胞数量均<5 个/高倍镜视野下,可排除假体周围感染;两组患者在年龄、手术时间、术中出血量上,差异无统计学意义,但观察组骨密度值低于对照组(见表1)。
表1 两组患者手术一般资料比较()
2.2 术后资料
患者获得随访12~67 个月,平均33.8 个月。两组患者均在术后3 d 内拔除引流管,14 d 左右伤口常规拆线,愈合良好;随访期间无明显假体松动、截骨块移位、假体周围骨折、假体周围感染等术后并发症。对照组1 例患者术后1年出现髋部疼痛、行走稍受限,服用依托考昔后疼痛缓解,复查X 线片未见明显假体松动、截骨块移位等表现。观察组截骨块愈合时间较对照组明显延长,差异有统计学意义(P<0.05,见表1)。观察组及对照组术前和末次随访Harris评分较术前均明显增加,差异有统计学意义(P<0.05)。两组患者术前Harris 评分组间对比差异无统计学意义,但术后观察组Harris 评分明显优于对照组(见表2)。
表2 两组患者Harris 评分统计(,分)
典型病例:患者,男,65 岁。因右侧髋关节假体无菌性松动行全髋关节翻修术,术中使用ETO 并联合使用骨板(见图1)。
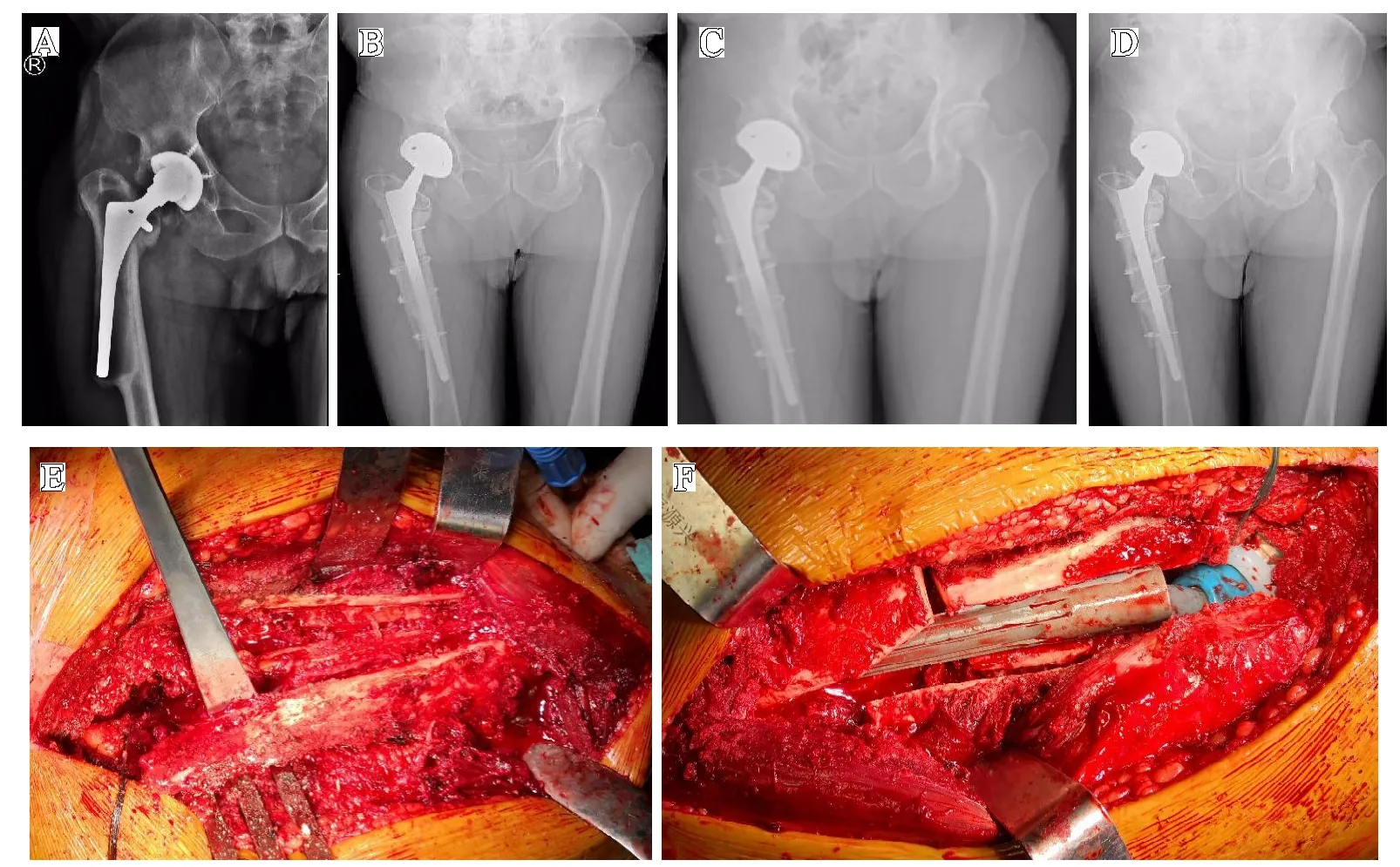
图1 A.术前:股骨柄突出于股骨外侧皮质;B.术后4 个月:截骨线稍模糊、少量骨痂形成;C.术后9 个月:连续性骨痂通过截骨线;D.术后2 年:假体位置良好,骨块完全愈合;E.术中为纠正股骨近端畸形行ETO;F.ETO 后安装股骨假体
3 讨论
3.1 股骨截骨方式的选择
在进行髋关节翻修的时候,我们常发现股骨柄难以取出、股骨髓腔内骨水泥无法彻底清除、手术视野显露不足、股骨近端畸形矫正困难、外展肌力臂需调整等问题,需要使用股骨截骨的方式处理。常用的截骨方式包括:大粗隆延长截骨、大粗隆滑移截骨、纵行劈裂截骨等方式。大粗隆延长截骨术的优点[3]在于充分暴露术区视野、较好地保留大粗隆血供、利于截骨块愈合、可调整外展肌力臂。但在临床应用中,笔者发现可能引发并发症[4],包括截骨块不愈合或延迟愈合、截骨块移位、股骨干骨折等。大粗隆延长截骨术已尽量减少软组织松解,可以保持股外侧肌的完整性以减少对大粗隆部血供的破坏,但仍有一定的截骨块不愈合、延迟愈合的发生率。而且有文献指出[5],翻修时使用骨水泥型股骨假体可能会导致部分骨水泥渗入截骨块与股骨干之间,影响截骨块血供,进而造成截骨块的愈合不良。因此我科在翻修中应用大粗隆延长截骨术时,均选用非骨水泥型股骨柄,且在截骨时保留了截骨块后方骨膜的完整性,可以进一步促进截骨块愈合。截骨块出现松动、移位、下沉等情况,多数因为固定不牢靠所致。在进行股骨截骨的时候,应采用斜形截骨面,增加截骨块与股骨之间的接触面积,必要时还可取自体骨填塞至两者之间的空隙,既可以促进骨的愈合,还能够增大摩擦力,使截骨块取得更好的稳定性。术中股骨干骨折多见于取出与打入股骨假体的时候,分析其原因为股骨经过大粗隆延长截骨后抗扭转力强度降低,且截骨块远端出现明显的“应力台阶”;在打入股骨假体时,可在复位截骨块并且牢靠固定后再安装股骨假体,若患者骨质条件较差,在股骨中远端捆扎钢丝或钛缆可降低术中骨折的发生率。本研究中无1 例患者出现大粗隆延长截骨的并发症,证实该技术具备良好的临床应用价值。
3.2 同种异体骨板的优缺点
在翻修的时候,我们常发现股骨假体周围存在大量骨缺损,应用大粗隆延长截骨术会造成这种趋势的加大,同时截骨后存在截骨块延迟及不愈合的可能。在翻修时使用钢丝、钛缆或钢板固定,由于局部应力集中易导致截骨块或股骨骨折,也会因为应力遮挡致使骨量丢失、截骨块不愈合趋势加剧[6]。而使用同种异体骨板可以将应力分散至骨板与股骨的整个接触面,也由于其具有与宿主骨相近的弹性模量,能够最大限度降低应力遮挡与应力集中的影响,应用于大量骨缺损的情况仍能有较好的临床疗效[7]。同种异体骨板通过增加了对股骨假体的压配力,为假体提供良好的早期稳定性[8],能够帮助患者早期下地进行功能康复。但同种异体骨板存在一定程度的免疫排斥反应,主要表现为伤口持续渗液、伤口延迟愈合、截骨块延迟愈合或不愈合等。随着医疗技术的改进,目前对于同种异体骨板的制备采用深冻技术,在降低免疫原性的同时保留一定的骨强度,因此我们也称同种异体骨板为“生物型钢板”。我们不能仅凭借骨密度值作为骨板的应用依据,更重要的是在术中对股骨骨质进行仔细研判,这对术者提出了更高的要求。同种异体骨板优异的临床效果已经在国内外近期的临床实践中得到验证[9-11],本研究中所有患者均未出现伤口渗液、感染等骨板免疫排斥反应。但本研究中部分患者出现截骨块愈合时间较股骨骨折愈合时间明显延长,分析原因如下[12]:①翻修患者经过多次手术,股骨血供减少;②翻修患者术后康复期较长,患肢完全负重时间晚,股骨所受应力刺激小;③同种异体骨板仍残留轻微免疫排斥反应,影响截骨块愈合。对于上述原因的探索也是笔者下一步研究的方向。
综上所述,同种异体骨板作为良好的生物型固定材料,联合ETO 应用于全髋关节翻修术中,能够恢复骨量、填补骨缺损、加强假体与骨的压配力量,从而提供良好的假体早期稳定性,帮助患者早期下地功能康复,取得较为出色的早期临床疗效,而对于其中远期临床疗效尚需进一步观察。

