美罗培南骨水泥的体外释放研究Δ
毛 璐,王晓雪,刘慧芳,林 平,张伯松
(1.北京积水潭医院药学部,北京 100035;2.中日友好医院药学部,北京 100029;3.北京积水潭医院创伤骨科,北京 100035)
骨感染是骨科医师面对的最具挑战性的疾病之一,因为全身应用抗生素在骨感染局部特别是存在有无血运的骨组织中难以达到有效的治疗浓度[1]。研究结果表明,骨科感染患者中,约49.72%由革兰阴性菌引起,排序居前3位的为铜绿假单胞菌、大肠埃希菌和阴沟肠杆菌。产超广谱β-内酰胺酶的大肠埃希菌和肺炎克雷伯菌检出率分别为54.29%和31.43%,上述细菌对碳青霉烯类抗生素的敏感性>70%[2-4]。研究结果发现,静脉给予美罗培南0.5 g,30~70 min后,美罗培南的骨浓度为其血药浓度的20%,为0.4~5.74 μg/g,给药80 min后,骨组织中几乎测不到美罗培南[5]。有效提高骨感染局部药物浓度,才可能发挥抗感染药的作用[6]。因此,临床尝试将美罗培南加入骨水泥中,用于骨感染的局部治疗,取得了较为满意的疗效[7-8]。但仅为临床个案报道或疗效观察,其释放规律尚不明确。为此,本研究进行美罗培南骨水泥的体外释放研究,观察其释放规律,为临床应用提供参考。
1 材料
1.1 仪器
Quattro PremierXE型三重四极杆质谱仪(美国Waters公司);Acquity UPLC型超高效液相色谱仪(美国Waters公司);电喷雾离子化源(美国Waters公司);Masslynx 4.1数据处理系统(美国Waters公司);美国Milli-Q Advantage A10型超纯水机(德国默克密理博公司)。
1.2 药品与试剂
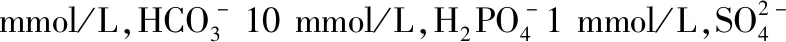
2 方法
2.1 模拟体液中美罗培南的检测方法
2.1.1 标准品及内标溶液制备:精密称取美罗培南标准品,加超纯水稀释获得储备液质量浓度为1 mg/ml,美罗培南-d6对照品内标液质量浓度为40 μg/ml。
2.1.2 线性关系考察、精密度和准确度:精密吸取空白模拟体液950 μl置于1.5 ml离心管中,精密加入含美罗培南储备液50 μl,用空白模拟体液进行等比稀释,分别配制成质量浓度为50、25、12.5、6.25、3.13、1.56、0.78及0.39 μg/ml的标准曲线点。取空白模拟体液加入储备液,配制成质量浓度为1.85、5.55及16.67 μg/ml的低、中及高3个质控样品。样本检测方法参照文献[9],在0.39~50 μg/ml内线性关系良好,线性回归方程为Y=0.223 1X-0.007 8,r2=0.999 4。质控浓度实测值为1.885、5.656及16.967,均在合格范围内。日间和日内标准偏差均<10%,低、中及高3个质量浓度的回收率均>85%。
2.2 体外释放试验
2.2.1 美罗培南骨水泥的制备:于100级层流台内混合含美罗培南10%(W/W)的骨水泥。将定量的注射用美罗培南和聚甲基丙烯酸甲酯骨水泥粉末置于研钵中充分混合,加入骨水泥标配的固化液搅拌,之后灌入不锈钢模具中,制成长度为10 mm、直径为3 mm的圆柱型美罗培南骨水泥药柱,待充分凝固后从模具中取出置入灭菌离心管中。用分析天平测定药柱的质量。
2.2.2 体外释放试验:于装有美罗培南药柱的离心管中加入模拟体液1 ml,放置于37 ℃恒温箱中。采用等距浸出法[10]观察其释放规律,根据文献报道调整时间点[11],分别于5 min,0.5、1、2、8、19、32、50、72、98、128、165、200、242、288、338、392、455、512及578 h,将浸泡的骨水泥药柱取出置于新的1 ml模拟体液中,之前的浸出液为待测液,置于-80 ℃保存待测。
3 结果
自制的美罗培南骨水泥药柱平均质量为(86.16±8.76) mg(n=3),平均美罗培南含量为(7.83±0.80) mg。药物释放时间曲线见图1,累积释药百分率取样时间曲线见图2。测得24 d累计释放率为6.00%,释药峰值出现在2 h,之后释药速率逐渐降低,19 h累计释放量达总释放量的92.37%,72 h可以达到总释放量的98.70%,释药规律数学模型拟合见表1。体外释放符合Weibull方程,r=0.915 1。

图1 药物释放-时间曲线Fig 1 Drug release-time curve
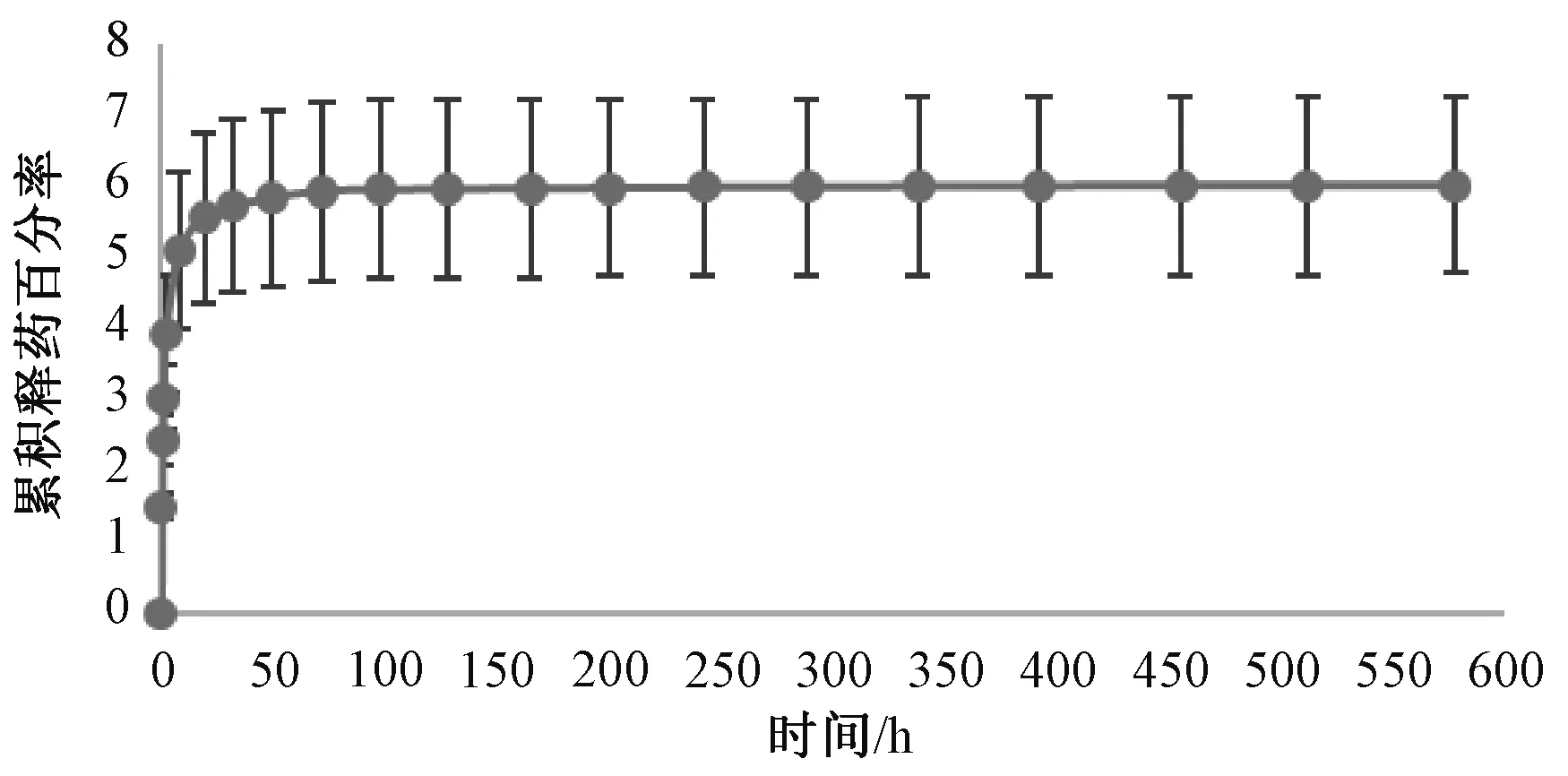
图2 美罗培南骨水泥累积释药-时间曲线Fig 2 Cumulative release-time curve of meropenem bone cement

表1 释药规律的数学模型拟合Tab 1 Mathematical model fitting of the drug-release pattern
4 讨论
4.1 选择美罗培南加入骨水泥的原因
在骨水泥中加入的抗生素要求水溶好、杀菌剂、对组织无毒、固体粉末即粉针剂型、致敏性低、能够覆盖骨感染的病原体以及对热稳定[12-13]。针对革兰阳性菌,国内外比较公认的是加入万古霉素;针对革兰阴性菌,国外多选用氨基糖苷类抗生素,如庆大霉素、妥布霉素等[14]。国内也曾尝试将依替米星粉针剂型加入骨水泥[11],但该剂型已停产,目前国内上市的氨基糖苷类抗生素均为注射液,无法满足要求。氟喹诺酮类药物因其在局部高浓度时表现出较强的细胞毒性而不建议加入骨水泥[15]。头孢菌素和青霉素类抗生素由于致敏性高,不建议加入骨水泥中。碳青霉烯类药物的抗菌谱较氨基糖类及氟喹诺酮类药物广,致敏性低,能够基本覆盖骨感染的常见革兰阴性致病菌及耐药菌。临床常用的碳青霉烯类抗生素有亚胺培南西司他丁和美罗培南。亚胺培南西司他丁是复方制剂,局部应用西司他丁无效,且占用有限的骨水泥载药空间。骨水泥聚合过程中会产热,通常峰值出现在15~17 min,最高温度为62.3 ℃,之后逐渐降低[16]。因此,对于载入的抗生素有一定的热稳定性要求。美罗培南热稳定性优于亚胺培南,在60 ℃条件下放置1~2 d,注射用美罗培南样品降解仅为2%~4%[17]。因此,美罗培南可耐受骨水泥聚合时的短暂高温。Gálvez-López等[18]的研究中,应用微生物法(大肠杆菌)检测美罗培南骨水泥洗脱液的浓度,可以证明加入骨水泥聚合后美罗培南仍可保持抗菌活性。美罗培南较为常见的不良反应包括腹泻、肠道菌群紊乱、肝酶升高、白细胞减少以及神经精神系统不良反应[19]。由于局部应用抗生素骨水泥后全身吸收很少,可以避免全身用药的不良反应[14]。因此,局部使用美罗培南骨水泥有其优势。
4.2 美罗培南加入骨水泥中的剂量
《假体周围感染国际共识》中提及,有将0.5~4 g的美罗培南加入骨水泥(40 g)占位器的报道[20]。矫形骨科将药物加入骨水泥时需要在考虑药物释放的同时考虑强度问题,而创伤骨科抗生素骨水泥无需承重,因此加入的药物可适当增加。有研究将美罗培南分别以1.25%、2.5%、5%及10%的浓度与骨水泥混合测定其体外释放,其中10%混合浓度药物释放最多,时间最长可以达27 d,比5%药物浓度释放增加44.7%[21]。因此,本研究选择美罗培南与骨水泥的质量比为10%(W/W)。
4.3 美罗培南骨水泥的释放量
既往文献报道,5%~10%的美罗培南骨水泥累计释放量为1.2%[21]~2.70%[22]。本次试验中,美罗培南骨水泥24 d累计释放率为6.00%,较其他研究高。分析主要有以下两方面原因:(1)本研究采用的美罗培南骨水泥较文献报道的细小,文献报道的为直径12 mm、长度16 mm的骨水泥柱[21]和直径6 mm、长度12 mm的骨水泥药柱[22],本研究采用直径3 mm、长度10 mm骨水泥柱。体积越大的骨水泥内部的药物释放越困难,由此可以推断,在实际临床使用中,如果自制的美罗培南骨水泥尺寸越大,则整体释放率越低。(2)本研究取样时间早期间隔较文献时间短。由释放曲线可知药物主要在早期快速释放,在此时测定间隔短则形成的漏槽效应更为明显,可以促进药物释放,同时更加接近于植入人体后的真实情况,因植入人体后早期局部引流量大。本研究中观察到在前19 h内释放量达总释放量的92.37%,前72 h可以达到总释放量的98.70%,后期释放量很少。Gálvez-López等[18]研究结果显示,美罗培南骨水泥在第4日及以后较前3 d有明显的洗脱降低,释放的绝大多数药物集中在前3 d,这与本研究观察的结果类似。
4.4 美罗培南骨水泥释放实验的局限性
美罗培南有β-内酰胺环,与不同输液配伍后,随时间延长会发生不同程度的降解,如与复方电解质葡萄糖注射液等输液配伍后8 h,美罗培南的含量降低32.2%~6.2%不等[23];与0.9%氯化钠注射液等4种输液配伍12 h可降解10%~30%不等[24]。既往美罗培南骨水泥释放研究采用的0.9%氯化钠溶液[22]及磷酸盐缓冲液[21]作为洗脱液,均有长时间的浸泡过程,但在分析中未考虑溶剂中美罗培南的降解问题,而实测发现5%、10%美罗培南骨水泥抑菌活性仍至少能维持3周[21-22]。可推测从骨水泥中释放的美罗培南随着取样间隔的延长会在洗脱液中有一定的降解,实际的释放量会较表观释放量高。本研究的洗脱液采用模拟体液,添加有更加丰富的离子,与既往研究相比可以更真实地模拟美罗培南骨水泥在体内的释放环境。本研究能够在一定程度上反映美罗培南骨水泥的释药规律,但美罗培南骨水泥植入体内后是否能维持较长时间的抗菌作用,值得进一步研究。

