Zn-MAF-6 修饰碳糊电极灵敏测定Pb2+的研究
朱 皓,刘 洁,张钱丽
(苏州科技大学 化学与生命科学学院,江苏 苏州 215009)
重金属铅离子具有毒性强、不可生物降解和生物累积性等特点,对神经系统、骨骼造血功能和消化系统均有危害[1]。儿童对铅尤其敏感,研究表明儿童的智力发展水平随Pb 污染程度的加大而下降。日常生活中,人们接触Pb 的途径多种多样,可能来自于土壤、尘埃、被污染的生物体、采矿炼铁及蓄电池等行业排出的废水。
原子吸收光谱法[2]和原子发射光谱法[3]是两种检测Pb2+常用方法,与原子光谱法相比,电化学检测方法不仅灵敏度高,响应快,还具有仪器简单、检测成本低、可发展在线监测等优点[4],因此受到广泛关注。
在电化学检测中,电极是影响检测性能的重要因素。碳糊电极(carbon paste electrode,CPE)由于具有成本低、残余电流小、表面易更新等优点,被广泛用于重金属离子的检测。为提高碳糊电极测定重金属离子的灵敏度和稳定性,研究者还发展了碳糊修饰电极。例如Oularbi 等[5]制备了由一种离子液体、碳纤维和铋颗粒组成的纳米复合材料修饰碳糊电极(BiPs-CNFs/[EMIM]-[NTf2]/CPE)实现了Pb2+和Cd2+的灵敏检测,Pb2+的检出限为0.12 μg·L-1。Moutcine 等[6]采用浸渍法制备了NP-Al2O3粉体,采用循环伏安法和方波伏安法研究了NP-Al2O3/CPE 修饰电极对Pb2+和Hg2+的电化学响应,对Pb2+的检测限为0.76 nmol·L-1。
金属有机框架(Metal organic frameworks,MOFs)是一类由无机金属离子或团簇与有机配体形成的结晶性多孔材料,具有高的比表面积和孔隙率,且孔道结构可调,在气体储存、催化、吸附等领域有广泛应用[7]。金属偶氮类框架材料(Metal azolate frameworks,MAFs)是MOFs 家族中的一个重要分支,有MAF-3、MAF-4、MAF-5、MAF-6 和MAF-32 等异构体,人们对MAF-3、MAF-4 的应用研究比较多,但其孔隙比较小。2015 年He 等[8]系统研究了MAF-6 的合成,表明Zn-MAF-6 是以Zn2+为中心离子簇,与两个2-乙基咪唑配体组成的十二面体三维结构,具有较大的孔隙、较强的憎水性能和良好的稳定性,且具有优异的吸附性能。
笔者成功合成了Zn-MAF-6,并构建Zn-MAF-6/CPE,基于阳极溶出伏安原理,在负电位下富集Pb2+后,用差示脉冲伏安法进行阳极溶出,能够灵敏检测溶液中的Pb2+。Zn-MAF-6/CPE 具有制备简单、灵敏度高、稳定性好和检出限低等优点。
1 实验部分
1.1 试剂与仪器
Zn(OH)2、NH3·H2O、H2SO4、HAc、NaAc、甲醇、甲基硅油购于上海润捷化学试剂有限公司,2-乙基咪唑、环乙烷、石墨粉购于阿拉丁试剂有限公司,药品纯度均为分析纯。
RST5000 电化学工作站(苏州瑞思泰电子有限公司),DHG-9030A 电热恒温鼓风干燥箱(上海精宏实验设备有限公司),ALC-1104 电子天平(德国赛多利斯股份公司),GL21M 高速离心机(长沙湘智离心机仪器有限公司),79-1 磁力加热搅拌器(金坛市科析仪器有限公司)。
1.2 Zn-MAF-6 的制备
Zn-MAF-6 的合成[8]:将新制备的Zn(OH)2(2 mmol)溶于40 mL 浓氨水(25%)中,记为溶液A。将2-乙基咪唑(4 mmol)溶于30 mL 甲醇-环乙烷(6.66%,v/v)的预混溶液中,记为溶液B。将溶液A 快速加入溶液B中,室温搅拌30 min,过滤收集白色沉淀,用甲醇洗涤,60 ℃下真空干燥。
1.3 Zn-MAF-6/CPE 的制备
Zn-MAF-6/CPE 的制备:称取0.38 g 石墨粉、0.012 g Zn-MAF-6 和0.20 g 甲基硅油在玛瑙研钵中充分混合均匀,将得到的碳糊紧实地填充到含铜导线的聚四氟乙烯管的电极孔中(直径为3 mm),用称量纸将电极表面打磨至光滑。纯碳糊电极制作方法和上述方法类似。
1.4 Pb2+的检测
电化学三电极体系:以碳糊修饰电极或碳糊电极为工作电极,Pt 丝电极为对电极,Ag/AgCl 为参比电极。在0.2 mol·L-1NaAc-HAc 缓冲液(pH=4.8)中,于-1.2 V 处搅拌富集200 s,静置20 s,在-0.8~-0.4 V 电位范围用差示脉冲伏安法进行阳极溶出,记录溶出伏安曲线,每个样品测量三次。每次测量后在空白溶液中扫描以活化工作电极。
2 结果与讨论
2.1 材料表征
用XRD 表征Zn-MAF-6 的晶体结构,结果如图1 所示。图1 中曲线a 是文中合成Zn-MAF-6 的XRD衍射图,曲线b 是标准品(购于西安齐岳生物科技有限公司)的XRD 衍射图,由图1 可知两者特征衍射峰位置基本一致,且与文献[8]报道Zn-MAF-6 的XRD 谱图基本一致,表明成功合成了Zn-MAF-6。
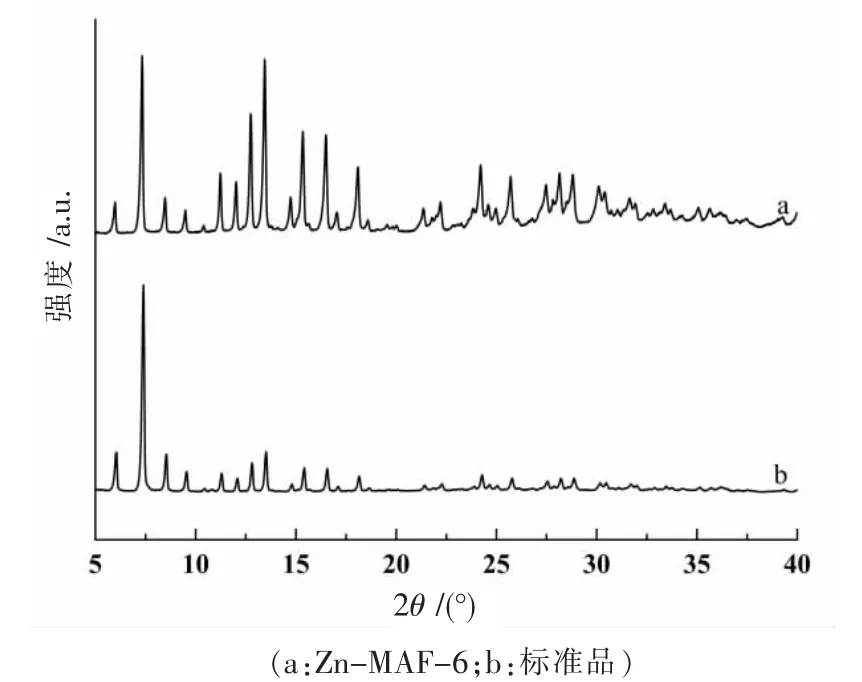
图1 XRD 图谱
图2 为Zn-MAF-6 的傅立叶变换红外光谱图,图2 中2 973 cm-1处的红外吸收对应于咪唑环上烷基取代基的C-H 伸缩振动吸收峰,1 581 cm-1处的红外吸收为咪唑环的骨架振动吸收峰,1 139 cm-1处的红外吸收对应于咪唑环的对称伸缩振动吸收峰,以上结果和文献[9]报道一致。

图2 Zn-MAF-6 的红外光谱图
图3 为Zn-MAF-6 的微观结构用扫描电子显微镜(SEM)表征,图3A 为低倍率下的SEM 图,图3B 为高倍率下的SEM 图。由图3 可知,合成的Zn-MAF-6 为十二面体结构,粒径分布均匀,约为0.8~1.0 μm。

图3 Zn-MAF-6 的SEM 图
2.2 Zn-MAF-6/CPE 的电化学性能
图4A 为Zn-MAF-6/CPE 和CPE 在10 mL 1 mmol·L-1[Fe(CN)6]3-/4-溶液中(底液为0.1 mol·L-1KCl)的循环伏安响应。图4B 为Zn-MAF-6/CPE 和CPE 在0.5 μmol·L-1Pb2+(缓冲底液为0.2 mol·L-1HAc-NaAc pH=4.8)中的溶出伏安图。由图4 可知,在1 mmol·L-1[Fe(CN)6]3-溶液中,Zn-MAF-6/CPE 的伏安响应电流比碳糊电极稍低,这是因为修饰剂Zn-MAF-6 的导电性不高,影响了电化学探针[Fe(CN)6]3-在Zn-MAF-6/CPE表面的电子传输。在0.5 μmol·L-1Pb2+溶液中,Zn-MAF-6/CPE 的溶出响应却大大高于碳糊电极,约为碳糊电极的5 倍。Zn-MAF-6 是富含N 元素的金属偶氮类框架材料,Zn-MAF-6/CPE 在含Pb2+溶液中负电位下富集时,除了碳糊电极上聚集的负电荷对Pb2+产生静电引力外,N 原子上的孤对电子也会对Pb2+产生静电引力,此外Zn-MAF-6 的特殊多孔结构为吸附Pb2+提供了更多的活性位点,基于以上原因Pb2+在修饰电极表面的富集效果增强,Pb2+在Zn-MAF-6/CPE 上的溶出峰电流大大增加。
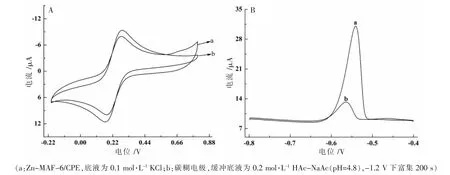
图4 1 mmol·L-1 Fe(CN)63-/4-溶液的循环伏安图(A)和0.5 μmol·L-1 Pb2+的溶出伏安曲线(B)
2.3 Zn-MAF-6/CPE 测定Pb2+
2.3.1 实验条件优化
缓冲溶液pH 值是影响Zn-MAF-6/CPE 测定Pb2+的重要因素。pH 值过低,修饰剂Zn-MAF-6 中吸附Pb2+的活性位点可能会质子化而不利于Pb2+的吸附富集;pH 值较高时,Pb2+可能会发生水解。笔者选择HAc-NaAc 缓冲溶液在pH=3.6~5.6 范围内探究pH 值对Pb2+测定的影响(如图5 所示)。由图5 可知,Pb2+溶出峰电流在低pH 值溶液中随着pH 值的增加而增大,当溶液的pH 值大于4.8 时,溶出峰电流值开始逐渐减小。主要是因为pH 值较低时,修饰剂Zn-MAF-6 中配体发生质子化,与Pb2+有静电排斥作用,影响了Pb2+在电极表面的富集;随着pH 值增加,溶液中OH-会使Pb2+水解。后续实验选择pH=4.8 的HAc-NaAc 为缓冲底液。
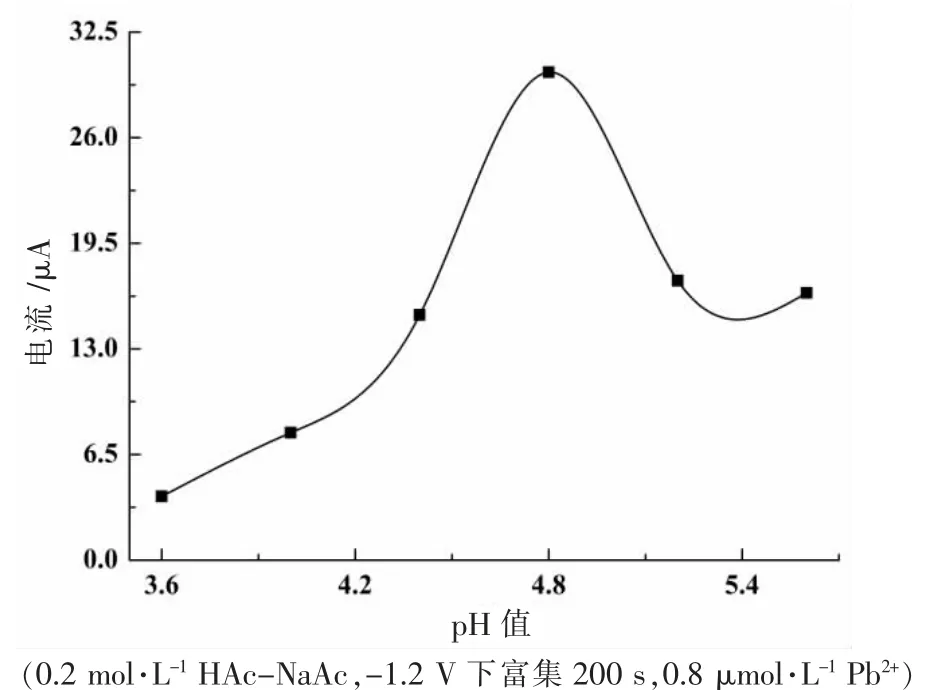
图5 缓冲底液pH 值的影响
在溶出伏安分析中,富集电位和富集时间是影响测定灵敏度的重要参数。在0.8 μmol·L-1Pb2+溶液中控制富集时间100 s,探究富集电位对峰电流的影响(图6A)。富集电位在-1.2~-0.9 V 范围内,溶出峰电流随着富集电位负移快速增大;当富集电位负于-1.2 V 时,溶出峰电流反而随着富集电位负移而减小,可能是因为在很负的富集电位下,电极表面逐渐开始发生析氢反应,抑制了Pb2+在电极表面的富集。图6B 是在0.8 μmol·L-1Pb2+溶液中控制富集电位为-1.2 V,富集时间对Pb2+溶出峰电流的影响,结果表明富集时间小于200 s 时,溶出峰电流随着富集时间的增加快速增大,当富集时间大于200 s 后,Pb2+溶出峰电流的增大趋势变缓。综合考虑检测灵敏度和检测速度,笔者后续实验选择在-1.2 V 下富集200 s。

图6 富集电位(A)和富集时间(B)的影响
2.3.2 线性范围和检测限
Zn-MAF-6/CPE 在不同浓度的Pb2+溶液中,于-1.2 V 处富集200 s 后溶出伏安曲线如图7A 所示,由图7可知Pb2+的溶出峰电流随浓度的增加而线性增大,图7B 为线性回归曲线。

图7 Zn-MAF-6/CPE 测定Pb2+的溶出伏安曲线(A)和线性曲线(B)
Zn-MAF-6/CPE 测定Pb2+的线性范围是0.1~1.0 μmol·L-1,线性回归方程Ip=63.05c-8.86(R2=0.99),检测灵敏度为63.05 μA/(μmol·L-1),检出限为2.35 nmol·L-1(S/N=3)。表1 列出了文章方法和文献报道的修饰电极方法测定Pb2+的线性范围和检测限,表明文章方法在线性范围和检测限方面均有可比性。对0.5 μmol·L-1Pb2+的溶液进行10 次连续测定,溶出峰电流相对标准偏差(RSD)为2.37%,表明Zn-MAF-6/CPE 测定Pb2+具有较好的稳定性。

表1 修饰电极测定Pb2+的线性范围和检出限
2.3.3 干扰实验
选择常见的阳离子为干扰离子,用0.5 μmol·L-1Pb2+的溶液试验干扰离子的影响,结果如图8 所示。由图8可知,100 倍的Cd2+、K+、Al3+、Fe3+、Zn2+和Co2+对Pb2+测定没有明显干扰(溶出峰电流超过±5%为有明显干扰),表明Zn-MAF-6 修饰电极测定Pb2+有一定的抗干扰能力。
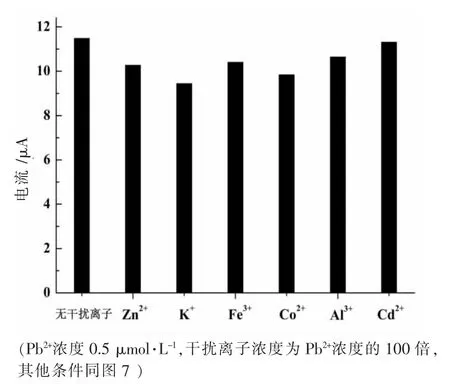
图8 干扰离子对Zn-MAF-6/CPE 测定Pb2+的影响
2.4 实际样品分析
取1 mL 河水,用45 μm 的水系滤膜进行过滤,加入9 mL 的0.2 mol·L-1NaAc-HAc(pH=4.8)中,插入三电极体系,记录Pb2+的溶出伏安曲线,结果表明该水样中未检出Pb2+。在水样中加入Pb2+标准溶液,进行加标回收实验,结果列于表2 中。Pb2+的回收率为92.3%~103.5%,表明Zn-MAF-6/CPE 可用于实际样品中Pb2+的检测。
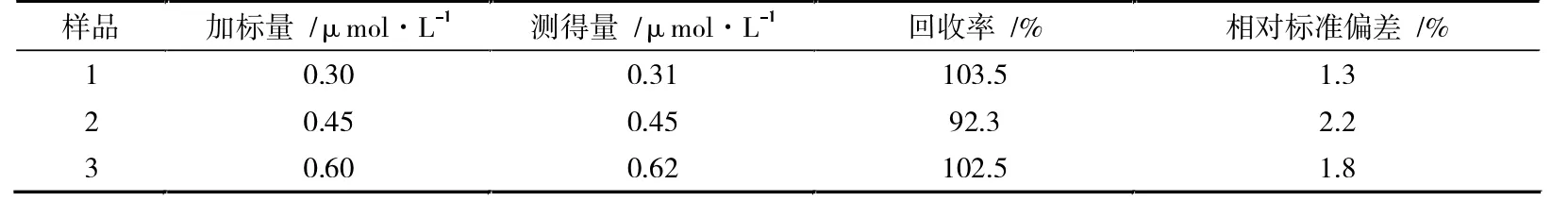
表2 加标回收实验
3 结语
用快速沉淀法成功合成了金属偶氮框架材料Zn-MAF-6,制备了Zn-MAF-6/CPE,基于阳极溶出伏安原理,构建了一种灵敏、快速、稳定的Pb2+电化学传感器。在0.2 mol·L-1HAc-NaAc 缓冲底液(pH=4.8)中于-1.2 V 处富集200 s,溶出伏安峰电流和Pb2+浓度在0.1~1.0 μmol·L-1范围内呈良好的线性关系,检测灵敏度和检出限分别为63.05 μA/(μmol·L-1)和2.35 nmol·L-1(S/N=3)。该修饰电极对环境样品中常见阳离子具有良好的抗干扰能力,用于河水中的Pb2+测定时加标回收率理想,该Pb2+传感器的构建为环境样品中Pb2+的检测提供了新的思路。

