布地奈德福莫特罗吸入剂治疗40例中重度慢性阻塞性肺病患者的临床疗效
邓丽娟 俞金梅 彭志群


摘 要 目的:分析布地奈德福莫特罗吸入剂治疗中重度慢性阻塞性肺病的临床疗效。方法:选取中重度慢性阻塞性肺病治疗的80例患者随机分为观察组(n=40)和对照组(n=40),观察组采用布地奈德福莫特罗吸入剂治疗,对照组采用乌美溴铵维兰特罗吸入粉雾剂治疗,对比两组患者咳嗽、气促、肺功能等疗效评分,睡眠、呼吸等生活质量评分,以及不良反应发生率。结果:观察组疗效和生活质量评分均高于对照组,不良反应发生率低于对照组(P<0.05)。结论:布地奈德福莫特罗吸入剂对中重度慢性阻塞性肺病患者疗效显著,可提高患者生活质量,减少不良反应发生率。
关键词 慢性阻塞性肺病 布地奈德福莫特罗吸入剂 疗效 生活质量
中图分类号:R974.3; R563 文献标志码:B 文章编号:1006-1533(2021)09-0023-03
Clinical efficacy of budesonide and formoterol in the treatment of 40 patients with moderate to severe chronic obstructive pulmonary disease
DENG Lijuan*, YU Jinmei, PENG Zhiqun
(Department of Geriatrics, the Peoples Hospital of Yingtan, Jiangxi Yingtan 335000, China)
ABSTRACT Objective: To analyze the clinical efficacy of budesonide and formoterol in the treatment of moderate to severe chronic obstructive pulmonary disease (COPD). Methods: Eighty patients with moderate to severe COPD were randomly divided into an observation group (n=40) and a control group (n=40). The observation group was treated with budesonide formoterol inhalation while the control group with umebromide and vilanterol inhalation powder. The scores of cough, shortness of breath, pulmonary function and so on and the incidence of adverse reactions were compared between the two groups. Results: The scores of curative effect and the quality of life were higher while the incidence of adverse reactions was lower in the observation group than the control group (P<0.05). Conclusion: Budesonide and formoterol inhalation has a significant effect on patients with moderate to severe COPD and can improve the quality of life and reduce the incidence of adverse reactions.
KEy WORDS chronic obstructive pulmonary disease; budesonide and formoterol inhalation; therapeutic effect; quality of life
慢性阻塞性肺病以不完全可逆的氣流受限为特征,临床主要表现为慢性咳嗽、咳痰、气短以及呼吸困难,不仅会对患者的呼吸功能造成损害,还会影响循环功能系统,情况严重时可威胁患者生命[1-2]。本文研究布地奈德福莫特罗吸入剂对中重度慢性阻塞性患者的临床治疗效果、生活质量评分以及不良反应发生率,报道如下。
1 资料与方法
1.1 一般资料
选取我院2017年9月—2019年12月接受中重度慢性阻塞性肺病治疗的80例患者,采用随机数字抽样法划分为观察组和对照组各40例。观察组:男25例,女15例,年龄55~70岁,平均年龄(62.84±3.85)岁,病程5~35年,平均病程(28.51±4.81)年;对照组:男24例,女16例,年龄56~71岁,平均年龄(63.17±3.62)岁,病程6~35年,平均病程(28.78±4.35)年。两组患者一般资料对比无明显差异,具有可比性(P>0.05)。
1.2 纳入和排除标准
纳入标准:在调查开始前1~2周未使用皮质激素者;中重度慢性阻塞性肺病者[3]。
排除标准:对相关治疗药物过敏者;沟通交流严重障碍者;不积极配合相关调查者[4]。
1.3 治疗方法
对照组采用乌美溴铵维兰特罗吸入粉雾剂治疗(商品名:欧乐欣,Glaxo Group Limited),经口吸入,每次吸入62.5 μg/25 μg,每天1次,上午9点用药,维持支气管的扩张作用。年龄在65岁以上、轻中度肾功能不全、轻中度肝功能不全等患者不需要对剂量进行调整。疗程3个月。
观察组采用布地奈德福莫特罗吸入剂治疗(商品名:信必可都保,AstraZeneca AB),经口吸入,每次吸入320 μg/9 μg,每天2次。剂量可根据患者的病情控制情况来进行调节;老年患者不需对吸入剂量进行调整[5-6]。疗程3个月。
1.4 观察指标
治疗后,观察两组患者疗效评分、生活质量评分和不良反应发生率。
1)咳嗽、气促、肺功能等方面疗效评分 采用自制评分表,由患者进行打分,分数在1~100分之间,分数越高,说明该种药品治疗效果越好。
2)睡眠、呼吸等方面生活质量评分 采用自制评分表,分数在1~10分之间,分数越高,代表此种药物对生活质量的提高效果越好。
3)口干、咽部不适、口腔霉菌感染等不良反应发生率。
1.5 统计学分析
2 结果
2.1 疗效评分对比
治疗后,观察组疗效评分高于对照组,差异具有统计学意义(P<0.05,表1)。
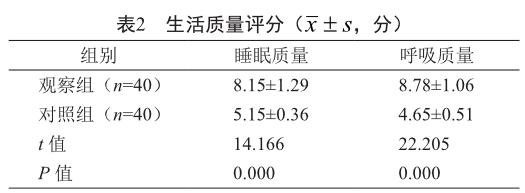
2.2 生活质量评分对比
治疗后,观察组生活质量评分高于对照组,差异具有统计学意义(P<0.05,表2)。
2.3 不良反应发生率对比
治疗后,观察组不良反应发生率低于对照组,差异具有统计学意义(P<0.05,表3)。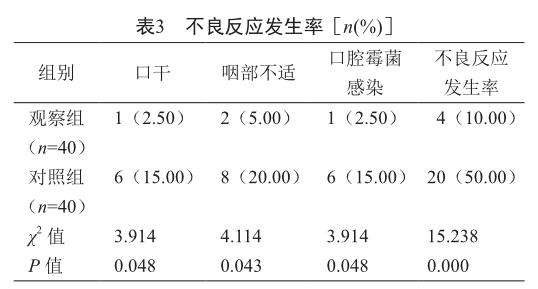
3 讨论
目前对慢性阻塞性肺病确切的病因大致可以分为环境和个体两方面的因素[7]。环境因素包括空气污染、吸烟以及呼吸道感染等方面;个体因素包括遗传、肺发育生长不良等方面。中重度患者的咳嗽、咳痰、氣短的症状会随着时间的发展愈来愈重,给患者的身体和心理都产生了很大的影响。此病的发病机制是以炎症为核心,因此抗炎治疗是其最主要的治疗手段。
乌美溴铵维兰特罗吸入粉雾剂是乌美溴铵与维兰特罗组成的复方制剂,乌美溴铵是长效毒蕈碱受体拮抗剂,主要通过竞争性抑制乙酰胆碱与呼吸道平滑肌上M3型毒蕈碱受体的结合而发挥支气管扩张作用,具有长效支气管扩张作用,适用于慢性阻塞性肺病的长期维持治疗。布地奈德福莫特罗吸入剂含有福莫特罗和布地奈德2种成分,其中福莫特罗是一种长效b2受体激动剂,具有舒张呼吸道平滑肌痉挛,促进纤毛运动,抑制炎症介质释放的作用;布地奈德是一种吸入糖皮质激素,可以减轻患者平滑肌的收缩反应,抑制气道的重塑。福莫特罗和布地奈德有相互协同的作用。本研究发现,使用布地奈德福莫特罗吸入剂的患者疗效和生活质量评分均高于使用乌美溴铵维兰特罗吸入粉雾剂,且不良反应发生率更低(P<0.05),与宋淑华等[8]的研究相符。
综上所述,布地奈德福莫特罗吸入剂对于中重度慢性阻塞性肺病患者的咳嗽、气促、肺功能等症状治疗效果作用明显,减轻了患者的发病痛苦,有利于改善其睡眠和呼吸功能,提高生活质量,减少不良反应的发生率。
参考文献
[1] 许朝霞. 信必可都保联合孟鲁司特治疗中、重度慢性阻塞性肺病疗效及安全性[J]. 航空航天医学杂志, 2019, 30(7): 832-833.
[2] 褚婉婷, 杜丽娟. 信必可都保用于治疗慢性阻塞性肺病的效果分析[J]. 医药前沿, 2019, 9(11): 76-77.
[3] 栗娜. 信必可都保配合思力华治疗我院81例严重支气管哮喘伴有慢性阻塞性肺疾病患者的临床疗效研究[J]. 湖南师范大学学报(医学版), 2018, 15(1): 113-116.
[4] 牟方红, 牟沧浪. 信必可都保联合多索茶碱对慢性阻塞性肺疾病患者肺功能及血气指标的影响[J]. 中国临床医生杂志, 2018, 46(9): 1034-1037.
[5] 王荣宝, 杨翠萍, 祝晶. 补肺纳肾平喘方联合信必可治疗哮喘—慢性阻塞性 肺疾病重叠综合征[J]. 吉林中医药, 2019, 39(2): 212-215.
[6] 秦长月. 信必可联合无创呼吸机治疗慢阻肺的应用价值分析[J]. 中国医疗器械信息, 2019, 25(24): 110-111.
[7] 黄壮志, 谭世繁, 陈春杰, 等. 信必可联合气道正压通气治疗慢性阻塞性肺疾病(COPD)合并睡眠呼吸暂停综合征患者疗效及安全性[J]. 吉林医学, 2019, 40(12): 2807-2809.
[8] 宋淑华, 王洪. 信必可都保联合无创通气对老年慢性阻塞性肺疾病合并呼吸衰竭患者的影响[J]. 中国医药指南, 2019, 17(17): 20-21.

