核桃仁中总糖的测定与评价
◎ 廖小丽,张洺榛
(1.武汉海关技术中心,湖北 武汉 430000;2.湖北江晓环保科技有限公司,湖北 武汉 430000)
核桃是胡桃属植物,与腰果、扁桃和榛子有世界著名“四大干果”之称。近年来,随着核桃的大量种植,核桃早已普及在家家户户,并得到了不同方式的利用。核桃的果实主要由核桃种皮、核桃种壳、核桃仁三大部分组成,由于实际生产需要,核桃的种皮和种壳无法食用,所以核桃仁成为了人们的关注重点。核桃仁的含油量高达60%,蛋白质含量也能够达到12%左右,并且富含钙、铁等微量矿物元,还有多种维生素,能够满足广大人群的食用和保健要求,是一种滋补佳品,深受人们的喜爱。随着人们对于生活质量要求的不断提高,对于很多食品的要求不再仅仅停留在最基本的饱腹层面,而更加关注其利用价值和一些营养组分的含量,也正是由于这一重大转变,使人们对于核桃仁的组分关注度逐渐提升[1]。
糖类作为人类生活中不可或缺的一个部分,但是不同糖类对于人体能够产生不同的作用,而人们根据自身需求对于不同糖类需求量和使用量有所差异,所以对于核桃仁中的糖类含量的直接测量可以有效加速产品品牌化以及各种基本参数的积累[2],同时也可以作为核桃品质的重要标准之一,对于核桃本身来说有着非常多的可研究路线和利用价值。本文通过3,5-二硝基水杨酸法配合相关合适的预处理方法对核桃仁中的总糖进行了有效测定,从而为核桃仁所含糖类的测定提供一定的技术参考。
1 材料与方法
1.1 材料与试剂
选取样品未当年新摘未变质的核桃仁样品,经过恒温(60 ℃)烘干处理,含水量低于2%。
3,5-二硝基水杨酸、丙三醇、氢氧化钠、盐酸及石油醚,均为分析纯,上海国药集团生产;葡萄糖,分析纯,上海阿拉丁生化科技股份有限公司生产;实验用水为实验室三级水。
1.2 仪器与设备
E7221型紫外可见分光度计、me2041型电子天平(感量0.0001 g)、SZF-06C型粗脂肪测定仪、HH-S1型恒温水浴锅。
1.3 溶液配制
(1)葡萄糖标准溶液的配制。准确称取5 g葡萄糖固体,充分溶解后定容至100 mL;再从定容后的试剂中准确量取1 mL溶液定容至100 mL,从而得到1 mg·mL-1的葡萄糖标准溶液。由于直接称取0.1 g的葡萄糖定容至100 mL过程性误差较大,所以采用逐级稀释的方法可以有效减小误差,同时可以将前者作为标准储备液进行保存,方便后续的相关测量和使用。
(2)3,5-二硝基水杨酸溶液(DNS溶液)的配制。溶液1:准确称取6.3 g 3,5-二硝基水杨酸固体,再加入2 mol·L-1的氢氧化钠溶液362 mL,将以上溶液混匀后再加入0.5 g结晶酚。溶液2:溶解0.075 g的亚硫酸钠固体,再分别称取2.5 g氢氧化钠和50 g的酒石酸钾钠充分混匀在一起[3]。溶液1和溶液2配制好以后,将其混匀后定容至500 mL,得到标准的3,5-二硝基水杨酸溶液,也就是本实验的显色剂。由于该试剂加入溶剂较多,所以配制相对复杂,所以需要掌握好配制顺序和配制要求。其中,结晶酚由于是固态且密度较大,可以在60℃溶解后取液体进行称量,称取0.5 g结晶酚进行混溶[4]。
(3)浓盐酸溶液的配制。将原盐酸用水1∶1稀释后即可得到6 mol·L-1的盐酸使用液。
(4)氢氧化钠溶液的配制。称取50 g氢氧化钠,定容至500 mL,进而得到10%(W/V)的氢氧化钠溶液,用于pH的调节[5]。
1.4 样品预处理
1.4.1 索氏除油
由于核桃仁样品中含有大量的油脂,当油脂含量过高,不仅会影响实验的精密度和准确度,还会由于油脂的非水溶性导致整体的样品浑浊,使介质不均一,最后导致结果出现较大的误差。通过差量法对含油率和含水率进行有效测定,由于该实验不具体计算含油、水量,故将其作为一个指标进行测定,含油、水总量=(索氏前总质量-索氏后总质量)/样品质量×100%,结果保留两位小数。
1.4.2 总糖的水解
核桃仁除了含有可溶解的还原糖之外,还含有淀粉、纤维素等不易水解的总糖,所以测定时要对核桃仁进行水解处理成为能够被检测的糖,将总糖水解生成原糖。将样品研磨之后,称取2 g的核桃样品,经过索氏提取后去除里面的油脂,充分测定其含油量之后,从已经索氏提取中的样品再称取0.5 g,用15 mL水溶解,再加入10 mL的6 mol·L-1的浓盐酸溶液,在100 ℃的水浴条件下水解30 min。
1.4.3 调节pH
由于在进行总糖水解的过程中加入的盐酸是过量的,所以会有残余的盐酸使整体pH偏低,所以此时需要用10%的氢氧化钠溶液进行pH的调节,一方面中性是一个较好的显色环境,使形成的物质方便被测量,另一方面在测量时,强酸性溶液会对人体和仪器造成一定的损害。用10%氢氧化钠将溶液pH调节至中性(7~8)后,减压抽滤后反复洗涤5遍,定容至250 mL,准备待测。
1.5 上机测定
将1 mL的样品置入玻璃试管中,加入1 mL DNS溶液,将玻璃试管沸水浴5 min后取出,在室内环境下冷却至室温后加入8 mL水,混匀后在540 nm处进行测定。
2 结果与分析
2.1 标准曲线绘制
配制浓度为1 mg·mL-1的标准溶液,取6支试管,分别加入0.0 mL、0.2 mL、0.4 mL、0.6 mL、0.8 mL和1.0 mL标准溶液,用80%的乙醇补至1.0 mL,再分别加入0.5 mL 8%香草醛溶液和5 mL 77%硫酸溶液,然后在540 nm下采用紫外可见分光度计测定,以吸光度为纵坐标,以糖浓度为横坐标绘制标准曲线,结果如图1所示。由图1可知,标准曲线方程为y=1.355 6x-0.004,线性相关系数为0.999 8。
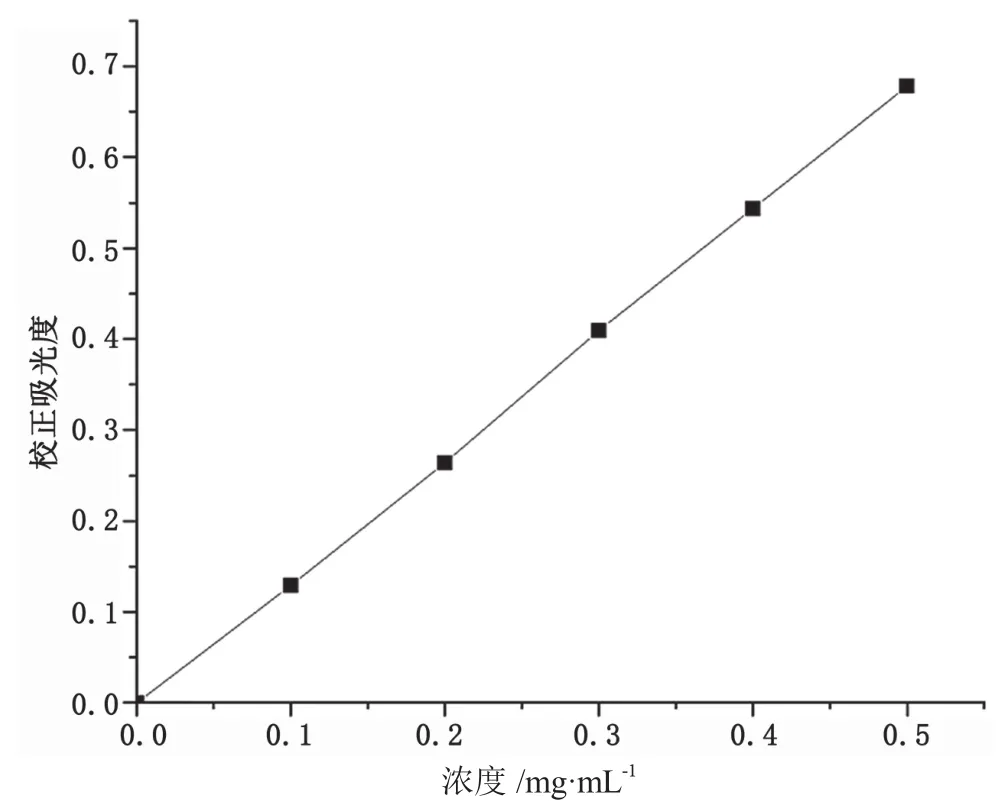
图1 葡萄糖标准曲线图
2.2 样品浓度区间估算
通过前期实验,对样品浓度的不断确定和稀释,可以初步确定核桃仁中的总糖含量在8%~12%,进而可以有效判定将含有0.5 g的样品溶液稀释至200~500 mL为宜,故前期设置的250 mL为合适的稀释体积。
2.3 核桃仁中总糖含量的测定
按照前期实验步骤进行实验,称取样品2.0 g左右,其含水量在65.9%~67.3%,在测定时,称取脱油脱水样品0.2 g左右,测定样品吸光度分别为0.403 8、0.379 9、0.401 1,带入标准方程y=1.355 6x-0.004,得到浓度分别为 0.300 8 mg·mL-1、0.283 2 mg·mL-1、0.298 8 mg·mL-1,换算成样品中总糖含量为12.08%、12.01%、12.00%。具体测定原始数据见表1。
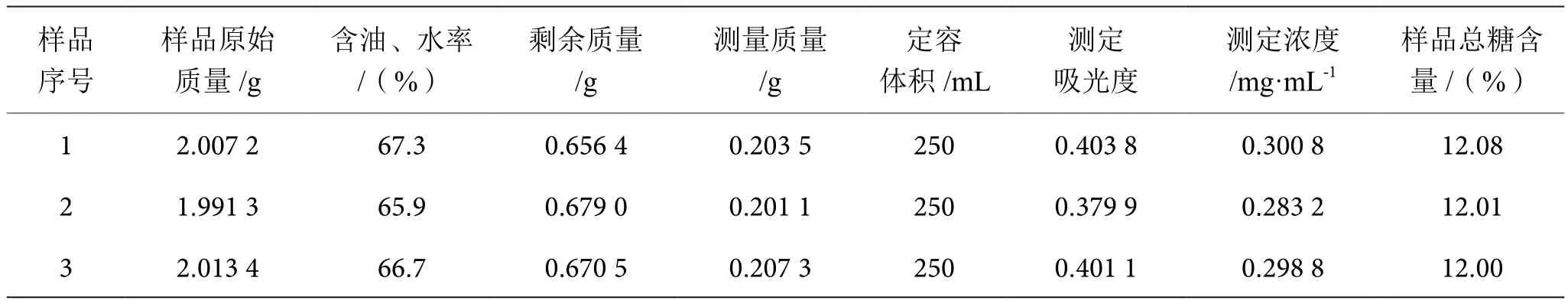
表1 原始数据表
2.4 精密度试验
通过对测试结果的相对平均偏差进行计算,Rd=0.91%,故该实验精密度为0.91%,符合相关测定要求。
3 结论
通过使用3,5-二硝基水杨酸法来测定核桃仁总糖的方法,也同样适用于测定核桃仁中还原糖的含量,由于该方法相对于蒽酮-硫酸法来说,使用的试剂更为温和,实验安全性能高。同时,该方法兼具重现性好、稳定性好、测定速率高等诸多优点,可以作为日常测定核桃仁中糖类的测定方法,同时在后期实验中也要注意对于油脂的处理,防止油脂影响实验结果。
该方法测定核桃中总糖含量,标准曲线方程为y=1.355 6x-0.004,线性相关系数为0.999 8,满足试验要求,测定精密度为0.91%,也符合化学分析的相关要求。通过此次实验,可以更了解核桃仁中的含糖量和测定核桃仁糖类的时候需要注意的事项,为后续的相关研究提供了一些借鉴性的依据,同时为基础数据的不断积累提供了有效途径。

