响应面法优化复方降脂片的成型性工艺及其降脂活性
张荣榕,马馨桐,王 苗,张红印,衣春光,严铭铭,4,*,赵大庆,*
(1.长春中医药大学吉林省人参科学研究院,吉林长春 130117; 2.长春中医药大学药学院,吉林长春 130117; 3.长春中医药大学基础医学院,吉林长春 130117; 4.吉林省中药保健食品科技创新中心,吉林长春 130117)
复方降脂片由三七、丹参、荷叶、山楂四味药材组成,其中荷叶具有祛湿化浊降脂的功效,山楂、丹参配伍使用具有消食化瘀降脂功效,三七具有良好的活血化瘀、健脾益气、通脉活络功效[1-2]。在中国,山楂、荷叶作为药食同源药材有长期食用的历史;丹参、三七长期应用于中医临床,且目前收录于卫生部公布的《可用于保健食品的物品目录》。以上四味药材相辅相成,具有化痰湿、畅气血之功效,且三七-丹参、丹参-山楂均为中医临床用药的常用药对,其中,丹参、山楂搭配食用降“三高”亦有良好口碑[3-6]。有研究表明丹参-山楂-三七常以角药形式存在,具有很好的调节血脂作用,故本研究以三七、丹参、荷叶、山楂四味药材为原料药,辅以相应辅料,将其开发成具有祛湿化浊降脂、畅气血之功效的保健食品。
片剂具有剂量准确、质量稳定、产量大、成本低、生产工艺简单、易于控制、卫生标准易于达到、在运输和储存过程中比较稳定、消费者携带和食用方便等优势,在保健食品、食品领域均有广泛应用[7]。为了更好地开发利用复方降脂方,本课题组将其开发成方便、稳定的中药片剂。课题组前期已确定复方降脂方的提取工艺,该法所制得的干浸膏粉吸湿性较强,易黏结成块,因此本文将采用Box-Behnken响应面法对复方降脂片的辅料配方及成型工艺进行优化,以改善浸膏粉的吸湿性,将其开发成质量可控、性质稳定的中药片剂。同时,使用高脂模型大鼠对复方降脂片降脂活性进行初步研究,旨在研制出一种口感适宜、风味独特,具有良好降脂活性的复方降脂片,为其后续深入研究、开发及生产应用提供可靠的理论依据。
1 材料与方法
1.1 材料与仪器
复方降脂提取物干粉 自制;羧甲淀粉钠 湖州展望药业有限公司,批号20171236;微晶纤维素 湖州展望药业有限公司,批号20171239);硬脂酸镁 安徽山河药用辅料股份有限公司,批号180229;乙醇 北京化工厂,批号20171013;阳性对照药辛伐他汀 山东罗欣制药厂;TC、TG、LDL-C、HDL-C、ALT、AST测定试剂盒 南京建成生物工程研究所(中国江苏南京);所有其他化学品 均为分析纯;Wistar大鼠 体重(180±10) g,雄性,购于长春亿斯实验动物技术有限责任公司,生产许可证号SCXK(辽)2016-0003,合格证号No.201700017184;动物实验环境 吉林省长春中医药大学药学实验楼SPF级动物实验室,设施使用许可证号SYXK(吉)2010-0059;在动物室中适应7 d,在12 h光暗循环下,将它们保持在受控的环境温度(24±2) ℃和湿度60%±10%下;随意获取水;动物方案经长春中医药大学动物伦理委员会批准(吉林长春)[批准号:20171011]。
TDP-1.5单冲压片机 上海嘉展仪器设备有限公司;YD-1片剂硬度测试仪 天津天光光学仪器有限公司;CS-2脆碎度测定仪 天津市光学仪器厂;BJ-2崩解时限测定仪 天津市国铭医药设备有限公司;CP223C电子天平 奥豪斯仪器有限公司;DZF-6050真空干燥箱 上海一恒科学仪器有限公司;ALB-224万分之一分析天平 德国赛多利斯公司;Agilent1260高效液相色谱仪 美国Agilent公司;AB265-S十万分之一分析天平 瑞士梅特勒托利多公司;KQ-250DB型数控超声波清洗器 昆山市超声仪器有限公司;UB-7 pH计 Denver Instrument;UV-1700紫外可见分光光度计 日本岛津仪器有限公司。
1.2 实验方法
1.2.1 复方降脂提取物的提取工艺 按处方称取荷叶3 g、山楂3 g、丹参2.5 g、三七1.5 g,将以上四味药材加水煎煮,浓缩得到复方降脂提取物。
1.2.2 复方降脂片的制备工艺 按比例精密称取主药、微晶纤维素及羧甲基淀粉钠,混合均匀后过80目筛,添加润湿剂制备软材,14目筛制备颗粒,55 ℃真空干燥箱干燥,16目筛整粒,收集颗粒,加入1.0%硬脂酸镁,混合均匀,即可压片,控制片剂硬度在8~10 kg。
1.2.3 单因素实验
1.2.3.1 主药与填充剂比例的确定 按中药汤剂服用量及复方降脂提取物的出膏率,结合预实验结果,确定复方降脂提取物添加量为65%~85%(相当于片重为1.0 g的复方降脂片中0.65~0.85 g复方降脂提取物)。以主药:填充剂分别为65∶30、70∶25、75∶20、80∶15、85∶10进行单因素实验,固定崩解剂用量为4.5%,润湿剂为75%乙醇。以颗粒成型性、片剂崩解时限及脆碎度为评价指标确定复方降脂片主药与填充剂的比例。
1.2.3.2 崩解剂用量的确定 通过预实验确定羧甲基纤维素钠作为复方降脂片的崩解剂,固定主药与填充剂的比例为80∶15,润湿剂为75%乙醇,以崩解剂的添加用量分别为4%、4.5%、5%、5.5%及6.0%进行单因素实验。以颗粒成型性、片剂崩解时限及脆碎度为评价指标,确定复方降脂片崩解剂的添加量。
1.2.3.3 乙醇浓度的确定 通过预实验确定乙醇作为复方降脂片的润湿剂,固定主药与填充剂的比例为80∶15,崩解剂的添加量为5%,分别以50%、60%、70%、80%及90%浓度的乙醇为润湿剂进行单因素实验。以颗粒成型性、片剂崩解时限及脆碎度为评价指标,确定复方降脂片润湿剂的浓度。
1.2.4 响应面试验设计 为了获得载药量大、崩解时限适宜、脆碎度合格的片剂,设计响应面试验对主药与填充剂比例、崩解剂用量及润湿剂用量进行了进一步的优选,以期获得最佳成型性工艺参数。根据Box-Behnken的中心组合试验设计原理,采用三因素三水平的响应面设计法(见表1),确定复方降脂片的最佳提取工艺条件[8]。
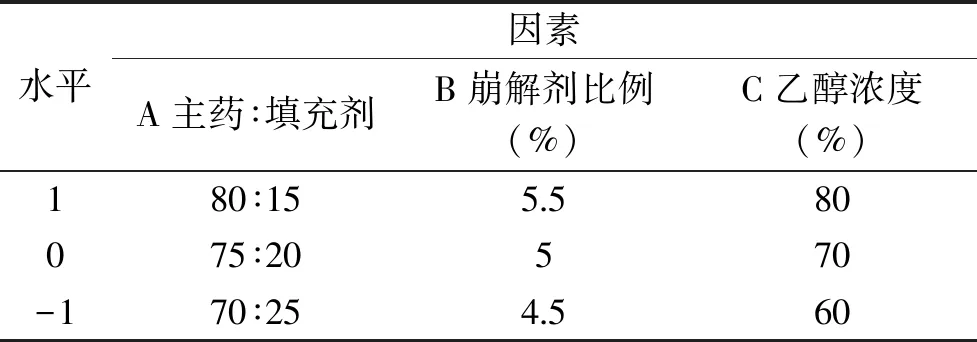
表1 响应面实验因素水平设计Table 1 Factors and levels design for response surface experiment
1.2.5 综合评分的计算 为了得到质量稳定,溶出度适宜的片剂,结合预实验及相关文献[9],确定了如下的综合评分计算方法:
综合评分(%)=[最小脆碎度/X组片剂脆碎度×0.2+最短崩解时限/X组片剂崩解时限×0.2+X组溶出度/最大溶出度×0.6]×100
1.2.6 指标测定
1.2.6.1 脆碎度的测定 按《中国药典》第四部通则项下的“片剂脆碎度检查法”测定复方降脂片的脆碎度,取复方降脂片10片,用吹风机吹去片剂脱落的粉末,精密称定,置圆筒中,转动100次。同法除去粉末,精密称重,减失重量不得超过1%,且不得检出断裂、龟裂及粉碎的片。
1.2.6.2 崩解时限的测定 按《中国药典》第四部通则项下的“崩解时限检查法”测定复方降脂片的崩解时限,取复方降脂片6片,分别置上述吊篮的玻璃管中,启动崩解时限仪进行检查,记录各片的崩解时限。
1.2.6.3 溶出度的测定 按《中国药典》第四部通则项下的“溶出度与释放度检查法”测定复方降脂片的溶出度,取6片中复方降脂片,以0.1 mol·L-1盐酸作为溶出介质,转速100 r·min-1,温度37 ℃,在10 min时取样2 mL,0.45 μm微孔滤膜滤过,取续滤液10 μL。以红景天苷为指标成分,测定其峰面积,计算溶出度。
1.2.7 降脂活性实验
1.2.7.1 高脂血症的诱导 参考文献报道[10-11]设计复方降脂片作用动物实验研究方案,大鼠正常饲养一周后,喂食高脂饮食(2%胆固醇,15%猪油,10%蛋黄,0.5%胆酸钠,74.5%维持饲料)(w/w)。四周后,使用血清胆固醇水平>140 mg/dL的高脂血症大鼠作为实验动物。
1.2.7.2 动物分组 大鼠84只,随机分成7组,每组12只,分为正常对照组(NC),给予生理盐水(10 mL/kg/d);正常给药组(ND)(复方降脂片治疗正常大鼠),剂量为417 mg·kg-1·d-1;高脂模型组(HC),给予生理盐水(10 mg·kg-1·d-1);高剂量组(GH),剂量为834 mg·kg-1·d-1;中剂量组(GM),剂量为417 mg·kg-1·d-1;低剂量组(GL),剂量为209 mg·kg-1·d-1;阳性对照组(ST)(辛伐他汀,4 mg·kg-1·d-1)。
1.2.7.3 给药剂量及给药方式 将复方降脂片溶解于0.9%盐水中,制成适当浓度的溶液,按照上述给药量,每只大鼠每天灌胃给药一次,持续4周。每天观察大鼠的行为活动,毛皮状况,水和食物摄入情况。
1.2.7.4 血清指标检测 给药结束后,大鼠禁食不禁水12 h,腹腔注射20%乌来糖(0.3 mL/100 g)麻醉动物。从腹部主动脉收集约9~10 mL血样,将血液样品以3000 r/min离心15 min,血清样本使用酶标仪测血清中谷丙转氨酶(Alanine aminotransferase,ALT)、谷草转氨酶(Aspartate aminotransferase,AST)、总胆固醇(Total cholesterol,TC)、甘油三脂(Triglyceride,TG)、低密度脂蛋白胆固醇(Low density lipoprotein cholesterol,LDL-C)、高密度脂蛋白胆固醇(High density liptein cholesterol,HDL-C)的水平。
1.3 数据处理

2 结果与分析
2.1 单因素实验结果
2.1.1 主药与填充剂比例的确定 由表2可以看出,处方2、3脆碎度较小,综合评分较高,处方4崩解时限较小,且颗粒成型率较高,综上,确定主药与填充剂比例选范围为70∶25~80∶15。

表2 主药与填充剂比例选择的实验结果Table 2 Experimental results for the selection of the ratio of main drug and filler

表5 响应面设计方案及结果Table 5 Design and results of response surface experiment
2.1.2 崩解剂用量的确定 由表3可以看出,处方2、3、4脆碎度较小,综合评分较高,处方3、4、5崩解时限较小,但处方5的综合评分较低,综上,确定主药与填充剂比例选范围为4.5%~5.5%。

表3 崩解剂用量的选择实验结果Table 3 Experimental results of choice of disintegrant dosage
2.1.3 乙醇浓度的确定 由表4可以看出,处方2、3、4脆碎度较小,综合评分较高,处方1、2崩解时限较大,颗粒成型性较低,综合评分低。综上,确定主药与填充剂比例选范围为60%~80%。

表4 乙醇浓度的选择实验结果Table 4 Experimental results of choice of ethanol concentration
2.2 响应面设计试验结果
2.2.1 回归方程拟合及方差分析 将所得实验数据采用Design-Expert 8.0.5.0软件进行多元回归拟合,得到综合评分对主药:填充剂(A)、崩解剂比例(B)、乙醇浓度(C)的二元多项回归方程:
Y=-311.49795+1.48445A+128.49003B+1.90514C-0.97233AB+0.15494AC-0.24250BC-0.86586A2-10.87B2-9.1775×10-3C2
为了检验方程的有效性,对综合评分的数学模型进行了方差分析,由表6可知,综合评分为响应值时,该二次方程模型极显著(F=21.49,P<0.0001)回归方程失拟性检验无统计学意义(P=0.0687>0.05),表明未知因素对试验结果干扰很小;模型的决定系数R2值为0.9651,接近于1,说明该回归模型与试验数据拟合度较高,可用此模型对综合评分进行分析和预测。该方程与实际情况拟合很好,较好地反映了综合评分与主药:填充剂比例、崩解剂比例、乙醇浓度三者之间的关系,因此,所得的回归方程能较好地预测综合评分随各参数的变化规律[12-13]。

表6 响应面试验方差分析Table 6 Analysis of variance of response surface experiment
由回归模型和方差分析可知(表6),方程一次项A、B及方程二次项C2对综合评分的影响达到显著水平(P<0.05);方程交互项AC、BC及方程二次项A2、B2对综合评分的影响达到极显著水平(P<0.01),根据F值可知,各因素对综合评分的影响的大小顺序为:B(崩解剂比例)>A(主药:填充剂比例)>C(乙醇浓度)。综合以上各参数表明该试验方法可靠,各因素水平间设计合理,因此可用该回归模型代替真实实验对结果进行分析。
2.2.2 交互作用分析 响应面图形是响应值对各试验因子A、B、C、D所构成的三维空间的曲面图,将两个因素固定在0水平,经Design-Expert 8.0.5.0软件分析,观察剩余两个因素的交互作用,从图1中可以看出,最佳参数及各参数之间的相互作用。

图1 主药与填充剂比例与崩解剂比例对综合评分的影响Fig.1 Influence of the ratio of main drug to filler and disintegrant on the comprehensive score

表7 验证实验结果Table 7 Verify experiment results
由表6可知,AC、BC两组因素交互作用极显著(P<0.01),其等高线图和响应面图见图2、图3。由图2可知,随着主药与填充剂的比例(A)与乙醇浓度(C)的增加,综合评分越来越高,达到极值后逐渐下降,且等高线图呈椭圆形,表明两者之间交互作用极显著。由图3可知,崩解剂的比例(B)与乙醇浓度(C)的等高线呈椭圆形,响应面曲线呈山丘形,随着崩解剂的比例(B)与乙醇浓度(C)的增加,综合评分越来越高,达到极值后逐渐下降,表明两者之间交互作用极显著,有极大值存在[14-15]。

图2 主药与填充剂比例与乙醇浓度对综合评分的影响Fig.2 Effects of the ratio of main drug to filler and ethanol concentration on comprehensive score
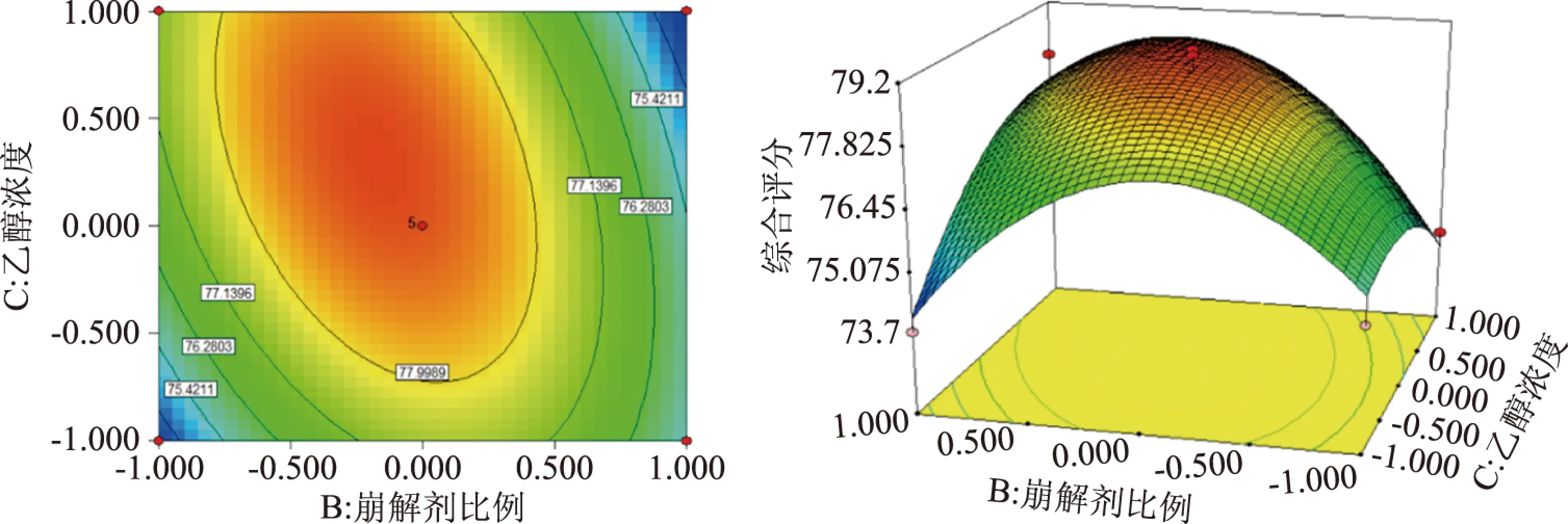
图3 乙醇浓度与崩解剂比例对综合评分的影响Fig.3 Effects of ethanol concentration and disintegrant ratio on comprehensive score
2.2.3 优化结果 在上述响应面模型分析的基础上,利用Design-Expert 8.0.5.0软件对综合指标的二次回归方程求解,得最佳工艺条件为A(主药:填充剂)80∶15、B(崩解剂比例)4.78%、C(乙醇浓度)80%,预测所得的综合评分为92.63%。
2.2.4 验证性实验 为方便实际操作,将响应面实验最终优化结果修正为A(主药∶填充剂)80∶15、B(崩解剂比例)5%、C(乙醇浓度)80%。按此工艺条件制备3批复方降脂片,分别测定三批样品的脆碎度、崩解时限及溶出度,并计算综合评分(结果见表),各批次样品综合评分为94.01%,与预测值相对误差为1.49%,且脆碎度和崩解时限均符合药典规定。以上结果表明,该成型性工艺稳定可行。
2.3 降脂活性实验结果
高脂饲料喂养4周后的大鼠与空白组正常饲料喂养的正常大鼠相比,体重极显著增加(P<0.01),且与空白组相比,模型组大鼠血清中TC、TG、AST、ALT和LDL-C水平均显著升高(P<0.05),符合高脂血症模型的特征,说明本次造模成功(见图4和图5)。
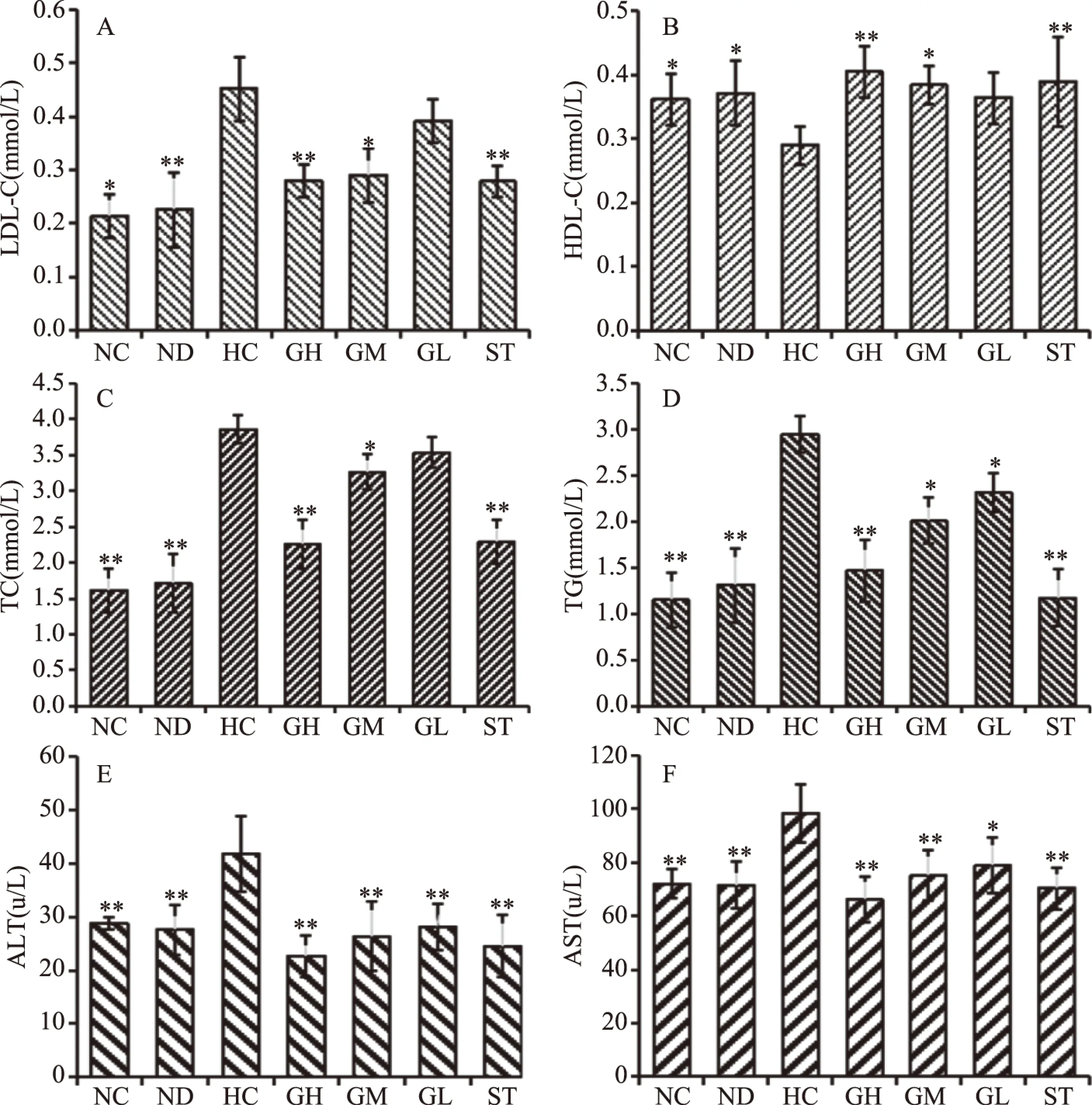
图5 复方降脂片对大鼠血清血脂水平的影响Fig.5 Effects of compound Lipid LoweringTablet on serum blood lipid level in rats

图4 各组实验动物体重变化Fig.4 Changes in body weight of experimental animals in each group注:与HC组相比,*表示显著(P<0.05), **表示极显著(P<0.01);图5同。
与模型组相比,复方降脂片各剂量组大鼠血清中,除高密度脂蛋白(HDL-C)外,其他指标均呈下降趋势,其中高剂量组各指标水平均呈极显著下降(P<0.01),中剂量组AST、ALT水平呈极显著下降(P<0.01),TC、TG及LDL-C的水平显著下降(P<0.05),说明复方降脂片可以通过抑制大鼠血清中TC、TG、AST、ALT和LDL-C的蓄积,降低高脂血症大鼠血清中的脂肪含量。实验结果显示,正常给药组大鼠血清的各项指标与空白组基本相同,未观察到明显的降低或升高,说明复方降脂片的使用不会导致大鼠体重的异常变化。与模型组相比,辛伐他汀组和复方降脂片高剂量组大鼠血清的HDL-C水平极显著升高(P<0.01),复方降脂片中剂量组大鼠血清的HDL-C水平显著升高(P<0.05)。以上结果表明,复方降脂片具有显著的降脂作用。
3 讨论与结论
高脂血症是我国老年人群中很常见的慢性疾病、是导致动脉粥样硬化的危险因素之一,它已经成为我国现目前不可忽视的社会公共卫生问题[16-17]。高脂血症往往会使机体脂质代谢紊乱,导致血清或肝组织中的HDL-C水平降低或者LDL-C、TG、TC等水平增高[18-20]。为了探究复方降脂片的降脂活性,本研究采用大鼠高脂血症模型对复方降脂片的降脂活性进行初步研究。实验结果显示,给药4周后,与高脂模型组相比,复方降脂片各剂量组大鼠血清中,除高密度脂蛋白(HDL-C)外,其他指标均呈下降趋势,其中高剂量组各指标水平均呈极显著下降(P<0.01);中剂量组AST、ALT水平呈极显著下降(P<0.01),TC、TG及LDL-C的水平显著下降(P<0.05),HDL-C增加,与HC组有显著差异(P<0.05)。
高脂血症的治疗,西医常用他汀类和贝特类,虽治疗效果肯定,但价格昂贵,且长期服用增加肝功能损害的风险,少数患者可出现转氨酶升高、肾功损害、胃肠道不适、皮疹、头痛、失眠、肌炎、甚至横纹肌肌溶解等不良反应。国内多项研究表明[21-22],中医药治疗高脂血症合并脂肪肝有其独特的优势。例如,卓冰帆等[23]探讨了山荷降脂汤(处方中含有山楂、丹参及荷叶药材)治疗痰湿内阻型高脂血症的临床疗效,结果表明山荷降脂汤能够明显降低血清中LDL、TG、ALT、AST的水平,从而达到降血脂的疗效,与本文所研究的复方降脂片疗效相似。
复方降脂方在临床上主要采用传统汤剂形式给药,存在着服用量大、患者服用顺应性差等局限,为开发具有良好降脂活性的中药保健食品,本研究采用响应面法对复方降脂片的成型性工艺进行优化。结果表明,使用优选工艺所制备的片剂在外观、硬度、崩解度、重量差异等均符合药典规定,提示该工艺用于复方降脂片的制剂成型具有可行性[24-25]。
综上所述,复方降脂片降脂活性良好,经优化所得到的成型性工艺操作简单,采用普通片剂生产设备生产即可达到要求,适合工业化生产,为复方降脂片的生产提供理论基础。且本研究对复方降脂片对高脂血症大鼠的作用进行初步试验研究,有助于明确复方降脂片对大鼠血脂的影响,并为相关的中药开发和临床应用提供一定的理论依据。

