利培酮对首发精神分裂症患者血清神经细胞因子的影响
王海燕
(靖江市第二人民医院精神科,江苏 泰州 214500)
精神分裂症临床表现主要包含阴性症状和阳性症状,其中阴性症状表现为语言贫乏、情感迟钝以及意志力减退等,阳性症状表现为幻觉、妄想、言语混乱以及行为紊乱等,若不及时接受治疗,将会诱发严重精神残疾,不仅影响患者正常生活和生活质量,而且将会给患者及其家属带来严重的心理负担。氯氮平具有镇静催眠作用,可以控制精神疾病中的幻觉、妄想、兴奋躁动等表现,但不良反应也相对明显,如嗜睡、食欲不振等[1]。随着药理学的不断发展,临床上逐渐将利培酮应用到精神分裂症患者治疗过程中,利培酮属于强有力的D2拮抗剂,可以改善精神分裂症的阳性症状,减少发生椎体外系不良反应的可能,可治疗急性和慢性精神分裂症,并可减轻与精神分裂症相关的情感表达,在临床上取得较好的效果[2]。本研究旨在探讨利培酮对首发精神分裂症患者血清神经细胞因子的影响,现报道如下。
1 资料与方法
1.1 一般资料 选取靖江市第二人民医院2018年3月至2020年5月期间入院接受治疗的80例首发精神分裂症患者为研究对象,采用随机数字表法分为两组,各40例。对照组患者年龄21~59岁,平均(40.89±2.79)岁;其中女性22例,男性18例。试验组患者年龄20~60岁,平均(40.63±2.81)岁;其中女性20例,男性20例。对比两组患者的一般资料(年龄、性别),差异无统计学意义(P>0.05),组间具有可比性。本研究已通过靖江市第二人民医院医学伦理委员会审核批准,且患者家属自愿在知情同意书上签字。诊断标准:参照《精神分裂症的治疗指南》[3]中首发精神分裂症的相关诊断标准。纳入标准:全部入组对象均符合上述诊断标准;经临床基础检查确诊为精神分裂症,且为首发患者;入组前3个月未接受任何相关药物治疗者等。排除标准;患有严重器官疾病和器质性疾病者;处于妊娠期或哺乳期的妇女;对本次试验用药产生不良反应或过敏者等。
1.2 方法 给予对照组患者氯氮平片(北京益民药业有限公司,国药准字H11020846,规格:25 mg/片)治疗,药物使用剂量为25 mg/次,3次/d,同时结合患者实际情况适当调整药物使用剂量。给予试验组患者利培酮片(浙江华海药业股份有限公司,国药准字H20052330,规格:1 mg/片)治疗,药物剂量为1 mg/次,1次/d,结合患者具体表现和病情发展情况合理调整用药剂量,最大剂量<8 mg/d。所有患者治疗时间均为8周,并随访6个月。
1.3 观察指标 ①治疗8周后的临床疗效。分为显效、有效、无效,显效表示为患者阳性和阴性症状量表(PANSS)评分[4]减分率≥80%;有效表示为PANSS评分减分率在45%~79%之间;无效表示为PANSS评分减分率<45%。总有效率=(显效+有效)例数 / 总例数×100%。②治疗前、治疗8周后血清神经细胞因子,于治疗前后分别采集两组患者空腹静脉血4 mL,离心分离血清(转速3 500 r/min,时间9 min),血清神经生长因子(NGF)、脑源性神经生长因子(BDNF)、胶质纤维酸性蛋白因子(GFAP)水平的测定采用酶联免疫吸附试验法。③治疗前、治疗后3个月、6个月PANSS评分,总分值100分,分数越高表示患者临床症状越严重。
1.4 统计学方法 采用SPSS 20.0统计软件进行数据分析,计量资料(血清NGF、BDNF、GFAP水平及PANSS评分)用(±s)表示,采用t检验,多时间点计量资料用重复测量方差分析;计数资料(临床疗效)用[例(%)]表示,采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 临床疗效 治疗8周后,试验组患者的临床总有效率高于对照组,差异有统计学意义(P<0.05),见表1。

表1 两组患者临床疗效比较[例(%)]
2.2 血清神经细胞因子 治疗8周后,两组患者血清NGF、BDNF水平均高于治疗前,且试验组高于对照组;两组患者血清GFAP水平均低于治疗前,且试验组低于对照组,差异均有统计学意义(均P<0.05),见表2。
表2 两组患者血清神经细胞因子比较(±s, μg/L)

表2 两组患者血清神经细胞因子比较(±s, μg/L)
注:与治疗前比,*P<0.05。NGF:神经生长因子;BDNF:脑源性神经生长因子;GFAP:胶质纤维酸性蛋白因子。
组别 例数 NGF BDNF GFAP治疗前 治疗8周后 治疗前 治疗8周后 治疗前 治疗8周后试验组 40 32.89±7.93 46.39±8.87* 28.24±6.43 39.14±6.21* 2.61±0.38 1.88±0.35*对照组 40 32.26±7.91 39.27±7.93* 28.28±6.26 32.85±6.22* 2.59±0.47 2.33±0.41*t值 0.356 3.785 0.028 4.526 0.209 5.280 P值>0.05<0.05>0.05<0.05>0.05<0.05
2.3 PANSS评分 与治疗前比,治疗后3~6个月两组患者PANSS评分均呈逐渐降低趋势,且试验组低于对照组,差异均有统计学意义(均P<0.05),见表3。
表3 两组患者PANSS评分比较(±s, 分)
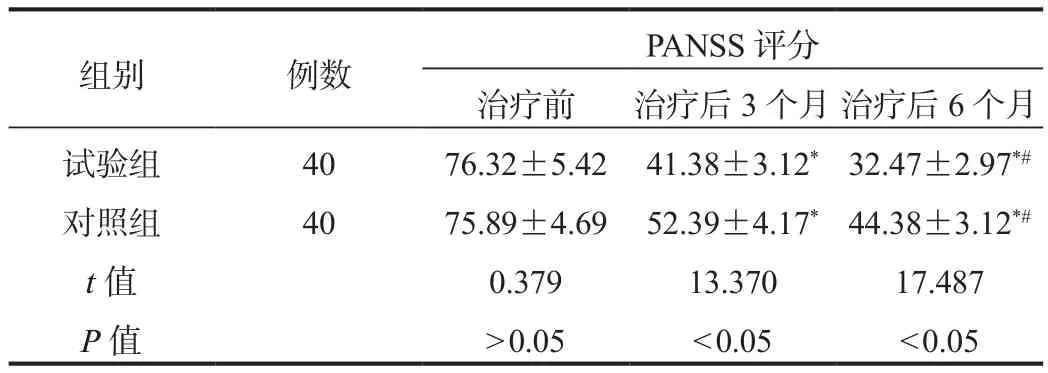
表3 两组患者PANSS评分比较(±s, 分)
注:与治疗前比,*P<0.05;与治疗后3个月比,#P<0.05。PANSS:阳性和阴性症状量表。
组别 例数 PANSS评分治疗前 治疗后3个月治疗后6个月试验组 40 76.32±5.42 41.38±3.12*32.47±2.97*#对照组 40 75.89±4.69 52.39±4.17*44.38±3.12*#t值 0.379 13.370 17.487 P值>0.05<0.05<0.05
3 讨论
精神分裂症属于精神科常见疾病,且发病年龄逐渐向年轻化趋势发展,具有易发作、难治愈等特点,一般多伴有精神、感知以及行为障碍,不仅对患者日常生活造成严重影响,而且在一定程度上加重其家庭负担。目前,临床上对精神分裂症发病原因尚不明确,可能与遗传因素、脑内部发生改变以及母亲孕期异常等具有密切联系。在传统治疗过程中,临床上主要采用氯氮平抗精神药物对患者进行治疗,但在长期使用过程中极容易使患者产生不良反应,导致临床效果受限[5]。
利培酮是一种新型治疗药物,其主要成分为苯并异噁唑衍生物,这种成分能够有效与ɑ1受体相结合,并且在应用过程中对改善患者阴性和阳性症状具有重要作用[6]。除此之外,相关医学专家表示利培酮对多巴胺受体和5-羟色胺具有较高亲和力,并且运动功能抑制、强直性昏厥等并发症发生率较低,在临床实践中具有极高的应用价值[7]。本研究中,治疗8周后,试验组患者的临床总有效率高于对照组;治疗后3~6个月试验组患者PANSS评分均低于对照组,提示利培酮在首发精神分裂症患者治疗中,能够改善患者阴性和阳性症状,效果显著。与正常人相比,精神分裂症患者体内神经营养因子水平较低。NGF、BDNF可直接作用于N-甲基-D-天冬氨酸(NMDA)受体,不仅能够有效清除自由基,而且有助于降低细胞内钙离子超载,进一步减小兴奋性氨基酸的毒性,从而实现保护神经元的目的;GFAP属于Ⅲ类中间丝状体,特异地表达于中枢神经系统星形胶质细胞胞质内,其水平高低与神经系统疾病严重程度呈正相关。利培酮口服后可被完全吸收,并且在1~2 h内达到血药浓度峰值,其半衰期为3 h左右,多数患者可在1 d内达到利培酮稳态,用药后经尿液和粪便排出,保护神经元,并且以最低程度的亲和力,和H1-组胺能受体与肾上腺素受体产生配对,增加其神经元因子水平[8]。本研究中,治疗8周后,试验组患者NGF、BDNF水平均高于对照组,GFAP水平低于对照组,提示利培酮在首发精神分裂症患者治疗中,有助于改善患者血清神经细胞因子水平,提高治疗效果。
综上,利培酮在首发精神分裂症患者治疗中发挥重要作用,不仅能够改善患者阴性和阳性症状,而且有助于改善血清神经细胞因子水平,效果显著,值得临床推广和应用。

