豆渣改性及其理化特性研究
向沁雪,张倩倩,李 伟,莫开菊
(湖北民族大学 生物科学与技术学院,湖北 恩施 445000)
膳食纤维(dietary fiber,DF) 通常被定义为食物中固有的不可消化的非淀粉多糖类物质[1].一般是生产过程中的副产物,由于口感不佳,缺少营养,因此不利于加工和直接食用,少部分用于动物饲料、土壤肥料,大部分直接丢弃,造成了资源的极大浪费和环境污染.膳食纤维包括可溶性膳食纤维(soluble dietary fiber,SDF)和不溶性膳食纤维(insoluble dietary fiber,IDF)[2].
近十几年膳食纤维的研究热点由膳食纤维的提取转换为膳食纤维的改性,改性的方法多种多样,分为物理改性、化学改性、物理化学联合改性方法.膳食纤维的改性效果通常用水合力、吸附力以及阳离子交换力来评价膳食纤维的改性效果,水合力包括膨胀力、持水力,水合力越大,膳食纤维的体积含水量越大,对膳食纤维在肠道内的排毒和排便体积、速度有直接影响,也是制备食品增稠剂和水分保持剂的重要指标之一[3];吸附力包括对葡萄糖、胆固醇、亚硝酸盐的吸附;另外,膳食纤维有较强的离子交换能力,具有一个弱酸性阳离子交换树脂的作用,因为其化学结构中包含一些如氨基、羟基和羧基等侧链基团,对电解质和各种矿物质元素,特别是重金属元素具有吸附作用[4].
豆渣本身就具有较强的水合力和吸附力,比苹果渣、甘薯渣[5-7]等的理化特性更加优异,另外豆渣的营养价值与大豆相似.豆渣作为研究一种重要营养丰富,天然,低热量,低脂肪,低糖的食品生产原料,具有一个很大的发展经济潜力[8].豆渣改性功能研究是目前的研究热点,探究改性豆渣的理化特性和生理功能够更加合理利用大豆资源,既增加了豆渣的利用价值,又杜绝了资源浪费.因此对豆渣进行各种改性方法的尝试,探讨理化特性之间的关联,是非常有必要的.
1 材料与方法
1.1 材料与试剂
豆渣(购于湖北省恩施市圆梦庄菜市场);D(+)-葡萄糖购于国药集团化学有限公司;邻苯二甲醛购于上海慧颖生物科技有限公司;胆固醇购于上海山浦化工有限公司;其他试剂与化学药品均为分析纯.
1.2 仪器与设备
SFT-250超临界萃取仪(赛普泰克有限公司);LD-Y500A粉碎机(上海顶帅电器有限公司);BXH0烘箱(上海博讯有限公司医疗设备厂);SB-5200D超声波(宁波新芝生物科技股份有限公司);TGL-16M离心机(湖南湘仪实验仪器开发有限公司);M200 Pro多功能酶标仪(瑞士帝肯公司);JSM-6510LV电子显微镜(日本电子株式会社).
1.3 方法
1.3.1 样品预处理 豆渣用纯水洗涤过滤至清水,以去除豆渣中的杂质及水溶性物质.
1.3.2 实验流程 实验流程为:样品→烘干(40 ℃)→粉碎→过筛(80目)→加入料液比为1∶9的反应液→不同改性环境下改性4 h→洗涤至水清→烘干→检测各项理化指标.综合以往学者的改性实验[9-13],确定豆渣改性的反应液种类为盐酸、氢氧化钠、磷酸氢二钠,这3种反应液对应着不同的质量浓度,分别为0%、0.001%、0.01%、0.1%、0.5%、1.0%、1.5%、2.0%.每种反应液浓度都有3种反应环境.超临界CO2处理(supercritical carbon dioxide,SC-CO2)反应条件为温度32 ℃、压力3 000 PSI;超声波处理(ultrasonic treatment,UT)反应条件为功率400 W、温度32 ℃;常温常压处理(normal temperature and pressure treatment,NPT)反应条件为温度30 ℃,在此条件下静置反应.
1.3.3 分析方法
1.3.3.1 改性豆渣膨胀力测定 根据Cummings[14]的方法加以改性,取样品1.00 g,置于试管中,加入纯水25 mL,充分震荡后,室温下静置,24 h后,记录膨胀后豆渣体积的大小,按照公式M1=V1/m1计算膨胀力M1.式中:V1为豆渣吸水后的体积(mL);m1为豆渣干质量(g).
1.3.3.2 改性豆渣持水力测定 根据Wennberg M[15]称取豆渣样品1.00 g放入50 mL离心管中,加入纯水25 mL,在37 ℃、140 r/min的条件下震荡下4 h后,离心(8 000 r/min)20 min,用滴管吸弃上清液,称量豆渣持水质量,按照公式M2=m1/m2计算持水力M2.式中:m1为豆渣吸水质量(g);m2为干样豆渣质量(g).
1.3.3.3 改性豆渣对葡萄糖吸附能力测定 根据Ahmed F[16]的方法加以改进,取浓度为10 mmol/L葡萄糖溶液25 mL,加入1.00 g豆渣膳食纤维,在37 ℃水浴摇床中振荡6 h,在8 000 r/min条件下离心20 min,用3,5-二硝基水杨酸法测定上清液中的葡萄糖含量,按照公式M3=(m1-m2)/m3计算吸附胆固醇力M3.式中:m1为吸附前葡萄糖的质量(mg);m2为吸附后葡萄糖的质量(mg);m3为豆渣质量(mg).
1.3.3.4 改性豆渣对胆固醇吸附能力测定 按照董森[17]的方法加以改良,取鲜鸡蛋黄,用9倍量纯水充分搅打均匀.称取1.00 g豆渣,置于50 mL离心管中,加入25 g的上述蛋黄液,搅拌37 ℃摇床振荡4 h,离心(8 000 r/min)20 min,采用邻苯二甲醛法测定胆固醇含量.依照公式M4=(m1-m2)/m3计算吸附胆固醇力M4.式中:m1为吸附前蛋黄液中胆固醇量(mg);m2为吸附后上清液中胆固醇量(mg);m3为豆渣质量(mg).
1.3.3.5 豆渣阳离子交换能力测定 根据黄六容[18]的方法进行测定,取1.00 g豆渣样品,置于小烧杯中,加入0.01 mol/L HCl溶液30 mL,振荡均匀,于4 ℃下过夜,用蒸馏水洗涤至中性,干燥,准确称取100 mg,用0.02 mol/L KOH溶液进行滴定,按照公式CEC=cV/m测定阳离子交换能力.式中:CEC为豆渣的阳离子交换能力(meq OH-/g);c为KOH溶液的摩尔浓度(mol/L);V为滴定所耗KOH溶液的体积(mL);m为称取豆渣样品的质量(g).
1.3.3.6 豆渣对亚硝酸根离子吸附能力的测定 根据张建利[19]的方法进行测定.吸附效果测定:设置吸附环境为pH 7.0,反应在250 mL三角瓶中进行,反应体积为100 mL,NO2-浓度为100 μmol/L,加入0.5 g膳食纤维,于37 ℃恒温条件下电磁搅拌反应,120 min后,各取1 mL样液,按标准曲线的方法测定NO2-的浓度,按照公式M6=(M1-M2)/m2计算其对NO2-的清除率M6.式中:M1为亚硝酸根离子初始含量(μmol/L);M2为溶液中亚硝酸根离子最终含量(μmol/L).
1.3.3.7 电镜观察 电镜扫描选取了0.1%、1%、2%三个质量浓度的盐酸、氢氧化钠、磷酸氢二钠反应液,以及各个浓度在超临界CO2、常温常压、超声波环境下改性4 h后的样品,每个样品在2 000倍下拍摄4张图片,选取清晰、具有代表性的图片进行结构比较.参考Ullah[20]的方法并改进,用扫描电镜观察豆渣膳食纤维粉表面形态.在样品台上贴上一层双面胶,将粉末轻轻撒在表面,用洗耳球轻轻吹去多余的粉末,在样品上喷金(厚度100 μm)后于加速电压为10 kV下观察并拍照,结合软件Image J测量孔径大小40次,并做显著性分析.
1.4 数据处理
结果以表格与折线图表示,采用SPSS 21进行显著性分析,采用Origin 8.0制图.
2 结果与分析
2.1 物理改性对豆渣各项指标的影响
首先研究了3种环境条件对改性的影响,研究中所有原料都以纯水为研究介质,仅比较3种物理条件的作用.通过纯水浸泡、超临界和超声波处理后,测定其理化指标,以比较3种环境的效果,结果见表1.
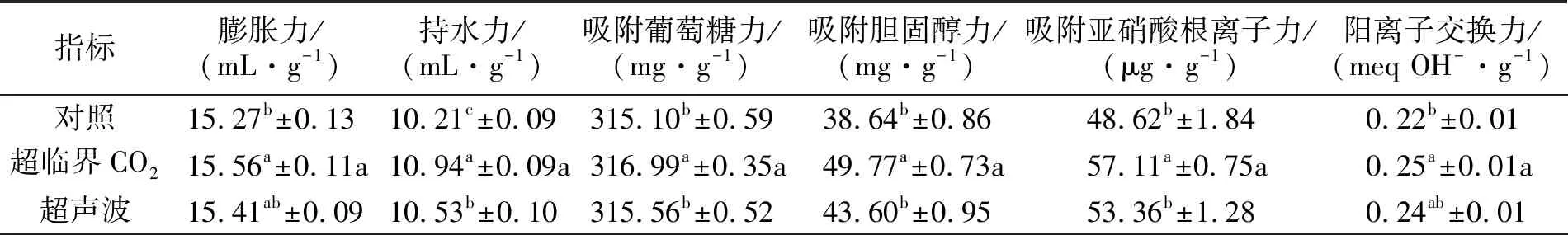
表1 改性豆渣的各项理化指标Tab.1 Physical and chemical indexes of modified soybean dregs
膨胀力和持水力是豆渣理化性质中最重要也是最基础的一项,是水合力的不同表现,水合力的增加能够使豆渣的含水量、体积增大,对于减轻体重[21]、缓解便秘[22]有积极作用.
由表1可得,在两种物理环境作用下,水合力均比常对照组要高,除了超声波改性豆渣的膨胀力无显著增大以外,其他均有显著提升,其中超临界CO2改性后的水合力显著增强.在吸附水的同时,豆渣还可以吸附一部分水溶性物质,例如葡萄糖、胆固醇、亚硝酸盐,有助于降低摄入食物的能量密度[23]、吸附有害物质[24-25],经过物理改性后,豆渣的吸附葡萄糖、胆固醇、亚硝酸根离子能力都增强,其中超临界CO2改性后的豆渣吸附力显著增强.阳离子交换能力使得阳离子与豆渣进行可逆的交换,这种可逆的交换能够调节离子的瞬间浓度,导致消化道的pH值、渗透压及氧化还原电位等发生改,营造一个更有助于消化吸收的缓冲环境[26],超临界CO2改性后的豆渣阳离子交换力增强明显,而超声波改性后的豆渣增强不明显.比较而言,超临界CO2改性后的理化指标增加0.6%~28.8%,超声波改性后的理化指标增加0.1%~12.8%.
2.2 化学改性对豆渣各项指标的影响
在化学改性中,选用最常见的盐酸、氢氧化钠以及磷酸氢二钠溶液作为改性试剂,这源于对前人研究的借鉴,改性膳食纤维的理化指标如图1所示.

a、b、c、d、e、f代表各项理化指标,分别为膨胀力、持水力、吸附葡萄糖力、吸附胆固醇力、吸附亚硝酸根离子力、吸附阳离子力.横坐标轴中A为对照组;B、C、D、E、F、G、H分别为浓度0.001%、0.01%、0.1%、0.5%、1.0%、1.5%、2.0%的不同溶液;下同.图1 改性豆渣的各项理化指标Fig.1 Physical and chemical indexes of modified soybean dregs
由图1可得,盐酸溶液对豆渣水合力没有积极影响,随着盐酸浓度的增加水合能力显著降低(P<0.05),当盐酸溶液浓度达到2%时,膨胀力、持水力达到最小,分别为8.63、5.51 mL/g;而磷酸氢二钠溶液和氢氧化钠溶液对豆渣有积极影响,随着溶度的增大,水合能力显著上升(P<0.05),当浓度达到1.5%时,磷酸氢二钠溶液改性的豆渣水合力最大值分别为18.84、12.28 mL/g;氢氧化钠溶液改性的豆渣水合力最大值分别为24.06、16.24 mL/g.
盐酸改性使豆渣对葡萄糖、胆固醇、阳离子的吸附力降低,当溶液浓度达到2%时,吸附力最小分别为303、19.64 mg/g、0.117 6 meq OH-/g;磷酸氢二钠溶液改性的豆渣吸附力呈缓慢上升趋势,当溶液浓度达到1.5%时,出现吸附力最高峰,吸附力最大值分别为最大值分别为324、53.76 mg/g、0.279 8 meq OH-/g;而随着氢氧化钠使豆渣的吸附力急剧上升,当浓度达到1.5%时,吸附力最大,分别为332、62.50 mg/g、0.358 3 meq OH-/g.
磷酸氢二钠和氢氧化钠改性对豆渣吸附亚硝酸根的作用仍然维持前述趋势,当溶液浓度均为1.5%时达到最大值,分别为60.16、92.87 μg/g.盐酸导致亚硝酸根吸附力持续上升,最大值为80.60 μg/g,溶液浓度为2%.这一表现区别于对其他成分的吸附力,这可能是由于pH值降低时,使膳食纤维表面的负电荷密度减小,导致对亚硝酸根离子的吸附力增大[27].
综上所述,对豆渣改性效果最好的是氢氧化钠,其次是磷酸氢二钠,而盐酸改性使豆渣的多数理化特性下降,仅提高其吸附亚硝酸根的作用.氢氧化钠、磷酸氢二钠改性使豆渣的理化指标分别提高5.5%~91.0%、2.9%~39.1%.盐酸使得吸附亚硝酸根能力提高了65.8%,而其他理化指标则降低4.0%~96.7%.然而有报道证明盐酸对麦麸[28]、胡麻渣[29]的改性效果良好,这可能源于不同的膳食纤维结构对盐酸水解作用的耐受性不同.
2.3 物理化学联合改性对豆渣各项指标的影响
当验证超临界和超声波对膳食纤维的组织结构均有良好影响后,采用不同溶液种类及浓度在不同物理条件下的联合改性.改性豆渣的物理化学特性变化见图2.图2中HCL&NPT表示盐酸溶液与常温常压的反应条件;HCL&SC-CO2表示盐酸溶液与超临界二氧化碳的反应条件;HCL&UT表示盐酸溶液与超声波的反应条件;NaOH&NPT表示氢氧化钠溶液与常温常压的反应条件;NaOH&SC-CO2表示氢氧化钠溶液与超临界二氧化碳的反应条件;NaOH&UT表示氢氧化钠溶液与超声波的反应条件;Na2HPO4&NPT表示磷酸氢二钠溶液与常温常压的反应条件;Na2HPO4&SC-CO2表示磷酸氢二钠溶液与超临界二氧化碳的反应条件;Na2HPO4&UT表示磷酸氢二钠溶液与超声波的反应条件.
由图2可得,物理化学联合改性使得豆渣的水合力有所变化.盐酸溶液条件下,浓度越大水合能力越低,超临界CO2、超声波的联合作用会加剧这一反应,且超临界CO2对改性豆渣的影响最大(P<0.05),膨胀力最小值为8.05 mL/g、持水力最小值为3.56 mL/g;当氢氧化钠溶液浓度增大时,水合力逐步增大,当浓度达到1.5%时,改性豆渣的膨胀力、持水力均达到最大,尤其是膨胀力在超临界CO2的作用下极显著升高(P<0.01),膨胀力、持水力最大值分别为32.19、16.93 mL/g;而磷酸氢二钠溶液对豆渣膨胀力的影响与前两者不同,随着磷酸氢二钠溶液浓度的升高,改性豆渣的水合力逐步上升,其中持水力在磷酸氢二钠溶液浓度达到0.5%之后变化变化平缓,其中超临界CO2的作用下增长最明显,水合力最大膨胀力为24.78 mL/g、持水力最大值为14.79 mL/g.
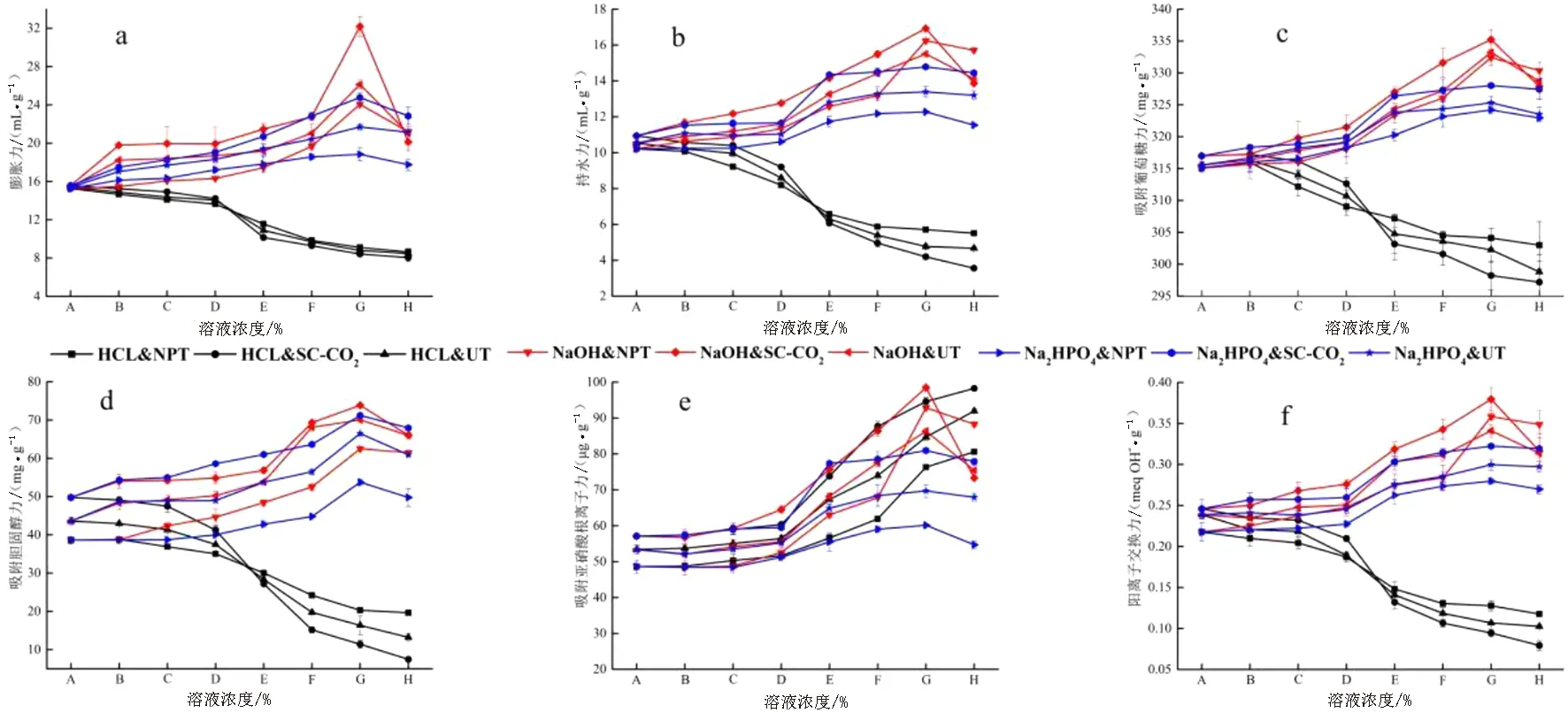
a、b、c、d、e、f分别代表膨胀力、持水力、吸附葡萄糖力、吸附胆固醇力、吸附亚硝酸根离子力、吸附阳离子力.图2 改性豆渣的各项理化指标Fig.2 Physical and chemical indexes of modified soybean dregs
盐酸与超临界CO2、超声波联合作用下,使得豆渣吸附葡萄糖、吸附胆固醇能力、阳离子交换力下降,且反应液的浓度越大,下降越快(P<0.05),最小值分别为297.20、7.46 mg/g、0.097 3 meq OH-/g.氢氧化钠和磷酸氢二钠溶液对改性豆渣的吸附葡萄糖、胆固醇力以及阳离子交换力有促进作用(P<0.05),与上述化学改性豆渣的趋势相似,在物理环境辅助作用下,理化指标有所提高(P<0.05),氢氧化钠溶液的吸附力最大值分别为335.24、73.85 mg/g、0.379 6 meq OH-/g,磷酸氢二钠溶液的吸附力最大值分别为328.04、71.21 mg/g、0.322 4 meq OH-/g.
除此之外,3种改性溶液都不同程度地增大了豆渣的亚硝酸根离子的吸附,其中盐酸溶液改性后的豆渣由于其自身的pH值发生变化,吸附亚硝酸根离子的能力也随着增大,氢氧化钠溶液和磷酸氢二钠溶液改性的豆渣吸附亚硝酸根离子的能力与上述吸附力的趋势相似.2%的盐酸溶液与1.5%氢氧化钠溶液条件下的亚硝酸根离子的吸附力持平,为98 μg/mL.改性豆渣的最大亚硝酸根离子的吸附力与对照组相比增大了2.03倍.
由以上可得,联合改性效果较好的最佳组合有1.5%氢氧化钠+超临界CO2、1.5%磷酸氢二钠+超临界CO2,其理化指标分别增加了5.5%~106.9%、2.9%~59.2%.
2.4 改性溶液种类及浓度对豆渣微观结构的影响
总结前人所做膳食纤维的理化特性与扫描电镜结果,发现它们之间存在一定联系[30-32],因此采用电子显微镜观察了豆渣形貌并分析了孔径大小.结果见表2和图3.
由表2得,在两种物理条件下,豆渣的孔径明显增大,其中超临界CO2要比超声波改性条件下的豆渣孔径要大.盐酸溶液使得豆渣孔径减小,浓度越高,孔径越小,孔状结构被破坏,空间结构收缩,超临界CO2复合处理使得打开的空间结构坍塌,结构变得紧实,出现较多层状结构(图3a);磷酸氢二钠溶液使得豆渣孔径变大,超临界CO2、超声波处理促使了结构被打开,出现许多“毛鳞片”状的结构,内部亲水结构暴露(图3b),超临界CO2复合处理和超声波复合处理后的豆渣孔径要比常温常压处理的豆渣孔径更大;不同浓度的氢氧化钠溶液使得豆渣的孔径被打开,超临界CO2、超声波处理使得孔径均变大,暴露了更多内部结构(图3c),当浓度达到1.5%时,孔径达到,改性豆渣的最大吸附力与对照组相比增大了1.51倍.
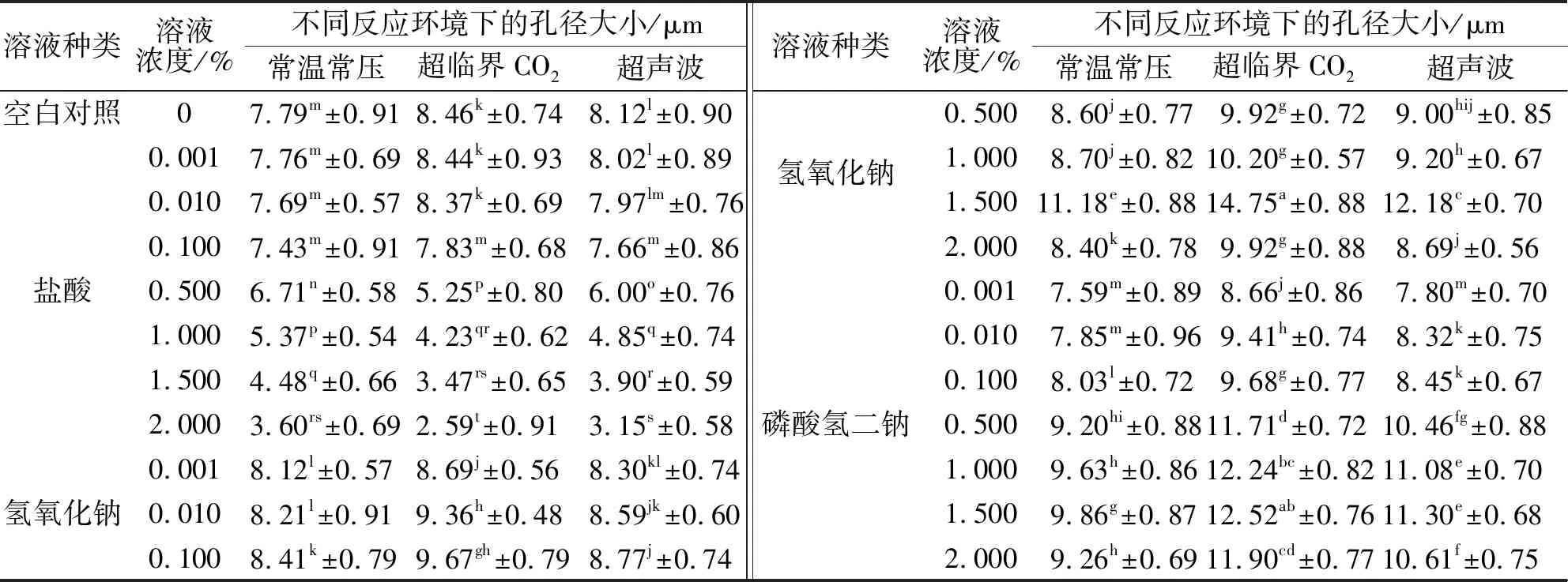
表2 改性豆渣的孔径大小Tab.2 The pore size of modified soybean dregs

a为超临界CO2条件下2%盐酸改性的豆渣孔径;b为超临界CO2条件下1.5%氢氧化钠改性的豆渣孔径;c为超临界CO2条件下1.5%磷酸氢二钠改性的豆渣孔径.图3 不同处理后豆渣的孔径Fig.3 The pore size of soybean dregs after different treatments
3 结论与讨论
豆渣经过物理、化学以及物理化学联合改性,获得良好的理化性质.物理改性对豆渣的微观结构和理化性质有一定影响,比较而言超临界CO2流体改性效果优于超声波的效果;三种化学试剂的改性效果,在相同质量百分数下,氢氧化钠的效果最好,磷酸氢二钠的效果次之,不同质量百分数的盐酸对豆渣的改性是不利的,除了提高亚硝酸盐的吸附力,其他理化指标都下降.化学试剂的改性效果与质量百分数有重要关系,存在最佳值,过低过高都会影响.本研究中最佳的质量百分数都是1.5%.物理化学联合改性显著增强改性效果,联合改性比单一物理改性、化学改性的各项理化指标分别提高了5.8%~106.9%、4.2%~33.8%.另外,本文显示盐酸改性能较好地提高亚硝酸根的吸附力,这是否具有普遍性,还需要深入研究.总的来说,改性最佳条件为1.5%氢氧化钠溶液和超临界CO2的联合改性.与以往研究相比,其理化特性值均高于超微粉碎[33]、微生物发酵[34]和动态高压微射流[34]、羧甲基豆渣膳食纤维处理[35]后的理化特性.
改性豆渣后获得良好的理化特性的主要原因与其微观结构关系密切,其微观孔口越多,孔径越大,其理化表现越好,在物理作用及碱性环境下,孔径增大,酸性环境则减小,且磷酸氢二钠溶液使豆渣出现较多“毛鳞片”状结构,猜测此结构有亲水性,所以增大了豆渣的水合能力以及吸附能力,这与氢氧化钠溶液改性的机理有所不同.
综上所述,改性豆渣较强的水合力使得膳食纤维的体积、含水量、吸附食物中的胆固醇、葡萄糖、亚硝酸盐等显著增加,有助于增加饱腹感,降低能量密度,排出有害物质,因此通过氢氧化钠和磷酸氢二钠改性的豆渣作为肥胖、三高人群的食品有着广泛的前景.

