新型FeCo双金属催化剂催化CO2加氢制低碳烯烃
董子超,吴玉,张博风,刘斯宝,刘国柱,赵杰
(1天津大学化工学院,天津300072;2中国石化石油化工科学研究院,100083)
引 言
我国提出在2030年前达到CO2排放峰值,2060年前实现碳中和的目标。面对日益严峻的低碳减排压力和碳市场增量,高效转化和利用CO2是目前C1化工领域研究的重点[1]。C2~C4低碳烯烃是基础化工原料,因此通过催化转化CO2加氢制备低碳烯烃具有重要意义[2-3]。
铁基催化剂广泛用于CO2加氢反应,首先,CO2由逆水煤气反应(RWGS)生成CO中间体,然后通过费托反应(FTS)生成碳氢化合物[4-5]。Fe3O4和Fe5C2通常被认为是两步反应主要活性位[6-7]。由于单一铁组分难以满足反应需求,可通过载体优化、助剂改性等策略来改善性能[8-9]。K、Na等电子助剂可以改变催化剂电子密度,调整表面的氢碳比以降低反应活化能[10-11]。而过渡金属如Mn[12]、Cu[13]、Zn[14]、Co[15]等也常被引入反应体系中。Mn可以促进金属还原并有效抑制产物二次加氢。Co具有高费托活性和链增长能力,可抑制积炭产生并增强催化剂稳定性。载体可通过影响金属分散,调节电子云密度和孔结构等来影响反应性能[16-18]。氧化物和分子筛载体应用最多,但氧化物与金属间强相互作用会抑制金属还原和碳化[19],而分子筛具有大量酸性位,不仅会损害催化剂表面碱度和渗碳能力,也会促进烯烃二次反应,造成芳构化和异构化,不利于低碳烯烃生成[20-21]。碳基载体水热稳定性和疏水性好,与金属较弱的相互作用有利于金属分散和渗碳,如碳纳米管(CNTS)、碳球(CS)、石墨烯等已引起大量关注[22-24]。此外向碳中掺入富电子N可以改变催化剂的结构和电子密度[25-26],进而改善CO2在表面的吸附。金属有机骨架材料(MOFs)可以用作牺牲模板,通过热分解形成多孔碳纳米材料,其热解过程能形成嵌入碳基质的金属或金属氧化物,从而减少催化剂烧结并提高其热稳定性[27-28]。本文作者[29]研究了ZIF-67衍生的FeCo双金属催化剂上的CO2加氢性能,发现通过浸渍法形成的双金属催化剂虽然具备较高的活性和烯烃选择性,但受限于MOFs骨架形成本身所需的高金属含量,难以有效地调节双金属比例,导致产物甲烷选择性偏高。
为了进一步降低甲烷选择性并提高低碳烯烃选择性,本文设计了Fe-MOF衍生的、铁钴比可控的双金属催化剂,期望通过FeCo双活性位协同作用,显著提高CO2加氢活性和低碳烯烃选择性。结合不同表征手段考察了催化剂的形貌结构和CO2加氢性能。
1 实验材料和方法
1.1 催化剂制备
将3.32 g对苯二甲酸和8.08 g Fe(NO3)3·9H2O分别溶解在60 ml DMF中,混合均匀后向其中添加8 ml NaOH溶液(4 mol·L-1)。在室温下搅拌60 min后,将所得产物在100℃烘箱内保持24 h。将获得的样品分别用DMF和甲醇洗涤3次,离心后取下层固体在80℃下干燥过夜。所得样品命名为MIL-88B。将MIL-88B用5%钠盐促进后干燥,在管式炉内以2℃·min-1的速率加热到600℃并保持1 h,之后冷却到室温,所得产物命名为Fe/MC。在金属物质的量总量不变的情况下,将一定摩尔比的Fe(NO3)3·9H2O和Co(NO3)2·6H2O混合后溶解在等量的DMF中,其余步骤与之前类似,得到FeCo(X∶1)/MIL-88B(X是Fe∶Co的摩尔比)。此样品经同样气氛条件焙烧所得产物命名为FeCo/MC。
1.2 催化剂表征
催化剂金属含量通过电感耦合等离子发射光谱仪考察(ICP,Optima 8300);采用X射线衍射仪(Rigaku Smartlab)来表征晶体物相。测试条件:Cu靶,Kα射线,步长:0.02°,扫描范围5°~80°;使用Q500A热重分析仪测试催化剂结构稳定性,在氮气氛围下以10℃·min-1升到800℃;使用高分辨透射电子显微镜(Thermo Fischer Talos F200X,测试电压200 kV)和扫描电子显微镜(S-4800,电压10~30 kV)观察催化剂颗粒微观形貌尺寸和晶格条纹等;使用Tristar3000吸附仪来测试催化剂比表面积信息,通过Brunauer-Emmett-Teller(BET)方法解析;采用AtuochemII 2920化学吸附仪确定催化剂表面碱类型、还原状态以及CO2吸附能力。通过拉曼光谱仪(invia reflex)表征碳载体石墨化程度,使用325 nm He-Cd紫外激光器。扫描范围:500~2000 cm-1。所得数据通过高斯拟合的方法计算D峰和G峰峰高比值得到ID/IG。
1.3 CO2加氢反应性能评价
采用常规固定床反应器来考察CO2加氢性能。取适量催化剂(0.5 g,0.55~0.83 mm)与3.5 g石英砂(0.55~0.83 mm)混合装填于反应管中部,两端装填0.83 mm石英砂并铺以少量石英棉。反应前用氮气吹扫30 min以除去管内残存空气。之后切换气体为高纯氢气,将催化剂在纯氢气中(40 ml·min-1)在400℃还原2 h。随后将反应器冷却至室温,并将H2/CO2/N2(69/23/8,N2作为内标气)混合进料至反应器中并将压力升高至2.0 MPa,升温至350℃,空速=6.24 L·g-1·h-1。采用气相色谱仪分析反应产物。使用配有TCD(氧化铝柱,PPU柱和MS5A柱)的GC Micro 490分析CO2、CO、N2和CH4。使用配有FID的(PONA毛细管柱)GC 2010分析碳氢化合物和含氧化合物。根据式(1)通过碳原子平衡计算CO2转化率:

式中,n为可检测到的烃类物质总个数。
2 实验结果与讨论
2.1 催化剂的结构物性
图1(a)中显示了催化剂未煅烧之前的热重曲线,100℃附近的信号与物理吸附水损失有关,其后样品处于梯度分解状态;100~300℃范围内的分解与残留的试剂分子及硝酸根热分解有关;300~500℃范围内较剧烈分解可能是MOFs骨架配体损失。样品在600℃后逐渐趋于稳定。可知载体分解程度并不与钴的含量呈线性相关,铁钴比为9的样品在相同温度下剩余的质量最多。
表1为催化剂的元素组成和孔结构信息。从ICP的结果可知,金属负载比例与投料量比例保持一致。由以往的经验可知,通过等体积浸渍的方式在MOFs中引入第二金属实现双金属的负载,会受限于MOFs自形成骨架结构所需的最低金属含量,难以有效地调控金属含量和比例,导致总金属含量过高而不利于金属分散,难以有效利用活性位。而通过前体进行金属掺杂有效地降低了总的金属含量和钴含量,并使得双金属中的铁占据主导地位。从图1(b)的BET测试结果可知,所有样品在较低的相对压力(<0.05)下显示出明显的N2吸收,表明其具有良好的微孔结构。同时吸附回滞环的产生表明具有Ⅳ型等温线特征,证明了介孔的存在。所有的样品显示出典型的H3型回滞环,说明热解后的催化剂的孔结构很不规整。在不同的样品中,铁钴比为9的样品显示出最大的比表面积(171.1 m2·g-1)和介孔体积(0.42 cm3·g-1),而铁钴比从3提升到6时,样品比表面积由152.9 m2·g-1降低到118.2 m2·g-1。
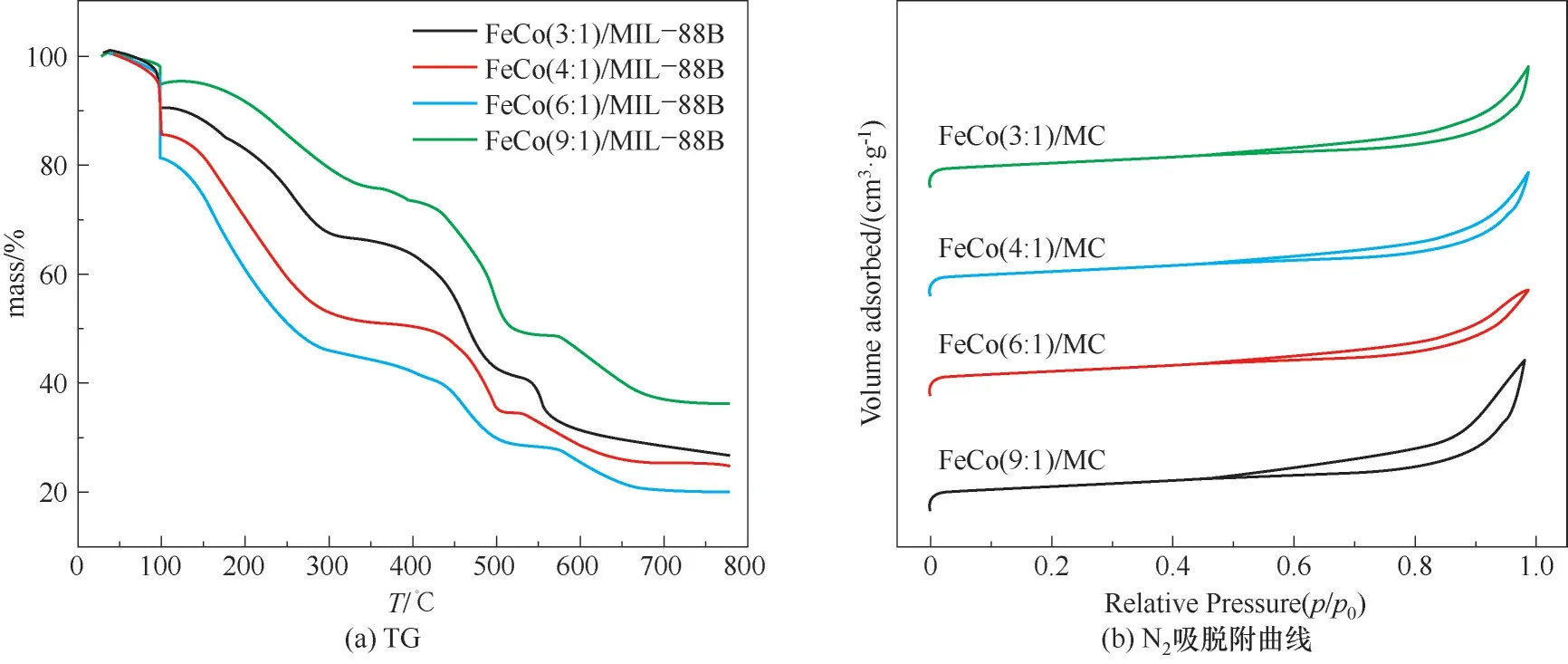
图1 催化剂热重和氮气-吸脱附表征Fig.1 TGcurves and N2 adsorption-desorption isotherms of catalysts
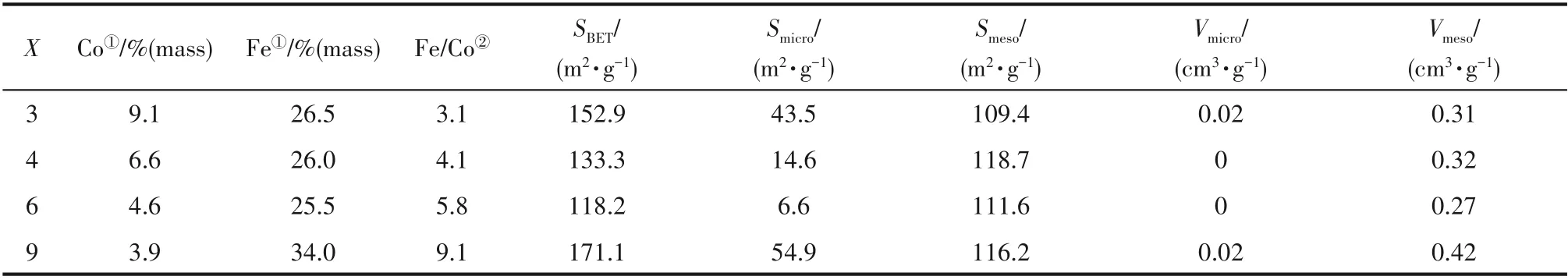
表1 FeCo(X∶1)/MC催化剂物理性质Table 1 Specific surface area properties of FeCo(X∶1)/MC catalysts
2.2 催化剂的形貌及金属相态
热解前后的催化剂SEM结果如图2所示。可以看出热解前催化剂呈现六边形棱柱的形貌,长度为250~350 nm,宽度为80~90 nm。随着铁含量的增加晶体边界逐渐模糊且不规则程度变大。从热解后的催化剂可以看出,在600℃下热解时载体本身形貌遭到一定程度的破坏且石墨化程度变大,出现交联的碳骨架,引入钴的催化剂热解后原始结构得到更好的保留。
通过HR-TEM进一步表征了样品微观结构和粒径分布,如图3所示。从图3(a)中可以看出热解后载体仍保留着部分六边形棱柱结构,金属被均匀地封装分散在载体内部。金属被嵌入到热解生成的均匀石墨碳层中,碳层厚度约为10 nm。这不仅有效地限制了金属的烧结,还控制了金属的尺寸和分散度。金属与碳层较弱的相互作用有利于金属的还原和碳化。此外,Fe/MC样品平均粒径为11.4 nm,而FeCo(9∶1)/MC的样品平均粒径为6.2 nm,表明少量钴的引入可以有效促进金属的分散从而降低颗粒尺寸。随着Co含量的增多,平均粒径上升到14.8 nm,说明纳米粒子尺寸受双金属比例影响。由图3(a)~(d)所示,所有含Co的样品测得的宽度为0.201 nm的晶格条纹,对应于FeCo(110)的特征晶面。从图3(e)可以看出不含Co的Fe/MC上发现了宽度为0.249 nm的晶格条纹,对应于FeO(111)晶面。
通过XRD鉴定了FeCo/MC样品中金属的相态组成,结果如图4(a)所示。对CO2加氢反应来说,金属在反应过程中会经历复杂的相态变化,演变为一个或多个活性相并最终转变成一个相对稳定的状态。而以前体形式引入双金属与单金属的相态形成有所差别,进而影响在活化过程中金属活性相的转变。在以往的经验中证实金属合金相有利于向反应活性相转变[29]。从结果可知,所有的含Co样品均找到44.82°和65.26°附近的特征衍射峰,可归属于FeCo合金相(JCPDS44-1433)。随着钴相对含量的增多(X值降低),铁钴合金相的结晶度变大,且最高强度峰的角度会向右偏移,对于Fe/MC样品则只找到FeO相的特征衍射峰(JCPDS06-0615),表现出与双金属掺杂形成合金相的明显区别。
2.3 FeCo/MC催化剂的表面性质
通过H2-TPR来进一步鉴定铁相并考察铁与碳载体之间的相互作用,结果如图4(b)所示。所有样品均在300~500℃的相似位置出现一个还原峰,根据文献报道通常归属于Fe2O3还原为Fe3O4的过程[30],这可能是因为少量分散在碳层表面的铁物种暴露于空气中氧化所致。且随着双金属中Fe比例的提升(X值变大),还原峰会逐渐向右偏移,表明金属与载体间相互作用力的增强,这有利于稳定金属纳米粒子尺寸,提高在载体上分散度,这与TEM上得到的粒径分布的趋势相吻合。通过拉曼光谱分析不同铁钴比样品石墨化程度,结果如图4(c)所示。所有样品均观察到约1342 cm-1的D峰和约1589 cm-1的G峰,D峰与碳质结构中存在缺陷或无序的碳基质有关,G峰与石墨层中sp2键合的碳原子的振动有关。D带与G带的强度比(ID/IG)表示碳材料的石墨化程度。随着Fe相对含量的升高(X值变大),ID/IG从1.17降低到0.85,材料石墨化程度变大,说明对于铁钴双金属而言,Fe相对含量的增加导致载体石墨化程度增大。

图2 热解前([a)~(d)]和热解后([e)~(h)]催化剂的SEM图Fig.2 SEM images of catalysts before[(a)—(d)]and after pyrolysis[(e)—(h)]
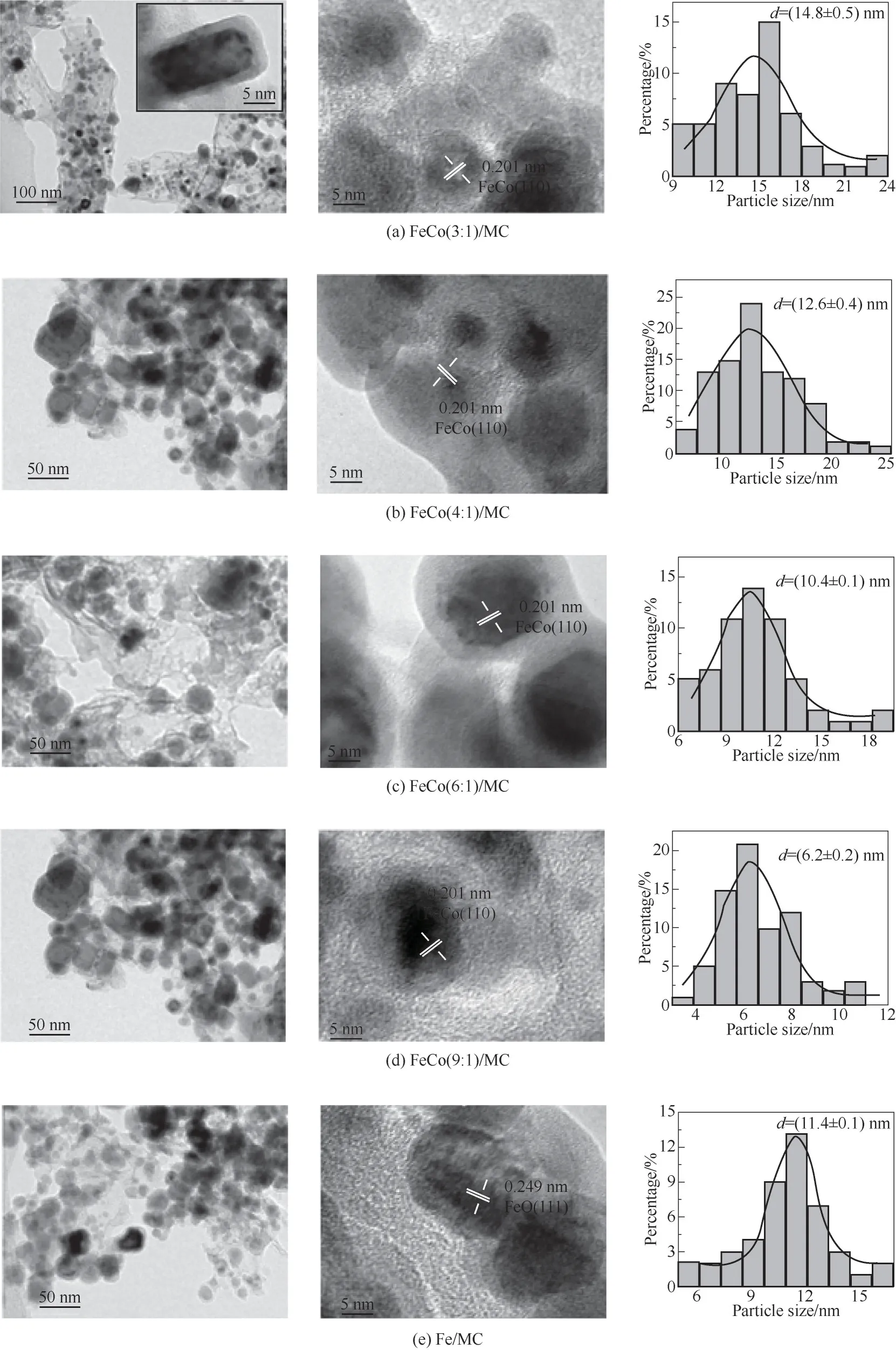
图3 FeCo/MC催化剂的HR-TEM图和粒径分布Fig.3 HR-TEMimages and particlesize distribution of FeCo/MCcatalysts
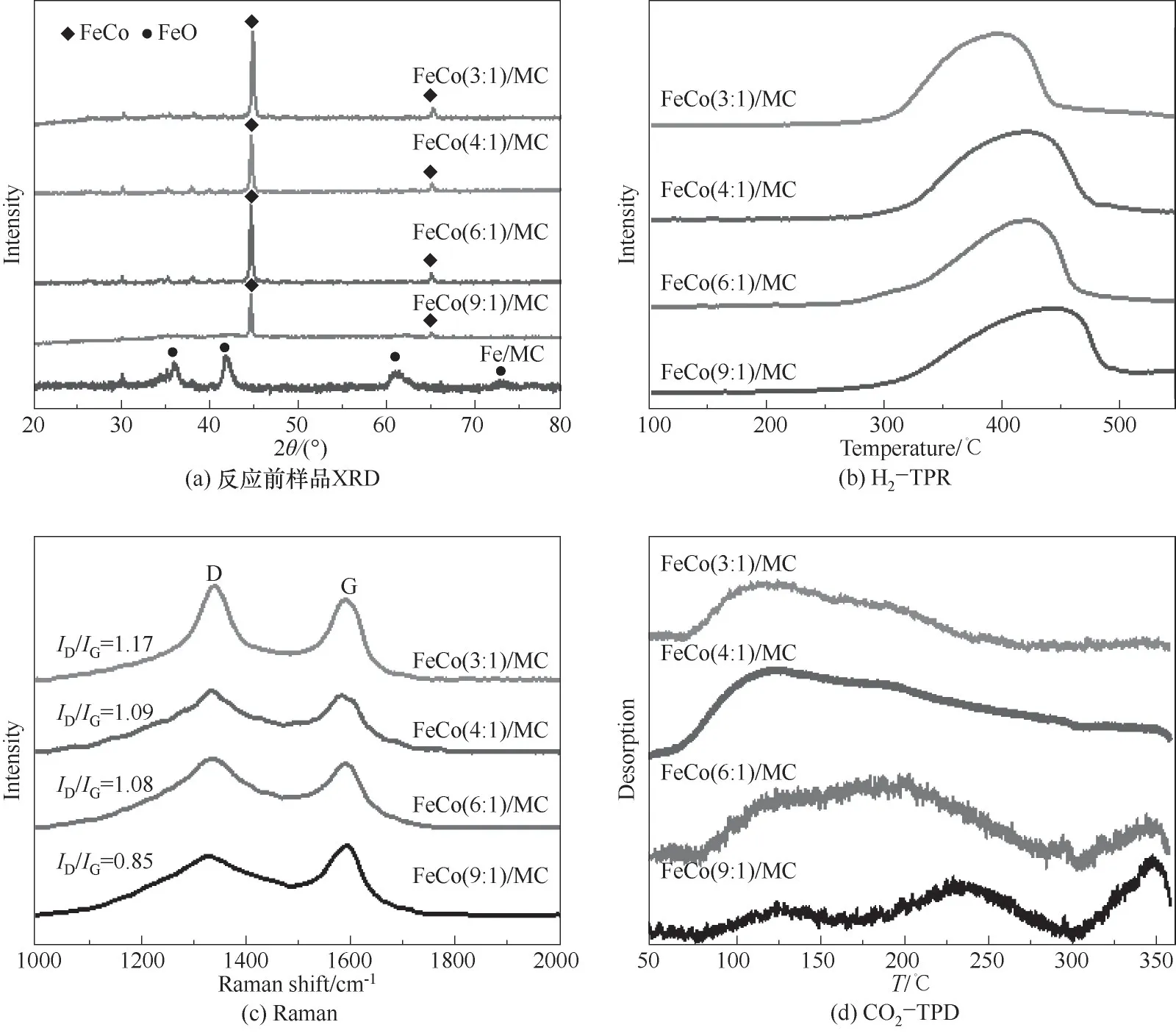
图4 催化剂性能表征Fig.4 Characterization of catalysts
为了研究催化剂表面碱度和CO2吸附能力,对样品测试了CO2-TPD,结果如图4(d)和表2所示,发现120、230和340℃附近有三种类型解吸峰。100~120℃附近的峰可归于催化剂表面上物理吸收的弱碱性位点,而230℃和340℃处的峰对应于中等强度化学吸附的碱性位点。可知随着Fe含量升高,100~120℃处弱碱性位点的峰会略微向高温区偏移,同时X=6时弱物理吸附的峰出现裂分且在340℃附近形成一个新的解吸峰,X=9时形成较为明显的三个解吸峰,且高温区的峰强变大。由图4(d)不同温度解吸峰的结果可知,低Fe含量的催化剂更倾向于形成物理吸附的碱性位点,随铁钴比增加,低温区峰面积减小,高温区峰面积增加,表明在高Fe量催化剂上更倾向于形成强化学吸附的碱性位点。但从表2可以看出,Fe/MC催化剂CO2吸附量很低,随着Co的引入,CO2吸附量逐渐升高,表明催化剂总碱量受Co影响更大,因此可以看出Co诱导的物理吸附的碱性位点更有利于CO2的吸附。
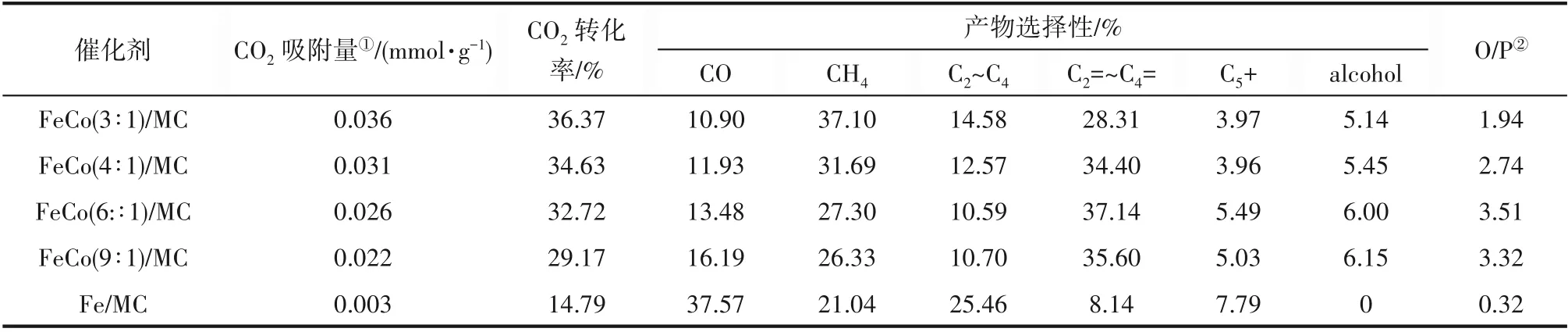
表2 FeCo/MC催化剂的CO2加氢性能Table 2 CO2 hydrogenation performance of FeCo/MC catalysts
2.4 FeCo/MC催化剂反应中的相转变
为了研究反应后催化剂中的物相组成,对反应后的样品进行了XRD测试,结果如图5所示。可以看出反应阶段金属相态的变化,所有的样品均出现类似的特征衍射峰。30.11°、35.46°、57.00°和62.60°附近的特征衍射峰可归属于Fe3O4相(JCPDS 89-0691)。在45.04°附近较杂的特征衍射峰可归属于Fe5C2相(JCPDS20-0509)。氧化物和碳化物相的出现证实了反应过程中合金相向活性相转变的过程。由于催化剂钴含量较低,未观测到明显的钴物种的峰。此外,反应过的Fe/MC样品上只观测到了Fe3O4相,没有看到Fe5C2相。通常在FTS反应期间,CO裂解的碳原子显示出对铁原子的高度亲和力,从而导致了碳化铁相的形成。Fe2C由于其热力学不稳定性,常出现于低温费托中,而Fe3C和Fe7C3则通常需要更高的反应温度和化学势才能稳定存在[31]。相对来说,在CO2加氢/高温FTS条件下,Fe5C2更能稳定地存在且最适合用于CO的吸附。
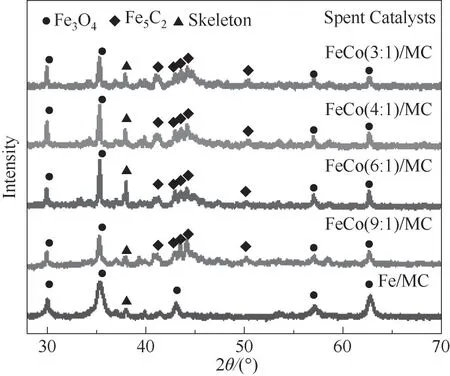
图5 反应后FeCo/MC催化剂的XRD图Fig.5 XRDimages of spent FeCo/MCcatalysts
2.5 FeCo/MC催化剂的CO2加氢性能
选择性仅为8.14%,加入适量的钴后最高可达到37.14%(X=6)。相对地,C2~C4的链烷烃选择性则明显降低,而低碳烃类的烯烷比(O/P)在添加钴之后显著增加,由Fe/MC的0.32上升到最高的3.51(X=6)。
从相态转变的角度进一步理解Co添加对活性位的影响。Fe/MC样品CO2转化率很低,而微量的钴加入(X=9)后反应活性会有明显提高。铁物种虽然具有催化RWGS和FTS反应的能力,但CO2是热力学稳定且化学惰性的分子。CO2-TPD的结果可以证实,仅含铁的催化剂总碱量较低,难以提供足够的碱性位来吸附活化CO2,Co的添加可以显著增加催化剂的总碱量,从而有效改善CO2吸附。此外,传统观点认为钴的水煤气反应(WGS)的活性较低,但具有较强的FTS活性和高稳定性,因此钴的引入可通过FTS途径的CO消耗促进RWGS反应正向进行,同时避免了WGS副反应的发生以促进CO2转化。

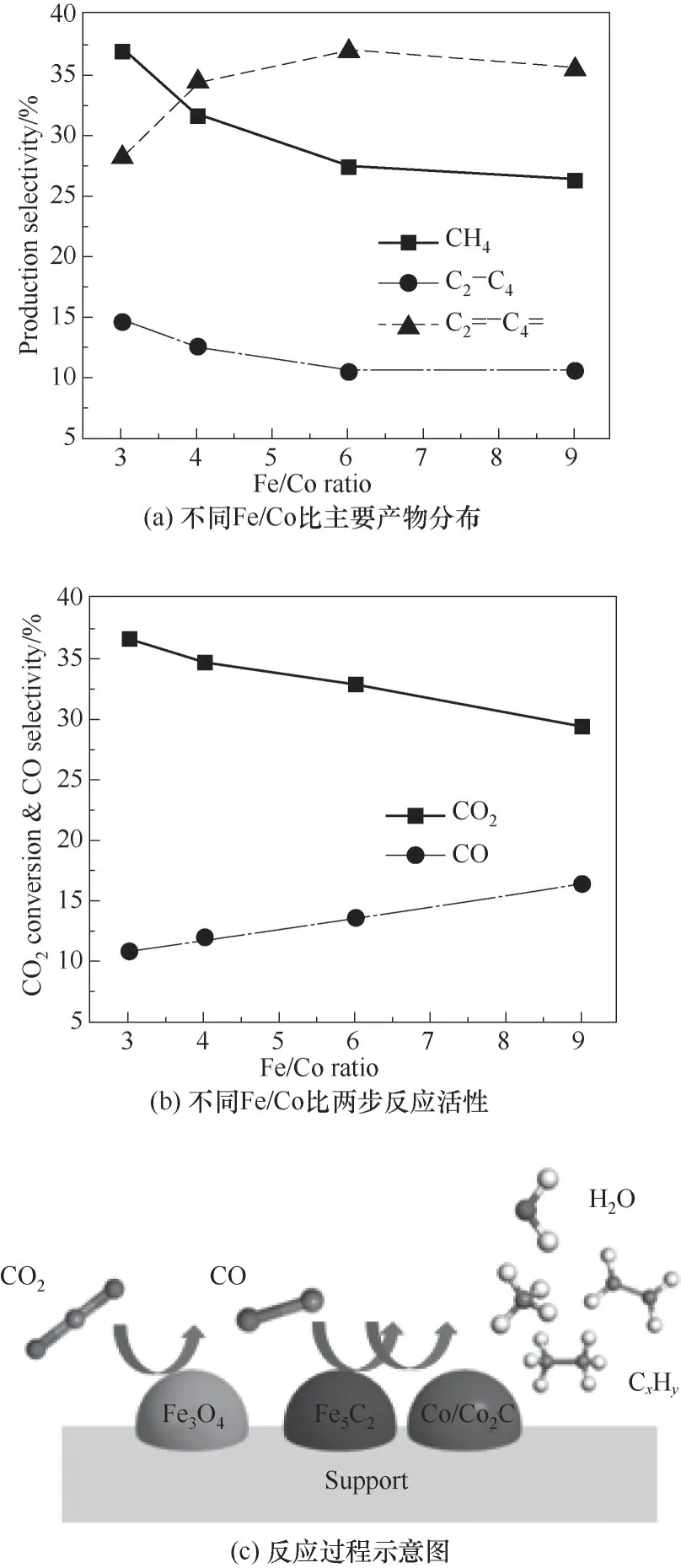
图6 不同Fe/Co比时的反应性能及反应过程示意图Fig.6 Reaction performance with different Fe/Co ratio and schematic diagramof the reaction process
此外,从图6可以看出,不同铁钴比例对反应活性和产物选择性有较明显的调节作用。在金属总量保持不变的情况下,CO2转化率随着样品中铁含量的上升而下降,CO选择性则与铁量变化趋势相同。这与前文TPD和XRD表征结果一致,对产物分布而言,随着铁量比例增加使得甲烷含量明显下降。而C2~C4的烷烃和烯烃的变化情况则不单调变化,低碳烯烃的选择性随X值增大出现先增后减,在X=6时出现了最大的低碳烯烃选择性(37.14%)。低碳烷烃选择性则与之相反,在X=6处出现最低的选择性(10.59%)。烯烷比(O/P)也在X=6处达到最高的3.51。此外,反应中还会生成少量的C5+以及醇类物质,由于不是主要的目标产物,所以不予过多讨论。但醇类的产生可能与钴以及碱金属钠的促进有关,虽然碱金属可以通过调节催化剂表面电子云密度增加CO的插入速率并降低氢化速率,有利于活性金属的碳化并提高链增长的可能性,但与Co联用时也有利于氧化物的产生,因此在产物中会检测到少量醇的存在[33]。样品在X=6处获得最高的烯烃选择性。分析其可能的原因,Co和Fe催化剂在CO2和CO加氢中的催化性质显著不同,这意味着控制C2+烃的C—C键形成对控制活性金属上CO2和H2的覆盖范围的重要性。可以通过改变样品中FeCo双金属的比例来改善CO2和H2的表面化学吸附特性,以利于C—C键的形成,从而增加高级碳氢化合物的含量。而对甲烷而言,适当的钴量可以将甲烷选择性控制在可接受的水平,该系列催化剂最高的甲烷选择性(X=3)达到37.10%,比之前工作中最低的甲烷选择性(44.50%)[29]还要有明显的下降,且可通过调控铁钴比例使其进一步下降到30%以下。
从构效关系看,适当的金属比例有助于改善铁钴之间的亲密度,从而有效地串联反应的不同活性位,如图6(c)所示。即对FTS反应而言,Co负责CO的解离,而Fe5C2负责350℃下的链增长生成烯烃的过程,通过不同活性位点的协同作用以增强反应性能。适当的钴量有助于维持与铁位点的密切接触,会使Co的周围保持相对较高的CO浓度,这有利于通过FTS反应生成C2+碳氢化合物。相反,过高的钴量降低了铁钴之间的亲密度导致钴位点上较低的CO浓度和较高的CO2浓度,这更倾向于形成CH4,而过低的钴量不利于铁相的转化,无法提供足够生产的烯烃的活性位点。
3结 论
(1)将少量Co以前体形式引入Fe-MOF中,可与铁以合金形式形成良好的双金属协同作用。Co可以有效增加催化剂表面总碱量,进而改善CO2吸附;另外,Co能有效促进铁的碳化并通过FTS路径的CO消耗促进RWGS的正向进行,从而高效地串联活性位点,与转变的铁相协同改善RWGS和FTS反应活性。
(2)通过调控铁钴比例可以获取最佳的低碳烯烃选择性并获得尽可能低的甲烷选择性,在所有的催化剂中,FeCo(6∶1)/MC展现出了最高的低碳烯烃选择性(37.14%)以及相对低的甲烷选择性(27.30%)。适当的金属比例有助于改善铁钴之间的亲密度,从而合理串联反应活性位,使低碳烯烃选择性大幅提高。
致谢:衷心感谢恩师天津大学米镇涛教授多年来的关心和指导,谨以此文祝贺他的80岁生日!

