浅谈化工流程题的高考二轮复习策略
河北
(作者单位:石家庄市第二十二中学河北定州中学)
化工流程题常以某种化工产品的制备为背景,要求考生综合运用物质的分离提纯、化学反应原理、元素及其化合物性质等相关知识合理分析工艺流程图等题给信息,考查考生在真实、复杂的问题情境中解决问题的能力。化工流程题因其具有陌生度高、信息量大、综合性强、能充分评价考生素养水平等特点,已成为高考必考题型,但也是得分率较低的题型。本文试对化工流程题的高考二轮复习思路和策略进行探讨,以期能够对师生有所帮助。
一、化工流程题的复习思路
化工流程题的复习可分两轮进行。一轮复习重在帮助学生了解试题结构,明确常见工艺操作步骤的作用,使学生初步学会分析工艺流程图,能够借助题干信息梳理出产品中核心元素的转化主线和杂质的分离过程及方法,完成简单的题目设置。二轮复习则强调综合性和应用性,着眼于引导学生完善解题模型,形成化工流程图包含“预处理、核心反应、产品提纯”三个主要组成部分的思维模式,综合利用所学知识和题目信息分析各转化步骤的操作和反应的意义及目的,熟练掌握解题技巧。
一轮复习后,学生在化工流程题型中常出现的问题有:死记硬背基础知识,不能综合所学知识处理陌生信息类试题;面对复杂多变的转化流程无法理清头绪;解题模型运用不灵活,考虑问题较片面,不能从全局分析物质转化过程。
为了提高复习效率,二轮复习不宜单纯采用刷题策略,建议采用“以点带面”的方式,选取具有典型性的物质制备工艺为情境,设计系列问题任务,通过问题解决促使学生进一步反思、优化相关知识结构。例如,过渡金属钒的工业价值高,价态多,存在形式会根据溶液pH的变化而改变,同时钒元素的分离提纯涉及萃取法、离子交换法、沉淀法等,使钒的工业提取涉及氧化还原反应、离子反应、平衡原理、物质分离基本方法等众多知识,因此钒的工业提取可作为教学情境范例。下文就以钒的工业提取工艺为例,浅谈化工流程题的二轮复习具体策略。
二、化工流程题的二轮复习策略
1.明目的,抓核心元素,明确产品转化主线
二轮复习中,教师应引导学生牢牢抓住工艺目的,从目的出发解析工艺流程图,对比原料和产品中的元素,分析哪些是产品元素,哪些是杂质元素,进而提取出产品中核心元素的转化主线和核心转化反应,明确杂质元素的分离操作步骤,将工艺流程图划分为原料预处理、核心转化反应和产品分离提纯三部分(见图1)。
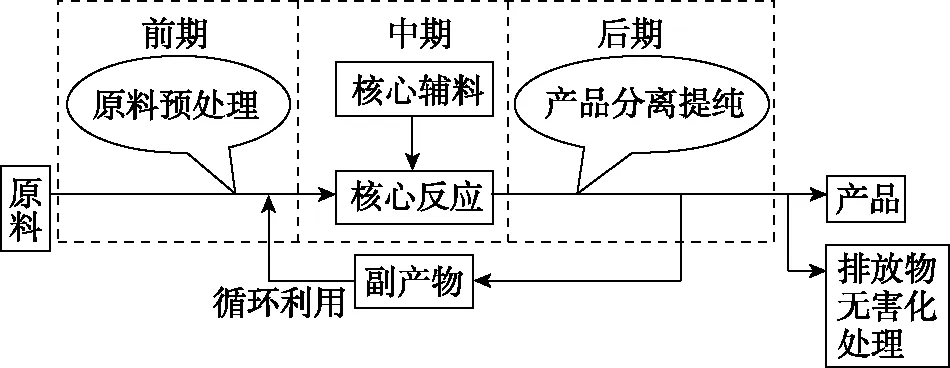
图1
钒的提取工艺主要有火法焙烧提钒和湿法浸出提钒两种方式。在复习时,可先设置学习任务1:根据工艺目的,自主分析钒的两种工业提取流程(见例1、例2),明确核心元素转化主线,按照图1所示将工艺流程图进行适当划分。
【例1】(2016·全国卷Ⅲ·28节选)以硅藻土为载体的五氧化二钒(V2O5)是接触法生产硫酸的催化剂。从废钒催化剂中回收V2O5既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为
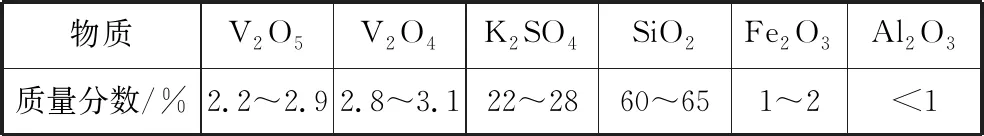
表1
图2是一种废钒催化剂回收工艺路线:
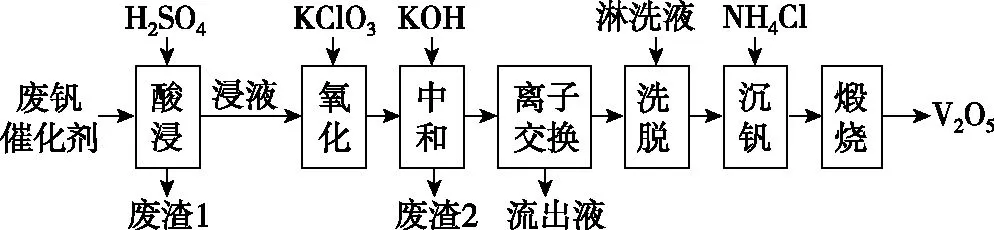
图2
【例2】(2020·济南市高三一模·16节选)利用某冶金行业废渣(主要含V2O3,还有少量SiO2、P2O5等杂质)制备(NH4)5(VO)6(CO3)4(OH)9·10H2O,生产工艺如图3:
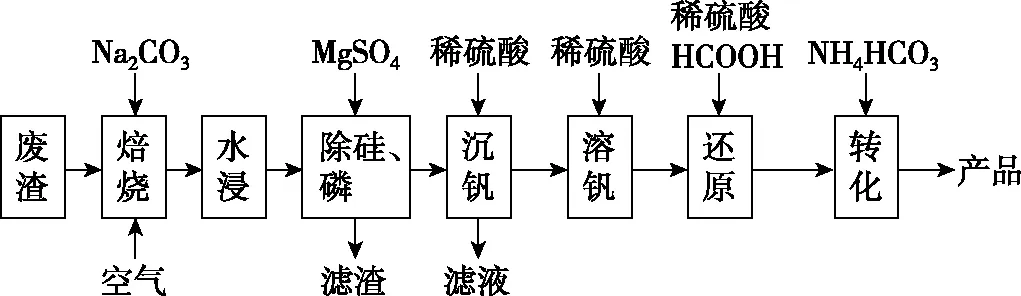
图3
学生通过自主思考、组内交流、展示汇报等环节完成学习任务1,分析结果如图4。然后进一步引导学生思考:钒的两种提取工艺流程的共性是什么?学生不难发现,两个流程都是先将钒元素从含钒原料转化成无机盐类化合物,利用浸取实现钒元素与难溶杂质的分离,再利用萃取-反萃取法或离子交换法实现钒元素的富集纯化,最后加入可溶性钙或铵盐沉钒、煅烧得到精品V2O5。这样设问的目的在于使学生体会复杂多变的工艺流程仍是有诸多共性的,学会从全局角度去分析工艺流程图,用元素守恒的思想分析元素的流向,用元素的价态观分析化学反应,就能消除分析工艺流程图时的惧怕心理。

图4
2.精析各工艺步骤,关注操作和反应
在宏观把握整个流程之后,教师需要引导学生聚焦于各个步骤,对于每一个步骤,既要关注操作,又要关注转化反应,可针对题给问题分析细节,无需把每个步骤的原理都搞清楚。
具体来说,可设置学习任务2:分析例1,回答以下问题:①酸浸的目的是什么?如何加快酸浸速率?②氧化步骤的目的是什么?请写出对应的化学方程式。还可以用什么氧化剂?③沉钒步骤的目的又是什么?
对于问题①,教师可在学生相互讨论补充的基础上,适时总结提高原料浸出效率的措施,明确目的在于实现核心元素和杂质元素的分离,提高钒的转化效率。对于问题②,教师要引导学生关注流程图中箭头的指向,前后比较,追溯物质转化过程,进而结合物质性质思考杂质元素分离方法,同时认识到由于原料中钒元素有+3、+5价两种价态,为便于后续生产,需要加入氧化剂将钒元素全部氧化为+5价,并通过书写方程式进一步巩固氧化还原反应和离子反应等知识。对于问题③,教师可进一步给出NH4VO3的溶度积常数,引导学生通过计算所需试剂浓度来巩固沉淀溶解平衡知识。在此之后,教师引导学生思考、总结杂质元素和核心元素分离的总体思路,即“转化→分离”。
3.解读陌生信息,感悟反应条件控制
化工流程题常设置陌生信息,考查学生有效提取、整合、应用新信息的能力。钒的工业提取中常出现的信息有:不同金属离子开始沉淀和完全沉淀的pH、钒元素存在形式与溶液pH的关系、钒元素的富集方法等。面对新信息,需要教师帮助学生理解提示信息,挖掘隐含作用,然后结合离子反应、平衡原理、实验基本知识等已学内容,把看似复杂、陌生的分离、富集、转化过程转化为化学知识去认识、去思考。
具体来说,教师可先提出学习任务3:结合信息,分析例3流程,思考如何选择调pH的合理区间。
【例3】(2020·全国卷Ⅰ·26节选)钒具有广泛用途。黏土钒矿中,钒以+3、+4、+5价的化合物存在,还包括钾、镁的铝硅酸盐,以及SiO2、Fe3O4。采用以下工艺流程可由黏土钒矿制备NH4VO3。
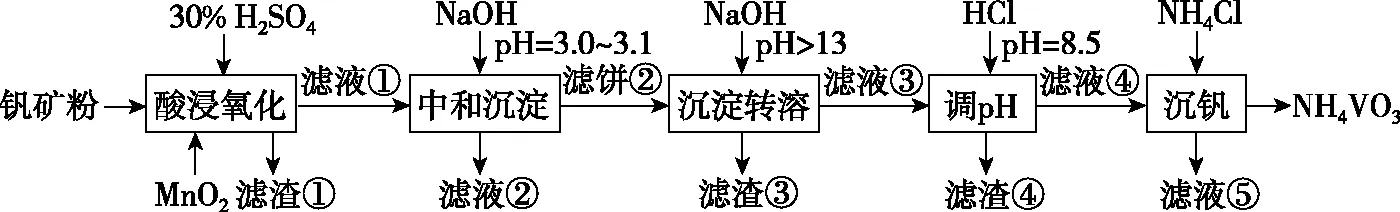
图5
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如表2所示:
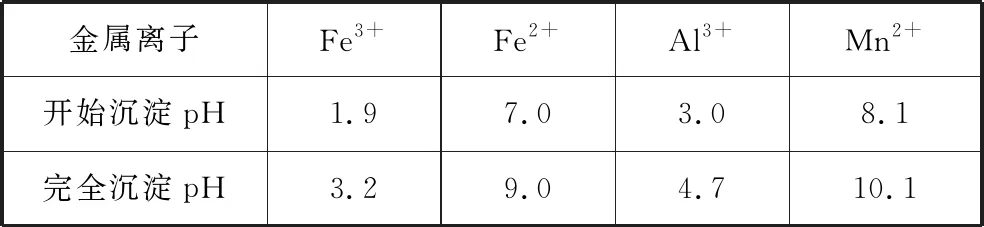
表2
学生依据“不增不减易分离”的除杂原则,经讨论得出答案,并总结出调节pH的方法:除去酸性溶液的杂质元素,多加入含核心元素的难溶氧化物、氢氧化物或碳酸盐等,以增大杂质离子水解程度,达到将杂质离子转化为氢氧化物沉淀而除去的目的,即杂质离子完全沉淀pH≤应调节的pH<核心离子开始沉淀pH,据此确定pH调节范围,如除去MnSO4中的Fe2(SO4)3应为3.2≤pH<8.1。
教师追问:要除去MnSO4中的FeSO4,应如何操作?调节溶液pH分离杂质时,一定要将杂质离子转化为沉淀而除去吗?这里要强调:面对沉淀pH较为接近的两种金属离子,需要加入试剂(如H2O2等氧化剂)转化金属离子形态,来增大沉淀pH的差距;而面对易溶的Na+、K+等杂质离子,需要逆向思维,将核心元素转化为沉淀与杂质离子分离。
接着,教师提出学习任务4:利用如下信息分析例2流程中钒元素的存在形式所发生的变化及对应步骤的作用。
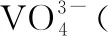
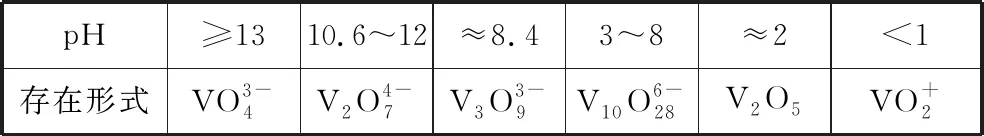
表3

教师再提出学习任务5:分析例4流程中萃取、反萃取两个步骤的作用,并结合信息思考如何提高萃取率?
【例4】从废钒(主要成分为V2O5、Fe2O3、SiO2等)中回收V2O5的一种工艺流程如图6所示:
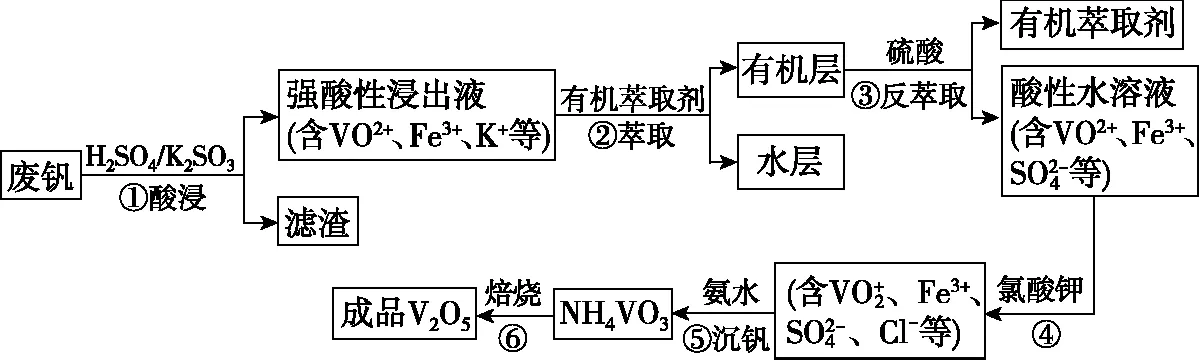
图6


最后,教师提出学习任务6:分析例1流程中离子交换和洗脱两步骤,并结合如下信息思考如何提高洗脱效率?
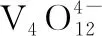
上述学习任务3-6重点在于引导学生学会解析信息、联系反应原理解决问题。面对陌生信息时,特别是萃取法、离子交换法等,需要引导学生围绕核心元素的转化去思考如何做到“去粗取精”,选择最佳转化条件,学会调取已掌握的相关知识综合解决。
4.注重引导学生反思,完善解题模型
针对化工流程题二轮复习,教师应引导学生对整个复习过程进行反思和总结,解答问题时要总揽全局、细致审题,紧紧抓住“原料→产品”这条主线,流程中每一步操作都是为了将核心元素向产品靠拢、杂质元素向与核心元素相反的存在形式转化。通过分段剖析、明晰细节,结合已有知识和设问信息,对每一设问步骤反复思考“反应物是什么?发生了怎样的反应?目的是什么?应采取怎样的操作?”从反应原理、环境保护、资源综合利用、循环回收等角度全面思考,使每种元素各有所归,做到规范作答。


