基于硫代水杨酸基电解液的纯铜电化学机械抛光反应机理研究
吴 頔, 康 仁 科, 牛 林, 潘 博, 郭 晓 光, 郭 江
( 大连理工大学 精密与特种加工教育部重点实验室, 辽宁 大连 116024 )
0 引 言
具有薄壁结构的铜材质精密零部件广泛应用于电子工业和精密物理试验中.电子工业和精密物理领域的迅速发展,对构件的径厚比要求不断增大,导致构件刚度减弱[1-2].在传统的机械加工过程中,构件在切削力的作用下容易发生变形,从而导致尺寸误差;同时,依赖机械作用的传统加工工艺不可避免地会造成表面损伤缺陷.
目前,通常采用化学机械抛光(CMP)工艺来实现弱刚性薄壁结构件的光整加工.然而,在CMP中,化学作用通常较弱,机械作用仍然起主导作用[3].因此,尽管通过CMP工艺可以获得超光滑表面[4],但磨粒的机械作用仍会在薄壁结构件表层引入应力,易引发变形.
电化学机械抛光(ECMP)是电化学作用与机械作用相结合的复合加工方法[5].在纯铜的ECMP 加工中,铜与电解液发生反应,在铜片表面形成一层膜阻碍阳极溶解.凸起部分的膜被磨粒去除后暴露出新鲜表面,将继续重复生成膜和膜被磨粒去除的过程;而凹陷处的膜不会被磨粒去除,可以对凹处起到保护作用,避免其与电解液发生反应被过度腐蚀.通过这一过程,凸起部分与凹陷部分的高度差逐渐减小,最终实现平坦化[6].由于磨粒的机械作用主要作用在膜上,ECMP的加工应力远低于CMP,同时可以避免划痕、磨粒嵌入等表面缺陷.此外,由于膜易于去除,相较于CMP,在同样的抛光压力下可以获得更高的材料去除率,因此,在保证同样材料去除率的状态下,ECMP所需的抛光压力更低,有助于抵制变形.
电解液是影响ECMP加工质量的重要因素,磷酸和磷酸盐是铜ECMP电解液的常用选择[7].而酸性电解液由于在晶粒、晶界处材料去除不均匀,易使粗糙度恶化.为了克服这一缺陷,通常采用碱性电解液来抑制腐蚀作用[8].然而,碱性电解液的抑制作用是有限的.为了获得较低的表面粗糙度,有必要使用合适的缓蚀剂.
目前,羟乙叉二膦酸(HEDP)经常作为缓蚀剂,其易与金属离子反应生成络合物,从而起到抑制金属腐蚀的作用.Wu等采用HEDP电解液实现了材料的快速去除,通过静态电化学实验,确定了电解被抑制的电位区域,通过表面形貌和粗糙度优化了HEDP电解液的工作电位.通过傅里叶变换红外光谱(FT-IR)对膜的成分进行测定,采用质谱分析确定膜的化学组成,从而阐明了HEDP电解液与纯铜工件的反应机理[9].但是由于HEDP电解液在ECMP加工过程中对表面质量改善效果有限,需要提出一种新的电解液体系来改善ECMP后的表面质量.硫代水杨酸(TSA)又称2-巯基苯甲酸,含有羧基和巯基,可以与金属离子结合成稳定配合物以抵抗腐蚀,因此可作为电化学加工的缓蚀剂[10].在之前的研究中,为了在短时间内获得高的表面质量,提出了一种两步ECMP组合工艺[11].在此工艺中,采用TSA基电解液获得了较好的表面质量,但反应机理尚未阐明.因此,为了改进配方、优化工艺参数以获得更低的表面粗糙度,纯铜材料与TSA基电解液的反应机理亟需阐明.
本文通过动电位极化和ECMP试验,选择TSA基电解液的最佳工作电位,在此基础上,通过对缓蚀膜主要成分的分析,探讨铜与TSA基电解液的反应机理.采用X射线能谱(EDS)、傅里叶变换红外光谱(FT-IR)和质谱分析对缓蚀膜的元素和化学组成进行测定,推断物质结构和反应机理.
1 试验方法
动电位极化和ECMP试验采用三电极体系,由铜工件作为工作电极(WE),饱和甘汞电极(SCE)作为参比电极(RE),石墨盘作为对电极(CE),如图1所示.利用PARSTAT 2273型电化学工作站作为电源并采集信号.试验前用800目砂纸打磨铜片,打磨后用去离子水冲洗.以质量分数4%甘氨酸、1.5%硫代水杨酸(TSA)、1%聚乙二醇、5%硅溶胶、2%氢氧化钾(KOH)和去离子水为电解液,pH为8.5.
动电位极化试验扫描速率为10 mV/s,扫描范围为-1.0~10.0 V(饱和甘汞电极为参考电极),使用尺寸为10 mm×15 mm×1 mm纯铜片.ECMP试验采用φ100 mm×3 mm大小的纯铜片.操作时间设定为30 min,所有试验均在25 ℃ 下进行.
以极化曲线中电解被抑制的电位区域作为ECMP的工作电位区域.用NV5000 5022S Zygo干涉仪测量去离子水和酒精清洗过的铜表面,获得不同工作电位下的表面粗糙度.ECMP工作台采用Liu等设计的聚氨酯材质叶序抛光垫[12].ECMP工作台工作压力为1.86 kPa,焊盘转速为40 r/min,铜片转速为45 r/min,电解液流量为1.8 L/min.
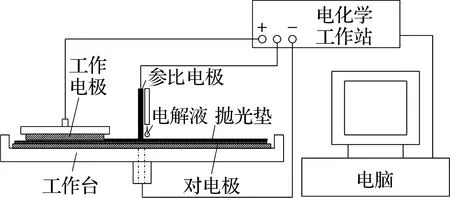
图1 动电位极化与ECMP试验装置
利用最低表面粗糙度对应的电位,采用ECMP 工具,电解1 min后在铜表面形成缓蚀膜.然后用EDS测定了膜的元素组成.
利用6700红外光谱仪测定了缓蚀膜红外光谱和官能团.FT-IR中使用的样品通常是一种包含近5 mg的缓蚀膜和150 mg的KBr固体粉末的特殊样本.最后,缓蚀膜通过质谱仪测定,确定其化学组成.
采用LTQ Orbitrap XL线性离子阱-高分辨液质联用仪对缓蚀膜的液相质谱进行测定.将粉状缓蚀膜称取50 mg溶于20 mL去离子水中,将该样本用于液相质谱检测.
2 结果分析与讨论
2.1 动电位极化和ECMP结果
电位-动态极化曲线显示了两个受电流密度限制的区域,如图2所示.第一个区域从0到1.5 V,该区域是该抛光液的钝化过渡区及钝化区.1.5~2.0 V是过钝化区,当电压升高,电流密度进一步升高.第二个区域从2到10 V,在此过程中工件表面有大量黑膜附着其上,电流密度保持在0.1 A/cm2左右.当电位大于3 V时,铜表面出现大量气泡,说明该电位区间对应于析氧区.
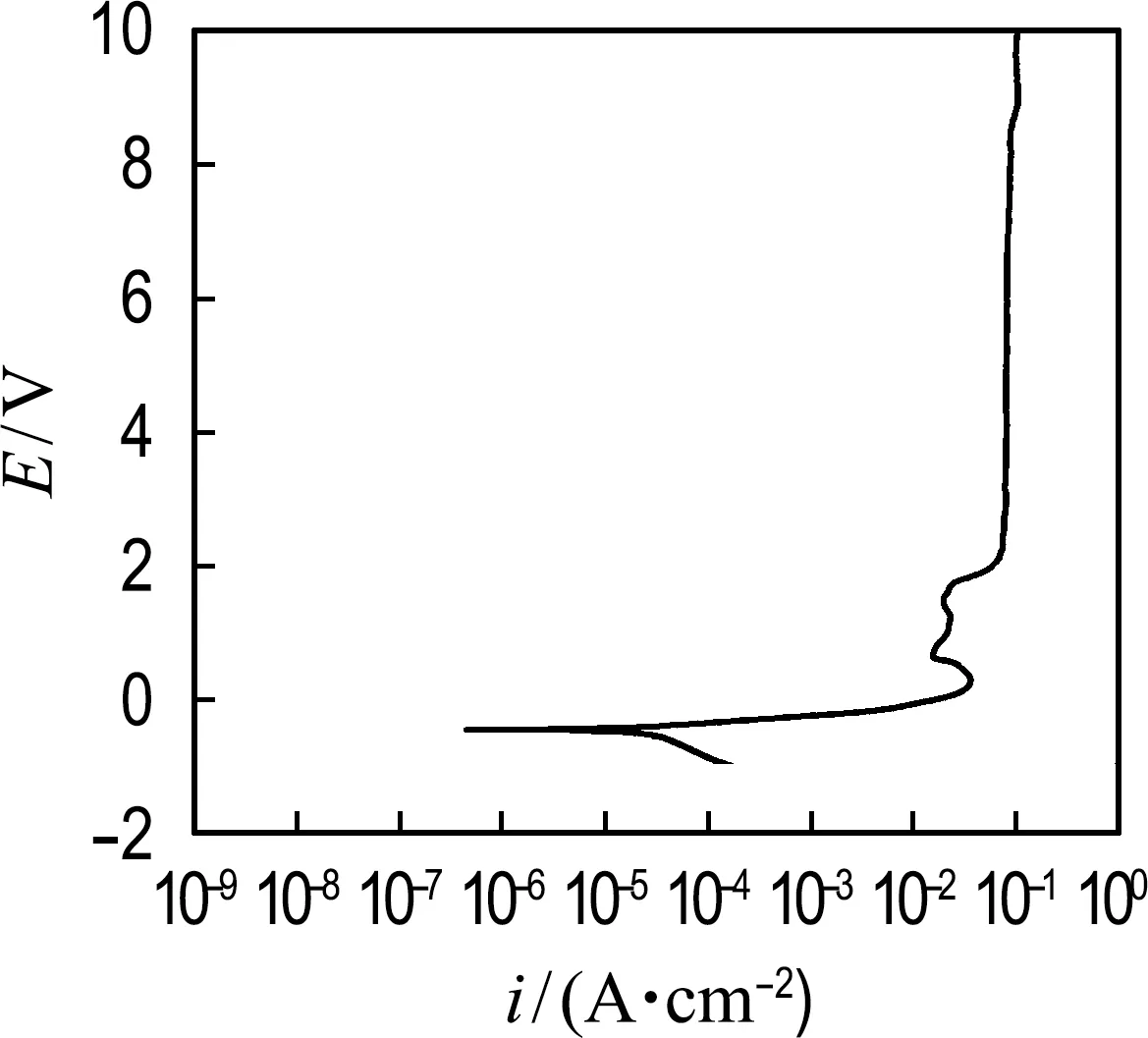
图2 TSA基电解液动电位极化曲线
为了给ECMP创造一个稳定的工作环境,需要在电流平阶区域选取操作电位.气泡对电场分布有较大的影响,会使表面粗糙度下降.因此,选择2 V作为操作电位.为了比较,在析氧电位4 V下也进行了试验,结果工件表面粗糙度表现出明显的差异.
如图3(a)和图3(c)所示,铜表面有很多划痕.抛光后,表面明显消除了划痕.如图3(b)所示,在2 V下获得的粗糙度为8.3 nm,这表明了这种TSA基电解液和所选择电位的有效性.如图3(d)所示,在4 V的电势下,虽然表面粗糙度从297.3 nm改善到113.7 nm,但铜表面仍有许多凹坑.结果表明,在TSA基电解液中,析氧区的电位不适合铜的ECMP加工.

(a) E=2 V,抛光前,Ra=251.7 nm

(b) E=2 V,抛光后,Ra=8.3 nm
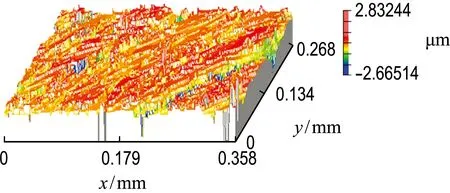
(c) E=4 V,抛光前,Ra=297.3 nm
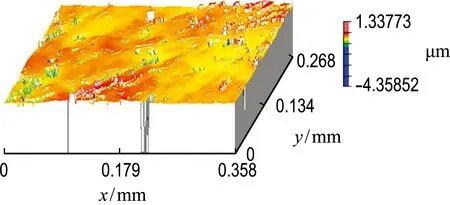
(d) E=4 V,抛光后,Ra=113.7 nm
2.2 缓蚀膜的FT-IR
通过ECMP工作台在2 V下的1 min的恒电位极化,在铜表面生成一层黑色缓蚀膜,最大厚度约4 mm.缓蚀膜的表面形态如图4所示.缓蚀膜蓬松多孔,易变形,用力搓揉会呈粉状.根据表1所示的元素组成,缓蚀膜中不含氮元素,即缓蚀膜中不含甘氨酸.然后刮取缓蚀膜做样品.用6700红外光谱仪对其进行了红外光谱分析.

图4 缓蚀膜表面形态

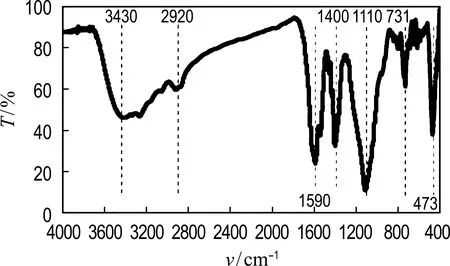
图5 缓蚀膜KBr压片样本FT-IR光谱
2.3 缓蚀膜质谱
根据缓蚀膜相应样本的红外光谱和质谱,得到了相应离子的分子结构.

表1 缓蚀膜的元素组成

(a) [C14H10O4S]的分子结构

(b) [C14H10O4S]的FT-IR光谱
由图7(a)可知,缓蚀膜中主要产物离子的质荷比分别为121.030 2、137.025 1、200.987 0、273.023 5、289.018 4和305.013 3.根据TSA质谱,其离子碎片[C7H5O2]-和[C7H5OS]-质荷比分别为121和137,与缓蚀膜的质谱对应,说明缓蚀膜中TSA含量较多.根据缓蚀膜的元素组成,缓蚀膜中含有Cu元素,TSA中的羧基易与金属离子结合形成配合物,所以缓蚀膜质谱中的质荷比200.987 0、273.023 5、289.018 4和305.013 3极有可能对应于TSA金属配合物的离子碎片.


图7 缓蚀膜液体样本质谱与相应离子结构
质谱结果表明,两个TSA双脱质子生成[C12H8(COO)2SO2]2-[14].除此之外,由于[C12H8(COO)2SO2]2-的COOasym基团可以转化为两个C—Osym基团,使[C12H8(COO)2SO2]2-转化为[C14H8O6S]4-[15].然后[C14H8O6S]4-与Cu2+结合形成配位化合物[C14H8O6SCu]2-,如图8所示.此外,在这个反应中还生成了[C12H8(COOH)2S2](二硫代水杨酸,DTSA).
DTSA是一种医药、染料、杀菌剂BIT和光引发剂ITX等重要中间体,添加于涂料和黏合剂中可提高防霉性能.其合成条件要求严格,而DTSA在电化学反应过程中可以快速生成,这为DTSA的合成提供了新的可能.

图8 TSA基电解液与铜反应机理
3 结 论
(1)ECMP可以将工件表面粗糙度在2 V下由251.7 nm改善至8.3 nm,减少96.7%.TSA基电解液由4%甘氨酸、1.5%硫代水杨酸(TSA)、1%聚乙二醇、5%硅溶胶、2%氢氧化钾(KOH)和去离子水组成,pH为8.5.
(2)TSA脱质子生成[C14H8O6S]4-,然后[C14H8O6S]4-与Cu2+结合形成配位化合物[C14H8O6SCu]2-.
(3)这种电化学反应过程可以快速生成DTSA,为DTSA合成提供了新的可能.

