后路枕颈融合内固定联合椎体成形术治疗枢椎转移瘤病理性骨折的疗效观察*
孙岩 董春科 王好 韦竑宇 杨峰 谭明生**
(1.北京中医药大学,北京 100029;2.中日友好医院骨科二部,北京 100029;3.首都医科大学附属北京中医医院骨科,北京 100010)
脊柱转移瘤的发病率为3%~30%,原发肿瘤以乳腺癌、肺癌、前列腺癌和肾癌为主[1-4]。脊柱转移瘤引起的疼痛、脊柱不稳定和神经症状严重影响患者的生活质量。外科手术能够有效提供脊柱稳定性、改善脊髓压迫症状,是目前主要的姑息治疗手段[5,6]。椎体是转移瘤常见的受累部位,而C2椎体转移瘤罕见[7],其位置紧邻延髓的呼吸及运动中枢,且活动度较大,容易造成序列不稳定从而引起疼痛,复杂的解剖结构也给手术带来难度,传统手术治疗易合并感染、言语不利、舌水肿、脑脊液漏等并发症[8-10],手术方式尚存争议。椎体成形术作为一种微创技术,具有快速有效缓解疼痛、固定椎体和一定的抗肿瘤作用,目前用于脊柱椎体转移瘤的治疗,然而涉及上颈椎区域的报道鲜见[11,12]。本研究探讨后路枕颈部融合固定术联合椎体成形术治疗转移性枢椎病理性骨折患者的疗效和安全性。
1 资料与方法
1.1 一般资料
纳入标准:①已经确诊的其他部位原发性肿瘤;②经过X 线片、CT、MRI 或PET-CT 等影像学检查确诊的单个C2 椎体转移瘤合并病理性骨折;③难治性疼痛、非手术治疗不能达到稳定和(或)存在进行性神经功能障碍;④预期存活时间>3 个月。排除标准:①脊柱原发性肿瘤患者;②累及范围超过C2 椎体的转移瘤患者;③严重内科疾病对手术不耐受者;④原发性肿瘤广泛转移及预计存活时间<3个月者。
回顾性分析2004 年3 月至2018 年8 月收治的符合纳入与排除标准的12 例C2 椎体转移瘤合并病理性骨折患者,男5 例,女7 例;年龄45~89 岁,平均(68.9±12.1)岁。原发肿瘤包括乳腺癌4 例,肺癌4例,前列腺癌2 例,肾癌2 例。术前均采用修订版Tokuhashi 评分系统预测患者的生存期[13],4 例患者为0~8 分(预期寿命<6 个月),8 例患者为9~15 分(预期寿命>6 个月);采用SINS 评分评估脊柱稳定性,5 例患者为7~12分(表示脊柱即将发生不稳定),7例患者为13~18分(表示脊柱不稳定),详见表1。
本研究经医院伦理委员会批准通过,所有纳入患者均签署相关知情同意书。
1.2 手术方法
采用全身麻醉,麻醉满意后取侧卧位,常规消毒铺巾,于髂前上棘处取出约3 cm×6 cm 髂骨,冲洗缝合。随后放置Mayfield 头架,翻身连接。颈枕部常规消毒铺巾,取后正中切口切开皮肤和皮下组织,小心剥离椎旁肌及枕肌,显露枕骨及C1 后弓及C2-C5 双侧侧块,并于C3-C5 拧入侧块螺钉。将枕骨板适当塑形置于枕后,于枕外隆突处拧入2 枚螺钉,并在透视下进行适当提拉复位。截取2根长度合适的钛棒,塑形后连接枕骨板及侧块螺钉,锁紧螺帽。仔细分离寰椎后弓至距中线约10 mm处,用尖嘴咬骨钳咬除寰椎后弓以解除压迫(图1A)。透视下经单侧C2 椎弓根置入椎体成形术工作套装,并用活检钳取出破碎骨质少许送病理,透视下注入适量骨水泥,待骨水泥完全硬化。打磨枕骨及C2棘突椎板及双侧侧块骨皮质,制备植骨床。修剪髂骨块,置于枢椎棘突及枕后部之间,并用双7 号丝线固定,将咬除的碎骨铺于植骨床(图1B)。冲洗伤口后放置引流管1根,之后逐层缝合。所有患者术后常规静脉应用抗炎、消肿、营养神经治疗,无脑脊液漏患者24 h 引流液<50 ml 即可拔除引流管。术后3~5 d 佩戴颈胸支具下地活动,严格佩戴支具3 个月。术后均转入肿瘤科进行放化疗或靶向治疗。
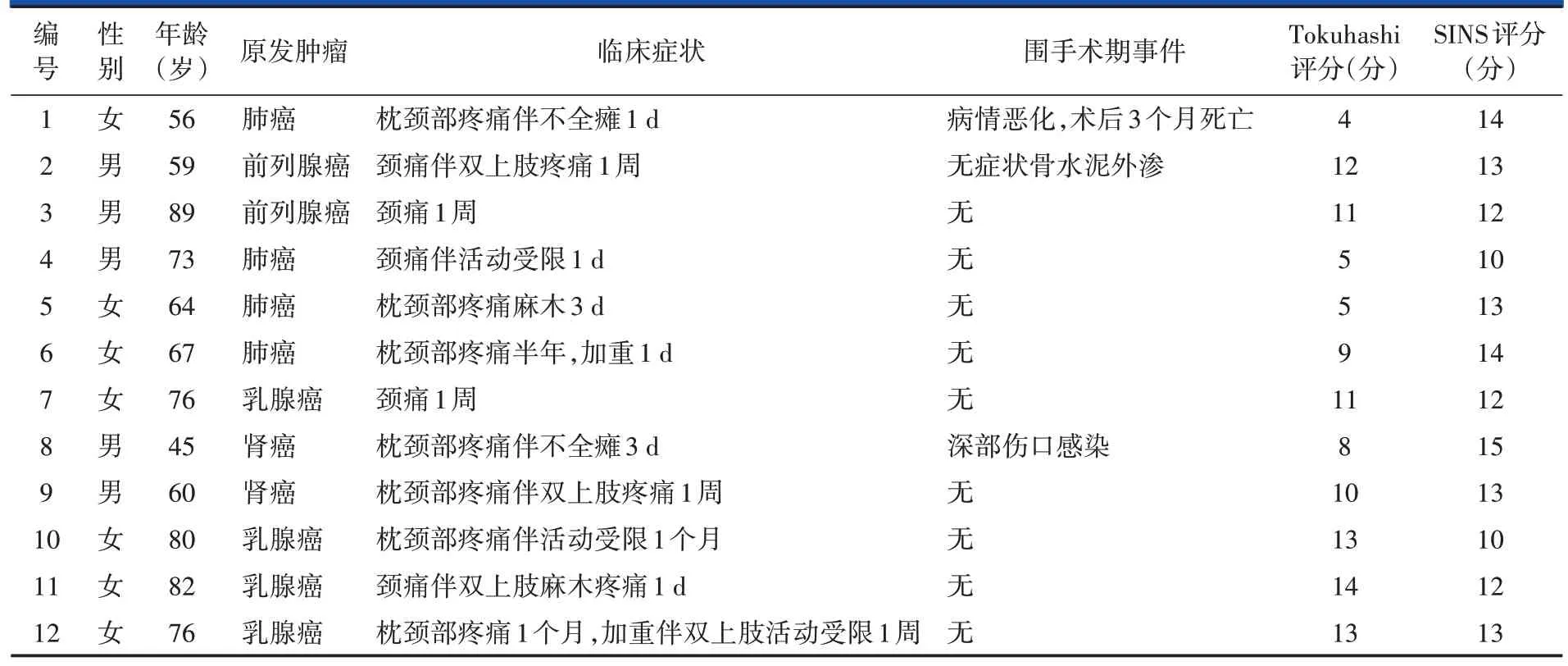
表1 12例患者的一般资料
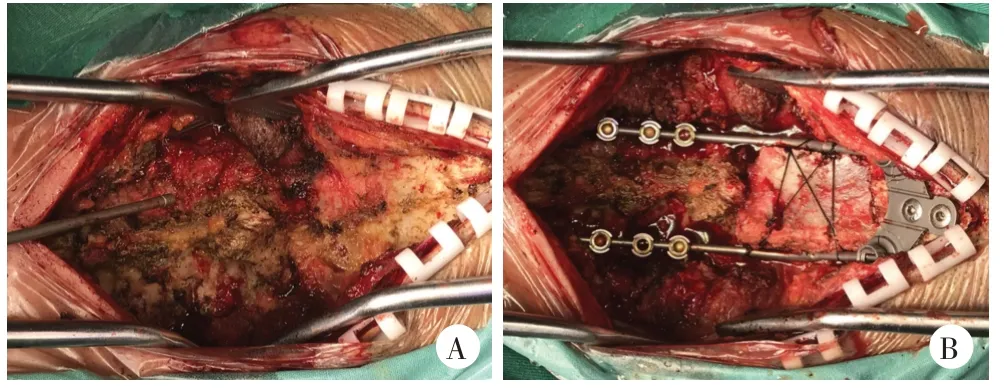
图1 手术操作示意图
1.3 评价指标
临床指标:①JOA 评分评估神经功能的改善情况,术后改善率=(术后评分-术前评分)/(17-术前评分)×100%;②NDI 指数评估颈椎功能改善情况;③VAS评分比较术前和术后的疼痛程度。
影像学指标:通过X线片、三维CT和MRI评估内固定物、椎体稳定性和骨水泥情况;测量脊髓有效空间(space available for the cord,SAC),选取齿突后缘至后椎板前缘的最短距离。
1.4 统计学方法
采用SPSS 20.0软件进行统计学分析。计量资料以均数±标准差表示,采用配对t检验,以P<0.05 为差异有统计学意义。
2 结果
2.1 手术及围手术期情况
12 患者均行后路枕颈部融合固定术,其中C0-C4 融合6 例,C0-C5 融合5 例,C0-C6 融合1 例,所有患者均于术中行C2 椎体成形术。手术时间为120~230 min,平均(167±30)min;失血量为200~450 ml,平均(293±73)ml;注入骨水泥量为2.4~3.2 ml,平均(2.8±0.2)ml。未进行任何肿瘤或椎体的切除,1 例患者出现深部伤口感染,采用清创治疗后好转;1 例患者出现无症状骨水泥渗漏;1例患者病情恶化,术后3个月死亡。无一例进行翻修手术。
2.2 随访结果
所有患者均获得随访,随访时间3~30个月,平均(17.7±9.1)个月。术前VAS 评分为(7.8±0.9)分,术后1 个月及末次随访分别降至(5.4±1.2)分和(4.1±1.2)分,疼痛明显缓解(P<0.05);术前JOA 评分为(7.3±2.5)分,术后1 个月及末次随访分别提高至(9.6±2.1)分 和(10.9±1.6)分(P<0.05),JOA总改善率为34.8%±4.6%;术前NDI 指数为(80.0±11.4)分,术后1个月及末次随访分别降至(63.2±15.6)分和(59.7±15.5)分(P<0.05),见表2。在整个随访期间,X 线片及CT 显示枢椎有不同程度复位,且内固定物位置良好、无松动,邻近椎体未再发现骨折及转移,1例出现无症状的骨水泥渗漏,1例患者出现深部伤口感染,采用清创治疗后好转,1 例患者病情恶化,3 个月后死亡。MRI显示术前的脊髓受压情况得到充分松解,SAC 由术前的(7.7±1.6)mm增加至术后的(12.3±1.5)mm和末次随访时的(11.9±1.6)mm,差异有统计学意义(P<0.05)。典型病例见图2。
表2 12例患者VAS、JOA评分,NDI指数及SAC值()

表2 12例患者VAS、JOA评分,NDI指数及SAC值()
3 讨论
3.1 手术目的及手术方式的选择
脊柱转移瘤的治疗需要考虑原发病、生活质量和预期寿命等多种因素,患者的一般状况、骨溶解、骨质疏松、脊髓压迫等情况都增加了疾病的复杂性[7],而手术方式的选择还需要考虑预期目标、转移的位置及数量等。上颈椎活动范围大,C2 椎体具有复杂的解剖结构,包括关节、韧带和软骨等,由于转移瘤造成C2 结构不稳定,而其位置紧邻延髓的呼吸及运动中枢,增加了手术难度。脊柱转移瘤手术治疗的目标不是根治性切除,而是缓解疼痛、预防神经功能障碍的加重和保持脊柱序列的稳定性[14-16],同时尽量避免并发症和二次手术。
对于传统开放性分离术式如椎体的分块或部分切除,其目的也并不是将脊柱肿瘤全部切除,而是通过手术解除压迫,在脊髓等重要结构周围创造出安全边界,从而为后续的放疗等肿瘤治疗创造条件[17],目前最常用于早期恶性肿瘤而不是转移瘤。对于枢椎转移合并病理性骨折的晚期患者,手术目的是重建脊柱稳定性,解除压迫,尽可能减轻临床症状,提高生存质量,全枢椎椎体切除术式创伤较大,其手术过程相对较长,有损伤血管导致出血的风险,无疑提高了术后并发症的发生率,研究表明微创技术术中失血少,手术时间短,住院时间短,并发症少,并且可以获得和传统分离手术相似的疗效,微创技术治疗脊柱转移瘤已被认可[18]。对于手术入路,既往文献并未达成共识[19,20],故须结合实际情况决定,考虑到口咽入路可能出现较多并发症如感染、舌咽水肿、脑脊液漏等,且内固定受技术条件所限,上颈椎区域仅能采用椎体间单纯植骨[21],也并不是治疗脊柱转移瘤尤其是枢椎转移瘤的最佳方案。
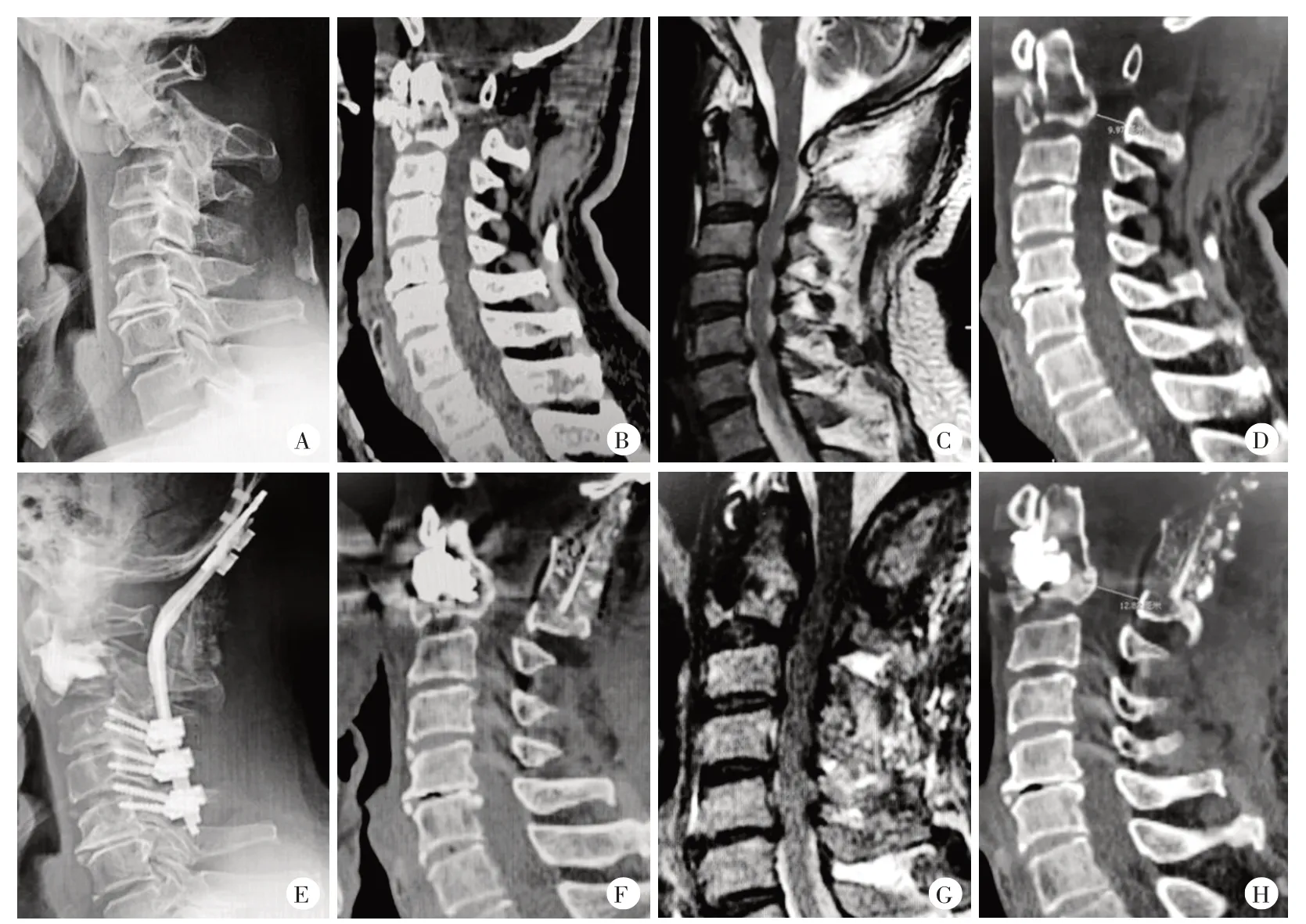
图2 典型病例(编号4),男,73岁,4个月前行PET-CT诊断为肺癌伴多发性骨转移,此次以“颈部外伤后颈痛伴活动受限1 d”收入院,行后路枕颈(C0-C5)融合固定术联合椎体成形术,术后疼痛明显缓解,肌力正常
本研究中12 例患者术前SINS 评分均大于7 分,7例患者在13分以上,均具有脊柱不稳定性,因而融合手术是必要的。选择枕颈后路固定、必要时减压并进行可视下复位,从而松解脊髓压迫成为解决枢椎椎体不稳、椎体塌陷以及脊髓受压的最佳治疗选择。叶曙明等[22]对36 例脊柱转移瘤患者行不同方式肿瘤切除,开放性手术时间1.8~5.0 h,平均2.9 h;术中失血量400~5700 ml,平均1442 ml。本研究中12 例患者的平均手术时间为(167±30)min,平均失血量为(293±73)ml,相较于传统肿瘤切除手术时间短、出血量少,术中可视下复位,影像学可见枢椎不同程度复位,尽可能的恢复了椎体序列从而充分松解脊髓,SAC 由术前(7.7±1.6)mm 增加至术后(11.9±1.6)mm,差异有统计学意义,明显减少了术后恢复时间、提高手术疗效,并降低了术后并发症发生率。
3.2 椎体成形术在脊柱转移瘤中的应用
椎体成形术首先应用于椎体血管瘤的治疗,后大量用于脊柱急性压缩性骨折,其能够迅速缓解疼痛及恢复脊柱序列,故被用于因转移瘤造成的脊柱压缩性骨折。目前,骨水泥已广泛应用于脊柱肿瘤的治疗,椎体成形术应用于脊柱转移瘤具有创伤小、恢复快以及术后并发症发生率低的优点,尤其适用于预后较差患者的姑息治疗,为椎板切除和椎体固定后可视下注入骨水泥增加了一定的安全性,如发现骨水泥渗漏可及时清除。Xie 等[23]对47 例脊柱转移瘤接受经皮椎体成形术的研究显示,患者VAS 评分从术前的8.4 分降至术后的3.4 分,提示经皮椎体成形术能够有效缓解脊柱转移瘤患者的疼痛。有中等证据表明,与接受常规治疗相比,接受椎体成形术治疗的患者在疼痛、生活质量及功能状态方面得分较高[24],其缓解疼痛的机制被认为是通过放热反应和化学及毒性作用阻止椎体微动以及破坏疼痛受体[25]。采用椎体成形术治疗的患者椎体高度也有较好的恢复,董晖等[26]通过姑息性切除减压内固定联合骨水泥填充治疗脊柱转移瘤,随访1年显示骨水泥能够有效维持椎体前中后缘高度,随访期间的差异无统计学意义。对于一般情况较差而不能耐受大型开放性手术的脊柱转移瘤患者,椎体成形术提供了新的选择,而且适用于复杂的上颈椎转移瘤的姑息治疗。有研究表明,骨水泥有抗肿瘤效果,可能是细胞毒性、热效应和局部缺血作用的结果[27,28]。然而,部分学者提出低复发率归因于较短的存活时间而非抗肿瘤效应。因此,抗肿瘤的相关作用机制和程度需要进一步研究。椎体成形术最常见的并发症是无症状的骨水泥通渗漏,其发生率为2.8%至9.3%。本研究中12例患者平均注入骨水泥量为(2.8±0.2)ml,与既往研究相近。可见,可视下操作能够有效避免骨水泥渗漏,以及出现骨水泥渗漏时及时采取清除减压等措施。
3.3 制订合理的手术方案
上颈椎活动度较大且缺乏支撑,如果患者临床状况良好且肿瘤稳定,强烈推荐延长后路固定(C0-C6)[29]。本研究中根据SINS 评分,患者有即将发生或已出现的脊柱不稳定,且长期卧床并营养不良,平均年龄为(68.9±12.1)岁,以上条件均适于进行延长的后路固定以实现最大和最持久的稳定性,而较短的后路固定有继发失稳的可能性并增加再次手术的风险。本研究中患者的VAS、JOA 评分及NDI 指数在术后1个月及末次随访时均有所改善,与术前相比差异有统计学意义(P<0.05),说明该治疗方案能够有效缓解疼痛,改善功能障碍,后期随访并未发现骨水泥渗漏及邻近椎体塌陷或转移,钉棒系统固定良好,显示该术式并发症发生率低,有效维持脊柱序列的稳定,对于改善患者生存质量具有积极的意义。需要注意的是,术后放疗和化疗对于延长寿命和改善生活质量也很重要。
3.4 本研究的不足之处
由于C2 椎体转移瘤实属罕见,故本研究所纳入病例数较少,未设置对照组,随访时间也较短。需要增加样本量,进行前瞻性设计的对照研究,同时延长随访时间,以进一步探讨不同入路及短节段固定的临床效果,为临床提供更详实的参考。
综上,后路枕颈部融合内固定联合椎体成形术是治疗枢椎转移的一种安全而有价值的姑息性治疗方法,能够迅速缓解疼痛,重建脊柱稳定性,改善功能障碍,提高患者生存质量。然而,脊柱转移瘤的治疗依然具有挑战性,多学科协作的治疗方式在脊柱转移瘤的治疗过程中尤为重要,以保证患者得到最佳的治疗。

