以辉锑矿为原料放电等离子烧结快速制备黝铜矿Cu12Sb4S13 及反应机理
李良,陈玉奇,朝仓贵一,平井伸治
(1.南阳师范学院机电工程学院,河南 南阳 473061;2.上海电机学院材料学院,上海201306;3.室兰工业大学工学院,北海道 室兰079-1100)
黝铜矿系Cu12Sb4S13 包含资源丰富的铜和环境友好的硫元素构成[1],同时具有金属-半导体转变[2]和良好的热电性能[3-4]。这种矿物近些年来已经引起研究者的关注,作为潜在的磁性材料,光电薄膜材料和热电材料[5]。
黝 铜 矿 系 Cu12+xSb4+yS13(0 ≤x ≤1.92,-0.02 ≤y ≤0.27)具有小范围波动的化学组成[6]。而且Cu12Sb4S13的稳定性跟Cu-Sb-S 三元相图中相变有关[7-8]。Cu12Sb4S13常用的制备方法是以元素粉[3,5,7,9-15],CuS, Cu2S and Sb2S4[16]或者CuS,Sb2S3and Cu[17]为原料,封管后高温熔融再长时间热处理制备。这种方法优点是纯度高,但耗时长(熔融约3 d,热处理2 周),能耗高[5]。为了缩短时间减少能耗,热处理时间对Cu12Sb4S13热电性能的影响已经被研究;同时一种快速高效的制备方法已经被提出[5,18]。如果采用放电等离子烧结技术,不需要长时间的热处理。另一方面,天然黝铜矿系列的磺酸盐矿物由于电阻值较高不能直接作为热电材料原材料使用[19],但是可以作为制备Cu12Sb4S13热电的“种子”促进Cu12Sb4S13合成[1-3,20]。
辉锑矿Sb2S3是冶炼金属锑的重要矿物原料;资源丰富,价格低廉。本研究尝试以辉锑矿Sb2S3为原材料制备Cu12Sb4S13。研究不同烧结程序工艺,烧结温度和保温时间,烧结块的粉碎球磨,再烧结条件,原料配比波动等因素对Cu12Sb4S13制备的影响。分析Cu12Sb4S13微观组织结构和成分分布。
1 实验材料与方法
1.1 实验过程
实验原料包括CuS 粉末(纯度99%,平均粒度150 μm),Cu 粉(纯度99.99%;平均粒度1 μm)和辉锑矿粉。为了确定辉锑矿粉末中具体元素成分和含量,采用电感耦合等离子体质谱法(ICP-MS法)对辉锑矿粉末进行化学分析见表1。
通过对比辉锑矿粉和高纯度Sb2S3粉末(纯度99.99%,)的化学成分,证实辉锑矿主成分是Sb2S3,且含有较高的Fe 和As 含量。因为辉锑矿粉是通过赤铜矿直接分离制备的。
为了研究烧结程序工艺,烧结温度和时间的影响,原材料按照Sb2S3: Cu : CuS = 2 : 5 : 7 的化学计量比进行称料混合。为了确定Cu 和CuS 成分波动的影响,Cu12+xSb4S13(-0.15 ≤ x ≤0.05)和Cu12-ySb4S13-y (0 ≤y ≤0.5)按照摩尔计量比进行称料。混合后的粉料被添加到内径10.5 mm的石墨模具中进行放电等离子烧结。由于CuS 在220℃以上分解为Cu2S。为了确定CuS 分解对制备Cu12Sb4S13的影响,本研究采用一步式和两步式(220℃保温)两种烧结程序。根据文献[6,16]报道Cu12Sb4S13 的稳定区域随着烧结温度变化而变化,同时反应和热处理温度至少需要400℃,因此烧结温度选定400 ~ 460℃。为了减少杂质相,先用手工或球磨机破碎和研磨初次烧结块。球磨时间限定1 h。同时研究在球磨过程中乙醇对二次烧结的影响。
1.2 材料表征
采用X 射线衍射(XRD)在40 kV 和20 mA的单色Cu Kα 辐射下检测烧结产物的相组成。合成的Cu12Sb4S13的形貌用扫描电子显微镜(SEM)进行了表征。
2 结果与分析
2.1 烧结温度的影响
图1 是烧结温度对合成Cu12Sb4S13的影响。
从图1 中可以看出,初次烧结可以合成高纯Cu12Sb4S13,但是存在第二相(Cu12Sb4S13,CuS1.95)。同时,Cu12Sb4S13 所有特征峰强度随温度的升高有向低角度偏移的趋势,表明晶格常数随烧结温度升高而增加。整体上二次烧结够进一步减少中间相Cu3SbS3和残留CuS。但二次烧结温度对合成Cu12Sb4S13的影响较小。文献[21]采用573 K 进行二次烧结减小第二相提高Cu12Sb4S13 纯度。
2.2 烧结时间的影响
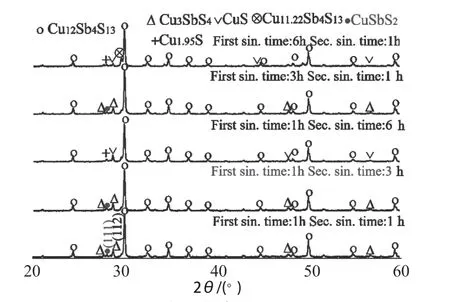
图2 不同烧结时间合成Cu12Sb4S13 的XRDFig. 2 XRD pattern of synthesized Cu12Sb4S13 at different sintering time
图2 是不同初次和二次烧结时间下合成Cu12Sb4S13的XRD。对于初次烧结1 ~ 6 h 的烧结产物主要是黝铜矿Cu12Sb4S13。第二相Cu3SbS4 和残留相CuS的特征峰随着烧结时间的延长而降低。在烧结时间延长到6 h 时出现富铜相Cu11.22Sb4S13的特征峰。与初次烧结相比,二次烧结后第二相Cu3SbS4和残留相CuS 的特征峰明显减弱。无论是初次烧结还是二次烧结,反应时间在小范围内影响第二相Cu3SbS4 和残留相CuS 的特征峰强度。本研究较短烧结时间1 h。
2.3 干磨和湿磨的差异
原料机械化球磨能够提高分散均匀性,但是干法球磨不可避免存在团聚。初次烧结后球磨再球磨不仅能减少未反应的残留相,还能增加晶界数量,有利于减小电阻率。

图3 干法球磨和湿法球磨后二次烧结Cu12Sb4S13 的XRDFig. 3 XRD pattern of secondary synthesized Cu12Sb4S13 after dry milling and wet milling
图3 是干法球磨和湿法球磨后再烧结Cu12Sb4S13的XRD 结果。湿法球磨的溶剂为无水乙醇。干磨的效果要好于湿磨。干磨碰撞更剧烈能够将未反应的残留相暴露出来,在二次烧结过程中参与反应。
2.4 微观形貌分析
图4是初次烧结Cu12Sb4S13的扫描电镜和能谱分析(SEM-EDS)。

图4 初次烧结的扫描电镜和能谱分析(SEM-EDS)Fig. 4 SEM-EDS images of primary sintered
结合图1 结果说明原料直接混合原位烧结Cu12Sb4S13是可行的,但是需要注意粉料团聚。整体上分析,初次烧结Cu12Sb4S13种存在中间相和团聚现象(约80 μm)。在团聚区域(图4 a 中红色圆圈),粉体在烧结过程中处于固体/半固体状态,热扩散速率较小,即使延长烧结时间也不能消除局部团聚。文献[21]中初次烧结合成Cu12Sb4S13,延长烧结时间到120 h 也不能消除不纯相。
另一方面,从Cu、Sb 的EDS 能谱分析结果可以看出,团聚区域的位置类似,且团聚区域的Cu 元素含量明显偏高,同时Sb 元素含量明显偏低。这种现象可以从两方面解释:(1)辉锑矿的主成分是Sb2S3,其常压下理论熔点是550℃。在烧结压力和微量杂质金属元素的影响下辉锑矿的液化温度有可能进一步降低。因此在400 ~ 460℃的烧结区间内Sb2S3的液化程度高,流动性好,不存在明显的团聚;(2) 原料中Cu 的熔点较高(熔点1083.4±0.2℃),且粒径较细(1 μm);CuS 的熔点220℃,但在220℃,CuS 发生分解生成高熔点Cu2S(α-Cu2S 熔点1130℃,β-Cu2S 熔点1100℃)。再结合S 元素的EDS 能谱结果,团聚区域的物相可能是未反应的Cu 或Cu2S(图4a 中蓝色圈和黄色圈)。

图5 二次烧结的扫描电镜Fig. 5 SEM images of secondary sintered
图5是二次烧结Cu12Sb4S13的扫描电镜结果。图5a 中按照计量比称料,Cu12Sb4S13存在明显的颗粒和孔洞(图5b 是局部放大结果),说明烧结反应是通过颗粒表面液化后粘结为整体,粉碎得到的颗粒形状不规则,但是可以将未反应的团聚颗粒破碎并暴露出来。结合之前的研究,减少Cu 或CuS 含量可以促进Cu12Sb4S13 的合成。图5c 是减少原料配比中Cu摩尔量Cu11.9Sb4S13的二次烧结结果。同时可以看出明显的晶粒痕迹,说明二次烧结可以增加晶界数量。图5d 是Cu11.9Sb4S13二次烧结后局部放大的结果。与图5b 相比,孔洞含量明显减少,致密性增加。图5e 是减少CuS 的摩尔含量Cu11.9Sb4S12.9的微观形貌。减少CuS 的摩尔含量同样可以提高颗粒之间的结合。
2.5 反应机理分析
Cu-Sb-S 三元体系在300 ~ 500 ℃的相图已经被报道[6-9,22]。CuSbS2(铜锑矿), Cu12Sb4S13(黝铜矿), Cu3SbS3(硫锑铜矿), and Cu3SbS4(法马丁矿)四种化合物稳定存在。Cu3SbS3中硫含量最低,Cu3SbS4中硫含量最高,非计量比Cu12Sb4S13的硫含量介于二者之间[22]。可能发生的反应为:

本研究中按照最理想的反应方程式(1)进程称量原料,但是混料不均匀和局部颗粒团聚导致原料配比的波动。反应方程式(2-4)导致杂质相(CuSbS2和Cu3SbS3/ Cu3SbS4)的生成(见图2、3)。CuSbS3的生成和Cu 含量过高有关。四方结构的CuSbS3层状薄膜可以通过CuS 和Sb3S3在400 ℃反应得到(如反应方程式2)[23]。
Cu3SbS3/Cu3SbS4 相的生成不仅跟烧结工艺有关还与硫磺蒸汽压有关。因为CuS 的分解导致局部硫磺蒸汽压较高。因此Cu3SbS4存在于烧结块的内部。真空气氛下烧结导致Cu3SbS3多存在于烧结块表面。Cu3SbS4失硫后形成Cu12Sb4S13(如反应方程式9)。
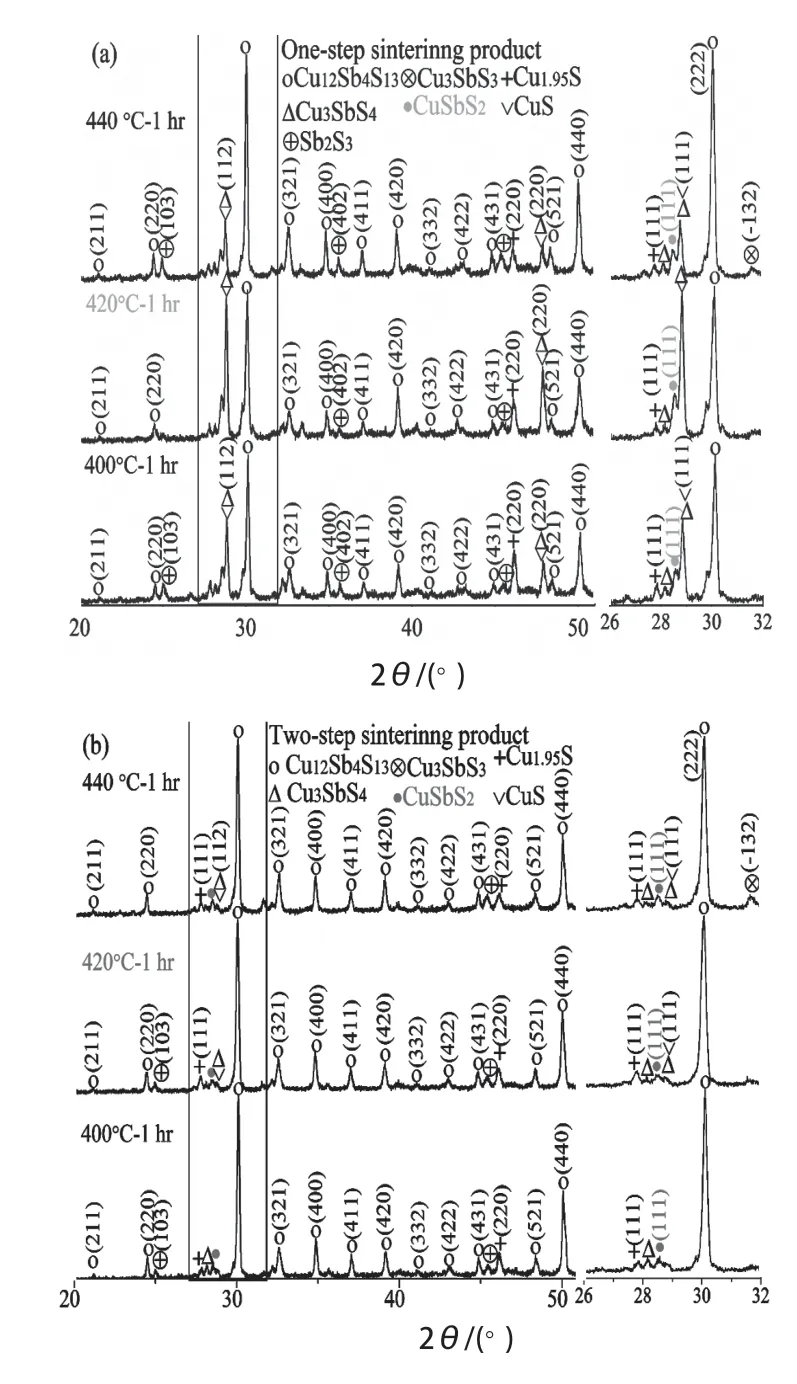
图6 一步式(a)和分步式(b)烧结工艺下合成Cu12Sb4S13块体表面的XRDFig. 6 XRD patterns of surface of Cu12Sb4S13 bulk by onestep sintering (a) and two-step sintering (b)
图6是不同烧结工艺下合成Cu12Sb4S13块体表面的XRD 结果。无论是采用一步式烧结工艺还是采用分步式烧结工艺,杂质相(CuSbS2和Cu3SbS3/Cu3SbS4)都比烧结块破碎后粉体对应的特征峰强。另一方面,一步式烧结工艺和分步式烧结工艺对表面组成影响较大,一步式烧结CuS 分解少,表面硫磺蒸汽压高,Cu3SbS4 的特征峰强;而分步法烧结表面CuS 在真空气氛下分解,表层硫磺蒸汽压相对降低,Cu3SbS4的特征峰减弱。
根据文献[22]的Cu-Sb-S 三元相图和本实验研究的变化参数,Cu12Sb4S13的反应机理见图7。

图7 合成Cu12Sb4S13的反应机理Fig. 7 Reaction mechanism of synthesis Cu12Sb4S13
在加热过程中,CuS 在220 ℃发生分解生成Cu2S(图7 中表示方程式5 的箭头方向)。Cu2S 与Sb2S3在400 ℃反应生成CuSbS2(图7 中表示方程式7 的箭头方向)。CuSbS2分解为Cu12Sb4S13和易气化的Sb2S3或易升华的Sb4类结构[22]。减少Cu或CuS 的摩尔配比能够减缓反应方程式(3)和(4)的进行,因此Cu3SbS4的相对含量减少。
3 结 论
本文研究以辉锑矿Sb2S3为原料制备高纯Cu12Sb4S13的合成工艺。在400℃保温1 h 可以快速合成主成分为Cu12Sb4S13 块体。通过粉碎机械化球磨和二次烧结可以进一步消除初次反应残留Cu2S 同时减少第二相CuSbS2和Cu3SbS3。结合XRD 结果和可能存在的化学反应,提出一种合成Cu12Sb4S13的反应机理。原料CuS 分解为Cu2S 同时提供富硫环境。Cu2S 和Sb2S3通过固相反应先生成CuSbS2 后转化为Cu12Sb4S13。硫化蒸汽压和Cu含量将会影响中间相的成分(CuSbS2,Cu3SbS3,Cu3SbS4)和相对含量。

