间充质干细胞治疗新型冠状病毒肺炎专家共识(2021年,北京)
国家感染性疾病临床医学研究中心,中华医学会感染病学分会,中国研究型医院学会生物治疗学专业委员会
一、概 述
新型冠状病毒肺炎(coronavirus disease 2019,COVID-19)是由新型冠状病毒(severe acute respiratory syndrome coronavirus 2,SARS-CoV-2)感染导致的肺炎。根据国家卫生健康委员会和国家中医药管理局联合发布的《新型冠状病毒肺炎诊疗方案(试行第八版)》[1],根据病情严重程度可分为轻型、普通型、重型和危重型。患者主要临床表现为发热、乏力、干咳,少数患者伴有鼻塞、流涕、腹泻等症状。重症患者多在发病1周后出现呼吸困难和(或)低氧血症,严重者可快速进展为急性呼吸窘迫综合征(acute respiratory distress syndrome,ARDS)、脓毒症休克、难以纠正的代谢性酸中毒、出凝血功能障碍及多器官功能衰竭等。我国已将COVID-19纳入《中华人民共和国传染病防治法》规定的按照甲类传染病管理的乙类传染病。2020年1月30日,WHO将COVID-19列为国际关注的突发公共卫生事件,并于2020年2月28日将其传播和影响的风险评估提高到最高等级。COVID-19作为亟待解决的重大公共卫生事件,急需寻找安全有效的治疗手段[2]。
SARS-CoV-2是有包膜的单股正链RNA病毒,呼吸道飞沫和密切接触是其主要的传播途径,接触病毒污染的物品也可造成感染。病毒的S蛋白通过与靶细胞表面的血管紧张素转化酶2(angiotensin-converting enzyme 2,ACE2)结合而进入细胞内进行复制和扩散[3]。感染SARS-CoV-2后,多数患者预后良好,少数患者病情危重,多见于老年人、有慢性基础疾病者、晚期妊娠和围产期女性、肥胖人群等。造成患者肺组织损伤的主要原因包括:①病毒感染直接引起的病理改变,包括肺泡细胞肿胀、坏死、脱落等导致的肺泡上皮细胞损伤;②机体抗病毒免疫反应引起的严重免疫紊乱,这在重型和危重型患者体内表现尤为明显。COVID-19的病理表现为:肺泡腔内纤维素性渗出物聚集,巨噬细胞和淋巴细胞浸润,肺泡间质淋巴细胞浸润,导致肺泡毛细血管通透性增加,肺透明膜形成,肺泡壁和细支气管管壁纤维素性坏死[4-5]。肺脏毛细血管内皮细胞及肺泡上皮细胞的弥漫性损伤,会进展为ARDS。除肺部病理损伤外,COVID-19患者尤其是重症患者外周血中淋巴细胞数量减少、血浆炎症因子水平显著升高[6],最后会导致休克及多器官功能障碍甚至死亡[7-8]。
COVID-19的临床诊治主要依据《新型冠状病毒肺炎诊疗方案(试行第八版)》[1]。主要治疗手段包括对症治疗、抗病毒治疗、呼吸支持治疗、免疫治疗以及中医药治疗等。由于SARS-CoV-2系新发病毒,目前尚无特效的抗病毒药物。前期研究显示,洛匹那韦/利托那韦、瑞德西韦等抗病毒作用有限[9-10]。对于重型与危重型患者,应积极防治并发症,及时进行呼吸支持治疗。中医治疗方面可根据患者病情、体质因素以及当地气候等进行辨证论治。
免疫治疗的目的是遏制炎症细胞的聚集性浸润、降低炎症因子水平和恢复免疫系统平衡。当前,免疫治疗方法主要包括:①针对炎症因子效应的抗炎症因子治疗。目前IL-1家族阻断剂、抗IL-6抗体等正处于临床试验阶段[11-12]。针对机体系统性免疫紊乱与耗竭,也有利用抗PD-1单克隆抗体等免疫检查点抑制剂来逆转COVID-19免疫耗竭的临床研究。②康复者恢复期血浆治疗。抗病毒中和抗体通过与SARS-CoV-2表面蛋白相结合,可有效阻止SARS-CoV-2感染细胞[13],已成为有效控制病毒复制、短期内迅速改善症状的重要手段[14]。③干细胞治疗。COVID-19疫情爆发以来,国内外已有多个团队完成了干细胞治疗COVID-19的I期和II期临床试验,III期临床试验正在进行中。现有结果表明,间充质干细胞(mesenchymal stem cell,MSC)治疗COVID-19安全性良好,在缩短病程、减轻肺部损伤、降低炎症因子水平等方面显示出较好的临床疗效[15-19]。
二、MSC治疗COVID-19的科学依据
MSC是一群来源于中胚层的多能干细胞,具有多向分化、促进组织器官修复和免疫调控等潜能。MSC可从骨髓、脐带、胎盘、脂肪、骨骼、牙髓和子宫内膜等多个组织中分离,MSC样细胞也可由胚胎干细胞或多能干细胞分化而来[20-21]。MSC具有低免疫原性,因不表达CD40、CD80、CD86等共刺激分子和主要组织相容性复合体Ⅱ类分子,所以引起免疫排斥反应的可能性较小[22]。同时因其对免疫细胞的调节效应不受主要组织相容性复合体分子的限制,对自体和异体的免疫细胞都可发挥免疫调节效应。MSC还具有炎症趋化特性,通过感知炎性信号(细胞因子、趋化因子受体和整合素等)而迁移至炎症部位,依赖细胞间直接接触和(或)旁分泌效应而发挥作用[23],如MSC可通过细胞间直接接触或分泌细胞因子的方式对激活的T淋巴细胞、B淋巴细胞、自然杀伤细胞、树突状细胞等的增殖、分化和抗体产生等发挥调控效应[24]。
有研究显示,外周静脉输入MSC后,1 h内约50%~60%的细胞停留在肺组织内,3 h后数量降至约30%,48 h后MSC会在肝脏和脾脏内聚集,10 d后仍可检测到细胞滞留[25]。MSC聚集在肺组织可分泌细胞营养因子如角质形成细胞生长因子(keratinocyte growth factor,KGF)、血管内皮生长因子(vascular endothelial growth factor,VEGF)和肝细胞生长因子(hepatocyte growth factor,HGF)等,促进II型肺泡上皮细胞再生,改善肺部微环境,促进ARDS损伤后肺泡上皮屏障的修复[21]。
目前已开展了多项MSC治疗肺损伤的临床研究。其中已报道的MSC治疗ARDS的临床研究超过15项,患者多为需要机械辅助通气的危重型呼吸衰竭患者[26-29]。输注细胞剂量从1×106cells/kg至1×107cells/kg不等,输注途径以外周静脉为主[30]。临床研究中未观察到明显不良反应。在肺部渗出明显阶段,MSC有助于改善氧合指数,降低肺部的炎性损伤,提示MSC治疗对ARDS有一定的治疗作用。除ARDS外,也开展了多项MSC治疗特发性或放射性损伤引起的肺纤维化的临床研究[31-32],初步结果显示患者耐受性良好,细胞治疗后纤维化无明显进展,6个月后各项肺功能指标稳定。对于H1N1、H5N1和H7N9等病毒感染引起严重肺损伤疾病,MSC可作为控制炎症、改善肺损伤的重要辅助手段[33-35]。
三、MSC治疗COVID-19的临床研究进展
目前,国内外已完成多项MSC治疗COVID-19的临床研究,超过10项研究结果已发表。李兰娟等[36]报道,2例重症患者接受每次1×106cells/kg剂量、连续3次、间隔1~3 d的冻存宫血MSC输注后,患者外周血淋巴细胞数量升高,炎症指标(IL-6和C反应蛋白)降低,肺功能改善,双侧肺渗出病灶吸收。赵春华等[37]报道,7例普通型、重型和危重型患者接受单次1×106cells/kg MSC输注后,所有患者在治疗后2 d症状明显缓解。3例患者包括2例普通型和1例重型患者在治疗10 d后出院。西班牙Sanchez-Guijo F等[38]报道,13例重型和危重型患者接受每次1×106cells/kg剂量、1~3次脂肪MSC输注后呼吸状况改善,炎症因子水平降低。冯干珠等[39]报道,41例重型和危重型患者接受单次2×106cells/kg脐带MSC输注后可获得更快的临床改善。胡敏等[40]报道,1例重症患者接受5×107cells/次、连续3次、间隔3 d脐带来源MSC输注后,炎症指标降低,胸部CT影像学改善。伊朗Hossein Baharvand等[41]报道,11例因COVID-19诱发ARDS的患者接受2×108cells/次、连续3次、间隔2 d脐带或胎盘MSC输注后呼吸窘迫症状缓解,炎症因子水平降低。胡宝洋等[42-43]报道了一项纳入27例发生肺纤维化COVID-19患者的非随机、开放I期临床研究,发现每次3×106cells/kg、1~3次人胚胎干细胞来源的基质和免疫调节细胞(human embryonic stem cell–derived immunity-and matrix-regulatory cells,hESC-IMRCs)输注可减轻肺纤维化程度。近期美国Camillo Ricordi等[15]报道了一项纳入24例危重型COVID-19相关ARDS患者的随机、对照、双盲研究,(10±2)×107cells/次、连续2次、间隔3 d的脐带MSC输注能显著改善患者存活率并缩短治疗时间。王福生等[16-17]报道了脐带MSC治疗COVID-19的临床Ⅰ期和Ⅱ期研究:Ⅰ期结果显示,3×107cells/次、连续3次、每次间隔3 d的脐带MSC输注对9例普通型和重型患者的安全性良好;在武汉地区开展的Ⅱ期多中心前瞻性随机双盲安慰剂对照临床研究中,共纳入100例重型患者,结果显示4×107cells/次、连续3次、间隔3 d的脐带MSC输注可有效减少重型COVID-19患者肺部损伤,改善患者活动耐力。
上述临床结果表明,普通型、重型、危重型的COVID-19患者接受不同来源的MSC治疗后均没有观察到与输注相关的不良反应,MSC治疗有助于降低患者炎症因子水平、促进肺部损伤修复、提高活动耐力、缩短住院时间。
尽管已报道的多个临床研究结果初步证实了MSC治疗COVID-19的安全性和有效性,但迄今接受MSC治疗的COVID-19患者数量有限,且各临床研究的MSC剂量和疗程不一。为了进一步规范和指导MSC治疗COVID-19的临床实践,提升COVID-19的治疗水平,我们组织国内前期参与COVID-19一线诊疗工作的专家,以及来自感染病学、干细胞生物学、呼吸与重症医学、影像学、病毒学、免疫学、统计学和药理毒理学等领域的权威专家共同商议,形成此共识。
四、MSC治疗COVID-19的建议
(一)患者的选择
1.患者入选标准
年龄16~85岁;临床分型为重型或危重型,分型标准依据《新型冠状病毒肺炎诊疗方案(试行第八版)》[1]。
2.排除标准
①既往有肿瘤病史或现患肿瘤者,或病理检查证实有癌前病变者;②急性心肌梗塞活动期或急性脑梗塞活动期患者;③妊娠或哺乳期患者;④心理疾病病情控制不佳的患者;⑤酒精或药物成瘾者;⑥不能或不愿签署知情同意书或依从性差者;⑦合并活动性结核或流感病毒、腺病毒以及其它急性呼吸道病毒感染患者;⑧临床医生认为不适于干细胞治疗的其他患者。
(二)细胞输注准备
1.MSC的采集、制备和质量控制
干细胞供者筛选应建立并执行评估标准,样本采集必须得到供者或其法定代表人、监护人的同意,签署知情同意书,并经伦理委员会批准;干细胞制备过程和质量控制应按照《药品生产质量管理规范》(GMP)要求严格执行。建议在开展临床治疗项目前将MSC制剂送交中国食品药品检定研究院等行业认可的第三方机构进行质量复核。具体规范和建议参见附件1。
2.MSC的准备
冻存细胞与新鲜培养细胞均可用于临床治疗。冻存细胞需提前做好复苏准备。输注前应仔细检查细胞袋外包装的完整性、生产(冻存)日期等信息。冻存细胞输注时首先确定好输注时间,细胞应在30 min内完成复苏、药物配伍流程并开始输注至患者体内,细胞输注应在2 h内完成。
3.MSC输注方法
①推荐剂量为每次1~3×106cells/kg,每次间隔3~7 d,共进行3次输注。②推荐使用输血过滤器进行输注,选取患者手臂较粗的静脉血管输注。③每袋细胞输注前轻轻颠倒数次,使细胞悬浮均匀。④输注前10 min缓慢静滴(20~30 滴/ min),10~15 min后如无特殊反应,可将滴速调整为40~50滴/ min,直至输注完成;若患者伴有心血管疾病,则应按医嘱控制滴速。⑤完成全部细胞输注后,用10~30 ml生理盐水冲洗输注袋。⑥输注完成后需密切观察患者生命体征。⑦对高度过敏体质患者建议输注细胞前使用甲基强的松龙(40 mg)预防过敏反应。
(三)细胞输注的监测和不良反应处理
1.治疗前准备
干细胞输注前72 h内应完善血常规、肝肾功能、C反应蛋白、炎症因子相关指标(IL-6、IL-8、TNF-α等)、凝血功能、降钙素原、血气分析、心脏功能、心电图和胸部CT检查等;详细询问并记录患者既往病史、过敏史等情况。
2.治疗过程监测
应在心电监护和经皮血氧饱和度监测下进行细胞输注,并做好急救措施准备。少数患者可能出现一过性的胸闷、自觉发热等不适,一般可自行缓解。如胸闷症状持续,应及时停止细胞输注,给予吸氧和生命体征监测,完善心电图、血气分析等检查,必要时对症处理。
3.治疗后监测和处理
根据MSC细胞治疗其他疾病的报道和治疗COVID-19的临床试验数据,目前其在临床应用中尚未发现严重的不良事件[16,44-48]。已经报道的安全性事件主要是细胞输注后低热和恶心,多为自限性,一般在24 h内缓解。个别患者可能出现高热,可给予物理降温及对症药物治疗。但仍不排除存在输液反应、过敏性休克等可能,一旦出现应积极对症治疗。MSC最后一次输注完成后3~7 d应复查血常规、肝肾功能、C反应蛋白、降钙素原、IL-6、血气分析和心脏功能等,对于治疗前存在明显肺部病变患者可复查胸部CT。目前尚未发现与MSC细胞治疗直接相关的远期不良事件,但仍建议在治疗后1~2年内定期检查血常规、肝肾功能、血糖、血脂、腹部彩超、胸部CT、心电图和肺功能等。
(四)疗效评价指标
评价指标包括:①临床症状评价:气短或呼吸困难可采用mMRC呼吸困难量表(见附件2)进行评估,临床综合情况可采用WHO临床过程综合评分(见附件3)进行评价[49]。②实验室检测指标:血常规、血气分析、氧合指数(PO2/FiO2)、C反应蛋白、炎症因子相关指标(IL-6、IL-8、TNF-α等)、淋巴细胞数量和亚群、乳酸脱氢酶、肝肾功能、D-二聚体、凝血功能、心肌酶等。③胸部影像学评价:建议进行高分辨胸部CT检查,对病变范围和特征等进行评估,可采用CT总严重程度评分(total severity score,TSS)等指标辅助判断[17]。④肺功能评价(出院后随访):在医疗条件和患者身体状况允许的情况下,可进行肺功能评价[50],主要包括限制性通气功能障碍、肺弥散功能和气道阻塞相关指标。⑤临床转归评价标准建议参考《新型冠状病毒肺炎诊疗方案(试行第八版)》[1]。

附件2 mMRC呼吸困难量表
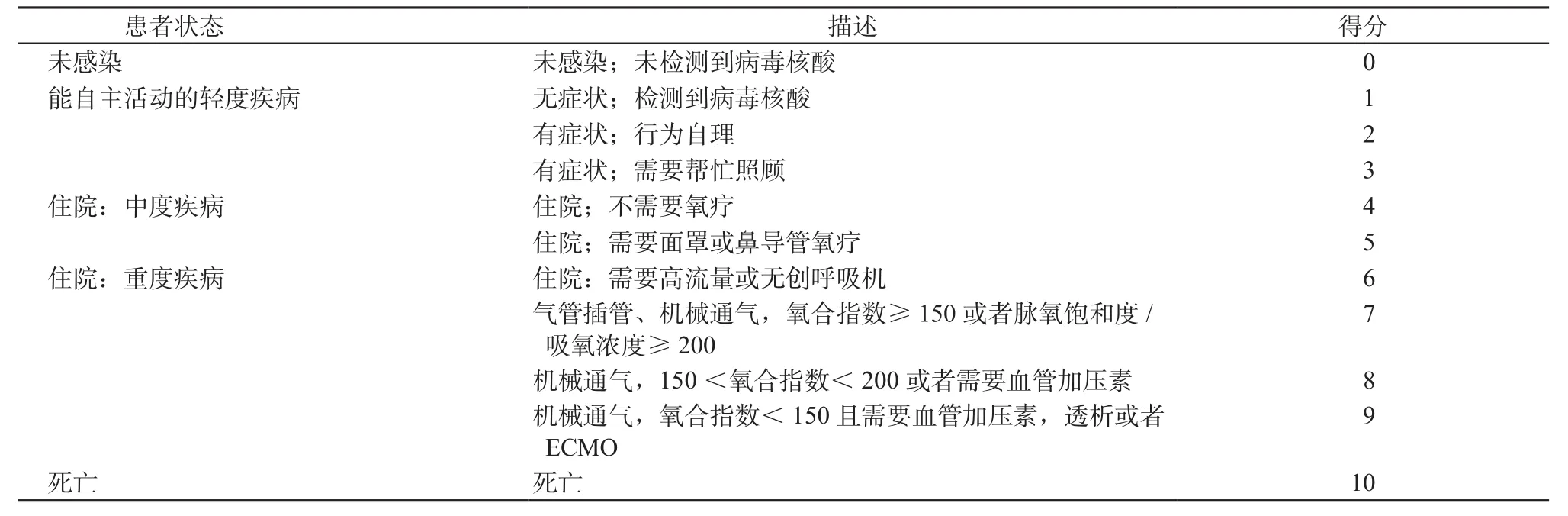
附件3 WHO临床过程综合评分
五、实施要求
基于上述共识并结合MSC治疗COVID-19的前期研究结果,为了提高COVID-19的救治效果、减少并发症,建议在COVID-19定点收治医院并按照国家有关管理办法开展MSC治疗。相关标准可参照《药品管理法》和国家食品药品监督管理总局颁布的《药品注册管理办法》,或原国家卫生和计划生育委员会和原国家食品药品监督管理总局联合制定的《干细胞临床研究管理办法(试行)》执行。
利益冲突所有作者均声明不存在利益冲突
共识制定专家名单(以姓氏笔画为序):
王福生(国家感染性疾病临床医学研究中心主任,解放军总医院第五医学中心感染病医学部主任)、王贵强(北京大学第一医院感染科兼肝病中心主任,中华医学会感染病学分会前任主委)、王霄英(北京大学第一医院影像科主任)、石磊(解放军总医院第五医学中心感染病医学部生物损伤救治科副主任)、刘中民(上海市东方医院院长)、孙云霞(北京昭衍新药研究中心股份有限公司副总经理)、李元元(解放军总医院第五医学中心感染病医学部副主任医师)、李太生(中华医学会传染病学分会主任委员,北京协和医院感染内科主任)、李永纲(解放军总医院第五医学中心感染病医学部副主任)、吴朝晖(中国医药生物技术协会驻会副理事长)、吴尊友(中国疾控中心流行病学首席专家)、张文宏(复旦大学附属华山医院感染科主任,中华医学会传染病分会副主委)、张宇(中源协和副总经理兼首席科学官)、苑鑫(解放军总医院第五医学中心感染病医学部呼吸与危重症医学科主任)、周琪(中国科学院副院长,北京干细胞与再生医学研究院理事长,中国科学院动物研究所研究员)、孟淑芳(中国食品药品检定研究院生物制品研究所细胞室主任)、孟繁平(解放军总医院第五医学中心感染病医学部生物损伤救治科副主任)、项春生(浙江大学传染病诊治国家重点实验室副主任,国家干细胞临床研究专家委员会委员)、赵春华(北京协和医学院细胞生物学系主任、中国医学科学院组织工程研究中心主任,国家干细胞临床研究专家委员会委员)、胡豫(华中科技大学同济医学院附属协和医院院长)、施明(解放军总医院第五医学中心感染病医学部研究所所长)、姚晨(北京大学第一医院医学统计室主任,北京大学医学院临床研究所副所长)、徐哲(解放军总医院第五医学中心感染病医学部生物损伤救治科主任)、徐若男(解放军总医院第五医学中心感染病医学部副研究员)、高晨燕(国家药品监督管理局药品审评中心生物制品临床部部长)、黄磊(解放军总医院第五医学中心感染病医学部感染性疾病科主任)、韩为东(中国研究型医院学会生物治疗学专业委员会主任委员,解放军总医院第五医学中心肿瘤医学部生物治疗科主任)、程涛[ 中国医学科学院血液病医院(血液学研究所)所院长]、谢渭芬(海军军医大学长征医院消化内科主任医师)、福军亮(解放军总医院第五医学中心感染病医学部感染性疾病科副主任)、魏于全(华西医院临床肿瘤中心主任,生物治疗国家重点实验室主任,国家干细胞临床研究专家委员会委员)
附件1:脐带MSC的采集、制备与质量控制
(一)脐带MSC采集
脐带MSC来源于健康胎儿的脐带组织,产妇(供者)筛选应建立并执行评估标准,筛查供者既往病史、家族史、当前健康报告和一般信息。既往病史和家族史要对遗传病(单基因和多基因疾病,包括心血管疾病和肿瘤等)相关信息进行详细采集。对用于异体干细胞临床研究的供者,必须经过检验筛选证明无人源特定病毒,包括艾滋病病毒(HIV)、乙型肝炎病毒(HBV)、丙型肝炎病毒(HCV)、人类嗜T 细胞病毒(HTLV)、EB 病毒(EBV)、巨细胞病毒(CMV)等的感染,以及无梅毒螺旋体感染。必要时需要收集供者的ABO 血型、HLA-I和II类分型资料,以备追溯性查询。此外必要时还应提供供者出入疫区等其他情况的报告并进行相关样本检测。样本采集必须得到供者或其法定代表人、监护人的同意,签署知情同意书,并经伦理委员会批准。样本的接收、转运应有专人负责,并做好标识和记录。
(二)脐带MSC制备
1.制备环境及工艺流程设置
应制定干细胞采集、分离和干细胞库建立的标准操作及管理规程,并在符合《药品生产质量管理规范》(GMP)要求的基础上严格执行,制备过程必须在B级洁净实验室内按照标准操作流程进行,严格无菌操作。非完全密封状态下的细胞操作(如分离、培养、灌装等)以及与细胞直接接触的无法终端灭菌的试剂和器具的操作,应在B级背景下的A级环境中进行。标准操作程序应包括:操作人员培训;材料、仪器、设备的使用和管理;干细胞的采集、分离、纯化、扩增和细胞(系)的建立;细胞保存、运输及相关保障措施,以及清洁环境的标准及常规维护和检测等。
为尽量减少不同批次细胞在研究过程中的变异性,可在工艺流程中建立种子库(master cell bank)和工作细胞库(working cell bank)等多级管理体系,其中种子库一般建议建立在P2代,工作细胞库一般建议建立在P4~P5代,同时可在不同级的细胞库中设置不同的细胞基本质量标准。在细胞采集、分离及细胞(系)建立阶段(如种子库),重点进行细胞鉴别、成活率及生长活性(包括细胞倍增时间、细胞周期、克隆形成率、端粒酶活性等)、外源致病微生物,以及基本的干细胞特性检测(包括特定表面标志物群,成脂、成骨和成软骨的分化潜能等)。而对经过复杂的体外培养和操作后的准备用于临床前及临床研究的细胞库(如工作细胞库)中的细胞,除进行上述检测外,还应当进行全面的内外源致病微生物和详细的干细胞特性检测(包括干细胞的表达产物、分泌的功能因子以及免疫学调控功能等),以及细胞纯度分析。
2.关键原辅料控制
体外培养和扩增的干细胞在培养过程中,需要注意定期更换培养液,及时传代。生产制备过程中使用的培养基、培养过程的添加物等重要原材料和辅料尽量使用经监管当局批准的产品(如药用辅料等),否则建议使用高质量级别的产品。特别是培养基成分,在满足干细胞正常生长的情况下,应符合无菌、无致病微生物及内毒素的质量标准,残留的培养基对受者应无不良影响;且不影响干细胞的生物学活性,即干细胞的“干性”及分化能力。在干细胞制剂制备过程中,应尽量避免使用抗生素。若使用商业来源的培养基,应当选择有资质的生产商并由其提供培养基的组成成分及相关质量合格证明。必要时,应对每批培养基进行质量检验。除特殊情况外,应尽可能避免在干细胞培养过程中使用人源或动物源性血清,不得使用同种异体人血清或血浆。如必须使用动物血清,应进行相关检测以确保其无特定动物源性病毒污染,不使用海绵体状脑病等传染病流行区来源的牛血清。若培养基中含有人的血液成分,如白蛋白、转铁蛋白和各种细胞因子等,应尽量采用国家已批准的可临床应用或GMP级的产品,同时应明确其来源及批号,并要求提供质量检定合格报告。
3.制备工艺研究与控制
MSC制剂的制备工艺包括干细胞的采集、分离、纯化、扩增和传代,干细胞库的建立、细胞冻存、复苏、分装和标记以及残余物去除,并建立培养基、辅料和包材的选择标准。建议根据质量源于设计(quality by design,QbD)的原则对制剂制备的全过程,包括细胞收获、传代、分装等操作,进行全面的工艺研究和验证,制定合适的工艺参数和质量标准,确保对每一过程的有效控制。从整个工艺制备流程到输入到受试者体内全过程,需要追踪观察并详细记录。对不合格并需要丢弃的干细胞制剂,需对丢弃过程进行规范管理和记录。对于剩余的干细胞制剂的处理必须合法合规并符合伦理要求,应制定相关的操作规程并严格执行。干细胞制剂的相关资料需建档并长期保存。制备的干细胞制剂可按照标准程序进行储存、解冻复苏。新鲜使用的细胞制剂只能在4~12 ℃短时间保存,建议在12 h内(具体新鲜制剂保存时间和有效期应通过稳定性实验确定)进行干细胞移植。液氮冻存的制剂建议进行长期稳定性实验以明确有效性、运输和使用条件等,复苏后尽量在30 min内进行回输。
(三)脐带MSC质量控制
由于干细胞制剂制备的最后过程往往无法进行过滤等除菌操作,因而过程和质量控制显得尤为重要。为确保制剂的质量及其可控性,干细胞制剂的检验可分为质量检验和放行检验。质量检验是为保证干细胞经特定体外处理后的安全性、有效性和质量可控性而进行的较全面质量检验,检测方法需要根据2020版《中国药典》的规定进行验证后施行,如为自主建立的新检测方法需进行全面的方法学验证后施行。放行检验是在完成质量检验的基础上,对每一类型的每一批次干细胞制剂,在临床应用前所应进行的检验。建议对多批次干细胞制剂进行质量检验,并在制备工艺、场地或规模等发生变化时,重新对制备过程进行工艺验证。可建立快速放行检验方法来确认细胞制剂的质量及安全信息,以保证临床使用的及时性。
干细胞制剂抵达医疗机构后,建议输注前可通过细胞计数和活力测定对干细胞进行质量检验,有条件的机构可使用流式细胞仪进行干细胞表型的鉴定。
1.制剂放行检验指标(表1)
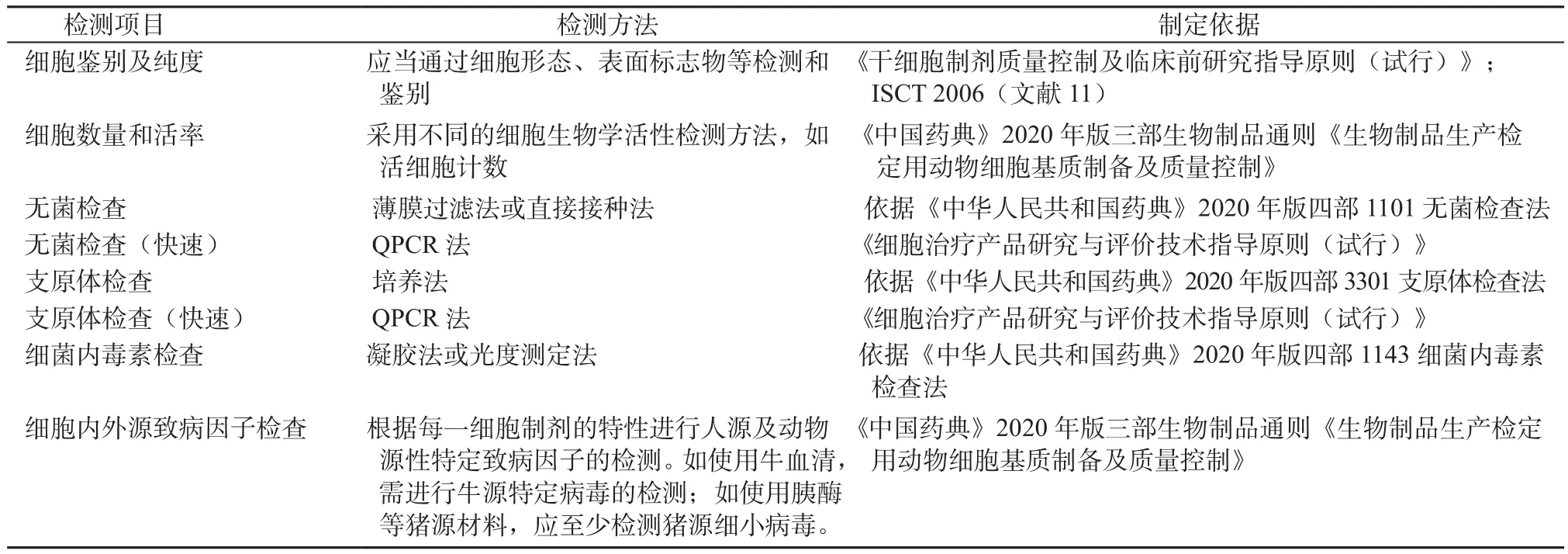
表1 制剂放行检验指标及制定依据
2.制剂医疗机构检测项目
指医疗机构对运抵医院的细胞制剂进行的检验以进一步检测输注前细胞的状态。至少应包括细胞计数和细胞存活率检测,有条件的可使用流式细胞仪进行干细胞表型的鉴定和细胞凋亡检测。
3.第三方机构检测
制备的MSC制剂建议临床治疗前送交中国食品药品检定研究院等权威第三方机构进行检定,以进一步明确其相关产品属性。
4.制剂的质量研究建议在临床前研究阶段,利用不同的体外和动物模型实验方法对干细胞制剂进行全面的安全性、有效性及稳定性研究。安全性研究主要包括:(1)生长活性和状态。生长因子依赖性的检测,在培养生长因子依赖性的干细胞时,需对细胞生长行为进行连续检测,以判断不同代次的细胞对生长因子的依赖性。(2)致瘤性和促瘤性。目前,普遍认为MSC“不致瘤”或具有“弱致瘤性”,但不排除其对已存在肿瘤的“促瘤性”作用。因此建议在动物致瘤性试验中,选择足够数量的细胞和足够长的观察期。另一方面,除啮齿类动物外可选择食蟹猴等大动物模型以明确长期安全性。(3)加强对培养过程中添加的成分残余量的检测,以控制残余的、影响干细胞制剂质量和安全性的成分,如牛血清蛋白、抗生素、外源细胞因子。有效性指标主要包括其生物学效应。随着研究的进展,建议针对临床治疗的适应症和其治疗机理,不断研究并更新生物学效应检测方法以找到替代性生物标志物。稳定性研究主要包括对干细胞制剂在储存(如一般生物制品运输温度,或液氮冻存和细胞植入前的临时存放)和运输过程中开展的一系列稳定性实验以确定制剂的有效期。检测项目主要包括细胞活性、密度、纯度、无菌性等。根据干细胞制剂稳定性试验结果,确定其制剂的保存液成分与配方、保存及运输条件以及有效期,同时确定与有效期相适应的运输容器和工具,以及合格的细胞冻存设施和条件。
编后语编辑部对所刊载内容未作编辑加工

