溴化锂及离子液体水溶液密度、黏度和表面张力测定与计算
曹燕,丁延,郭义仓,汪城,刘英杰,陶磊,李进龙
(1 常州大学石油化工学院,江苏常州213164; 2 常州大学石油工程学院,江苏常州213164)
引 言
吸收式制冷/热泵循环系统的热力性能与工质对的选择密切相关[1-4]。目前,常用的工质对有氨/水[5-6]和水/溴化锂[7]两种,前者以氨为制冷剂、水为吸收剂,后者则以水为制冷剂、溴化锂为吸收剂。氨具有很高的汽化潜力,迁移能量能力强,可获得零度以下的冷量,但其毒性较大,易爆炸,工作条件苛刻,且呈碱性的氨水溶液易腐蚀金属材料,因而其使用受到很大限制;对水/溴化锂工质对,虽被广泛使用,但仍存在低温易结晶和腐蚀等固有问题。因此,探索能够替代氨/水和水/溴化锂的工质对成为近年来的研究热点。
离子液体(ILs)[8-11]是由阴阳离子构成、在室温或近室温条件下以液态形式存在的盐,其具有良好的热稳定性和化学稳定性,且液程宽、不易挥发及可设计,作为一种理想的绿色溶剂在催化、分离、电池等[9,12-14]不同领域已获广泛关注。在吸收制冷或热泵系统中,工质对循环工作于发生器、冷凝器、蒸发器、吸收器,而吸收剂只循环于发生器和吸收器,其中主要涉及工质对的输送、热量和质量传递等物理过程,而这些过程运行及能量传递特性与工质对的密度、黏度、表面张力等基础物性息息相关。据此,可根据ILs 的可设计性及其他特性获得具优良性能的离子液体吸收工质对。目前,对含ILs 的吸收工质对的基础理化性质(密度、黏度、表面张力、溶解性等[15-19])的研究已有相关报道,其中涉及的制冷剂包括水、氨、烷烃、芳香烃及醇类化合物等[20-23],离子液体吸收剂以咪唑基阳离子及Cl-、Br-、BF4-、PF6-、[DMP]-、[DEP]-、[NTf2]-等[24-28]阴离子为主。同时,由于水的良好性能和水/溴化锂工质对的广泛使用,水/ILs 工质对的基础物性和热力性能研究[29-31]得到了很大重视。Almeida 等[32]测量了8种1-乙基-3-甲基咪唑类ILs+水的表面张力,研究了阴离子性质对表面张力及其表面排序的影响;Freire等[33]探讨了水含量对[BMIM][PF6]和[OMIM][PF6]表面张力的影响;为研究烷基链长对ILs性质的影响,Martins等[34]考察了咪唑类离子液体[CnCnim][NTf2]+水的密度和黏度等热力学性质;Liu等[35]则对[BMIM][BF4]水溶液的物理性质进行了考察;Xu 等[36]还报道了293.15~333.15 K 下[AMIM][Cl]+水二元体系的黏度。以水+ILs 为工质对的吸收式制冷/热泵循环性能与ILs 的吸湿性能有很大关系,粟航等[37]研究表明,在工作温度较高时,[EMIM][OAC]+水工质对的性能系数优于LiBr+水体系及国内外学者已研究的一些其他ILs体系;Zhang 等[38]指出[EMIM][DMP]+水工质对的性能系数与LiBr+水工质对相当,且制冷温度低于LiBr+水工质对。鉴于此,本文选取两种吸水性强、可能成为新一代吸收工质对的离子液体(1-乙基-3-甲基咪唑醋酸盐([EMIM][OAC])和1-丁基-3-甲基咪唑硫氰酸盐([BMIM][SCN]))水溶液作为研究对象,实验测定其密度、黏度和表面张力,同时以水/溴化锂工质对物性为基准进行比较,为以ILs 为吸收剂的吸收工质对的设计开发以及工业应用提供支撑。
1 实验部分
1.1 实验试剂
溴化锂水溶液,质量分数≥55%,国药集团化学试剂有限公司。卡尔费休液,分析纯,德国默克公司。蒸馏水,实验室自制。离子液体[EMIM][OAC]+水混合物,其中[EMIM][OAC]质量分数≥82%;[BMIM][SCN],质量分数≥99.0%,购自上海默尼化工科技有限公司。实验前,离子液体在363.15 K 下经24 h 真空干燥处理(压力0~5 kPa),卡尔费休检测[EMIM][OAC]含水量≤7.03%(质量)、[BMIM][SCN]含水量≤0.86%(质量)。
1.2 实验方法
在常压和一定温度范围(283.15~343.15 K)条件下,实验测定了LiBr、[EMIM][OAC]及[BMIM][SCN]三种水溶液的密度、黏度和表面张力。密度采用MDY-2型电子液体密度仪(上海方瑞仪器有限公司)测量,密度实验值的不确定度为0.0001 g·cm-3;黏度测量选用乌氏黏度计,溴化锂水溶液的黏度计规格为0.4~0.5 mm,离子液体的为0.7~0.8 mm 和0.9~1.0 mm;表面张力由BZY-2 型全自动表面张力仪(上海衡平仪器仪表厂)通过白金板法测量。以上温度均由恒温水浴控制(±0.1)。密度、黏度及表面张力测量均先用自制蒸馏水校准。实验中,采用卡尔费休滴定法(Metrohm,KF 831)测定ILs 中水含量,再配制不同组成下的ILs 水溶液,每一实验点测试三次取平均值。
2 结果与讨论
2.1 密度
图1~图3 分别绘出了不同浓度下LiBr、[EMIM][OAC]和[BMIM][SCN]水溶液密度随温度的变化关系,密度均随温度的升高而降低,也即摩尔体积随着温度升高而增加,且溴化锂水溶液的密度随着浓度变化的变化率较大。另外,在相同条件下,LiBr水溶液的密度值明显高于ILs 溶液。图1 中还给出了溴化锂水溶液密度的文献值[39],可以看出,本文实验测量值与文献吻合良好。上述水溶液不同浓度和一定温度范围(303.15~343.15 K)的详细密度实验值见附录表A1~表A3。

图1 不同温度下LiBr(xA)+H2O(1-xA)密度的实验值(点)和计算值(线)Fig.1 Experimental(symbols)and calculated(lines)density of LiBr(xA)+H2O(1-xA)
为了获得密度模型化参数,鉴于实验密度值与温度(T)的良好线性关系,本文采用线性方程[式(1)]拟合密度实验值ρ:

式中,Aρ和Bρ是模型参数,表达为溶质浓度的二次函数[式(2)、式(3)]:


图2 不同温度下[EMIM][OAC](xA)+H2O(1-xA)密度的实验值(点)和计算值(线)Fig.2 Experimental(symbols)and calculated(lines)density of[EMIM][OAC](xA)+H2O(1-xA)

图3 不同温度下[BMIM][SCN](xA)+H2O(1-xA)密度的实验值(点)和计算值(线)Fig.3 Experimental(symbols)and calculated(lines)density of[BMIM][SCN](xA)+H2O(1-xA)
式中,下角标a、b、c 表示不同系数。式(2)、式(3)的 方 程 系 数 见 表1,LiBr、[EMIM][OAC]和[BMIM][SCN]体系的模型关联总体平均绝对偏差(AAD)分别为0.78%、0.02%和0.12%,模型计算结果同样绘于图1~图3中,可见模型可高精度重现实验结果。
2.2 黏度
LiBr、[EMIM][OAC]和[BMIM][SCN]体系在不同浓度和温度(303.15 ~343.15 K)条件下的黏度实验值随温度和浓度变化关系如图4~图6 所示,详细数据列于附录表A4~表A6。图4中同时给出了溴化锂溶液黏度文献值[39]。实验结果表明,本文工作与文献结果一致,LiBr、[EMIM][OAC]及[BMIM][SCN]溶质的加入均使水溶液体系的黏度增加,且ILs 体系的值要高于LiBr 体系。另外,由图可见黏度与温度间关系为非线性,此可借助Vogel-Tammann-Fulcher(VTF)方程[16,28,40-41]拟合[式(4)]:

表1 水溶液密度模型化参数Table 1 Correlated model parameters of densities for aqueous solution

图4 不同温度下LiBr(xA)+H2O(1-xA)黏度的实验值(点)和计算值(线)Fig.4 Experimental(symbols)and calculated(lines)viscosity of LiBr(xA)+H2O(1-xA)

图5 不同温度下[EMIM][OAC](xA)+H2O(1-xA)黏度的实验值(点)和计算值(线)Fig.5 Experimental(symbols)and calculated(lines)viscosity of[EMIM][OAC](xA)+H2O(1-xA)

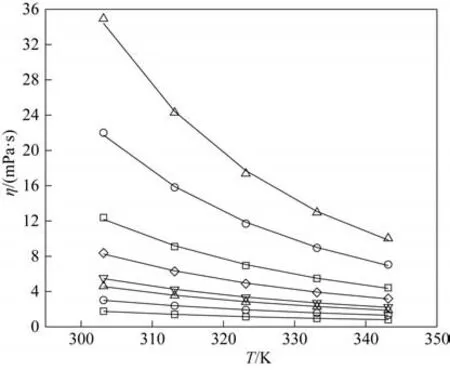
图6 不同温度下[BMIM][SCN](xA)+H2O(1-xA)黏度的实验值(点)和计算值(线)Fig.6 Experimental(symbols)and calculated(lines)viscosity of[BMIM][SCN](xA)+H2O(1-xA)
式中,η 是动力黏度,mPa·s;T 是温度,K;Aη和Bη是模型参数,同样表示为溶质浓度的函数[式(5)、式(6)]:

拟合获得的模型参数列于表2,各体系的AAD分别为0.77%,1.48%,1.07%,模型计算结果如图4~图6所示,模型和实验结果完全吻合。
从分子层面看,黏度的大小反映的是流体内部剪切应力内阻,相较普通有机分子溶剂,多数ILs 均具更高的黏性,因为高分子量和多分子间相互作用(色散和静电相互作用)具更高的内阻力,可以通过能量势垒(Eη)[40]进行表征,Eη越大,表明流体中粒子迁移越困难。能量势垒可由黏度与温度的关系确定[34,42]:

式中,R=8.314 J·mol-1·K-1是气体常数。根据黏度实验和模型结果得到的Eη如图7所示,可见ILs体系的Eη远高于LiBr 体系,表明ILs 水溶液中粒子的迁移需要更高能量来打破能量势垒;同时,可看出[EMIM][OAC]的Eη较[BMIM][SCN]值大,说明[BMIM][SCN]体系中粒子较[EMIM][OAC]系统更易移动,在输运过程中可能产生更薄的边界层,使流体在管道中流动更均匀。从图7 还可看出,[BMIM][SCN]的Eη与浓度几乎呈线性关系,而[EMIM][OAC]的Eη随着离子液体摩尔分数增大,增加速度减缓,此可能因为[BMIM][SCN]体系中粒子相互作用随着ILs浓度的变化近似线性改变,而对[EMIM][OAC]体系,由于其特殊的氢键作用,在低浓度区可表现出良好的线性性能,但随着[EMIM][OAC]浓度增加,局部组成和粒子相互作用发生改变,促使Eη增加减缓。另外,LiBr体系能量势垒总体随浓度变化较小,且无明显规律,此可能由无机盐小分子溶解固有特性或实验测量偏差引起。

表2 水溶液黏度模型化参数Table 2 Correlated model parameters of viscosities for aqueous solution

图7 能量势垒与溶质溶度关系Fig.7 The relationship between energy barrier and solute concentration
2.3 表面张力
实验测定了LiBr、[EMIM][OAC]和[BMIM][SCN]水溶液在不同浓度和温度范围下的表面张力,ILs溶液中ILs 的浓度范围为0~0.05,实验数据分别列于附录表A7~表A9,同时绘于图8~图10,图8 中同时给出了LiBr水溶液表面张力文献值[43]。结合图表可见,本文表面张力实验结果可靠,LiBr 水溶液的表面张力要远远高于ILs 体系,同时可看出微量ILs的加入可快速降低水的表面张力,后随着ILs 浓度的增加而基本维持不变;而LiBr 则表现出完全不同的性质,随着LiBr 的增加,表面张力值逐渐增大。另外,各体系的表面张力随温度升高均降低,且呈近似线性相关,由此可获得表面热力学性质,即表面熵Sσ和表面焓,见式(8)、式(9):
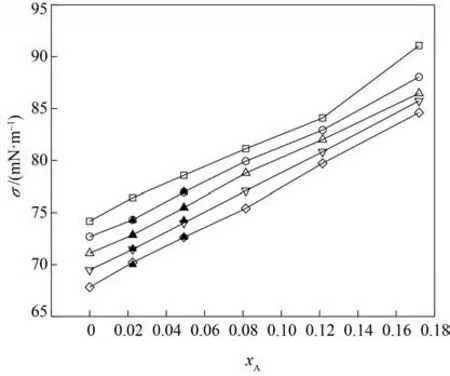
图8 LiBr的表面张力与组成关系Fig.8 Plot of surface tension and composition of LiBr

图9 [EMIM][OAC]的表面张力与组成关系Fig.9 Plot of surface tension and composition of[EMIM][OAC]

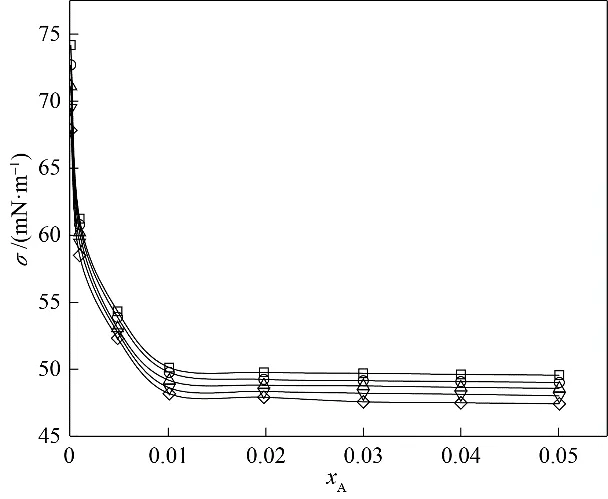
图10 [BMIM][SCN]的表面张力与组成关系Fig.10 Plot of surface tension and composition of[BMIM][SCN]

表3 表面热力学性质Table 3 Surface thermodynamic properties
式中,下角标P 代表恒压。计算的表面热力学性质列于表3。与溴化锂体系相比,ILs 体系表面熵较低,表明ILs 流体中存在高表面组织及较高的表面排序。有研究表明[33,46],表面焓和表面熵主要受构成ILs 的阴离子性质支配,且还受阳离子链长影响,表面焓随着链长的增加而减少。在本文研究的两种ILs 中,它们具有不同的阴离子,从离子结构上看,[SCN]-持完全线性特征,而[OAC]-为非线性,同时[BMIM][SCN]具有较长链长的阳离子,因此在相同条件下[BMIM][SCN]体系的表面焓和熵较低,即具有更高的表面排序。实际上,离子液体体系随着ILs 的增多表面熵呈逐渐减小趋势[44],且变化幅度较小,[EMIM][OAC]和[BMIM][SCN]均遵循了这样的基本规律,但后者在研究的浓度范围内表面熵整体变化较小,此可能与具线性特征阴离子[SCN]-的特殊结构有关。对溴化锂溶液体系,在研究的最高浓度点,表面熵突然增大,可能由于在低温高浓度条件下溴化锂溶液中出现微小晶核,导致表面性质的突变。
3 结 论
(1)实验测定了不同浓度和温度(283.15~343.15 K)范围LiBr、[EMIM][OAC]和[BMIM][SCN]水溶液的密度、黏度和表面张力,丰富了基础物性数据库。
(2)通过线性和VTF 模型分别成功关联了密度和黏度实验值,为过程设计和计算提供了可靠的物性计算模型化参数;同时通过黏度获得的能量势垒表明不同体系中粒子迁移难易程度遵循[EMIM][OAC]>[BMIM][SCN]>LiBr。
(3)由表面张力获得了表面熵和焓的热力学性质,显示ILs 体系具有高表面组织和较高的表面排序,且[BMIM][SCN]>[EMIM][OAC]。

