杂质在沉积电子级锰过程中的行为研究
李武斌,黄 健,李 勇,杜洪伍,张 谊,叶昌美,刘益宏
(1. 贵州省新材料研究开发基地,贵州 贵阳 550014; 2. 四川省讯益节能科技有限公司,四川 成都 610000)
金属锰用途广泛,在钢铁工业中,锰的用量仅次于铁,90%的锰用于钢铁工业,10%用于有色冶金、化工、电子、电池和农业等行业[1]。我国锰矿资源较为丰富,储量较大,主要分布在广西、湖南、重庆和贵州[2],其中贵州铜仁地区已查明的锰矿储量约7亿t。由于产能过剩和经济环境等问题导致产品价格持续走低,开发高附加值的高纯锰尤为重要。高纯锰可以广泛应用于磁性材料、电池材料和溅射靶材等行业[3],随着冶金工业的技术进步,冶金用锰的新趋势对电解金属锰的精细化、多样化提出了特殊的要求,有色冶金工业对特殊金属锰的需求不断增大。锰系动力电池正极材料,特别是CoNiMn三元正极材料的快速发展,对高纯含锰化合物提出了严格的品质要求,作为重要的高纯含锰化合物的基础材料,高纯金属锰的市场需求也逐年增加[4]。因此,电解电子级金属锰是制备高纯锰的基础环节,高纯锰产业是锰产业高新技术的发展方向。
杂质元素对电解过程的电流效率和锰的纯度均有影响,金属锰中的杂质含量太高,会影响金属的可塑性,工业和信息化部2015年4月30日发布《电解金属锰》(YB/T051-2015)行业标准[5],标准中对相关杂质做出明确规定。本文采用SEM-EDS对电子级金属锰进行表针并对杂质元素进行化学分析,明确了杂质元素在沉积电子级锰过程的行为,对高纯锰的电解生产的具有理论和实践指导意义。
1 实 验
1.1 实验原料
实验在贵州某电解锰公司实施,实验原料采用除杂净化后的硫酸锰电解溶液,电解液含Mn2+36 g/L,硫酸铵浓度100 g/L,添加剂SeO2浓度0.03 g/L。
1.2 实验条件
槽电压4.2 V,阴极电流密度320 A/m2,阳极电流密度600 A/m2,电解温度为42℃,电解液pH值7,电解周期24 h。
1.3 实验原理
电解金属锰采用不锈钢板做阴极,铅锡锑银四元合金作为阳极电解硫酸锰溶液,电解总反应为:
阴极反应为:Mn2++2e=Mn
阳极反应为:2H2O-4e=O2↑+4H+
即阴极析出金属锰,阳极析出氧气。
2 表征与分析
2.1 SEM-EDS分析
图1是纯锰的SEM-EDS分析,晶体内没有任何杂质元素存在;图2是金属锰样品含有杂质区域的SEM-EDS分析,杂质以夹杂物[6-7]的形式存在,杂质元素为C、O、Mg和S;图3是金属锰有附带物的SEM-EDS分析,存在的杂质元素为O、Fe、Se、Pb。
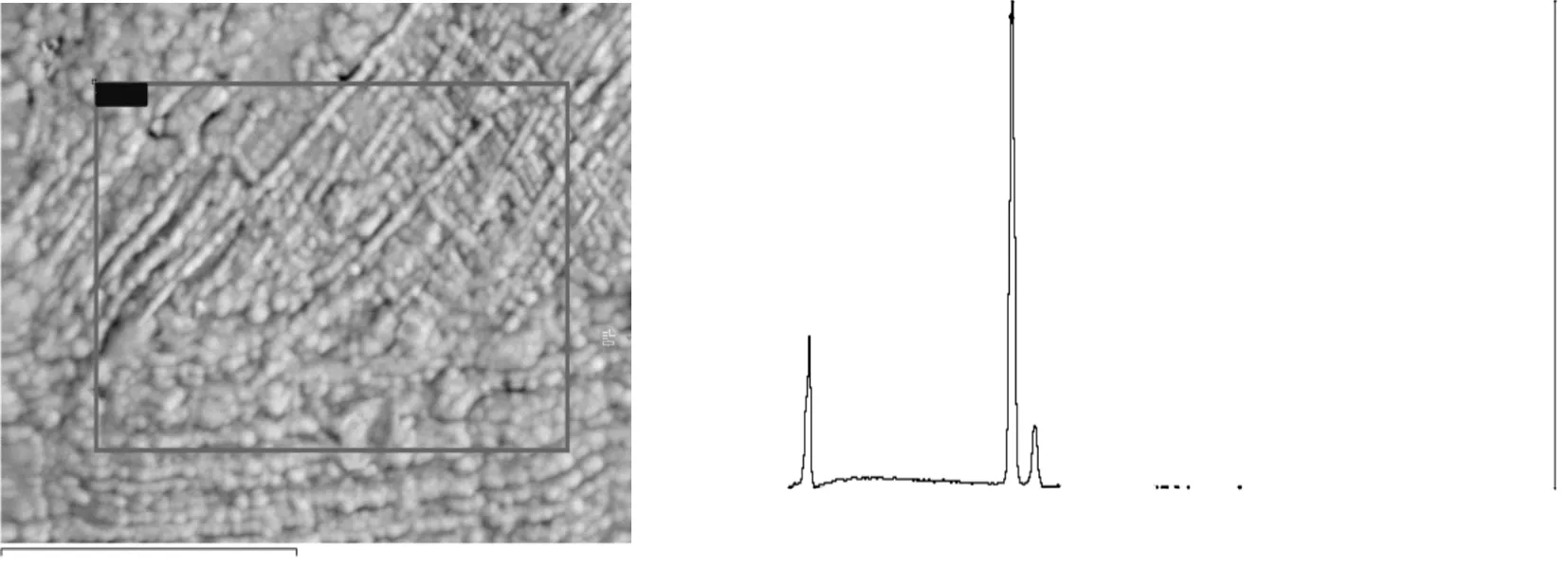
图1 金属锰SEM-EDS分析

图2 金属锰夹杂区域SEM-EDS分析

图3 金属锰附带区域SEM-EDS分析
2.2 杂质元素化学分析
样品的杂质含量分析结果与《电解金属锰》YB/T051-2015标准电子级金属锰比较见表1,样品中杂质元素均未超标。
表1 样品杂质含量与YB/T051-2015标准电子级锰对比

注:杂质铅在YB/T051-2015标准未作要求。
3 结果与讨论
3.1 C、O、S、Se杂质元素分析
图2的SEM-EDS中可见,杂质在金属锰的夹杂区域中存在,存在的杂质元素为C、S和O。在工业化生产中,硫酸锰溶液中加入SDD(二甲基二硫代氨基甲酸钠)除去溶液中的金属离子。SDD是一种水溶性物质,化学式为(CH3)2NCSSNa,在碱性介质中较稳定,在酸性及高温条件下易分解,生成CS2等极细的胶状颗粒选悬浮于硫酸锰溶液中,在电解过程中被金属锰吸附和包裹,使产品中C和S超标。实际生产过程中,可以通过测定硫酸锰溶液中金属离子总量加入适量的SDD以控制产品金属锰中C和S的量;O存在的可能原因为金属锰夹带的MnSO4未清洗干净;Se超标的原因为在电解过程中加入添加剂SeO2。SeO2可以促进锰电解反应及抑制析氢反应,在电解液中水解,SeO2加入到电解液中溶解,发生一系列水解反应[8]:
SeO2+H2O=H2SeO3
H2SeO3HSeO3-+H+
HSeO3-SeO32-+H+
在不同的还原电位下,含有Se(Ⅳ)的水解产物会还原成单质硒:
SeO32-+3H2O+4e-Se+6OH-
在阴极上发生还原反应[9-10]生成单质硒沉积在金属锰中:
Se+2e-→Se2-
Se2-+Mn2+MnSe
Se2-+2H2OHSe-+OH-+H2O⟺H2Se+2OH-
MnSe+2e-→Mn+Se2-
3.2 Pb2+、Fe2+和Mg2+杂质元素分析
工业生产中,硫酸锰溶液的Mg2+无法进行除杂处理,Pb2+和Fe2+加入硫化剂(以RS表示)去除,化学反应式为:
PbSO4+RS→PbS↓+RSO4
FeSO4+RS→FeS↓+RSO4
两种沉淀按照溶度积规则[11]换算为金属离子的溶解度,Fe2+、Pb2+、Mn2+均用M2+表示:
C(Fe2+)·C(S2-)=Ksp(FeS)(Cθ)2
C(Pb2+)·C(S2-)=Ksp(PbS)(Cθ)2
查表[11]得金属离子放电的标准电极电势,如下式:
按照能斯特方程[12]计算金属离子放电的还原电势,如表2所示:

表2 3种沉淀的溶度积与溶液中金属离子浓度
由表3可见:电极电势大小为φ(Pb2+/Pb)>φ(Fe2+/Fe)>φ(Mn2+/Mn)>φ(Mg2+/Mg),阴极上优先发生电极电势较高的反应,Fe2+和Pb2+优先于Mn2+析出,金属锰中的杂质Fe和 Pb是由硫酸锰溶液经过电解沉积在金属锰产品中;Mg2+与Mn2+相比,Mn2+发生放电反应,由图2可见,Mg、S和O同时存在于金属锰的夹杂物中,其原因为:碳酸锰矿中的杂质元素镁在酸浸过程中产生硫酸镁,在电解循环利用过程中不断累积形成饱和溶液,且无法通过沉淀的方式去除,在40℃时,MnSO4-(NH4)2SO4溶液体系MgSO4可以高达120 g/L[13],在电解过程中,硫酸镁在金属锰夹杂物处结晶。

表3 金属离子标准电极电势
3 结 论
1)金属锰中存在的杂质元素为C、O、Mg、S、 Fe、Se和Pb,以夹杂物或附带物的形式存在,与YB/T051-2015标准电子级锰,杂质元素均未超标;
2)金属锰中非金属杂质元素的主要来源为除杂净化过程加入SDD和添加剂二氧化硒造成;金属杂质元素的主要来源为:Fe2+和Pb2+的电极电势大于Mn2+,发生了优先放电反应;而Mg2+的电极电势小于Mn2+,硫酸镁在金属锰夹杂物处结晶造成;
3)控制金属锰中杂质含量较好途径为:控制添加剂加入量、筛选除杂效果较好的添加剂、清洗等方式解决。

