高效液相色谱法快速测定红糖中丙烯酰胺
郑莛予,陈杰博,王 璐,郑明锋,汪 鹏,褚杜娟
(1福建农林大学食品科学学院,福建福州350002;2福建农林大学国家甘蔗工程技术研究中心,福建福州350002;3福建农林大学生命科学学院/农业生态研究所,福建福州350002)
0 引言
丙烯酰胺(Acrylamide),其化学式为 C3H5NO,在常温下为白色晶体状,无气味,易溶于水、乙醇、丙酮等极性溶剂中。人体可以通过消化道、呼吸道、皮肤黏膜等多种途径接触并吸收丙烯酰胺。1993年世界卫生组织将其评估为致癌风险物质。1994年,丙烯酰胺被国际癌症研究机构列为2A级致癌物[1]。2002年4月,瑞典国家食品管理局宣布在加工食品中发现了丙烯酰胺,此后食品中的丙烯酰胺得到了广泛的关注[2]。加工食品中的丙烯酰胺多产生于食品内部的美拉德反应,因此在咖啡、面包、薯片或其他经过热处理的淀粉类食品陆续检测出了丙烯酰胺[3-8]。
在中国,红糖不仅作为一种甜味剂,还是一种功能食品,中医认为红糖具有滋补气血、健脾养胃等功能,女性在月子、月经期间大量饮用红糖及其制品,这被认为具有排恶露和暖宫的作用。现代研究表明,红糖富含酚类、维生素、矿物质以及多种人体必需氨基酸等营养物质[9],具有抗氧化、防衰老和美容养颜等功效。作为红糖生产的原料——甘蔗汁,其富含葡萄糖、果糖等还原糖和天冬氨酸等氨基酸,这些在蔗汁熬煮过程中通过美拉德反应和褐变反应,使红糖产生特有的香味和颜色,也产生了中医认为的红糖的温热属性,但同时,还原糖与氨基酸发生的美拉德反应也容易产生如丙烯酰胺、5-羟甲基糠醛等有害物质。Hoenicke[10]、Cheng[11]采用LC/MS/MS和GC-MS等对当地红糖/黑糖的丙烯酰胺进行了抽样检测;Gómez-Narváez[12]等对南美洲和欧洲等国家的 2种不同外观形式的红糖“Panela”共计40款进行了丙烯酰胺检测,这2种形式的红糖中均检测出了丙烯酰胺,部分红糖中的丙烯酰胺含量高达2632 ug/kg±111 ug/kg。但是,目前食品中丙烯酰胺的检测方法主要是基于高淀粉类食品,采用高效液相色谱-质谱联用法、气相色谱-质谱联用法、毛细管电泳法等[13-14]。质谱在定量检测中运用广泛,且具有更高的灵敏度与精确度,但质谱的检测成本昂贵,对仪器、试剂和样品的前处理要求很高,大多需要对样品进行衍生化或固相萃取技术。Castle[15]等对丙烯酰胺的溴化使其具有了高挥发性,使得溴化后的丙烯酰胺可应用于气相色谱检测中,提高了检测的选择性,但溴化方法费时费力,反应时间长,需要严苛的温度控制,并且溴化液对环境造成污染。Pedersen[16]等基于索氏提取方法,用甲醇连续提取样品10天后无需衍生化便可用GC-MS进行检测。Cavalli[17]等采用固相萃取设备(SPE)与加速固相萃取装置(ASE)结合对样品进行除杂处理,丙烯酰胺的回收率为60%~95%。Achim[18]采用离子肼LC-ESI-MS/MS检测丙烯酰胺,检出限低至0.55 ng/mL。红糖主要成分是糖分,其最大的特点是具有高的水溶性,这些基于高淀粉样品发展起来的检测方法,由于需要对样品中的淀粉、油脂等组分进行去除,存在着操作繁琐、设备要求高、检测成本高等问题。然而,红糖的糖分和丙烯酰胺均为强极性物,这就需要更多关注强极性组分之间的分离作用,因此,开发如红糖高水溶性样品的丙烯酰胺快速、低成本的检测方法,对保证红糖食品安全具有重要的意义。
高效液相色谱法(High Performance Liquid Chromatography,HPLC)具有高效、检测成本低等优点。Hypercarb液相色谱柱采用独特的100%多孔石墨碳作为填料,它的化学表面特性明显区别于传统的硅胶基质填料,如键合硅胶及聚合物等[19-20],对高极性分析物具有出色的保留能力[21-22]。丙烯酰胺在210 nm左右有较强的紫外吸收,而蔗糖、葡萄糖等糖组分没有紫外吸收,可以减少糖分对丙烯酰胺检测的干扰。因此,采用HPLC-UV结合Hypercarb色谱柱,有望实现对红糖中丙烯酰胺的快速高效低廉的检测。
1 材料与方法
1.1 材料与试剂
10种不同品牌的红糖,购自福州超市和淘宝网;丙烯酰胺标准品(纯度≥99%),上海阿拉丁生化科技有限公司;甲醇(色谱纯),美国Thermo Fisher公司;实验用水由Milli-Q超纯水机系统制得。所有的试剂和溶液在进入检测器之前都要用0.22 μm微孔过滤膜过滤,超声除气。
1.2 仪器与设备
Waters 2695高效液相色谱系统配2998光电二极管矩阵(PDA)检测器,美国Waters科技有限公司;Hypercarb多孔石墨碳液相色谱柱(4.6 mm×100 mm,3 μm),美国Thermo Fisher公司;电子分析天平(感量0.1 mg),瑞士梅特勒-托利多国际有限公司。
1.3 方法
1.3.1 丙烯酰胺标准储备溶液的配制
准确称取丙烯酰胺标准品0.0500 g,用去离子水溶解后置于1000 mL容量瓶中,用去离子水定容,配置成质量浓度为50 μg/mL的丙烯酰胺溶液,再取1 mL该溶液于棕色容量瓶中稀释至100 mL,配置成0.5 μg/mL的丙烯酰胺标准储备液,置于4℃冰箱内保存备用。
1.3.2 红糖样品的前处理
分别取上述10种红糖适量,研磨成粉,准确称取0.50 g(精确到0.01 g)红糖样品充分搅拌溶解,配置成不同溶度的红糖溶液,0.22 μm滤膜过滤后用于高效液相色谱分析。
1.3.3 色谱条件
色谱柱选择 Hypercarb多孔石墨碳液相色谱柱(4.6 mm×100 mm,3 μm);进样量 20 μL;色谱柱温度35℃;流速1.0 mL/min;流动相:甲醇-水(15∶85,V/V);检测波长:210 nm,利用保留时间定性,峰面积定量。
1.3.4 标准曲线的绘制
取不同体积(0.2、0.8、1.4、2.0、2.6、3.2 mL)的1.3.1节配制的丙烯酰胺标准储备液,用去离子水定容于10 mL容量瓶中,涡旋振荡摇匀,配制成浓度分别为 0.01、0.04、0.07、0.10、0.13、0.16 μg/mL的系列标准品工作液,分别进行HPLC分析。以质量溶度(μg/mL)为横坐标,以峰面积为纵坐标绘制标准曲线,计算丙烯酰胺的线性范围、回归方程及相关系数。
在相同的色谱条件下进行样品的测定,根据标准品丙烯酰胺的保留时间对样品进行定性,根据峰面积和标准曲线进行定量,每个样品平行测定3次,结果以平均值±标准差表示。
2 结果与分析
2.1 色谱条件的优化
2.1.1 检测波长
由于甲醇在200 nm处具有紫外吸收,而丙烯酰胺在190~240 nm之间有紫外吸收,因此,吸收波长的选择对样品检测灵敏度有重要的影响。通过对15%甲醇水溶液流动相和丙烯酰胺标准溶液的全波长扫描比较,可以看到丙烯酰胺在200 nm处有最大的吸收(图1),但在210 nm处流动相的响应值远低于200 nm处(图1),其紫外吸收光谱受流动相基质干扰小,故选择210 nm作为检测波长。
2.1.2 流动相的选择
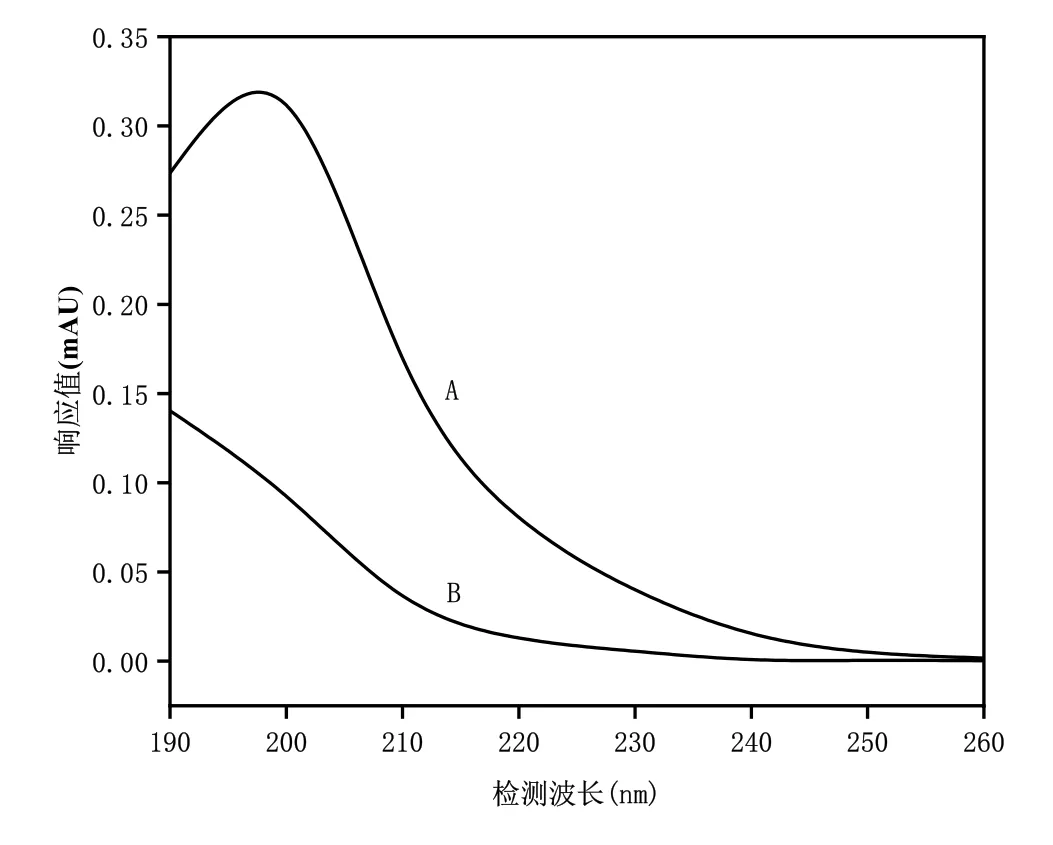
图1 检测波长对分离效果的影响
丙烯酰胺是强极性化合物,在反相色谱柱上的保留较弱,流动相常采用有机溶剂和水的混合物,通过调节流动相的比例,可以得到较为理想的分离效果。本研究采用黏度和毒性较低的甲醇进行优化实验,同时考察流动相酸性对分离效果的影响,由图2可见,随着流动相甲醇含量的增加,流动相对丙烯酰胺的洗脱能力增强,其保留时间由 3.8 min减少至2.0 min,甲醇含量的增加,丙烯酰胺的峰型逐渐尖锐,当甲醇含量为15%时,基线平稳,没有明显的漂移,丙烯酰胺的峰型尖锐,对称性良好,保留时间较为适宜,避开了杂质峰的干扰。而在流动相中添加磷酸时,基线漂移较为严重。综上,选择15%的甲醇水溶液作为流动相。
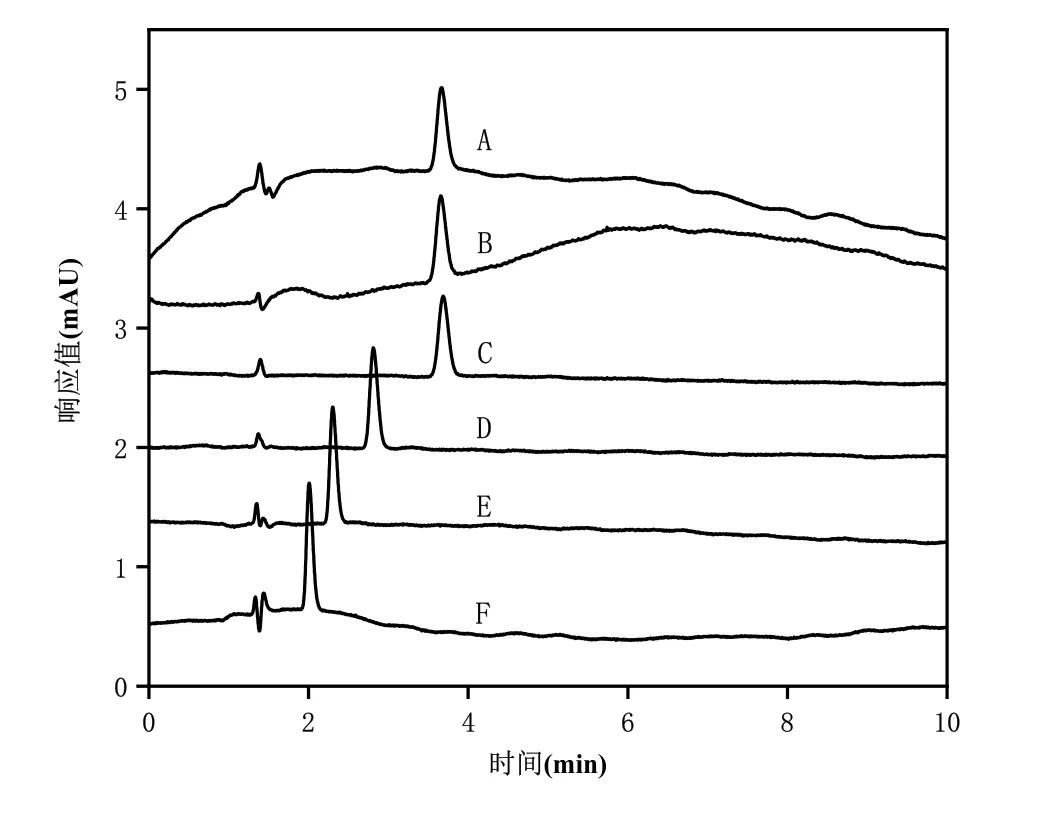
图2 流动相对分离效果的影响
2.1.3 样品浓度
红糖大部分的组分具有较强的水溶性,红糖溶液的浓度对丙烯酰胺与其他组分的分离有重要影响,红糖水浓度高容易造成其他组分对丙烯酰胺色谱峰的掩盖,而浓度低,丙烯酰胺峰不明显。因此,采用15%甲醇水溶液作为流动相,1.0 mL/min的流速,210 nm检测波长,图3比较6种不同浓度的红糖水溶液(1%、2%、5%、10%、20%、30%)丙烯酰胺的分离效果。随着红糖水溶液浓度的增加,丙烯酰胺色谱峰逐渐明显,当红糖浓度为20%,能明显看到丙烯酰胺峰,继续提高红糖浓度至30%时,基线漂移较大,红糖中杂质对丙烯酰胺峰造成了干扰,同时红糖溶液的粘性增加,可能使色谱柱堵塞的几率增大,从而可能降低色谱柱的使用寿命,故选择20%红糖溶液作为红糖中丙烯酰胺检测的最佳浓度。
2.2 方法评价
2.2.1 线性关系与最低检出限
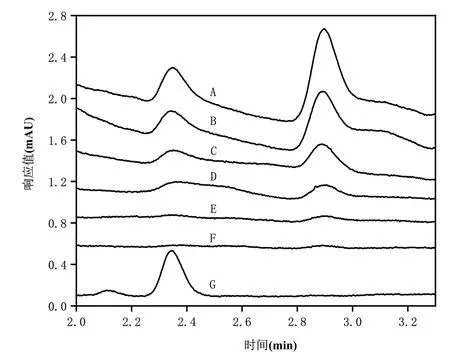
图3 9号红糖样品溶液的浓度对分离效果的影响
将浓度为0.01~0.16 μg/mL的丙烯酰胺标准品溶液分别进样,采用HPLC进行分析。相同质量浓度重复进样3次,取3次进样的平均峰面积(y,mAU)及标准品浓度(x,μg/mL)进行线性回归。丙烯酰胺在0.01~0.16 μg/mL范围内峰面积和质量浓度呈良好的线性关系,线性回归方程为y=0.5224x+0.0020(r2=0.9991),如图4所示。
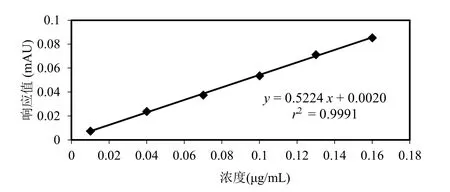
图4 丙烯酰胺标准曲线图
检出限是衡量仪器或方法灵敏度的指标,定性检出限(LOD)是在色谱图上可以清楚确认地分析目的物色谱峰的下限,通常为噪音的3倍,定量检出限(LOQ)指样品按照分析方法的要求进行提取处理并检测,能区分于噪声的最低检出浓度,通常为噪音的10倍。分别取3倍信噪比和10倍信噪比计算该方法的检出限(LOD)为 0.003 μg/mL和定量限(LOQ)为 0.01 μg/mL。丙烯酰胺标准品溶液色谱图见图5。
2.2.2 样品加标回收率和精密度
方法的准确度由加标回收率进行评定。取实验配制的等体积的9号红糖样品溶液3份,分别添加体积分数低、中、高3个水平(0.018、0.042和0.064 μg/mL)的标准品溶液,进行HPLC分析,测定丙烯酰胺的保留时间和峰面积,计算丙烯酰胺的加标回收率。日内精密度和日间精密度用于评估方法的重复性和重现性。日内精密度为在一天内平行测定 5次样品,而日间精密度为连续3天进行精密度实验,结果以峰面积的相对标准差(RSD)表示。如表1所示,丙烯酰胺在低、中、高的平均回收率分别为93.4%、86.4%和 92.0%,方法的平均日内精密度为 1.06%、3.29%、2.69%,平均日间精密度为 3.86%、2.34%、4.40%,说明本方法的随机误差较小,因而可以满足定量分析。
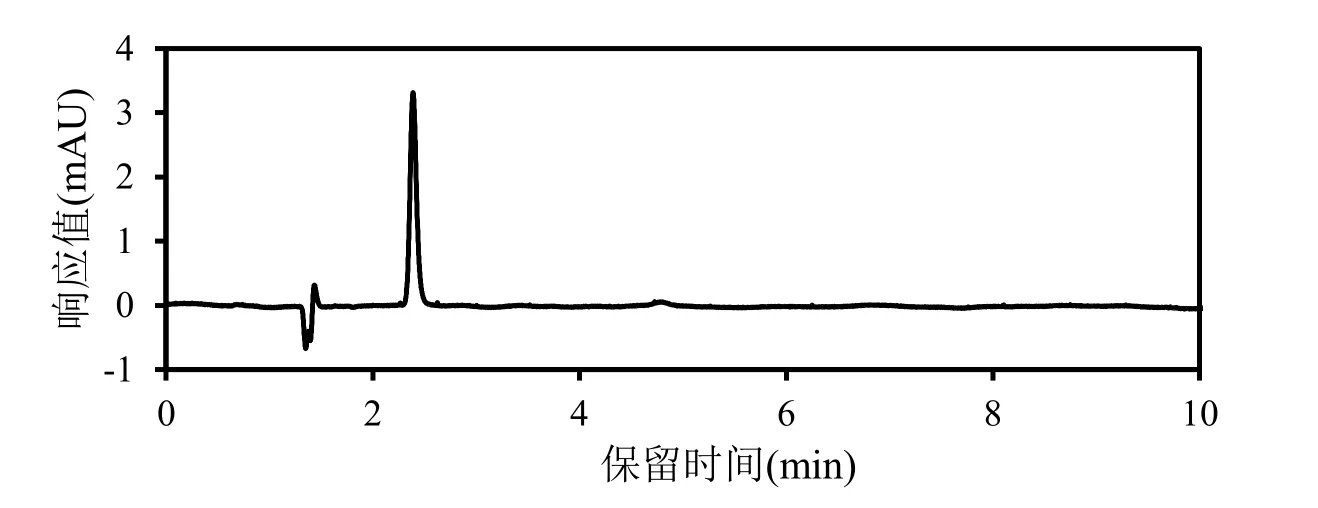
图5 丙烯酰胺标准品高效液相色谱图
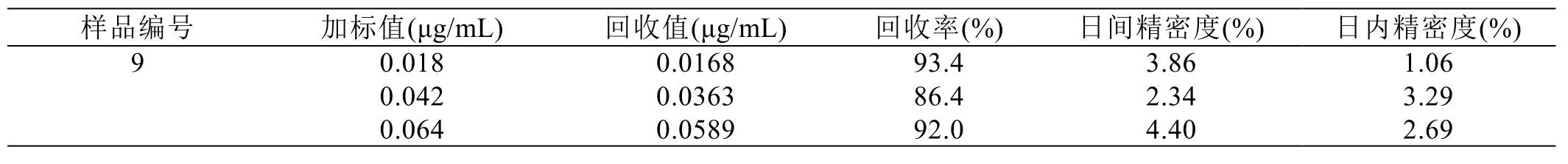
表1 9号红糖样品中丙烯酰胺的加标回收实验结果
2.2.3 样品分析及含量测定结果
经过条件优化后获得了最优HPLC分析条件:以 Hypercarb多孔石墨碳液相色谱柱(4.6 mm×100 mm,3 μm)进行分离;流动相∶甲醇-去离子水(15∶85,V/V);流动相流速为1.0 mL/min;检测波长为210 nm,柱温35℃。图6为其中一个红糖样品的色谱图。

图6 红糖样品高效液相色谱图
对市售的10个红糖样品按1.3.2节步骤进行预处理,并采用优化后的检测方法进行分析,将这些样品的色谱图和丙烯酰胺标准品色谱图进行比较,样品在2.4 min附近均有色谱峰出现,表明这些市售红糖样品均含有丙烯酰胺,详见表2。样品全部检出丙烯酰胺,检出浓度范围为 243.67~1739.33 μg/kg,最高含量达1739.33 μg/kg,平均含量为806.52μg/kg。目前国内对红糖中丙烯酰胺的含量并没有相关政策进行约束,但欧盟自2017年便已实施关于丙烯酰胺的相关法规[23]。该法规所规定的大部分食品中的丙烯酰胺都必须低于500 μg/kg,儿童食品更是低至 40 μg/kg,结合本研究结果,过半样品的丙烯酰胺含量都超过500 μg/kg,因此精确定量并控制红糖中丙烯酰胺的含量是十分重要的,过量丙烯酰胺对食品安全存在的风险的影响应当引起国家监管部门及生产企业的重视。
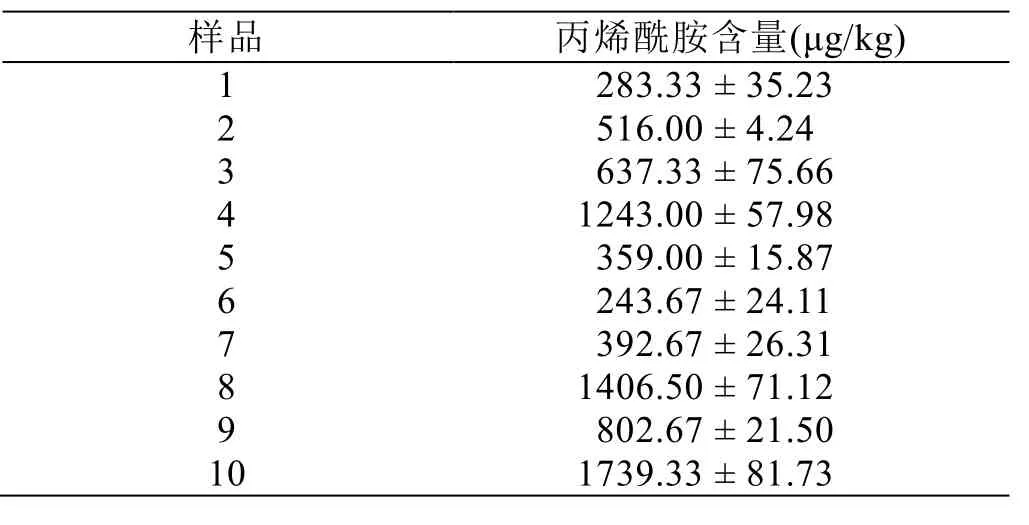
表2 各红糖样品中丙烯酰胺的含量
3 结论
本实验建立了红糖中丙烯酰胺的高效液相色谱检测方法,该方法为高水溶性食品中丙烯酰胺的分离检测提供了指导。运用该方法丙烯酰胺实现了快速高效的分离,样品加标回收率为 86.4%~93.4%,日内精密度在 1.06%~3.29%,日间精密度在2.34%~4.40%。该方法定性检出限为0.003 μg/mL,定量限为0.01 μg/mL。本方法操作简便,无需固相萃取,简化了样品预处理操作步骤;与目前广泛运用的检测方法相比,本方法大幅降低了检测成本;对所需液相色谱仪器的要求较低,可在大多数实验室中进行,具有较好的推广价值。

