食品中含硫氨基酸含量测定前处理条件的研究
叶颖慧,别致,唐凌轩,田燕
1(中国检验检疫科学研究院,北京,100123)2(中检科(北京)测试技术有限公司,北京,100123) 3(中国检验检疫科学研究院综合检测中心,北京,100123)
胱氨酸和蛋氨酸为食品中常见的含硫氨基酸。蛋氨酸又称甲硫氨酸,化学名为2-氨基-4-甲巯基丁酸,蛋氨酸参与人体内蛋白质合成,同时也参与肾上腺素、胆碱、肉碱等的合成。胱氨酸又称双硫丙氨酸,化学名为3,3′-二硫代二丙氨基酸,可形成谷胱甘肽、高半胱氨酸和牛磺酸3种主要产物,进而对人体免疫功能产生影响[1-4]。食物中含硫氨基酸的含量是蛋白质质量评价的重要指标,也是婴幼儿配方食品氨基酸模式的重要评价因素[5-7]。此外,有研究表明在美拉德反应中含硫氨基酸对风味物质的产生发挥了重要作用。在油炸条件下含硫氨基酸还具有与叔丁基对苯二酚相当的抗氧化能力,因此可以作为抗氧化剂添加于食品中,以延长食品的货架期[8-9]。因此,有必要测定食品中含硫氨基酸的含量,对其检测方法进行探讨。
食品中含硫氨基酸含量测定的研究分为游离含硫氨基酸含量和总含硫氨基酸(即游离的和蛋白质中的含硫氨基酸之和)含量的测定研究。对游离含硫氨基酸含量测定的研究通常是在食品中多种游离氨基酸含量测定的一小部分,研究方向偏重于液相色谱法、液相色谱质谱联用法等仪器方法的开发。总含硫氨基酸含量检测的样品前处理方式有直接酸水解法、保护试剂法和氧化水解法[10-11]。直接水解法会破坏—SH键,结果往往偏低。保护试剂法虽然可以一定程度上提高含硫氨基酸的测定结果,但与样品中的实际含量仍存在较大差异。氧化水解法可以将含硫氨基酸中的蛋氨酸氧化为蛋氨酸砜,胱氨酸氧化水解为半胱磺酸。这2种物质相对稳定,因此,氧化水解法的测定结果更加接近真实值。氧化水解法最重要的是样品的氧化效率。此外,由于食品样品基质复杂,也可能在氧化过程中产生不同的氧化效果。采用氧化法测定含硫氨基酸含量的研究样品基质多以饲料、发酵液、乳粉和医药等为主,以及环境检测中污泥中含硫氨基酸的测定等。研究的重点多放在色谱条件的改善和不同前处理方法对比(如酸水解与氧化水解)等方面。对于氧化水解法中影响氧化过程的因素没有细致的研究,同时也未见全面研究食品中含硫氨基酸含量检测的报道[12-24]。鉴于以上情况,本文选取谷物、豆类、肉类、乳制品、蛋类中5种典型食品样品,探讨氧化水解过程中氧化剂配制比例、氧化温度、氧化时间对不同食品基质中含硫氨基酸含量测定结果的影响。
1 材料与方法
1.1 仪器与试剂
S-433D氨基酸分析仪,德国赛卡姆公司;NDO-400恒温电热箱,上海爱朗仪器有限公司;Vortex-Genie 2涡旋混合仪,美国Scientific Industries公司;N-EVAPTM 112 氮吹仪,美国Organomation Associaes, Jnc 公司;ME204E电子天平,瑞士梅特勒-托利多国际有限公司;0.45 μm 津腾针式过滤器,天津市津腾实验设备有限公司。
L-磺基丙氨酸一水合物(纯度99%),百灵威公司;DL-蛋氨酸砜(纯度≥99.0%),美国Sigma公司。
甲酸(分析纯),Sigma公司;盐酸(优级纯),国药集团化学试剂公司;双氧水(含30%过氧化氢),北京化工厂;氢溴酸(33%乙酸溶液),百灵威公司;氮气(纯度≥99.9%),北京北氧振兴气体工程技术开发有限公司。
1.2 试验方法
1.2.1 溶液的配制
磺基丙氨酸标准储备液(211 μg/mL):准确称取23.4 mg磺基丙氨酸于50 mL烧杯中,加入5 mL 6 mol/L的盐酸溶液溶解,用水转移稀释定容至100 mL,混匀。
蛋氨酸标准储备液(200 μg/mL):准确称取24.3 mg蛋氨酸砜于50 mL烧杯中,加入5 mL 6 mol/L盐酸溶液溶解,用水转移稀释定容至100 mL,混匀。
含硫氨基酸混合标准工作液:分别吸取1 mL蛋氨酸标准储备液和1 mL磺基丙氨酸标准储备液,用水稀释定容至25 mL,混匀。
过甲酸溶液:取双氧水和甲酸不同体积比混匀,放置1 h后使用。现用现配。
盐酸溶液(6 mol/L):取500 mL 盐酸加水稀释至1 000 mL,混匀。
不同pH和离子强度的洗脱用缓冲溶液:钠系统缓冲溶液。
茚三酮溶液:钠系统缓冲溶液。
1.2.2 前处理方法
(1)采样和试样制备
乳粉、全蛋粉、玉米粉:取有代表性的样品, 用四分法缩减至200 g, 混匀, 装入自封袋中, 避光, 备用。
黄豆:取有代表性的样品, 用四分法缩减至200 g, 粉碎后过0.4 mm孔径的分析筛, 混匀, 装入自封袋中, 避光, 备用。
鱼肉:取新鲜鲤鱼肉,去骨去皮后进行粉碎,混匀后装入自封袋中,冷冻备用。
(2)样品测定
准确称取一定量试样(精确至0.000 1 g)于水解管内,加入2 mL不同比例的过甲酸溶液,在不同温度下,氧化不同时间。反应完成后加入400 μL氢溴酸,放置30 min,在50~60 ℃下将水解管内的溶液用氮气吹干。加入10 mL 6 mol/L盐酸溶液,封口,放入(110 ±1) ℃的恒温电热箱内,水解22 h后,取出冷却至室温。打开水解管,将水解液全部过滤转移至50 mL容量瓶内,用水定容至刻度,混匀。准确吸取1 mL滤液在40~50 ℃下氮气吹干,干燥后残留物用1 mL蒸馏水溶解,混匀,过0.45 μm滤膜,得到仪器待测液。
本文对前处理因素的考察为过甲酸配制比例、氧化时间、氧化温度的影响。首先分别采用双氧水与甲酸体积比为1∶3、1∶5、1∶7、1∶9、1∶11、1∶13的氧化剂在0 ℃氧化样品16 h,考察过甲酸配制比例对不同食品基质中含硫氨基酸含量测定结果的影响。确定过甲酸配制比例后,考察氧化时间、氧化温度2个影响因素。考察的氧化温度为70、50和0 ℃。当氧化温度为70℃时,考察的氧化时间分别为1.0、2.5、5.0、7.5和10 min;当氧化温度为50 ℃时,考察的氧化时间分别为5.0、10、15、20和25 min;当氧化温度为0 ℃ 时,考察的氧化时间分别为8、12、16、20和24 h。
1.2.3 仪器测定
色谱条件:色谱柱:钠系统分析柱(4.6 mm×150 mm);进样量:50 μL;检测波长:570 nm;梯度程序:见表1。流动相A为pH 3.45柠檬酸钠-柠檬酸缓冲溶液(钠离子浓度为0.12 mol/L);流动相B为蒸馏水;流动相C为pH 10.85柠檬酸钠-柠檬酸缓冲溶液(钠离子浓度为0.20 mol/L);流动相D为2%氢氧化钠溶液。
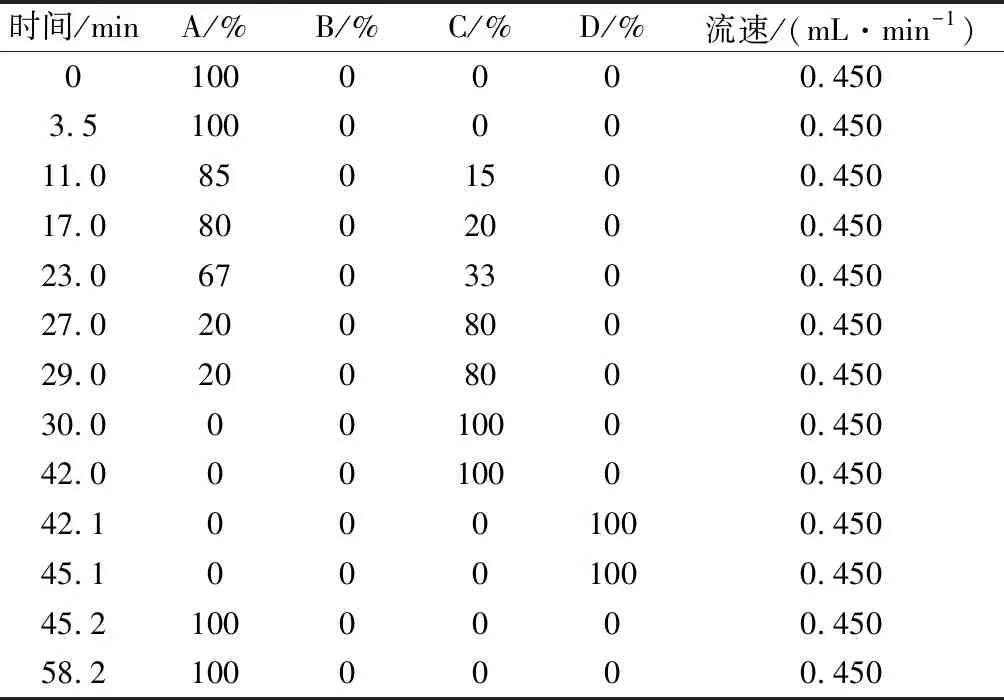
表1 氨基酸分析仪流动相的洗脱梯度Table 1 Elution gradient of mobile phase of amino acid analyzer
2 结果与分析
2.1 氧化剂配制比例对含硫氨基酸检测结果的影响
本文使用的氧化剂是过甲酸,由双氧水与甲酸反应生成。过甲酸在酸性介质中产生活性氧,进而氧化样品中的胱氨酸和蛋氨酸。过甲酸配制过程中双氧水与甲酸的体积比会影响过甲酸中活性氧的浓度。本文采用6种不同体积比的双氧水与甲酸,配制成不同浓度的过甲酸。在0 ℃氧化样品16 h后,完成后续测定,得到5种食品中含硫氨基酸的含量。设双氧水与甲酸体积比为1∶9时,样品中胱氨酸和蛋氨酸的氧化率分别为100%,过甲酸的不同配制比例对食品中胱氨酸氧化率的影响见图1,对蛋氨酸氧化率的影响见图2。
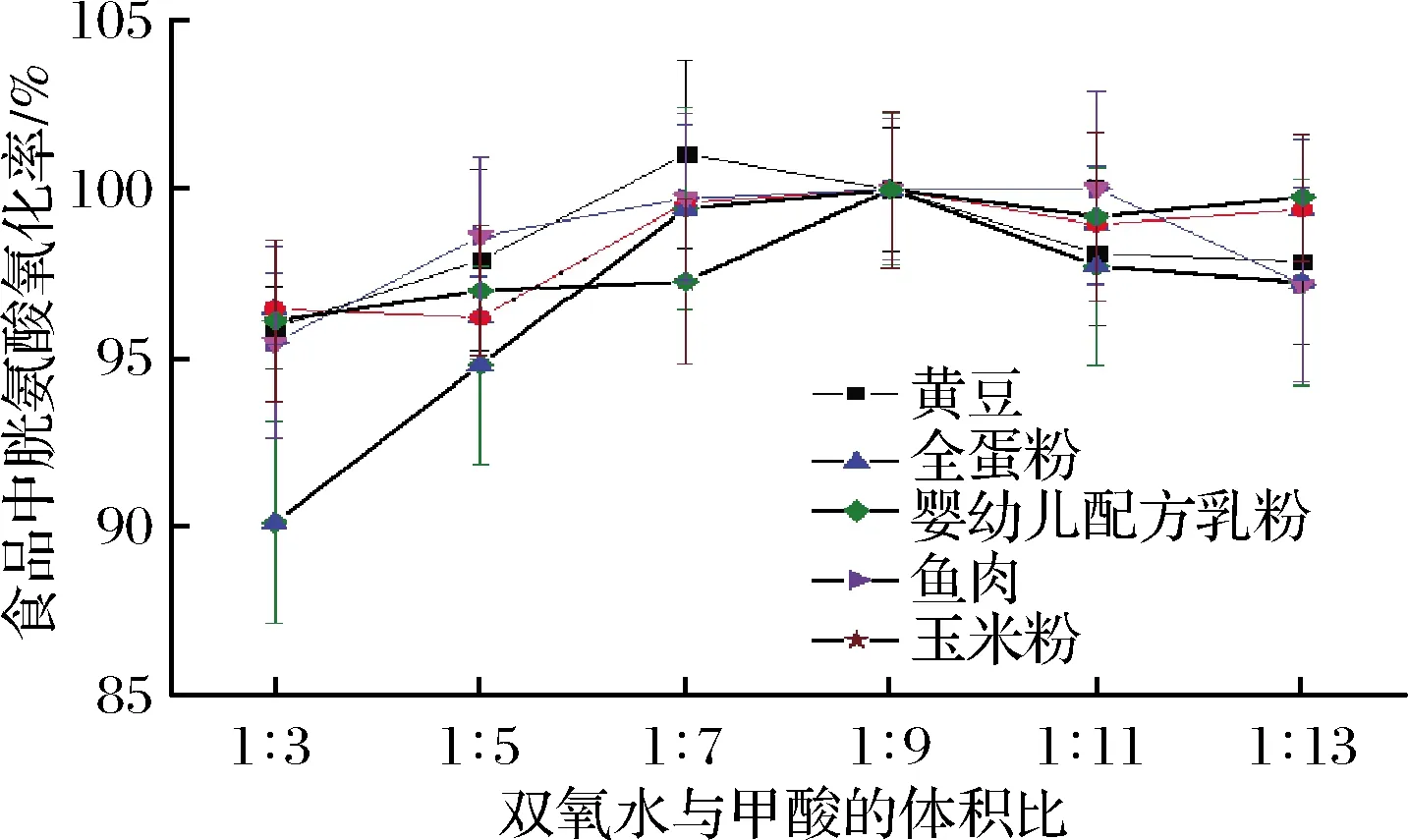
图1 过甲酸的不同配制比例对食品中胱氨酸氧化率的影响Fig.1 The influence of different proportion of performic acid on the oxidation rate of cystine in food
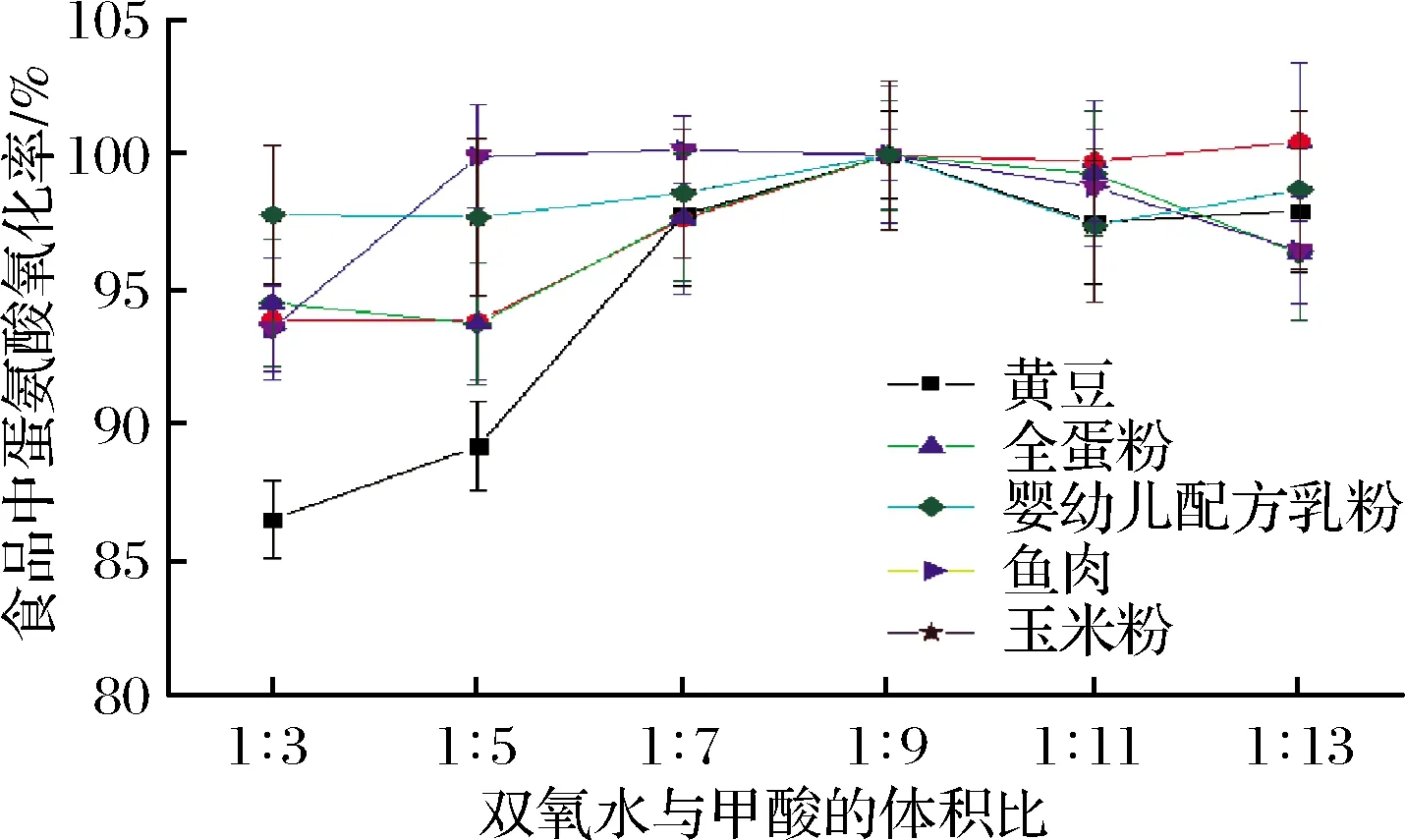
图2 过甲酸的不同配制比例对食品中蛋氨酸氧化率的影响Fig.2 The influence of different proportion of performic acid on the oxidation rate of methionine in food
由图1可以看出,使用6种不同配比的氧化剂对样品进行氧化,黄豆、婴幼儿配方乳粉、鱼肉和玉米粉中胱氨酸的氧化率都处于95%~105%。仔细观察可以发现,随着过甲酸中双氧水含量的减少,这4种食品中胱氨酸的氧化率呈现先升高后降低或趋于稳定的现象,但影响比较小。这说明,当双氧水与甲酸的体积比为1∶3~1∶13时,双氧水与甲酸的比例对这4种食品中胱氨酸检测结果的影响有限。对于全蛋粉,当双氧水与甲酸体积比为1∶3时,胱氨酸的氧化率低于95%,其误差低限低于90%,随着过甲酸中双氧水含量的降低,胱氨酸氧化率逐渐升高,当双氧水与甲酸体积比为1∶7时,胱氨酸氧化率达到95%以上,在双氧水与甲酸体积比为1∶9时达到最高值后,则有轻微的下降,但也可以保持在95%以上。通过图2 可以看到,过甲酸的配制比例对黄豆中蛋氨酸氧化率的影响比较大。当双氧水与甲酸体积比为1∶3和1∶5时,其蛋氨酸的氧化率不足90%。对于全蛋粉和玉米粉而言,过甲酸的配制比例对蛋氨酸氧化率影响不大。此外,通过趋势线可以看到,随着过甲酸中双氧水占比的降低,婴幼儿配方奶粉、鱼肉、黄豆中蛋氨酸氧化率也出现了先升高后降低的趋势。
以上的情况可以看到,配制过甲酸时,并不是双氧水浓度越高,氧化效率越高。双氧水与甲酸在特定比例下,才能得到较理想的氧化效果。有研究表明,在过甲酸的配制过程中,虽然双氧水浓度的增加可以提高溶液中活性氧的含量,但也加速了过甲酸的分解反应。在实验中同时发现,甲酸溶液中双氧水的量偏高将导致在加入终止剂后反应过于激烈,大量的溴溢出,出现部分迸溅现象,易发生危险[26]。此外,对于这5种不同类型的食品,过甲酸配制比例对于胱氨酸和蛋氨酸检测结果的影响出现了不同的反应,这极有可能是样品基质差异造成的。通过氧化剂的不同配制比例的影响因素分析可知,过甲酸中双氧水的占比并非越高越好,需要控制在适当的范围内才能得到更好的结果。在实际检测应用过程中,同一批次可能会涉及多种类型的样品。因此,本文选择1∶9的体积比配制过甲酸溶液,确保多数样品得到充分的氧化,量值偏低的样品结果也能够控制在合理的误差范围内。
2.2 不同氧化时间检测结果的影响
含硫氨基酸氧化的程度受到反应时间的影响,不同的样品基质在不同的氧化温度和时间条件下可能产生不同的结果。本文探讨了70 ℃、50 ℃、0 ℃温度下不同氧化时间对胱氨酸和蛋氨酸结果的影响,见表2~表4。
由表2和表3可以看出,在70 ℃和50 ℃下短时间氧化下,各样品中含硫氨基酸含量的测定结果相对标准偏差在10%以内,没有明显的差异。通过数据间细微差异分析发现,无论50 ℃还是70 ℃,氧化时间为5 min时该温度下样品中含硫氨基酸含量的检测结果均接近最大值。同时发现,在这2个较高温度下,当氧化时间超过5 min以后,鱼肉的胱氨酸含量略有下降。
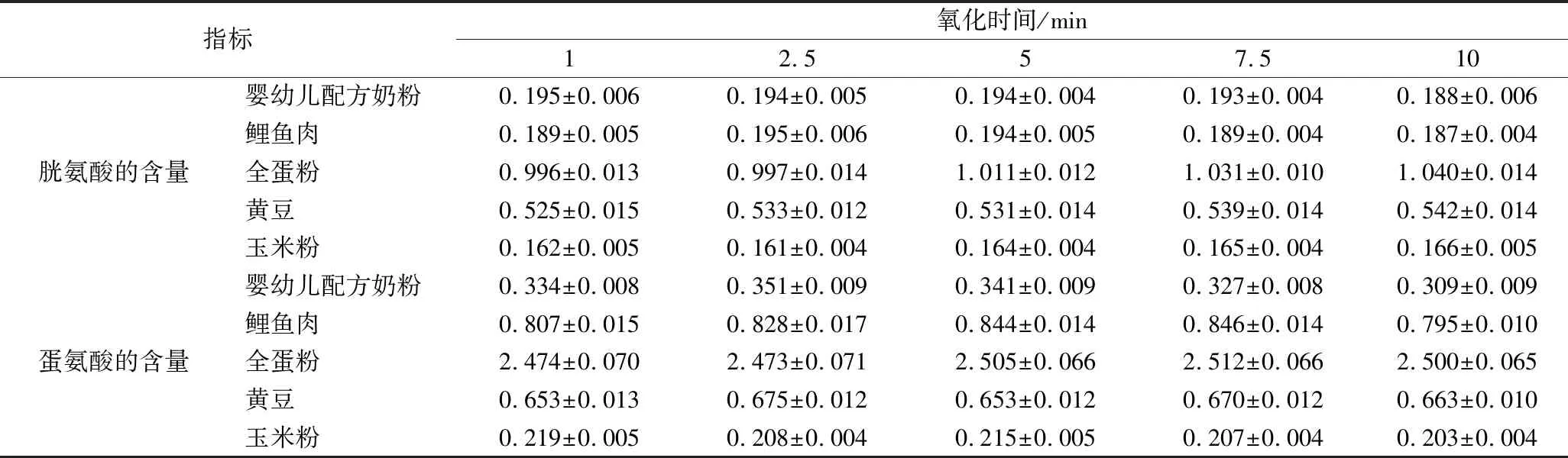
表2 70 ℃下不同水解时间对食品中含硫氨基酸含量测定结果的影响 单位:g/100g

表3 50 ℃下不同水解时间对食品中含硫氨基酸含量测定结果的影响 单位:g/100g
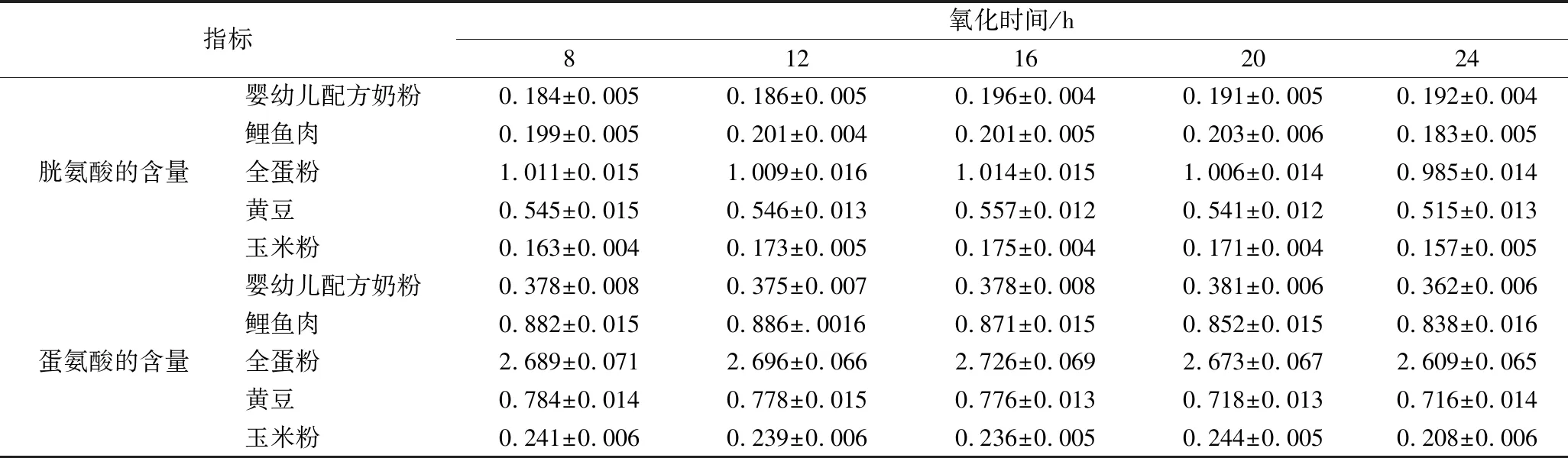
表4 0 ℃下不同水解时间对食品中含硫氨基酸含量测定结果的影响 单位:g/100g
从表4中看出,采用0 ℃长时间氧化法,氧化时间不足16 h时,随着氧化时间的延长,玉米粉中的胱氨酸含量和全蛋粉中的蛋氨酸含量的检测结果有所升高,其余基质样品的含硫氨基酸含量的检测结果没有明显的升高;当氧化时间为16 h时,各基质样品中胱氨酸和蛋氨酸含量的检测结果最高;继续增加氧化时间,黄豆、鲤鱼肉、玉米粉中的胱氨酸含量和全蛋粉中的蛋氨酸含量的检测结果呈现了降低的趋势,分析原因可能是氧化的产物与样品基质中的其他物质发生反应而产生了降解。
通过以上分析,选择70 ℃下氧化5 min、50 ℃下氧化5 min、0 ℃下氧化16 h可以作为各温度下氧化的最佳条件。
2.3 不同氧化温度不同时间对检测结果的影响
本文分别选取实验得到的0 ℃、50 ℃、70 ℃的最佳条件,测定5种不同基质食品中含硫氨基酸的含量。不同氧化条件对这5种食品中胱氨酸和蛋氨酸含量检测结果的影响见图3和图4。
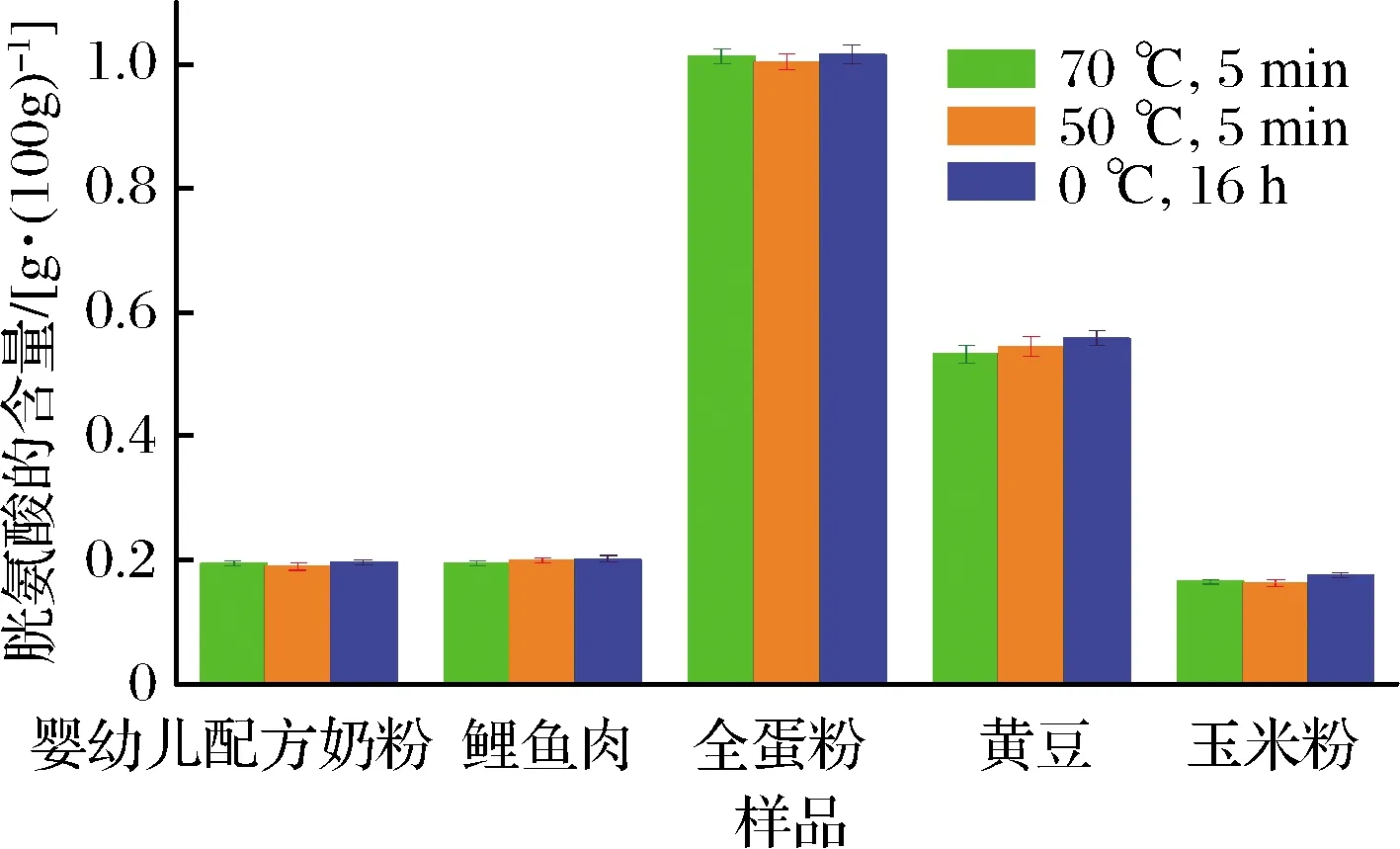
图3 不同氧化条件对食品中胱氨酸含量测定结果的影响Fig.3 The influence of different oxidation conditions on the determination of cystine content in food
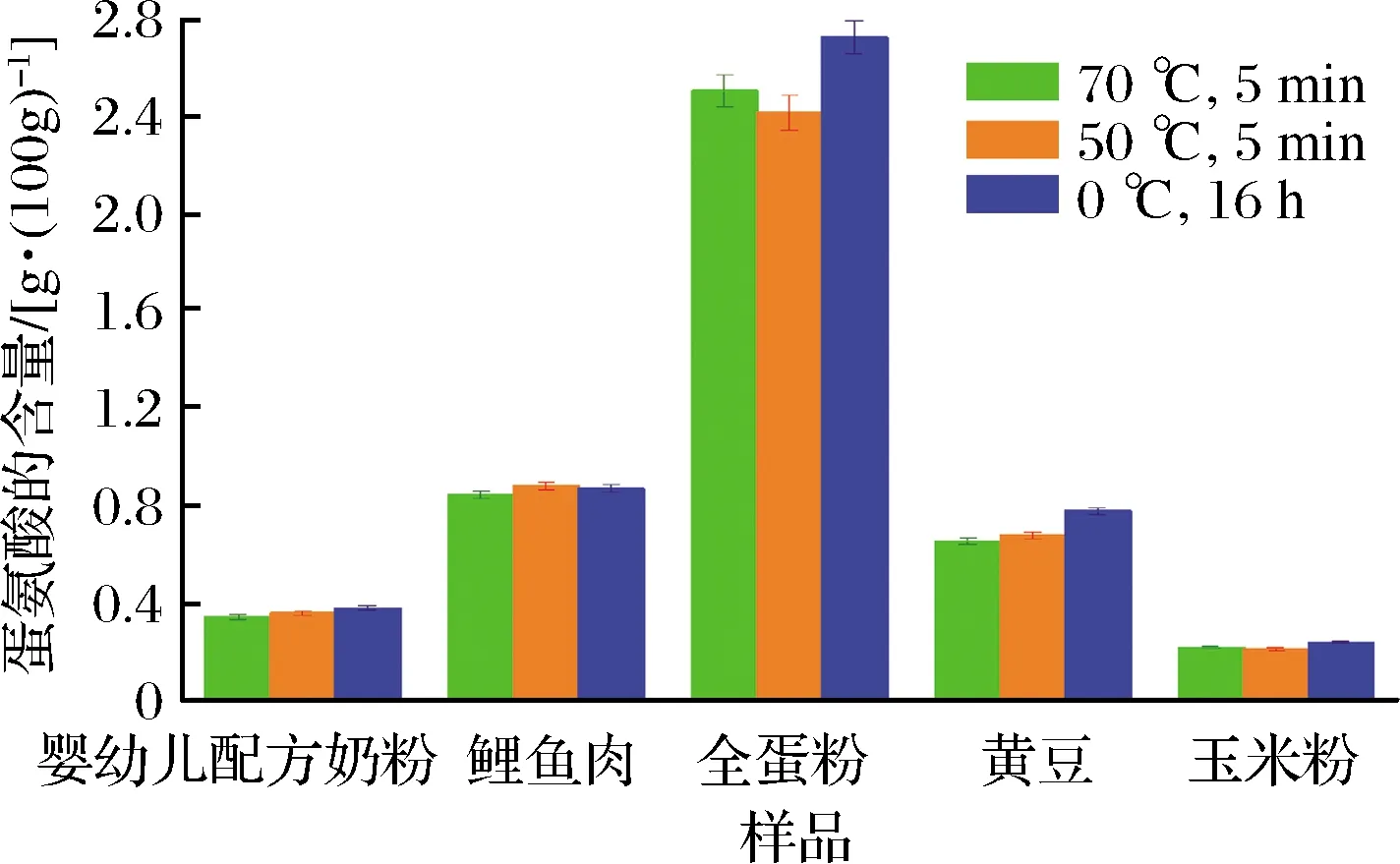
图4 不同氧化条件对食品中蛋氨酸含量测定结果的影响Fig.4 The influence of different oxidation conditions on the determination of methionine content in food
由图3和图4可知,不同的氧化条件下这5种基质样品中胱氨酸和蛋氨酸含量的检测结果呈现不同的反应。几乎所有基质的样品在50 ℃和70 ℃的短时间氧化条件下测得的含硫氨基酸含量的结果差异并不大。但采用0 ℃长时间氧化条件时,不同基质的样品得到的含硫氨基酸的检测结果出现了分化。当0 ℃氧化16 h时,黄豆和玉米粉中胱氨酸含量的检测结果略高于50 ℃和70 ℃氧化5 min得到的结果,而其余4种基质样品中胱氨酸含量的检测结果则没有明显差异;在同样条件下,全蛋粉和黄豆中蛋氨酸含量的检测结果明显高于50 ℃和70 ℃氧化5 min得到的结果,而其余3种基质样品中蛋氨酸含量的检测结果没有明显差异。曾有研究表明,在温度较高的情况下,过甲酸中的活性氧会加速溢出挥发到空气中,从而降低溶液中活性氧的含量。同时,这5种食品中全蛋粉和黄豆的蛋白质总量比较高,这有可能是样品氧化不完全,检测结果偏低的原因[26]。
通过对不同温度不同氧化时间下不同样品基质中含硫氨基酸含量检测结果的分析,0 ℃下氧化16 h可以取得5种食品中含硫氨基酸含量检测的均比较满意结果。当检测周期较短时,对于鱼肉、婴幼儿配方奶粉和玉米粉,也可以选用50 ℃氧化5 min作为氧化条件。
2.4 线性关系和检出限
配制磺基丙氨酸和蛋氨酸的标准工作溶液,磺基丙氨酸通过分子质量折算为对应的胱氨酸含量。以标准溶液浓度(μg/mL)为横坐标,以峰面积为纵坐标,绘制标准曲线,通过回归计算求得回归方程和相关系数。以3倍信噪比对应的目标物含量为此方法该化合物的检出限,10倍信噪比对应的目标物含量为该化合物的定量限。胱氨酸和蛋氨酸的线性范围、回归方程、相关系数、检出限和定量限见表5。结果表明,胱氨酸和蛋氨酸都具有很好的线性关系,相关系数r值均大于0.999。

表5 胱氨酸、蛋氨酸的线性范围、回归方程、相关系数、 检出限和定量限Table 5 Linear ranges, regression equations, correlation coefficients, LODs and LOQs of cysteine and methionine
2.5 回收率和精密度
按照选定条件对以上5种样品进行了3水平加标回收试验,加标水平为样品中胱氨酸(或蛋氨酸)含量的50%、100%和150%添加,回收率和重复性结果见表6。结果表明,对于以上5种食品胱氨酸的回收率为85%~102%,蛋氨酸的回收率为82%~94%,5种样品胱氨酸和蛋氨酸加标回收率的RSD均小于5%,方法的准确性和重复性较好。
2.6 样品的测定
选择16个不同的样品按照选定条件测定样品中含硫氨基酸的含量,实验结果如表7所示。
3 结论
综上,氧化剂配制比例、氧化温度、氧化时间3个因素对于文中涉及的5种食品中含硫氨基酸含量的检测结果均有不同的影响。首先,过甲酸中双氧水的占比并非越高越好,应保持适度。其次,由于氧化产物可能与食品中其他物质反应,氧化时间也不是越长越好。最后,测定鱼肉、婴幼儿配方乳粉和玉米粉中含硫氨基酸的含量时,采用50 ℃和70 ℃也可以得到较好的氧化效果,同时缩短氧化时间。通过对本文选取氧化条件的重复性、准确性、线性关系、检出限和回收率的验证,对于大多数食品基质,选取双氧水与甲酸体积比为1∶9、氧化温度为0 ℃时氧化16 h的氧化条件,可以得到较好的检测结果。

表6 五种食品中胱氨酸、蛋氨酸含量测定的加标回收结果Table 6 Recovery results for determination of cysteine and methionine in these five kinds of food
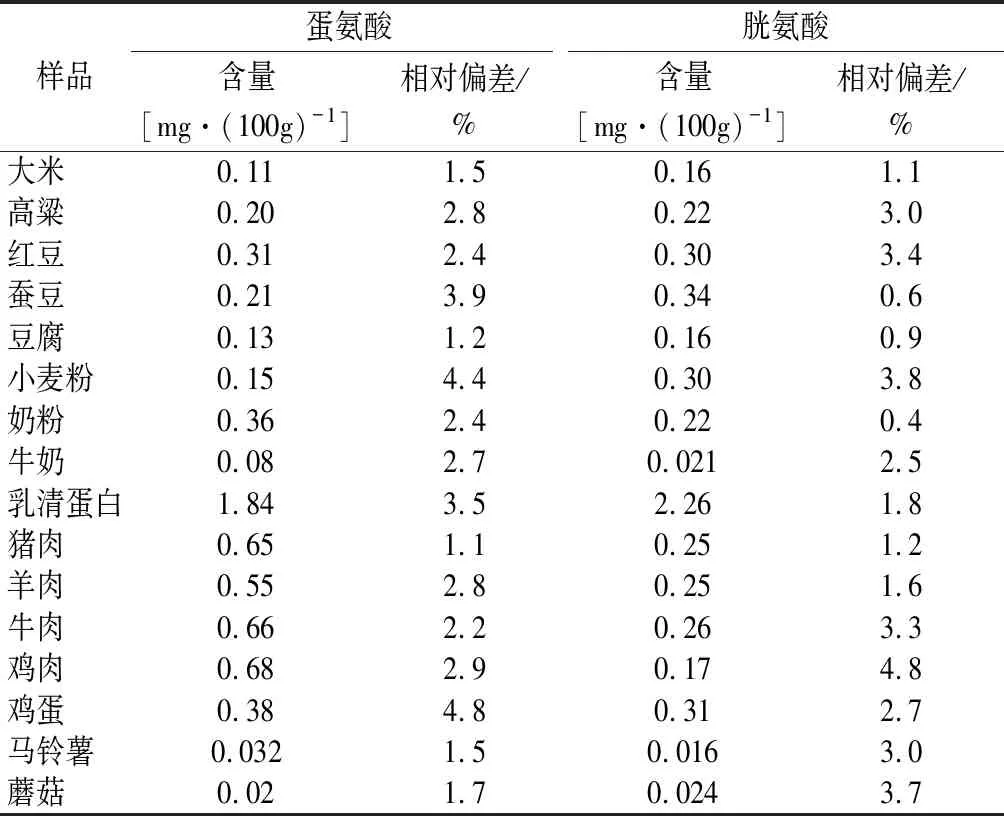
表7 不同食品中含硫氨基酸含量的测定结果Table 7 Determination results of sulfur-containing amino acids in different foods
通过本文的数据可以看出,由于这5种食品的基质差异较大,产生的影响是不完全一致的。食品基质非常复杂,不同食品中蛋白质的结构和含量不同,各基质食品中的脂肪、碳水化合物、氯化物等含量也不相同,食品基质中的哪类物质是对氧化效果产生较大影响的因素还需进一步探索研究。

