康柏西普不同玻璃体腔注射方案治疗湿性年龄相关性黄斑变性的疗效及安全性比较
张鹏 高蕾 王淑静 李一啸 王红
年龄相关性黄斑变性(AMD)是老年人群中常见的严重致盲性眼病之一,包括干性AMD和湿性AMD,其中湿性AMD对视力的损伤更严重,治疗难度大,预后较差。脉络膜新生血管(CNV)引起的渗出、出血及纤维瘢痕是导致湿性AMD视力丧失的主要原因[1,2]。血管内皮生长因子(VEGF)在CNV形成过程中发挥促进作用,为目前CNV治疗的主要靶点[3]。但由于抗VEGF药物半衰期短,因此要达到治疗目的或维持视力需多次进行玻璃体腔注射。研究发现抗VEGF药物玻璃体腔注射时机不合适,有可能会导致视力损害或丧失[4-6],这就意味着患者需要每1~2 个月就要进行复查和重复注射,给患者带来了一定的经济及心理负担,也增加了眼内炎及其他眼部并发症的风险[7]。因此延长药物玻璃体腔注射时间间隔,减少给药频次是目前抗VEGF药物治疗的研究焦点。康柏西普是一种新型重组可溶性VEGF受体蛋白,具有多靶点、亲和力强、作用时间长等特点,PHOENIX研究证实康柏西普采用(Oncemonthly for the first 3 months,followed by one injection every 3 months,3+Q3M)注射方案治疗湿性AMD是安全和有效的[8]。目前我国康柏西普治疗湿性AMD普遍采用中华医学会眼科学会眼底病学组推荐的(Oncemonthly for the first 3 months,then pro re nata,3+PRN)方案[9]。鲜见康柏西普3+Q3M注射方案与3+PRN方案的疗效比较研究。因此,本研究探讨康柏西普3+Q3M与3+PRN方案治疗湿性AMD的疗效及安全性,报告如下。
1 对象与方法
1.1 对象
纳入2018年8月至2019年8月在山东大学齐鲁医院就诊的湿性AMD患者106 例,双眼患者仅选择右眼,共纳入106眼。所有患者均经荧光素眼底血管造影(FFA)和吲哚青绿血管造影(ICGA)检查确诊。参照文献[10-13]的标准制定纳入和排除标准。纳入标准:①年龄≥50岁;②AMD眼经FFA和ICGA检查有中心凹下或中心凹旁CNV;③依从性好,自愿按期随访。排除标准:①曾接受抗VEGF药物玻璃体腔注射或视网膜激光光凝治疗者;②有除白内障以外的其他内眼手术史;③其他原因引起的CNV;④合并有其他视网膜疾病;⑤合并影响玻璃体腔注射的严重全身性疾病;⑥屈光介质不清。根据药物注射方案不同将患者分为3+PRN组和3+Q3M组。3+PRN组患眼采用中华医学会眼科学会眼底病学组推荐的方案:每个月注射1次,连续3个月,以后出现以下情况选择重复注射治疗[14,15]:①OCT显示视网膜下或视网膜内积液持续存在或复发;②黄斑区新的出血灶;③FFA检查显示CNV病灶渗漏增加或新病灶出现;视力下降>1 行或自觉视力下降。3+Q3M组患眼按照PHOENIX研究方法:每个月注射1次,连续3个月后,每3个月注射1次,共6次[8]。本研究经山东大学齐鲁医院伦理委员会审核批准(批号:2018058),所有受检者均了解本研究治疗方法和目的、治疗中及治疗后可能发生的风险及术后可能的并发症,并签署手术知情同意书。
1.2 方法
1.2.1 康柏西普玻璃体腔注射 所有患眼由同一位有丰富经验的临床医师行康柏西普玻璃体腔注射。术眼治疗前3 d用质量分数0.5%左氧氟沙星滴眼液(日本参天公司)点眼,4次/d。术中常规消毒铺巾,术眼用盐酸奥布卡因滴眼液点眼行表面麻醉,开睑器开睑,用质量分数5%聚维酮碘冲洗结膜囊90 s,大量0.9%氯化钠溶液冲洗。将30G一次性无菌注射针于颞下方角巩膜缘外3.5 mm处由睫状体平坦部垂直眼球进入玻璃体腔,注入0.05 ml(0.5 mg)康柏西普注射液(成都康弘生物有限公司),以棉棒轻压针口15 s。指测法评估术眼眼压,眼压较高者行前房穿刺并放出少量房水,同时检查术眼有无光感。术毕以妥布霉素地塞米松眼膏(西班牙ALCON CUSI公司)涂眼,用无菌敷料包盖。术后次日用0.5%左氧氟沙星滴眼液点眼,4次/d,连续点眼3 d。
1.2.2 术后随访及评估指标 术后共随访12 个月。于术后第1、2 周进行随访,以后每个月随访1次。所有术眼采用国际标准小数视力表测定最佳矫正视力(BCVA)并换算为最小分辨角对数视力(LogMAR)用于统计;采用非接触眼压计(CT-80,日本TOPCON株式会社)测量眼压;采用Visdcam(德国PRO NM公司)进行眼底照相;采用Spectralis HRA仪(德国Heidelberg Engineering有限责任公司)分别行FFA和ICGA检查,由同一名有经验的医师评估渗漏面积;采用光学相干断层扫描仪(OCT)(HD-OCT 4000,德国Cirrus Zeiss公司)测定中央视网膜厚度(Central retinal thickness,CRT)。
1.3 统计学方法
前瞻性临床研究。采用SPSS 22.0统计学软件进行统计学处理。计量资料采用Shapiro-Wilk检验进行正态分布检验,证实呈正态分布,数据以均数±标准差表示,计数资料数据以频数和百分数表示。3+PRN组与3+Q3M组术眼在不同时间点BCVA、CRT、眼压差异比较采用重复测量两因素方差分析,多重比较采用LSD-t检验;不同组别注射频次比较采用独立样本t检验进行分析;不同视网膜血管渗漏面积眼数分布、不同注射频次眼数分布和不良反应发生率差异比较均采用Chi-squareχ2检验。以P<0.05为差异有统计学意义。
2 结果
所有患者均完成12个月的随访。2组患者基线资料比较差异无统计学意义(P>0.05),见表1。
2.1 2组术眼注射频次比较
3+PRN组:注射3次者3眼,注射4次者13眼,注射5次者23眼,注射6次者11眼,注射7次者4眼,注射8次者1眼,3+PRN组55眼平均注射(5.3±1.0)次;3+Q3M组:每人均注射6 次。2 组术眼注射频次比较差异有统计学意义(t=5.231,P<0.001)。
2.2 药物注射前后2组术眼BCVA变化
2 组术眼注射前后不同时间点BCVA总体比较差异有统计学意义(F分组=7.834,P=0.006,F时间=96.033,P<0.001),术后2组术眼BCVA均优于术前,差异均有统计学意义(均P<0.05);术后9、12个月3+Q3M组术眼BCVA均优于3+PRN组,差异均有统计学意义(均P<0.05),见表2。
2.3 药物注射前后2组术眼CRT变化
2 组术眼注射前后不同时间点CRT总体比较差异有统计学意义(F分组=1.014,P=0.048,F时间=263.393,P<0.001),术后各时间点2 组术眼CRT值较术前均明显下降,差异均有统计学意义(均P<0.05),术后9、12 个月3+Q3M组术眼平均CRT值明显低于3+PRN组,差异均有统计学意义(均P<0.05),见表3。
2.4 药物注射前后2 组术眼不同CNV渗漏面积眼数分布
末次随访时,3+Q3M组术眼经FFA、ICGA检查发现CNV渗漏完全消失眼数明显多于3+PRN组;3+PRN组CNV渗漏面积缩小眼数多于3+Q3M组,3+PRN组CNV渗漏面积不变或扩大者多于3+Q3M组,但差异均无统计学意义(χ2=0.447,0.136,0.291,P>0.05),见表4。
2.5 2组术眼不良反应发生率比较
3+P R N 组结膜下出血出现1 0 例(1 8%),3+Q3M组出现8 例(16%),差异无统计学意义(P=0.732);一过性眼压升高3+PRN组(n=55)出现3例(6%),3+Q3M(n=51)出现2例(4%),差异无统计学意义(P=0.710)。随访期间均未见视网膜脱离、视网膜撕裂、眼压持续升高、眼内炎等严重眼部并发症,亦未见全身不良反应。
3 讨论
湿性AMD因严重影响老年人的生活质量已经成为严重的社会公共卫生问题,目前抗VEGF 药物玻璃体腔注射是其首选的治疗方法[16]。然而,大部分老年患者随访及治疗的依从性较差,而且频繁的复查、检查及治疗也给他们带来一定的经济负担。除此之外,药物的玻璃体腔多次重复注射有导致眼内炎和其他不良反应发生的风险,抗VEGF药物的注射次数与黄斑区地图样萎缩的发生率也有关[17,18]。因此既能减少抗VEGF药物注射频率,又能保证治疗效果的注射方案是目前抗VEGF治疗研究的热点。

表1.2组患者基线特征比较Table 1.Comparison of demography between two groups
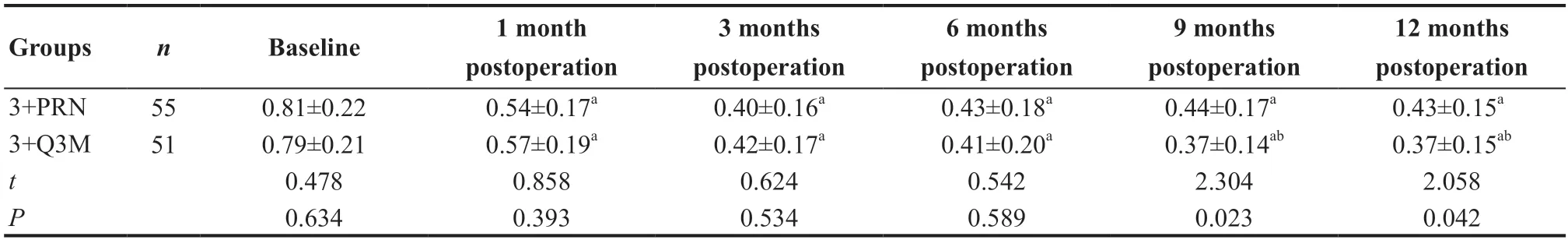
表2.2组手术前后不同时间点最佳矫正视力比较(LogMAR)Table 2.Comparison of BCVA in various time points between two groups (LogMAR)
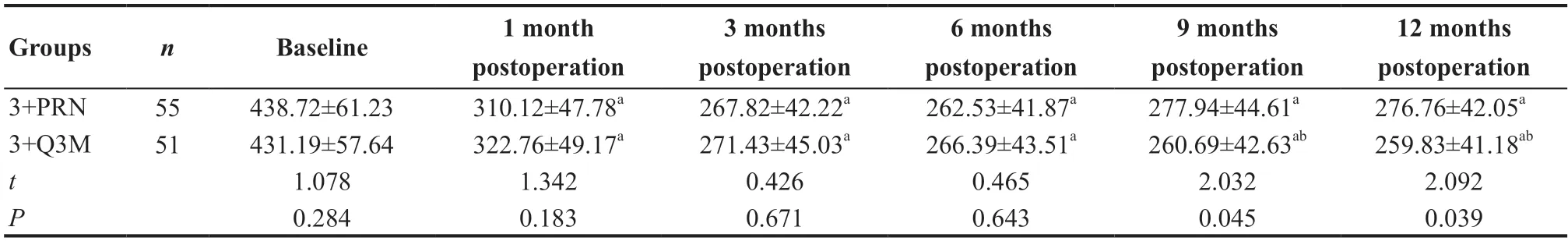
表3.2组手术前后不同时间点中央视网膜厚度比较(μm)Table 3.Comparison of CRT in various timepoints between twogroups (μm)

表4.2组不同脉络膜新生血管渗漏面积变化眼数[n(%)]Table 4.Eye number of CNV leakage area in different groups [n(%)]
各种抗VEGF药物对于治疗湿性AMD注射方案的探讨从未停止过。MARINA和VIEW1/VIEW2研究已证实了雷珠单抗每个月注射和阿柏西普起始每个月注射连续3针后间隔每2个月注射(3+Q2M)方案对湿性AMD 治疗的有效性和安全性[6,19]。为解决频繁注药的问题,PrONTO(Prospective Optical Coherence Tomography Imaging of Patients with Neovascular AMD Treated with intra-Ocular Ranibizumab)探讨了OCT引导下雷珠单抗3+PRN治疗湿性AMD的疗效,根据患者随访时OCT检查结果,如出现视力下降≥ETDRS 5 个字母,同时显示黄斑积液或中央视网膜厚度增加≥100 μm,新的黄斑区出血及新的CNV病灶等,则需要再次注射治疗,这种注射方案可以在一定程度上减少注射次数。研究中发现治疗12 个月时平均注射次数为5.6 次,视力增加了9.3 个字母数[14,20];TREND(TReat and extEND)研究证实T&E方案与每个月给药方案的临床疗效类似[21]。目前对于延长期如何给药问题仍然存在争议。
针对康柏西普的AURORA临床试验对3+PRN方案和每个月注射方案进行比较,结果显示治疗后12个月术眼视力分别提高了9.31和14.30个字母数,提示延长治疗期的不同给药方案疗效稳定[22]。3+Q3M注射方案是国际上针对康柏西普玻璃体腔注射治疗湿性AMD的Ⅲ期临床试验,即PHOENIX研究,每月注射连续3 针后将给药间隔延长至3 个月,旨在探讨延长药物玻璃体腔注射间隔时间对疗效和安全性的影响。目前这种新的3+Q3M注射方案的疗效和安全性尚未与以往经典的治疗方案进行对比,本研究将3+PRN与3+Q3M 2种注射方案的疗效和安全性进行比较,发现延长治疗间隔时间能够达到或优于传统方案的效果,为临床上抗VEGF药物玻璃体腔注射治疗湿性AMD的疗法选择提供参考依据。本研究发现,治疗12个月时,3+PRN组和3+Q3M组患眼BCVA均明显改善,CRT值均下降,治疗后9、12 个月3+Q3M组患眼平均BCVA优于3+PRN组,CRT值下降较3+PRN组更为明显,末次随访时3+Q3M组CNV渗漏的改善情况明显好于3+PRN组,表明康柏西普玻璃体腔注射治疗湿性AMD的3+PRN和3+Q3M方案均安全有效,但3+Q3M在视力改善和降低黄斑区CRT厚度方面疗效更为显著。
目前有关雷珠单抗3+PRN和3+Q3M注射方案的对比研究甚少。雷珠单抗PIER和EXCITE研究中对比3+Q3M和Q1M给药方案,虽然证实了3+Q3M方案能有效提高患者BCVA,但接受Q1M给药方案的患者能获得更好的视觉效果,而且每3个月给药间隔中黄斑厚度有平均恶化的趋势,随时间变化可观察到“锯齿”样模式[23]。雷珠单抗采用3+Q3M注射方案并不具备优越性,可能与单抗类抗VEGF药物学特性有关。以康柏西普为代表的融合蛋白类抗VEGF药物与雷珠单抗相比,结合靶点更多,且亲和力更高;雷珠单抗显著抑制湿性AMD患者眼内VEGF-A的平均时间为(36.4±6.7)d,而康柏西普显著抑制VEGF-A的平均持续时间为(73.5±18.0)d[24,25],所以康柏西普采用3+3QM注射方案能有效提高视力和降低黄斑区CRT厚度。
湿性AMD的疗效与抗VEGF药物治疗的次数有明确关系,在一定的限度内,随治疗次数的增加,视力提高明显[26],但是临床工作中,每次玻璃体腔注射都有导致眼内炎和其他不良反应发生的风险,药物玻璃体腔注射的感染性眼内炎的发生率为0.02%~0.09%,而降低给药频次可相应降低眼内感染的风险[27,28]。PRN和Q1M方案行玻璃体腔内注射康柏西普治疗湿性AMD的研究表明,治疗12 个月2 种治疗方案疗效接近,而3 +PRN组平均注射次数明显少于3+Q1M。本研究中3+PRN组平均注射次数明显少于3+Q3M组。由于本研究观察期较短,治疗12个月时3+PRN组仍有10.9%的患者黄斑区CNV渗漏面积扩大,仍需继续治疗,推测随着观察期的延长,可能3+Q3M的注射次数会少于3+PRN,但需要更长期的研究进一步证实。
康柏西普具有良好的组织容受性,本研究中患者治疗过程中最常见的眼部不良反应是注射部位球结膜下出血和暂时性的眼压升高,但未发现严重的全身不良反应。康柏西普的相对分子质量大(143 000 Da),穿过血-眼屏障的能力受到限制,而相关研究表明,与全身用药相比其全身不良反应发生率较低和作用时间延长[29]。本研究发现无论是3+Q3M方案还是3+PRN方案,随访期间均未见局部及全身不良反应,但本研究样本量较小,观察时间也不足够长,今后仍须进一步观察用药安全。
本研究结果表明,采用3+Q3M方案进行康柏西普的玻璃体腔注射治疗湿性AMD既延长了给药间隔时间,也可明显改善术眼视力,降低黄斑区CRT值,减少CNV渗漏面积,为临床上解决降低注射频次的难题提供了切实可行的方法,为湿性AMD的规范化治疗提供了新的思路。
利益冲突申明本研究无任何利益冲突
作者贡献声明张鹏、高蕾:收集数据;参与选题、设计及资料的分析和解释;撰写论文;对编辑部的修改意见进行修改。王淑静、李一啸:参与选题、设计和修改论文的结果、结论。王红:参与选题、设计、资料的分析和解释;修改论文中关键性结果、结论;对编辑部的修改意见进行核修

