光降解苯酚用rGO/Mo@TiO2纳米复合材料的制备及性能表征*
谢欣颖,李 娟
(重庆大学 环境与生态学院,重庆 400030)
0 引 言
TiO2材料由于其无毒、高化学稳定性、低成本等优点,已被许多研究人员广泛应用于光催化应用中[1-3]。然而,TiO2是一种宽禁带材料,只吸收太阳光谱的紫外光,而且TiO2中光生电子与空穴的瞬时复合会影响其催化活性,这是TiO2材料作为光催化剂的两个主要缺点[4-6]。因此,许多研究都集中在带隙研究上,以扩展TiO2材料对可见光区域的吸收[7-8]。然而,光催化剂材料不仅需要在可见光下产生电子-空穴对,而且同时光生电子在与价带中的空穴复合之前应到达表面活性中心。因此,科研人员提出了多个研究方向,如掺杂金属/非金属、负载贵金属纳米粒子(NPs)、与染料分子敏化以及与其它半导体材料结合等[9-12]。目前,由于TiO2具有较高的催化活性和表面酸性,Al、Mo掺杂的TiO2越来越引起大家的兴趣[13-14]。比如,用类似钼(Mo6+)的高价阳离子来修饰TiO2的电子结构,它可以作为电子陷阱,并有助于增加激发态电荷载流子的寿命[15]。
Guo等[16]研究发现,Mo和Fe共掺杂只能改善和延缓本体TiO2的复合过程,而TiO2表面存在作为复合中心的缺陷。因此,为了提高光催化活性,还应考虑表面复合,以利用最大数量的分离形式的电荷载流子。徐剑峰[17]从拓宽光谱响应范围、有效抑制光生电子-空穴对复合以及解决催化剂固载化问题考虑,进行了碳材料/贵金属表面复合修饰改性TiO2基复合光催化剂的研究,结果证明了有机钛源制备得到的TiO2含有对光生电子的分离和迁移产生重要作用的无定形碳层复合结构,且发现随着贵金属的浓度增加,可见光催化活性出现了不同程度的下降。因此,活性炭、碳纳米管、富勒烯和石墨烯等碳基材料具有较高的电荷载流子迁移率和较大的比表面积,是最有前途的耦合材料[18]。研究表明,TiO2-CNT和TiO2-富勒烯复合材料有几个缺点[19-20],如到达催化剂表面的光强度降低,CNT与普通溶剂的润湿性较差,且不易分散等。而石墨烯及其衍生物石墨烯氧化物(GO)、还原石墨烯氧化物(rGO)作为优良的载体材料,则具有比表面积大、电荷载流子迁移率提高、导热系数高、化学稳定性好等优点[21]。与石墨烯相比,rGO是亲水性的,因为存在与碳支架结合的氧原子,使其很容易分散在水中[22]。rGO同时含有芳香族(sp2)和脂肪族(sp3)区域,能进一步扩大与表面可能发生的相互作用的类型。据报道,用rGO耦合TiO2材料,通过将电子从TiO2纳米粒子负载到rGO上,能抑制光生电子和空穴的复合,提高催化活性。最重要的是,在表面缺陷上,从TiO2到rGO发生的电子转移过程比电子-空穴复合更快[23]。
本文采用Mo掺杂修饰TiO2材料,提高其光催化活性,并将改性后的Mo@TiO2沉积在GO表面,在紫外线作用下使GO在TiO2上发生还原,制备了rGO/Mo@TiO2纳米复合材料。通过降解有机污染物对硝基苯酚(p-NP)评价了纳米复合材料的光催化效率。
1 实 验
1.1 TiO2和Mo@TiO2纳米粒子的制备
以钛(IV)正丁氧化物(Ti(OC4H9)4)和二水钼酸钠(Na2MoO4·2H2O)作为原材料,采用溶胶-凝胶法制备了TiO2和Mo@TiO2纳米粒子。
TiO2纳米粒子的制备:首先,将Ti(OC4H9)4和乙醇混合,搅拌1 h,制备出前驱体溶液;其次,将H2O、乙醇和硝酸(催化剂)混合加入三口烧瓶中,搅拌1 h,均匀混合后逐渐加入到前驱体溶液中;然后,将所得溶液进一步搅拌2 h,得到均匀溶液,Ti(OC4H9)4/H2O/乙醇/硝酸的摩尔比保持在1/30/20/0.1;接着,将上述所得溶液在室温下陈化24 h,用水和乙醇混合溶液,多次洗涤最终产物,并在120 ℃下干燥3 h;最后,将所得粉末在空气中于400 ℃下煅烧2 h,即得TiO2纳米粒子。
Mo@TiO2纳米粒子的制备:首先,同样将Ti(OC4H9)4和乙醇混合,搅拌1 h,制备得到前驱体溶液;其次,将钼酸钠、H2O、乙醇和硝酸(催化剂)组成的溶液搅拌1 h,均匀混合后逐渐加入到前驱体溶液中;然后,所得溶液进一步搅拌2 h,得到均匀溶液;接着,将上述所得溶液在室温下陈化24 h,用水和乙醇混合溶液,多次洗涤最终产物,并在120 ℃下干燥3 h;最后,将所得粉末在空气中于400 ℃下煅烧2 h,即得Mo@TiO2纳米粒子。
1.2 GO、rGO/TiO2和rGO/Mo@TiO2复合材料的制备
用改进的Hummer’s法合成了氧化石墨烯GO。制备方法如下:首先,选择典型的合成方法,使用硫酸剥离商业石墨粉,并用KMnO4和NaNO3等强氧化剂氧化得到氧化石墨;其次,用H2O2终止反应,将得到的氧化石墨悬浮液用HCl和蒸馏水过滤和洗涤5次;然后,用乙醇洗涤,将所得产物在真空中干燥24 h;最后,将石墨氧化物分散在蒸馏水中,超声作用1 h,转化得到GO。
rGO/TiO2纳米复合材料的制备:首先,将GO和TiO2水溶液分开超声处理1 h;其次,将GO的悬浮液加入到TiO2悬浮液中再搅拌1 h,均匀混合;然后,将所得溶液在紫外光照射下持续搅拌24 h;最后,在紫外光照射下,TiO2的导带和价带分别产生电子-空穴对,这些空穴对能够还原GO片表面的羟基、环氧基和羧基官能团,将GO转换为rGO,制备得到rGO/TiO2纳米复合材料。同样按照上述方法制备了rGO/Mo@TiO2纳米复合材料。制备过程中,m(TiO2)∶m(GO)=1∶2,因为在合成纳米复合材料时,TiO2的数量不足,有可能不足以将所有GO转化为rGO。Mo@TiO2材料中Mo的掺杂量为1%(原子分数)。
1.3 样品的表征与测试
采用X射线衍射仪(Rigaku 日本理学)对所有样品进行晶格结构表征;用紫外-可见-近红外分光度计(Cary),在200~800 nm范围内的漫反射模式下测定所有光催化剂的光学带隙;采用扫描电子显微镜(S4800,日立)测定样品的表面形貌;采用多功能型扫描XPS微探针(PHI5000日本Ulvac-Phi)测定样品的X射线光电子能谱,研究样品中原子的化学状态;在室温下,采用FT-IR光谱仪(Nicolet iS5 赛默飞)在4 000~400 cm-1的光谱范围内,进行FT-IR测试;利用紫外-可见分光光度计(日产公司)测定样品的紫外-可见光(UV-Vis)吸收光谱,测试所用的标样为硫酸钡。
1.4 光催化活性测量
在150 W氙灯下,通过光降解对硝基苯酚(p-NP)来评价所有样品的光催化活性。将10 mg光催化剂分散在50 mL的p-NP溶液中(1×10-5)。在光照射前,将溶液在黑暗中搅拌30 min,使催化剂达到p-NP的吸附解吸平衡。光源与反应器的距离保持在47 cm不变。在固定的时间间隔后,过滤,然后用紫外-可见分光光度计测量p-NP的吸光度。为了评价光催化活性,测量了p-NP在320 nm处吸收带的归一化强度,并将其绘制为辐照时间的函数。所有的光催化实验都是在室温25 ℃下进行的。
2 结果与讨论
2.1 样品的XRD和光吸收特性分析
图1为TiO2、Mo@TiO2、rGO/TiO2和rGO/Mo@TiO2样品的XRD图谱。从图1可以看出,所有样品中均能观察到锐钛矿型TiO2的特征峰,分别出现在25.3,37.7,48.1,53.8和55.1°,对应(101)、(004)、(200)、(105)和(211)晶面。rGO/TiO2和rGO/Mo@TiO2样品在紫外线照射下还原后,在11°处GO主峰强度变得非常弱,这说明在材料合成过程中,大量的GO(约95%以上)被还原为rGO,而由于锐钛矿TiO2的峰强大,导致在相同的衍射角度处没有观察到rGO的峰。

图1 TiO2、Mo@TiO2、rGO/TiO2和rGO/Mo@TiO2样品的XRD图谱
图2为TiO2、Mo@TiO2、rGO/TiO2和rGO/Mo@TiO2样品的UV-Vis吸收光谱。由图2可知,TiO2样品的吸收谱带出现在400 nm处,其在紫外光区域内有较大吸收量,在可见光区域内吸收量较少;而Mo@ TiO2、rGO/TiO2和rGO/Mo@TiO2样品的吸收谱带向可见光区域内明显移动。因此,纳米复合材料能够提高可见光利用率,其中rGO/TiO2和rGO/Mo@TiO2对可见光的吸收强度更大,可见rGO的引入,增强了TiO2对可见光的吸收。
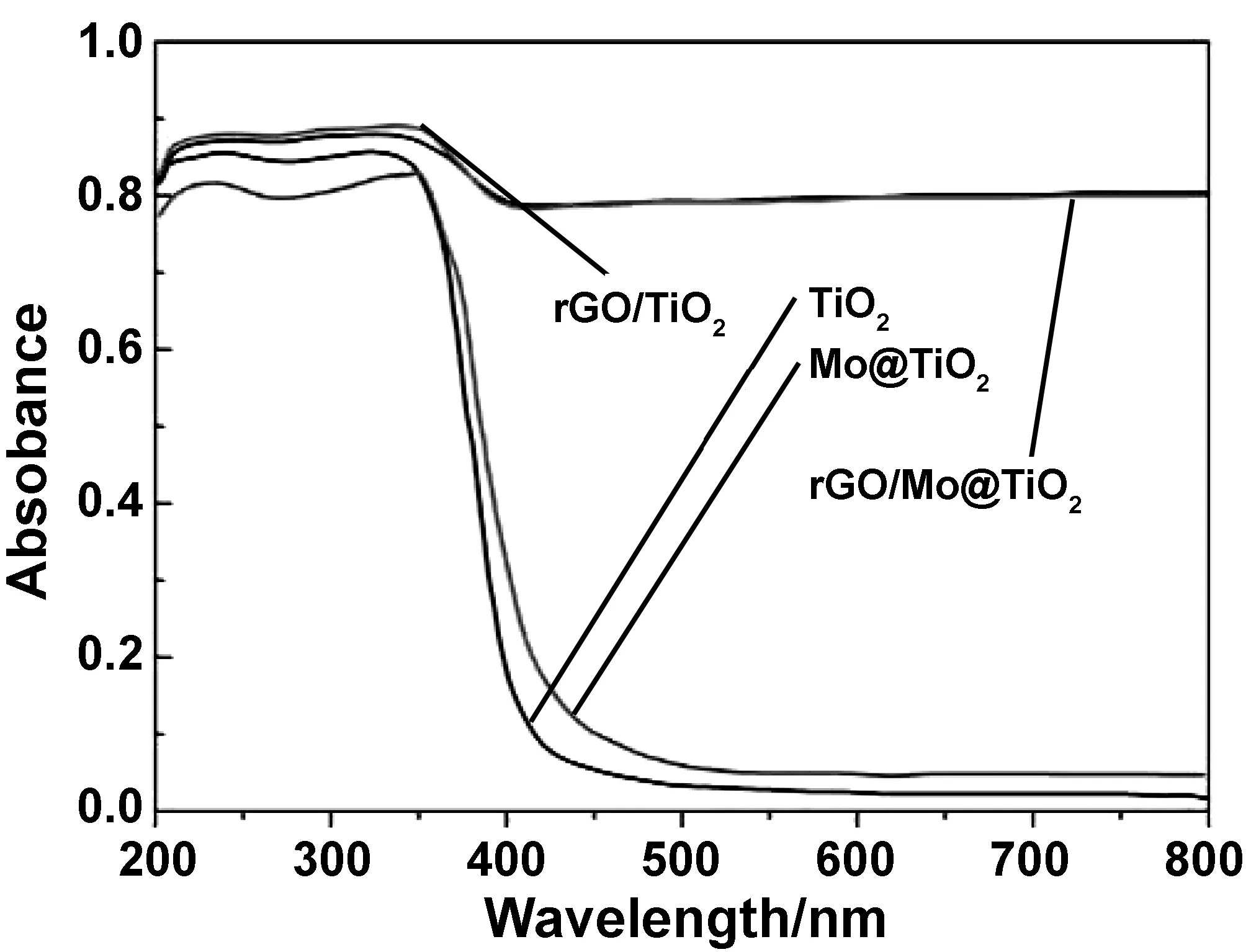
图2 TiO2、Mo@TiO2、rGO/TiO2和rGO/Mo@TiO2样品的UV-Vis吸收光谱
2.2 样品的XPS分析
图3(a)为TiO2、Mo@TiO2、rGO/TiO2、rGO/Mo@TiO2样品的Ti2p的XPS光谱曲线。从图3(a)可以看出,在Ti2p光谱曲线中,对于纯TiO2和Mo@TiO2样品,在458.8和464.5 eV处有两个明显的特征峰,分别归属于Ti4+的Ti2p3/2和Ti2p1/2。然而,引入rGO后,rGO/TiO2和rGO/Mo@TiO2样品在Ti2p3/2状态的结合峰正向移动0.9 eV至459.7 eV处。这种向更高的结合能的转变表明,通过形成结合键,大量电子从TiO2转移,使它们之间产生强烈的相互作用,而由于rGO遮挡住TiO2颗粒,样品的Ti2p光谱强度降低。
图3(b)为Mo@TiO2、rGO/Mo@TiO2样品的Mo3d的XPS光谱曲线。由图3(b)可知,在Mo3d光谱曲线中,Mo@TiO2样品中的Mo是以Mo6+形式存在的,峰值出现在231.5和234.2 eV处,分别对应Mo3d5/2和Mo3d3/2;rGO/Mo@TiO2样品中由于大量的电子从TiO2往rGO转移,导致TiO2表面化学环境发生变化,从而Mo的两个峰向较高的结合能232.1和235.9 eV处偏移。
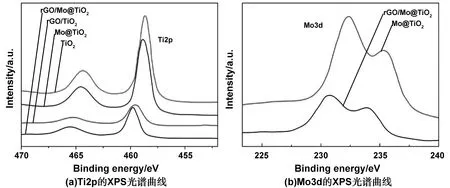
图3 TiO2、Mo@TiO2、rGO/TiO2、rGO/Mo@TiO2样品的Ti2p的XPS光谱曲线和Mo@TiO2、rGO/Mo@TiO2样品的Mo3d的XPS光谱曲线
2.3 样品的拉曼光谱、FT-IR和SEM分析
图4为TiO2、Mo@TiO2、rGO/TiO2和rGO/Mo@TiO2样品的拉曼光谱。由图4可知,纯TiO2颗粒在145,396,515和640 cm-1波段处出现振动峰,分别对应锐钛矿型TiO2的Eg,B1g,A1g和B2g振动模式。然而,Mo元素的掺杂、rGO的引入使振动峰向左偏移了5~10 cm-1,红移主要是由于晶体尺寸的变化引起的声子限制效应造成的。在rGO/TiO2样品中,由于TiO2和rGO之间存在强的相互作用,从而产生表面应变,影响TiO2的晶体尺寸,导致红移。这与XPS结果一致,表明TiO2和rGO之间存在牢固的结合作用。

图4 TiO2、Mo@TiO2、rGO/TiO2和rGO/Mo@TiO2样品的拉曼光谱
图5为GO和rGO/Mo@TiO2样品的FT-IR红外光谱。由图5可知,在3 000~3 500 cm-1处的宽峰对应于—OH和/或物理吸附H2O的伸缩振动。rGO/Mo@TiO2样品的该峰强度降低,表明含水量降低。在1 714,1 625,1 220和1 040 cm-1处的振动峰分别对应COOH基团的C—O伸缩、C—C、C—O—C和C—O伸缩振动。1 579 cm-1处的振动峰是由rGO的骨架振动引起的。对于rGO/Mo@TiO2样品,GO中的含氧官能团的振动峰要么完全消失,要么强度显著降低,表明GO大部分被还原成rGO。

图5 GO和rGO/Mo@TiO2样品的FT-IR光谱
图6为rGO/Mo@TiO2样品的SEM图。从图6可以看出,Mo@TiO2样品为纳米颗粒,均匀涂覆附着在rGO表面,并未出现Mo@TiO2颗粒团聚,只是Mo@TiO2样品的涂覆层存在龟裂现象;rGO仍保持原有的多层片状结构,即使在表面沉积Mo@TiO2颗粒后,其形貌也保持不变。在rGO表面和其它地方未观察到松散的Mo@TiO2颗粒,证实了rGO和TiO2之间具有良好相互作用,形成了纳米复合材料,与XPS、拉曼光谱和FT-IR结果一致。

图6 rGO/Mo@TiO2样品的SEM图
2.4 光催化性能
图7为TiO2、Mo@TiO2、rGO/TiO2和rGO/Mo@TiO2样品光催化降解p-NP的性能。从图7可以看出,rGO/Mo@TiO2样品的光催化活性最高,3 h对p-NP的光催化降解率为84%,而TiO2、rGO/TiO2和Mo@TiO23 h对p-NP的光催化降解率分别为26%、42%和61%。rGO/Mo@TiO2样品比TiO2、rGO/TiO2和Mo@TiO2样品具有更高的光催化活性,主要是由于激发电子从TiO2到rGO的快速转移所致,此外在复合材料中引入Mo能够作为电子的俘获位点来延迟带隙复合。因此,在rGO/Mo@TiO2中实现了这两个特性,创造了一种协同效应,有效地分离电荷,有利于电荷传输到表面,从而提高了材料的光催化活性。
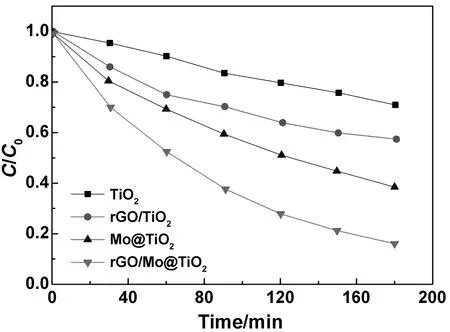
图7 TiO2、Mo@TiO2、rGO/TiO2和rGO/Mo@TiO2样品光催化降解p-NP的性能
3 结 论
利用溶胶-凝胶法,制备了TiO2和Mo@TiO2纳米粒子,采用液相沉积法,将TiO2和Mo@ TiO2纳米粒子沉积到GO上面,制备了rGO/TiO2和rGO/Mo@ TiO2复合材料,分析了TiO2、Mo@TiO2、rGO/TiO2和rGO/Mo@TiO2样品的XRD、XPS、拉曼光谱、FT-IR、SEM、光吸收特性和光催化性能等,得出以下结论:
(1)制备的所有样品中的TiO2均为锐钛矿型,颗粒尺寸为纳米级,GO大部分被还原成了rGO,且TiO2纳米颗均匀粒沉积在rGO表面,形成了纳米复合材料。
(2)Mo和rGO的引入,一方面,使Mo@ TiO2、rGO/TiO2和rGO/Mo@TiO2样品的吸收谱带向可见光区域内明显移动,增强了TiO2对可见光的吸收,提高了纳米复合材料的可见光利用率;另一方面,使TiO2表面化学环境发生变化,样品的特征峰在Ti2p和Mo3d的XPS光谱向较高的结合能处偏移。
(3)拉曼光谱分析表明,TiO2和rGO之间存在牢固的结合作用,从而产生表面应变,影响TiO2的晶体尺寸,导致红移;FT-IR分析表明,rGO/Mo@TiO2样品中GO大部分被还原成了rGO;SEM分析可知,rGO和TiO2之间具有良好相互作用,形成了纳米复合材料。
(4)rGO/Mo@TiO2样品的光催化活性最高,3 h对p-NP的降解率为84%,而TiO2、rGO/TiO2和Mo@TiO23 h对p-NP的降解率分别为26%,42%和61%。

