基于Cu-BTC骨架的Cu2O-CuO复合材料的制备及吸其附性能
唐安宇, 何曼丽, 陈九玉, 周鑫浩, 王丙佳, 王俊议, 杨 毅
(1. 南京理工大学 环境与生物工程学院; 江苏省化工污染控制与资源化重点实验室, 江苏 南京 210094;2. 陆军工程大学 基础部, 江苏 南京 210001)
传统化石燃料引发了越来越多的环境问题,我国将发展核电作为清洁能源的主要补充。根据世界核协会公布的数据,目前中国有22个核电单位(19 GWe)在运营, 还有26台(28 GWe)正在建设中[1-2]。然而,核电能源的高速发展导致了大量潜在的放射性碘污染,放射性碘污染会持续而且稳定地放射毒性,直至其放射性核素完全衰变[3-4]。此外,由于放射性污染在表现形式上,不同于传统的物理化学性质的污染,这种污染无法被感知,潜在性危害极其严重[5],因此,针对有效去除放射性碘污染的研究具有重要的意义。目前,国内外用于去除废水中的放射性碘离子的方法有生物修复法[6]、 反渗透法[7]、 离子交换法[8]、 吸附法等[9]。其中,吸附法因高效、 操作简单、 价格低廉等优点,成为最受关注的放射性碘污染的去除方法,而选择高效、 高选择性、 成本低的吸附剂成为了吸附应用的关键点[10-11]。
铜基材料作为放射性污染物的吸附剂,通常掺杂贵金属改性[12-13]。铜基均苯三甲酸(Cu-BTC)是一种典型的金属有机骨架(MOFs)材料,呈规整的八面体晶状结构,具有良好的吸附特性以及较大的比表面积和高热稳定性[14]。Cu-BTC对污染物的吸附-解析过程可逆,热重分析结果显示其在270 ℃时,仍能保持框架结构稳定[15],本身的中空结构赋予其良好的吸附特性;但由于Cu-BTC具有水解性和亲水性等特点,因此无法被直接用于水体中放射性碘的吸附[16]。
双组分过渡金属氧化物(如CuO-Cu2O)通常可以结合其双组分的优异特点[17], 在实际应用中表现出强大的协同作用以及吸附性能提升[18]。 铜作为过渡金属, 具有廉价的成本、 较好的机械强度和良好的物理化学性能等优点; 然而,由于表面氧化作用, 铜基吸附剂表面易氧化形成CuO致密薄膜[19], 因此无法形成有效的化学吸附。 鉴于此, 本研究使用改变调节剂月桂酸的比例, 首先合成立方体和十二面体2种形貌的Cu-BTC,然后以此为基础, 通过煅烧保留其碳结构骨架, 获得双组分Cu2O-CuO氧化物(分别简写为C-Cu2O-CuO和D-Cu2O-CuO)。 得到的复合材料表面形成疏松多孔结构, 并具有丰富的吸附活性位点, 研究3种材料Cu-BTC、 C-Cu2O-CuO、 D-Cu2O-CuO对碘离子的吸附性能, 并探究其吸附机理。
1 实验
1.1 实验试剂与仪器
试剂: 三水硝酸铜(Cu(NO3)2·3H2O,分析纯,上海百灵威化学技术有限公司);月桂酸(C12H24O2,分析纯,阿拉丁试剂有限公司);碘化钠(NaI,分析纯,阿拉丁试剂有限公司);1,3,5-苯三甲酸(C9H6O6,分析纯, 上海迈瑞尔化学技术有限公司);正丁醇(C4H10O,分析纯,阿拉丁试剂有限公司)。
仪器: 紫外分光光度计(UV-1600型); X射线衍射仪(Bruker-AXS D8 Advance型); 日本电子JSM-IT500HR扫描电镜; 热失重分析仪(TGA, SDTA851E型)。
1.2 制备方法
1.2.1 立方体Cu-BTC的制备
称取164 mg硝酸铜Cu(NO3)2·3H2O, 溶于40 mL正丁醇, 超声搅拌获得透明溶液后, 称取80 mg 1,3,5-苯三甲酸与14 g月桂酸加入所得溶液,获得深蓝色澄清透明溶液。倒入100 mL聚高压反应釜四氟乙烯内衬中,升温至140 ℃并维持温度反应3 h后,于空气中冷却;将所得溶液离心获得蓝色固体,真空干燥备用。
1.2.2 十二面体Cu-BTC的制备
称取164 mg硝酸铜Cu(NO3)2·3H2O,80 mg 1,3,5-苯三甲酸与7.608 g月桂酸,溶于40 mL正丁醇,室温下搅拌获得透明溶液后倒入100 mL聚高压反应釜四氟乙烯内衬中,升温至140 ℃并维持温度反应3 h后,于空气中冷却;将所得溶液离心获得蓝色固体,真空干燥备用。
1.2.3 立方体Cu2O-CuO的制备
取真空保存下立方体Cu-BTC样品250 mg, 均匀铺开于坩埚底部, 置于管式炉中, 氮气气氛中以1 ℃/min的速率升温至330 ℃,并煅烧40 min,随后于氮气氛中冷却至室温,获得黑色粉末状样品。
1.2.4 十二面体Cu2O-CuO的制备
取真空保存下十二面体Cu-BTC样品250 mg,均匀铺开于坩埚底部,置于管式炉中,氮气气氛中以1 ℃/min的速率升温至370 ℃,并煅烧60 min,随后于氮气氛中冷却至室温,获得深蓝黑色粉末状样品。材料制备过程中的合成示意图如图1所示。
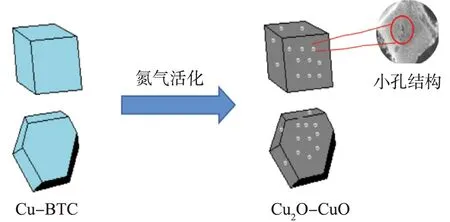
图1 Cu-BTC煅烧合成Cu2O-CuO的示意图Fig.1 Schematic diagram of synthesis of Cu2O-CuO produced by Cu-BTC calcining
1.3 样品的表征
将样品置于喷金仪(Q150T)进行喷金预处理,采用日本电子JSM-IT500HR扫描电镜对样品的形貌以及颗粒性进行表征;利用Bruker-AXS D8 Advance型X射线衍射仪(XRD, 德国 Bruker公司)对样品的物相组成进行测试,扫描角度2θ范围为10 °~70 °;通过热失重分析仪(TGA, SDTA851E型),以1 ℃/min的速率升温到1 000 ℃, 检测样品的质量随温度的变化情况。
1.4 吸附实验
利用紫外分光光度法,测定待测溶液在227 nm处的吸光度,并根据标准曲线求得溶液中碘离子的质量浓度。在溶液pH=7条件下,设置吸附剂质量浓度为1 g/L,吸附时间为6 h,在碘离子质量浓度为30~250 mg/L内,对2种材料进行不同温度吸附实验,吸附剂对碘离子的平衡吸附量为
qe=(ρ0-ρe)V/m,
(1)
式中:ρ0为碘离子的初始浓度, mg/L;ρe为碘离子的平衡浓度, mg/L;V为溶液体积, L;m为吸附剂质量, g。
吸附动力学实验:设置反应温度为298 K、溶液pH=7的条件下,碘离子质量浓度为120 mg/L的溶液,取200 mL溶液加入0.2 g吸附剂,间隔相应时间取样,并进行吸光度(227 nm)检测,计算碘离子吸附容量。
2 样品的结构表征
2.1 材料的微观形貌分析
立方体和十二面体2种形貌的Cu-BTC,以及煅烧后Cu2O-CuO的扫描电镜(SEM)图像如图2所示。从图2 a)、 2 b)中可以看出,合成的2种前驱体样品均具有完整的晶型结构,分别呈立方体和十二面体,大小分布均匀。其中,立方体样品粒径约为600~1 000 nm,十二面体样品粒径约为1~1.5 μm。煅烧后的Cu2O-CuO样品如图2 c)、 2 d)所示。由图可见:煅烧后2种形貌的样品表面均产生坍缩,出现褶皱,但两者均保留有较完整的Cu-BTC结构骨架。此外,2种材料表面出现小孔(图2c)中立方面体样品更清晰),表明成功合成了保留良好Cu-BTC骨架的Cu2O-CuO材料。
2.2 X射线衍射分析
为掌握材料煅烧前后的晶体结构变化,对煅烧前后材料进行XRD测试,材料的衍射谱图如图3所示。由图3 a)可知,Cu-BTC的XRD图谱在6.7 °、 9.5 °、 11.6 °、 13.4 °处具有4个特征峰,其分别对应为材料的(200)、 (220)、 (222)、 (400)晶面,与相关文献报道的一致[20]。2种材料的主要特征峰并无明显差异,这说明成功合成了Cu-BTC样品,且2种样品形貌晶体结构相似。
由图3 b)可见,2种材料在35.5 °、 38.7 °、 48.6 °均有明显的特征峰,其分别对应CuO的(002)、 (111)、 (-202)晶面。同时,在36.4 °、 42.1 °和57.8 °处观测到Cu2O特征峰,该峰对应Cu2O的(111)、 (200)、 (220)晶面[21]。表明本研究制得的Cu2O-CuO样品完整保留了Cu-BTC骨架,并产生中空孔道,且包含Cu2O的预期材料。
在图3 b)中, 吸附碘离子后的材料(I-C-Cu2O-CuO和I-D-Cu2O-CuO)的XRD图谱中,位于25.5 °、 43.2 °、 50.6 °均出现了CuI的特征峰,且Cu2O特征峰有所降低。表明一方面材料的骨架结构能够捕获碘离子,另一方面材料能够通过离子交换作用吸附碘离子。2种机制的协同作用使得材料对碘离子拥有良好的吸附效果。

a)C-Cu-BTCb)D-Cu-BTCc)C-Cu2O/CuOd)D-Cu2O/CuO图2 Cu-BTC及其煅烧后的Cu2O/CuO样品扫描电镜图像Fig.2 SEMimageofCu-BTCanditscalcinedCu2O-CuOsample

a)煅烧前b)煅烧后图3 Cu-BTC煅烧前后的XRD图谱Fig.3 XRDpatternsofCu-BTCbeforeandaftercalcined
由图2所示SEM表征图与XRD图谱结果推测,Cu-BTC经煅烧后,其苯环包围的小孔结构被破坏,从而失去亲水性,赋予其在水相中吸附碘离子的能力。煅烧后所得Cu2O-CuO,产生了可供碘离子吸附的开放位点,有利于提升对碘离子的去除效率。而对于典型的D-Cu2O-CuO组,高温煅烧在保留部分Cu-BTC结构的同时,去除了材料本身的结晶水,并产生内外连接的中空孔洞,使得碘离子能够通过孔洞进入吸附剂内,有利于提升吸附效率。

图4 Cu-BTC及其煅烧材料的FT-IR图谱Fig.4 FT-IR patterns of Cu-BTC and its calcined materials
2.3 红外光谱测定分析
为了确定煅烧前后样品的基团变化,分别对立方体和十二面体2种形貌的Cu-BTC和Cu2O-CuO材料进行红外测试,Cu-BTC样品及其煅烧材料的傅里叶红外光谱(FT-IR)谱图如图4所示。由图可以看出,属于Cu-BTC的典型特征峰处于1 646、 1 448、 1 374、 761和730 cm-1处[22], 而煅烧后的Cu2O-CuO材料也可以观测到上述峰, 表明煅烧后的Cu2O-CuO材料仍保留有部分有机骨架, 这与图3所示的XRD测试结果相符。
此外,在立方体Cu-BTC(C-Cu-BTC)样品位于3 434 cm-1处,还观察到了宽吸收峰,这属于层间水分子的伸缩振动;但煅烧后的样品(C-Cu2O-CuO)在该处不再存在该宽吸收峰, 转而在3 370、 3 220 cm-1处形成了2个峰,表明煅烧使得材料孔道内物理吸附的水和洗涤样品时的乙醇基本脱除。

3 吸附性能测试
3.1 标准曲线绘制
本研究采用非放射性129I替代放射性同位素进行吸附实验,采用分光光度法检测溶液中碘离子浓度,并与标准曲线对比,从而计算得到材料的吸附容量。
标准曲线绘制:配置质量浓度分别为1、 2、 3、 4、 5、 6、 7、 8、 9、 10 mg/L的NaI溶液,对所得标准曲线进行紫外光度测试,吸光度设置为227 nm。以碘离子浓度为横坐标,吸光度为纵坐标,绘制得到标准曲线:y=13.32x-0.001 8,标准曲线的相关系数R2=0.999 87。
3.2 等温吸附实验
2种形貌Cu2O-CuO在不同温度下的吸附等温线如图5所示。由图可知,在相应温度梯度下,2种形貌Cu2O-CuO吸附剂吸附量均呈增加趋势,且最终在碘离子质量浓度超过120 mg/L时趋于饱和,饱和吸附容量分别达到49.84、 91.91 mg/g。而作为前驱体材料的Cu-BTC,本身对碘离子没有吸附能力,只是因为煅烧使其产生中空孔洞,使得材料能够提供更多的吸附活性位点,且煅烧产生亚铜离子与碘离子结合,进一步增大了材料的吸附能力。

a)C-Cu2O-CuOLangmuir拟合b)D-Cu2O-CuOLangmuir拟合c)C-Cu2O-CuOFreundlichc拟合d)D-Cu2O-CuOFreundlichc拟合图5 2种Cu2O-CuO的等温吸附线及其等温方程拟合结果Fig.5 AdsorptionisothermsandtheirfittingresultsoftwokindsofCu2O-CuO
为了进一步探究材料的吸附机理, 运用Langmuir与Freundlich模型对吸附数据进行进一步拟合。 由图5可以看出, 2种吸附剂对碘离子的吸附过程均更加符合Langmuir模型, 在各个温度下, 吸附碘离子的拟合相关系数均大于0.99, 明显优于采用Freundlich模型的拟合结果, 表明2种形貌的Cu2O-CuO对碘离子的吸附均为单层吸附。 在298 K条件下, 根据Langmuir模型计算, 2种吸附剂对碘离子的最大吸附容量分别达到49.85、 91.91 mg/g, 与实验结果较为吻合, 由此推测材料对碘离子吸附为单层吸附。

图6 2种形貌Cu2O-CuO材料吸附碘离子的动力学曲线Fig.6 Kinetic curve of I- adsorption of two morphologies Cu2O-CuO
3.3 动力学吸附实验
图6为2种形貌Cu2O-CuO材料的吸附动力学曲线图。 由图可以看出, 2种材料的动力学曲线变化趋势十分相似。 在反应温度为298 K, 溶液中碘离子初始质量浓度为100 mg/L时, 立方体和十二面体Cu2O-CuO对碘离子的吸附饱和容量分别为47.46、 70.19 mg/g, 且均在反应120 min左右达到吸附平衡。
利用Lagergren一阶与二阶动力学模型,对实验数据进行拟合,进一步分析材料的吸附过程。其中,一阶和二阶动力学模型分别适用于评估物理吸附[19]为主和化学吸附[20]为主的吸附过程。2种模型的方程分别为

(2)
式中:qt为t时刻吸附剂对碘离子的吸附量, mg·g-1;t为吸附时间, min;K1为一级动力学常数, min-1;K2为二级动力学常数, g·mg-1·min-1。2种形貌Cu2O-CuO吸附碘离子的吸附动力学拟合曲线如图7所示。

a)一阶动力学模型b)二阶动力学模型图7 2种形貌Cu2O-CuO材料对碘离子的吸附动力学拟合结果Fig.7 KineticfitresultsoftheadsorptionoftwomorphologiesmaterialsforI-adsorption
由拟合曲线和动力学模型拟合结果可以看出,2种材料对碘离子的吸附过程均更加符合2阶动力学模型,其相关系数在0.99以上,说明2种材料的吸附以化学吸附为主导。从一阶动力学拟合曲线看,相关系数大于0.93,说明2种材料的吸附也存在一定程度的物理吸附。此外,由图7还可以看出,在相同温度与相同吸附时间内,D-Cu2O-CuO对碘离子的吸附均优于C-Cu2O-CuO材料。在二阶动力学模型下,2种吸附剂对碘离子的理论饱和吸附容量均与实际吸附容量较接近。
3.4 干扰离子对Cu2O-CuO碘离子吸附性能的影响
动力学研究结果表明,Cu2O-CuO材料吸附过程以化学吸附为主,而化学吸附过程中,其他阴离子存在会竞争吸附剂上的吸附活性位点,影响吸附剂对碘离子的吸附性能,因此,为了探究吸附剂的抗干扰性能,研究了干扰离子对吸附剂吸附碘离子的性能影响。


图8 不同干扰离子存在下Cu2O-CuO对碘离子吸附效果图Fig.8 Diagram of the adsorption effect of Cu2O-CuO for iodine ions in the presence of different interfering ions

4 结论
本文中以具有稳定框架结构和大比表面积及孔隙率的Cu-BTC作为基体材料,通过煅烧制备了一系列具有获得2种形貌骨架的Cu2O-CuO MOFs材料,并研究各材料对溶液中I-的吸附性能,通过一系列表征方法确定了煅烧前后,以及吸附前后的材料的微观结构和形貌变化,实验得到的主要结论如下:
1)通过在氮气氛中升温煅烧前驱体材料,可以获得保留大部分Cu-BTC结构骨架的Cu2O-CuO复合材料,使2种材料在298 K时的饱和吸附容量分别达到49.84、 91.91mg/g。
2)Cu2O-CuO对碘离子的吸附更符合Langmuir吸附模型,主要为单分子层吸附,吸附过程为放热反应,故而温度升高会不利于吸附过程的进行。
3)Cu2O-CuO对碘离子的吸附更符合Lagergren准二级动力学,说明Cu2O-CuO对碘离子吸附以化学吸附为主。
4)阴离子的存在会竞争吸附剂上的吸附活性位点,影响吸附剂对碘离子的吸附性能,弱酸根离子会阻碍材料对碘离子的吸附,而强酸根离子则能一定程度上促进吸附,提升吸附剂的吸附性能。

