获得性免疫缺陷综合征患者颅内隐球菌感染的临床及影像表现
尹悦,李宏军
作者单位:首都医科大学附属北京佑安医院放射科,北京100069
隐球菌是一种酵母样真菌,主要存在于自然环境中,尤其是被鸟粪污染的土壤和腐烂的木材中[1]。当获得性免疫缺陷综合征(acquired immunedeficiency syndrome,AIDS)患者CD4 细胞<100 个/μL时,容易发生隐球菌感染[2],其中新型隐球菌是感染人体、引发AIDS 相关脑膜炎的主要病原菌[3]。隐球菌脑膜炎(cryptococcus meningitis,CM)是由新型隐球菌感染脑膜和(或)脑实质所致的颅内机会性感染。AIDS患者合并CM 的比率为7%~16%[4],死亡率可高达40%,在条件有限的地区死亡率甚至更高[5]。对AIDS 合并CM 的诊断尤为重要,因为多项研究显示对于此类患者,应先进行一段时间抗隐球菌治疗后再进行抗逆转录病毒治疗,否则会增加死亡率[6-7]。笔者通过回顾性分析20例AIDS合并CM患者的临床和影像资料,旨在提高对该病的认识和影像诊断水平。
1 材料与方法
1.1 研究对象
回顾性分析2015 年1 月1 日至2019 年12 月31 日于我院住院治疗且确诊为AIDS 合并CM 的患者20 例,本单位伦理委员会批准该研究免除受试者知情同意。AIDS 合并CM 的诊断标准如下:(1)确诊为HIV 的患者:所有患者经酶联免疫吸附实验初筛及蛋白印迹确诊为HIV感染;(2)确诊为CM患者:患者存在临床症状且均进行脑脊液墨汁染色涂片,新型隐球菌荚膜抗原测定与快速新型隐球菌抗原鉴定检查。
1.2 方法检查
所有患者均进行MR扫描。所有患者均采用德国Siemens 公司Magnetom Trio Tim MR 3.0 T 扫描仪进行颅脑扫描。平扫序列包括横轴面T1WI (TR 452 ms,TE 2.46 ms)、T2WI (TR 6000 ms,TE 93 ms)、液体反转恢复序列(T2-FLAIR,TR 9000 ms,TE 93 ms)、弥散加权成像(TR 4200 ms,TE 93 ms,b=0,b=1000),同时生成ADC图像。增强扫描采用T1WI (TR 471 ms,TE 2.46 ms)行横轴面、冠状面及矢状面扫描,层厚4 mm,层间距1 mm。对比剂为钆喷替酸葡甲胺(Gd-DT-PA),剂量为0.1 mmol/kg,注射速度2~3 mL/s,肘正中静脉注射。
1.3 统计学方法
应用SPSS 25.0统计软件,计量资料以服从正态分布者以均数表示(±s),不服从正态分布者以中位数(四分位数)表示,计数资料以百分率表示。
2 结果
2.1 患者一般资料
本研究共收集20 例AIDS 合并CM 的患者,18 例患者墨汁染色结果阳性;1 例患者墨汁染色阴性,快速新型隐球菌抗原测定为强阳性;1 例患者墨汁染色阴性,新型隐球菌荚膜抗原测定、快速新型隐球菌抗原测定阳性,存在临床症状,且未有其他感染。其中男性17例,女性3例。年龄25~63岁,平均年龄为40.4岁。基线CD4计数1~162个/μL,中位个数为26 个/μL (5.25,45)。脑脊液检查中,脑脊液葡萄糖含量(2.45±1.090) mmol/L,脑脊液氯含量(119.86±4.669) mmol/L。
2.2 临床表现
头痛是最常见的临床症状(80%)、其次是恶心呕吐(15%)。其他还包括无中枢神经系统症状、意识障碍、视物模糊、发热等(表1)。
2.3 影像表现
本组共纳入20 例患者,均行头部MRI 检查,其中18 例患者行增强扫描,19 例患者行DWI 扫描。20 例患者的影像表现如下:(1)病灶分布:16例患者存在多发病灶,4 例患者存在单发病灶。基底节区域受累最为常见,12 例患者存在基底节区域受累,其余部位包括丘脑、小脑齿状核、额叶、顶叶、枕叶和脑膜。(2)病灶形态:11 例以累及血管周围间隙为主,存在血管周围间隙显示或扩张或胶样假囊形成的表现,多为双侧受累;6 例患者以脑膜炎或(和)脑膜脑炎为主;1 例患者同时存在血管周围间隙扩张和脑膜受累的表现;1 例患者同时存在脑膜受累及粟粒样结节的表现,1例患者为其他表现。(3) MRI信号特点:在12例存在血管周围间隙受累的患者中,1 例患者未进行DWI 及增强扫描。所有患者MRI 上DWI 均未扩散受限,病灶于T1WI呈低信号,T2WI、FLAIR呈稍高或高信号,增强后,7 例患者的部分病灶存在小点状强化,其余4 例未强化(图1,2)。在粟粒样结节为主的病变中,患者为多发病灶,有呈簇状分布趋势,病灶于T1WI 呈稍低信号,T2WI、FLAIR 呈稍高信号,DWI 扩散未受限,病灶周围可见大片水肿,邻近脑膜有强化。1 例患者表现为T1WI、T2WI、FLAIR 上未见异常,增强后,右侧额叶见点状强化,周围无水肿(图3)。在7 例存在脑膜炎或(和)脑膜脑炎的患者中,1 例患者仅存在脑膜受累,其余患者同时存在脑膜及邻近脑实质受累。1例患者受累脑膜于T1WI、T2WI、FLAIR上未见明确显示,增强后显示细线样强化;其余6 例患者受累脑膜于T1WI、T2WI、FLAIR上显示明显增厚,于T1WI呈等、稍低信号,于T2WI、FLAIR呈等、稍高信号,增强后可见明显线样强化(图4)。2 例患者受累脑膜邻近脑组织出现明显水肿信号,其余5例未见水肿信号。

表1 患者临床表现Tab.1 The clinical feature of patients
3 讨论
隐球菌是一种条件性致病真菌,广泛存在于自然界中,目前已被鉴定出30多个种属,其中具有致病性的有新型隐球菌与格特隐球菌[8],主要致病菌为新型隐球菌[9]。新型隐球菌更容易感染免疫功能缺陷的患者[10],并且隐球菌对中枢神经系统具有高度侵袭性,容易引起中枢神经系统的感染,产生相应的影像学改变及一系列的临床症状。
3.1 隐球菌颅内感染的临床表现
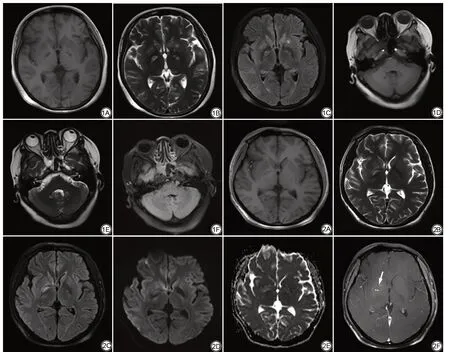
图1 女,38岁,头痛2个月余。双侧基底节、双侧小脑齿状核胶样假囊形成,于T1WI呈低信号,T2WI FLAIR呈高信号(A~F) 图2 男,25岁,间断抽搐15 d。右侧基底节可见血管周围间隙显示,于T1WI呈稍低信号,T2WI、FLAIR呈稍高信号,DWI ADC未见扩散受限(A~E),增强后可见点状强化(F,箭)Fig.1 A 38 year-old female with headache for more than 2 months. Pseudocyst were found in the bilateral basal ganglia and the bilateral dentate nucleus of cerebellum, presenting hypointense on T1WI and hyperintense on T2WI FLAIR (A—F). Fig.2 A 25 year-old male with intermittent convulsions for 15 days.Dilated perivascular spaces (PVS) were seen in the right basal ganglia, slightly hypointense on T1WI, slightly hyperintense on T2WI FLAIR, DWI ADC shows no restriction(A—E),after contract,dot enhancement were seen in the right basal ganglia(F,arrow).
本组研究显示AIDS 合并CM 的患者最主要的临床症状为头痛,其次为恶心呕吐、其余症状还包括意识障碍、视物模糊、发热。本研究结果与既往结果相似[4,11]。隐球菌颅内感染首发症状通常为头痛[12],可伴有发热、咳嗽等。若患者颅内压增高,则可能伴有呕吐、视物模糊、意识障碍等症状,严重者甚至出现视盘水肿,视力丧失、脑疝等症状。头痛虽然常见但不具有特异性,若艾滋病患者合并头痛,首先要考虑到颅内机会性感染的可能。此外本组患者CD4 计数中位数为26 个,提示本组患者免疫功能严重受损。当CD4 计数<200 个/μL时,容易并发机会性感染,而当<100 个/μL时,患者很容易存在隐球菌感染[2,13],本研究结果与既往研究结果比较一致。因此,对于此类CD4 计数低的艾滋病患者,若存在头痛、颅内压增高等临床症状时,需要考虑颅内隐球菌感染的可能并进一步检查。本研究显示脑脊液葡萄糖(2.45±1.090) mmol/L,在正常范围内,脑脊液氯含量(119.86±4.669) mmol/L,稍微低于正常水平,本结果与既往研究结果基本一致[4]。
3.2 隐球菌颅内感染MRI影像表现
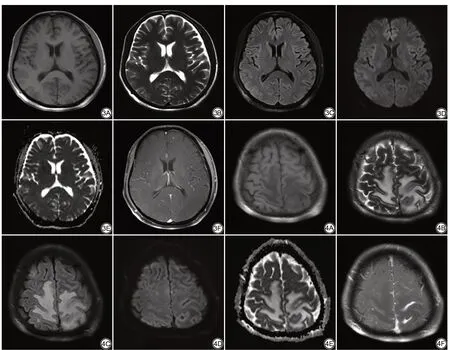
图3 男,34 岁,头痛伴有恶心呕吐2 周。T1WI、T2WI、FLAIR、DWI、ADC 上未见异常信号影(A~E),增强后左侧额叶可见点状强化(F) 图4 男,25 岁,头痛一周。左侧额顶部脑膜增厚,于T1WI、T2WI、FLAIR 上呈等信号(A~C),DWI、ADC 未见扩散受限(D、E),增强后脑膜明显强化(F)。双侧额顶叶见大片状水肿影Fig.3 A 34 year-old male,headache accompanied by nausea and vomiting for 2 weeks.There was no abnormal signal on T1WI,T2WI,FLAIR.DWI,ADC (A—E), after contract, punctiform enhancement in the left frontal lobe (F). Fig.4 A 25 year-old male, headache for 1 week. The meninges of the left frontal-parietal area are thickened, with isointense on T1WI, T2WI, FLAIR (A—C), DWI ADC shows no restriction (D, E), significantly enhanced after enhancement (F). Large edema were seen in bilateral frontal and parietal lobes.
AIDS合并CM的患者的影像表现具有多样性,现笔者将其进行如下分类:(1)血管周围间隙(perivascular spaces,PVS)显示或者扩张,胶样假囊形成。颅内隐球菌感染容易发生在基底节区域、小脑齿状核区域,常常引起血管周围间隙显示或者扩张、胶样假囊形成。基底节区域的穿支小动脉表面由两层脑膜构成,外层与皮层软脑膜相连,内层紧贴血管壁,两层脑膜构成基底节区域的PVS,此处PVS与基底池相通,从壳核底部开始扩张向上延伸[14-15]。通常情况下,血液中含有隐球菌的巨噬细胞进入毛细血管后小静脉,通过内皮细胞层及基膜进入PVS,此后巨噬细胞通过胞吐作用释放隐球菌,从而使隐球菌在PVS 聚集[16]。正常PVS 在MRI 上不显示,当大量隐球菌聚集在PVS 时,可以使PVS 扩张。血管周围间隙扩张也被认为是隐球菌颅内感染的早期特征性影像学表现[17]。扩张的PVS在T1WI上呈现低信号,T2WI和FLAIR上呈稍高、高信号,DWI 上扩散不受限,增强后一般不强化[18],但本组病例中部分病例存在强化,笔者认为其原因可能如下:毛细血管后静脉内局部干扰素和肿瘤坏死因子浓度较高,会引起内皮细胞的激活,从而利于巨噬细胞的粘附迁移,在此过程中,血管的完整性被破坏,在影像上表现为血管的强化[16]。在实际工作中,若AIDS 患者存在头痛等临床症状,并且MRI 上显示基底节区域存在PVS显示或者扩张,要考虑到隐球菌感染的可能,增强扫描可能有助于进一步诊断,此外还需进行实验室检查来确诊该疾病。隐球菌囊体可以产生黏液,分泌胶冻样物质,这些物质聚集在PVS使其空间明显增大,形成胶样假囊。在MRI上,胶样假囊呈现典型的“皂泡状”改变,T1WI 上呈现低信号,T2WI 和FLAIR 上呈稍高、高信号,DWI 上部分病灶会表现为扩散受限,这可能与隐球菌荚膜分泌黏稠胶样物质有关[19],而在本组中未见有扩散受限的病例。(2)脑膜炎和脑膜脑炎。隐球菌可以经过PVS 累及软脑膜,形成脑膜炎。受累脑膜在MRI 上表现为局部明显或不明显增厚,于T1WI、T2WI、FLAIR 上呈等信号,增强后受累软脑膜线样明显强化。邻近脑组织可伴或者不伴有水肿。水肿可能与水蛋白通道(aquaporins,AQP4)的表达有关。AQP4存在于血管周围星形细胞的足突,毛细血管内皮细胞,软脑膜等位置,是CNS中较重要的水转运通道[20]。曾有研究显示隐球菌小鼠脑组织水肿程度与AQP4 表达呈正相关[21]。受累脑膜邻近脑实质的炎症可由脑膜炎继发引起,也可以通过软脑膜血管上的内皮细胞通过吞噬作用进入脑实质内引起。在MRI 上受累脑实质通常表现为斑片状异常信号影,在T1WI 呈稍低信号,T2WI、FLAIR 呈稍高信号,DWI、ADC 上扩散不受限,增强扫描强化或者不强化。在本组以脑膜炎和脑膜脑炎为特点的病例中,仅有1 例患者单独存在脑膜炎,影像表现为脑膜强化;其余6例均存在脑膜与邻近脑组织的受累,影像上表现为受累脑膜明显增厚,增强后明显强化,临近脑组织存在片状异常信号影,伴或者不伴有水肿。(3)隐球菌肉芽肿。隐球菌肉芽肿又称隐球菌瘤[22],少见,可继发于脑膜脑炎或者胶样假囊。隐球菌肉芽肿在MRI 上的表现依赖于其组成成分,在T1WI呈等或稍低信号,T2WI、FLAIR上呈低、等、稍高信号,其中T2WI低信号为较特异性的表现,DWI、ADC 上扩散不受限,增强后可见明显强化。但本组病例中未见典型的隐球菌肉芽肿表现。(4)粟粒样结节。在本研究中,粟粒样结节表现仅有1 例,相对较少,此研究结果与既往结果一致[23]。(5)其他表现:其他表现包括脑积水、脑萎缩、血管炎等。脑积水是常见并且严重的并发症,其继发颅内高压是死亡原因之一,因此发生脑积水应积极引流。当颅内隐球菌感染时,脑脊液中可能会存在大量隐球菌,隐球菌的荚膜多糖及菌体聚积使蛛网膜颗粒堵塞,导致脑脊液回流障碍引起脑积水[24]。长期脑积水压迫周围脑组织可能会引起脑萎缩。但本组病例中未发现此类患者。在本组病例中,1 例患者表现为T1WI、T2WI、FLAIR 上未见异常信号,增强显示右侧额叶皮层下白质点状强化,可能与右侧额叶皮层下微小血管炎有关。笔者认为,当带有隐球菌的巨噬细胞穿过微小血管时,微小血管结构破坏,通透性增强,因此在增强扫描时会出现强化现象。
3.3 鉴别诊断
本病主要与以下疾病鉴别:(1)颅内结核。颅内结核主要分为脑膜结核,脑实质结核与混合型结核[25]。结核性脑膜炎(tuberculous meningitis,TBM)与CM一样,是AIDS患者常见的机会性感染,也是引起患者死亡的原因之一[26-27]。两者的鉴别主要依赖于实验室检查,但部分临床及影像学特征可以起到一定的提示作用。结核性脑膜炎患者呼吸道症状与抽搐发生率较CM高,TBM患者的CD4细胞计数高于CM患者(CM 中位数为23.5,TBM 中位数为61)[28-29]。结核杆菌密度较大,入颅后容易沉积在颅底的软脑膜和室管膜上,因此TBM 好发生于基底池与侧裂池,而CM则更好发生于血管周围间隙[30];结核瘤与结核结节病理基础为中央干酪样坏死,周围肉芽组织增生,中央坏死区域一般于T1WI呈等、稍低信号,T2WI可高或者低信号,周围肉芽肿壁于T1WI 等、稍高信号,T2WI 呈等信号,增强后呈现环形强化[25]。而隐球菌脑实质内病灶环形强化少见。另外结核瘤通常簇状分布,周围水肿明显,有研究调查显示TBM 周围脑组织水肿ETR II 级以上的比例高于CM[30]。(2)病毒性脑炎。病毒性脑炎病灶范围广,常呈多发性。额叶、颞叶、顶叶、枕叶与岛叶均可受累,皮层及皮层下白质均可受累。在MRI 上呈现斑块、斑片状异常信号,于T1WI 呈稍低信号,T2WI、FLAIR呈稍高信号。而隐球菌感染通多数呈现PVS分布特点。(3)进行性多灶性白质脑病。进行性多灶性白质脑病(progressive multifocal leukoencephalopathy,PML)好发于AIDS 患者,由JC 病毒引起,好发生在大脑半球,通常为双侧多发非对称分布,最常累计皮层下弓形纤维,呈现“贝壳”、“指状”形态[31-32]。幕下相对少见,主要发生在桥臂及邻近的桥脑与小脑。MRI上,于T1WI呈低信号,T2WI、FLAIR呈高信号,活动期时增强扫描病灶周边强化[30]。
综上所述,AIDS 合并CM 的患者CD4 计数较低,主要临床表现为头痛,其影像学表现具有一定的特征性:双侧基底节PVS扩张并伴有胶样假囊形成时高度提示该病。AIDS 合并CM 死亡率较高,需要及时采取合适的治疗措施。因此在临床工作中如果碰到伴有头痛的AIDS患者,要考虑到机会性感染的可能,根据患者实际情况对其进行实验室检查、影像学检查等,提高对该疾病的诊断率,从而进行有效的治疗,改善患者预后,提高生存率。
作者利益冲突声明:全体作者均声明无利益冲突。

