最小表观扩散系数值鉴别诊断巨细胞型胶质母细胞瘤与胶质母细胞瘤
张斌,薛彩强,林晓强,景梦园,邓靓娜,韩涛,周俊林
作者单位:兰州大学第二医院放射科 兰州大学第二临床医学院 甘肃省医学影像重点实验室,兰州730030
胶质母细胞瘤(glioblastoma multiform,GBM)是原发于颅内最常见的恶性肿瘤之一,而巨细胞型胶质母细胞瘤(giant cell glioblastoma,GCG)是其少见的分子分型。2016 年WHO 中枢系统肿瘤的新分类将GCG 归为IDH-野生型胶质母细胞瘤的范畴[1]。MRI 是目前诊断中枢神经系统病变最敏感的检查方法,然而,GCG 的常规MRI 征象与GBM 相似,通常难以鉴别。而且与经典的GBM 患者相比,GCG 患者有更长的中位总生存时间,以及更高的5 年生存率[2],因此,准确的术前诊断对患者的精确和个体化治疗至关重要。本研究通过对比分析GCG及GBM的MRI征象、DWI表现及ADCmin值,探讨ADCmin值对二者的鉴别诊断价值。
1 材料与方法
1.1 一般资料
收集2014 年6 月 至2019 年12 月我 院30 例 胶 质母细胞瘤患者,其中,GCG 11 例,男8 例,女3 例,年龄32~73 岁,平 均(52.6±11.2)岁;经 典 的GBM 19 例,男12 例,女7 例,年龄27~77 岁,平均(50.6±14.4)岁。纳入标准:(1)所有患者均为初诊,MRI 检查前均未接受放化疗及活检手术;(2)通过手术病理证实为GCG或GBM患者;(3)术前MRI检查资料完整,包括轴位T1WI、T2WI、DWI及T1WI增强扫描等;(4)MRI图像清晰,无明显伪影。两种肿瘤主要临床症状均表现为头痛头晕、恶心呕吐、肢体功能障碍及视物模糊等。本研究经过本单位医学伦理委员会批准(批准文号:2020A-070),免除受试者知情同意。
1.2 仪器与方法
头颅MR 平扫及增强扫描采用德国西门子Verio 3.0 T 超导MR 扫描仪,患者取仰卧位。扫描参数:T1WI (GRE 序列) TR 550 ms,TE 11 ms,层厚5 mm,层间距1.5 mm,视野(FOV) 260 mm×260 mm,矩阵256×256;T2WI (TSE序列) TR 2 200 ms,TE 96 ms,层厚5 mm,层间距1.5 mm,FOV 260 mm×260 mm,矩阵256×256。DWI (SE 序列)参数为:TR 4 000 ms,TE 100 ms,层厚5 mm,层间距1.5 mm,FOV 260 mm×260 mm,矩阵256×256,b值分别为0和1 000 s/mm2。增强扫描在轴位、矢状位及冠状位上行T1WI扫描,对比剂采用0.1 mmol/kg 的拜耳先灵Gd-DT-PA 经肘静脉团注,扫描参数同平扫。
1.3 图像分析
所有病例均由2 名经验丰富的神经放射学医生以盲法独立观察图像,记录肿瘤的生长部位、是否囊变、瘤周水肿、增强程度。然后根据原始图像计算表观扩散系数(ADC),并将其转移到西门子后处理器中,测量肿瘤实体部分的ADC 值,实体部分由T2WI 和增强对照确定。人工将感兴趣区域(ROIs)放置在肿瘤实质区域的连续水平ADC 图上,ROI 大小为15~20 mm2,避开坏死、囊变及出血区,测量2~3 个层面,并选择ADC 值最低的区域(ADCmin),然后计算2 名放射科医师ADCmin值的平均值。
1.4 统计学分析
采用SPSS 25.0统计学分析软件,经正态分布检验后,采用独立样本t检验比较GCG与GBM的最小ADC值,以P<0.05 为差异有统计学意义。绘制ROC 曲线,分析GCG 与GBM 的最佳诊断阈值以及相应敏感度与特异度。由于本组样本量n<40,两组间计数资料差异采用Fisher 确切概率法检验,以P<0.05 为差异有统计学意义。
2 结果
2.1 常规MRI表现
11 例GCG 中,病灶主体位于小脑1 例,颞叶7 例,额颞叶1 例,顶叶1 例,额叶1 例;7 例呈囊实性,4 例呈实性。病灶实质部分T1WI 均呈等低信号,T2WI 呈等高信号。均有瘤周水肿,其中瘤周轻度水肿5 例,中、重度水肿6 例。增强扫描肿瘤呈轻中度强化5 例,呈明显强化6 例。DWI 上,11 例肿瘤实性部分均呈斑片状稍高及高信号(图1)。
19 例GBM 中,病灶主体位于基底节区1 例,颞叶9例,顶叶1例,顶枕叶3例,枕叶2例,额叶3例;15例呈囊实性,4例呈实性。病灶实质部分T1WI均呈等低信号,T2WI 呈等高信号。均有瘤周水肿,其中瘤周轻度水肿4 例,中、重度水肿15 例。增强扫描肿瘤呈轻中度强化3 例,呈明显强化16 例。DWI 上,18 例肿瘤实性部分呈斑片状稍高及高信号,1 例呈等略低信号(图2)。
本组GCG与GBM的MRI征象中,病灶主体位置、病灶性质、瘤周水肿及增强程度差异采用Fisher 确切概率法检验无统计学意义(表1,2)。
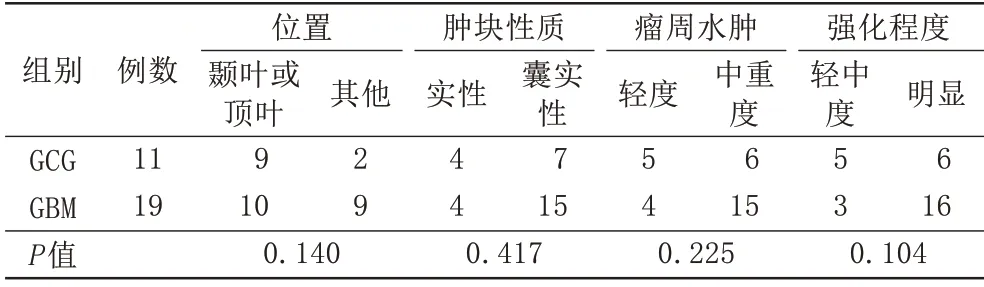
表1 两组患者MRI征象比较(例)Tab.1 Comparison of MRI signs of patients in two groups(n)

表2 GBM与GCG实性部分ADCmin值Tab.2 GBM and GCG solid fraction ADCmin values
2.2 GCG与GBM最小ADC值分析
GCG 的最小ADC 值为(0.989±0.104)×10-3mm2/s,GBM 为(0.837±0.111)×10-3mm2/s ,差异有统计学意义(t=3.671,P=0.001;表2),最小ADC 值鉴别诊断GCG与GBM 的ROC 曲线的AUC 为0.852 (P=0.002),95% CI为(0.716,0.988);以最小ADC 值=0.880×10-3mm2/s为临界值时,鉴别诊断两种肿瘤的敏感度为90.9%,特异度为68.4% (图3)。
3 讨论
GCG 是一种非常罕见的胶质母细胞瘤亚型,约占所有GBM的1%[3]。2016年更新的WHO中枢神经系统肿瘤分类首次引入了结合表型基因型方法优化肿瘤诊断的概念,将GCG 认为是IDH 野生型胶质母细胞瘤的变种[4],是介于原发性和继发性胶质母细胞瘤之间的一种亚型[5]。在IDH 检测为野生型的情况下,如果可以组织学排除巨细胞型胶质母细胞瘤、胶质肉瘤和上皮样胶质母细胞瘤,则可以使用非特定类型(NOS)GBM诊断,即经典的GBM[2]。
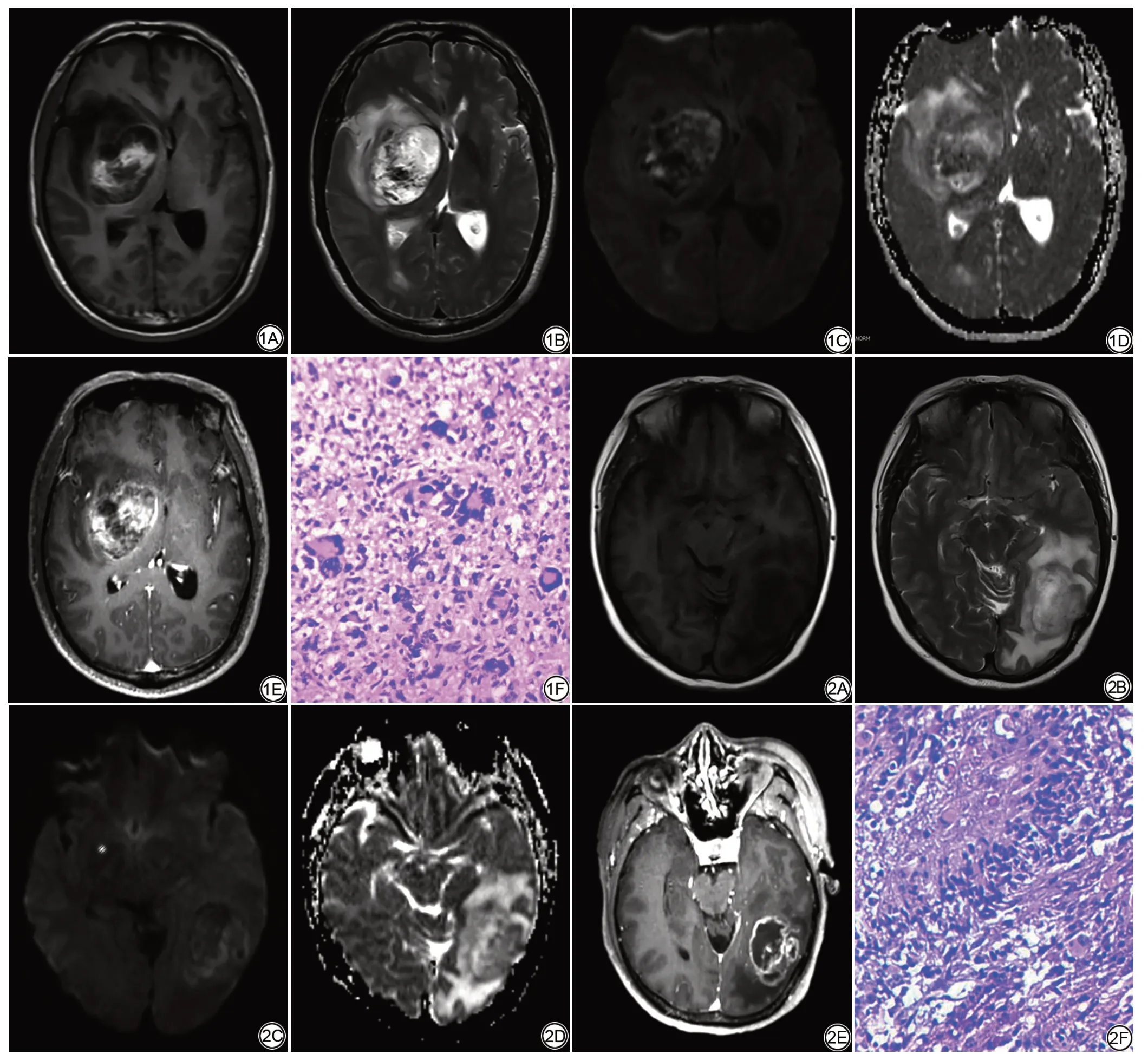
图1 男,45 岁,右侧颞叶巨细胞型胶质母细胞瘤。A:T1WI 示右侧颞叶实性占位,呈不均匀等低信号,内部可见斑片状高信号;B:T2WI 示病灶呈周围高信号,内部不均匀低信号,周围可见水肿;C:DWI(b=1 000 s/mm2)示病灶呈混杂稍高信号;D:ADC 图呈不均匀等高信号;E:增强扫描呈明显环形强化;F:病理图显示肿瘤细胞大小不一,有较多瘤巨细胞,形态怪异,胞浆丰富,核大、异型明显,核分裂象多见(HE×200) 图2 女,54岁,左侧颞顶叶胶质母细胞瘤。A:T1WI示左侧颞顶叶囊实性占位,囊性成分呈低信号,边缘可见斑片状等信号;B:T2WI示病灶呈不均匀等高信号,周围可见水肿;C:DWI(b=1 000 s/mm2)示病灶呈混杂等高信号;D:ADC图呈不均匀等高信号;E:增强扫描呈不规则环形强化;F:病理图显示肿瘤细胞呈多形性,核异型性明显,周围可见大量栅栏状坏死组织(HE×200)Fig.1 Male,45 years old,with giant cell glioblastoma of the right temporal lobe.A:T1WI shows a solid space in the right temporal lobe,showing uneven low signal,with patchy high signal inside.B:T2WI shows the lesion with peripheral high signal,uneven internal low signal,and edema around it.C:DWI(b=1 000 s/mm2)showed that the lesion was mixed with slightly high signal. D: ADC image showed uneven and high signal. E: Enhanced scan showed obvious circular enhancement. F:Pathological image showed tumor cells of different sizes, with more tumor giant cells have weird morphology, rich cytoplasm, large nucleus, and obvious atypia,with frequent mitotic images(HE×200).Fig.2 Female,54 years old,with glioblastoma in the left temporal parietal lobe.A:T1WI shows a solid cystic space in the left temporal parietal lobe, the cystic component shows a low signal, and a patchy signal is seen on the edge. B:T2WI shows the lesion has uneven and high signal with edema around it. C: DWI (b=1000 s/mm2) showed that the lesion showed mixed contour signal. D:ADC image showed uneven contour signal. E: Enhanced scan showed irregular ring enhancement. F: Pathological image showed tumor cells were pleomorphic and nuclear atypia obviously, a large number of fence-like necrotic tissues(HE×200)can be seen around.
相比于GBM 患者,GCG 患者的生存期提高15.5 个月,接受手术切除、放疗和化疗及系统治疗的患者,其预后更好,中位生存期17.55 个月[6]。Taemin 等[7]报道将GCG完整手术切除,联合放疗和替莫唑胺可以延缓肿瘤进展,接受该系统治疗的患者的中位无进展生存期更高,为32.9 个月。Kaoru 等[8]研究称GCG容易受到DNA 损伤,从而使增殖细胞失去干细胞性,发生有丝分裂和四倍体或多倍体化,最终可能导致衰老,而对GBM 抗DNA 损伤的干细胞标记物已被报道多种[9],这可以解释GCG较经典GBM预后更好。与GBM一样,完整的手术切除、放疗和化疗是GCG 治疗的主要手段,但TP53 基因突变在GCG 中常见,约占80%[10],这与Ji 等[11]报道TP53 突变在GCG (84%)中比GBM(23%)更常见的结果一致,同时该研究还认为PTEN突变在GCG中也较为多见,约占33%,这些突变状态可能有助于靶向治疗。因此,术前鉴别诊断GCG与GBM,可以为患者个体化治疗方案的选择提供重要的临床参考。
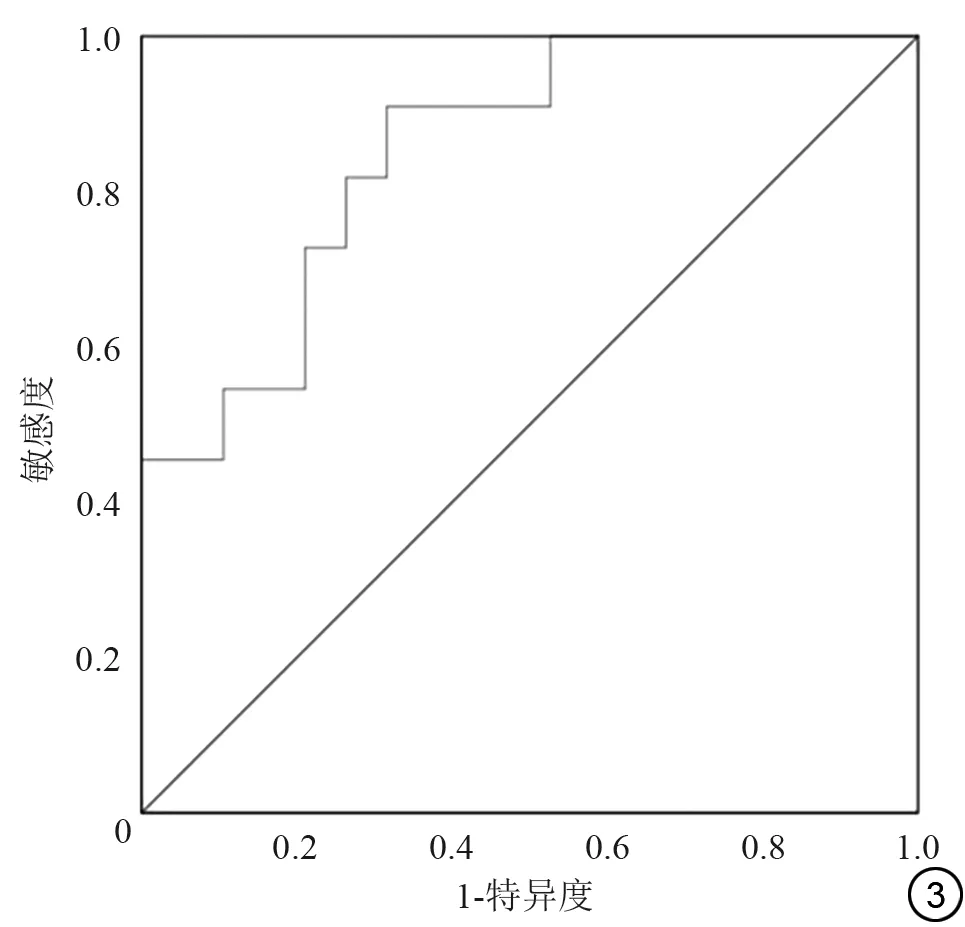
图3 最小ADC值鉴别诊断巨细胞型胶质母细胞瘤与经典的胶质母细胞瘤的ROC曲线Fig.3 Minimum ADC value for differential diagnosis of giant cell glioblastoma and glioblastoma.
3.1 常规MRI表现的局限性
临床上GCG 常生长于大脑表浅部位,通常以颞、顶叶皮层下多见[12]。本组病例MRI显示GCG肿瘤实质部分均位于大脑表浅部位,其中颞叶7 例,顶叶1 例,但本组病例GCG 与GBM 在生长部位并无统计学差异。GCG 患者多见于成年人,以40 岁后患病率最高,通常GCG 发病年龄较GBM 小[13],但本组病例GCG 发病年龄平均值大于GBM。
MRI是颅内肿瘤的常用检查方法,但常规MR扫描中GCG 相较于GBM 无明显特异性表现,导致术前诊断困难。GCG 肿瘤组织内常可见囊变坏死,实质部分表现为T1WI等低信号、T2WI等高信号,增强后多呈显著强化,并可见瘤周水肿,DWI 呈稍高及高信号[14]。有文献报道GCG 瘤周水肿程度低于GBM[15],本组病例二者无显著性差异。
3.2 ADC值与两组肿瘤病理基础的相关性
DWI是一种基于水分子在组织中的扩散的功能性MRI 技术,它取决于核浆的比例和细胞质中大分子的含量。DWI 广泛应用于各种脑肿瘤的分型、分子分型和鉴别诊断,由于水分在组织中的扩散高度依赖于细胞内与细胞外间隙的比例,晚期肿瘤中较高的细胞密度通过限制可用的细胞外间隙来减少水分子的扩散。ADC 值的大小代表细胞的疏密程度,肿瘤细胞增殖程度越高,ADC值越低,反映肿瘤恶性程度越高[16]。
本研究之所以选用ADCmin值鉴别诊断二者是因为该值测量方法简单,易于使用及相对可重复性[17],结合其他相关的临床和放射学研究,ADCmin值术前准确预测肿瘤组织学的能力更强[18],Yao等[19]将ADCmin值应用于儿童胶质瘤分级中表现出较好地效能,显示了ADCmin值对肿瘤异质性较好的预测能力。同时,ADCmin值可以避免囊变、水肿等致肿瘤异质性大的混杂特征,使二种肿瘤大量重叠的ADC 值降低,相较于其他特定区域测量的ADC值更加客观,能够更好地区分肿瘤类型[20]。本组结果显示,GCG 与GBM 实质部分的最小ADC 值差异有统计学意义(t=3.671,P=0.001),以最小ADC 值=0.880×10-3mm2/s 为临界值时鉴别二者的敏感度为90.9%,特异度为68.4%。最小ADC值鉴别诊断二种肿瘤的效能较高。
GBM 最小ADC 值低于GCG,其可能原因是GCG 的组织病理学特征是含有大量嗜酸性细胞质的多核巨细胞[21]。多核巨细胞异型性明显,形态怪异,胞浆丰富,体积巨大,直径大于0.5 mm,呈单核或多核,可见核内假包涵体、坏死及灶性血管增生[12,22]。GCG瘤体的细胞密度要低于GBM,而经典的GBM细胞排列更紧密,核浆比更高,水分子扩散受限,从而GCG 的ADC 值相较于GBM更高,这也从侧面反映了GCG的恶性程度小于GBM。
本研究的局限性:(1)为回顾性研究,可能存在样本选择性偏倚;(2) GCG 发病率较低,故样本量相对较少。
综上所述,用常规MRI征象鉴别GCG与GBM比较困难。通过本研究分析,最小ADC值在二者的鉴别诊断中具有较高临床应用价值,可为临床进一步治疗及判断预后提供指导。
作者利益冲突声明:全体作者均声明无利益冲突。

