水热法合成硫化铜微米花及其电化学性能
曲佳伟,陈秀娟,2,范影强
(1.兰州理工大学材料科学与工程学院,甘肃兰州 730050;2.兰州理工大学机电工程学院,甘肃兰州 730050)
锂离子电池(LIBs)作为一种相对成熟的储能方式具有优越的电化学性能和绿色环保的优势,在移动电子应用中扮演着重要角色,并已大规模用于移动电话、笔记本电脑和其他电子产品中。目前锂离子电池材料正被研究者广泛研究,以获得适用于所有类型电池系统的新型电极材料。在锂离子电池负极材料中,传统石墨材料具有循环稳定性高、使用安全、循环寿命长等优点,但其能量密度低,理论比容量低(仅372 mAh/g)[1-3],难以满足日益增长的电池容量和快速充放电循环的要求。相对而言,过渡金属化合物,特别是过渡金属硫化物作为锂离子电池的负极材料,具有能量密度高、理论容量大等优点,受到了科学界的广泛关注[4-5]。Sonia[6]使用一种低温工艺合成了由纳米钉组成的3D 硫化镍结构,其制备的材料具有极高的纯度,电化学测试表明材料的比容量为550 mAh/g,显示出了优良的电化学性能。
过渡金属硫化物CuS 作为一种重要的p型半导体材料,因其优良的比容量(560 mAh/g),优良的电子导电性(10-3S/cm)、相对平坦的放电/充电平台、安全且成本低而成为锂离子电池最有前途的负极材料之一[7],引起人们的广泛重视。Li 等利用水热法制备得到纳米棒状CuS 电极材料,在高电流速率下,CuS 电极可以保留超过370 mAh/g 的比容量[8]。尽管CuS负极材料有诸多优点,但CuS 负极材料也存在容量衰减严重,循环性能较差的问题,这主要是由于充放电过程中电极材料体积变化较大以及锂多硫化物溶解、反应而产生的多硫化物产生穿梭效应导致的,材料的微米/纳米化可以在一定程度上解决这一问题[9-11]。近年来,人们用各种方法制备了具有不同微观结构的CuS 材料,如纳米颗粒[12]、纳米棒[13]、纳米线[14]、纳米薄片[15]和空心球[16]。
本文以CuCl2·2 H2O 和CH4N2S 为原料,聚乙二醇(PEG)为表面活性剂,采用操作简单、低成本的水热法成功制备出了由片层结构组装而成的微米花,利用X 射线衍射光谱法(XRD)、扫描电子显微镜法(SEM)、透射电子显微镜法(TEM)、选区电子衍射法(SAED)、高分辨率透射电镜法(HRTEM)对样品的组成和形貌进行表征,探究了铜源、硫源物质的量的比对产物组成以及形貌的影响,并在此基础上研究了Cu7.2S4的存在对材料电化学性能的影响,实验结果表明,Cu7.2S4的存在一定程度上提高了电池容量的保持能力。
1 实验
1.1 材料的制备
取适量的二水合氯化铜、硫脲以及聚乙二醇分别加入三个装有20 mL 蒸馏水的烧杯中,磁力搅拌分别得到蓝色均匀氯化铜水溶液,无色均匀硫脲水溶液和聚乙二醇水溶液,将聚乙二醇水溶液与氯化铜水溶液混合搅拌10 min 后,将硫脲水溶液缓慢滴加入混合溶液中,超声均匀后得到白色乳状液。将混合好的白色乳状液转移至内附聚四氟乙烯内衬的100 mL 反应釜中,利用水热法在150 ℃下反应10 h,待反应结束冷却后,用去离子水和无水乙醇将所得沉淀交替洗涤5次,经干燥以及研磨后即可得到黑色粉末。
1.2 样品的表征
采用X 射线衍射仪对所得材料的物相组成以及晶体结构进行分析;选用冷场发射扫描电子显微镜对所得材料微观下的组成结构和形貌进行分析;采用JEM-2010 透射电子显微镜对样品的晶体结构进行进一步分析。
将制得的电极材料与乙炔黑以及聚偏氟乙烯(PVDF)按80∶10∶10 的质量比经玛瑙研钵研磨均匀,滴入N-甲基吡咯烷酮(NMP)经玛瑙研钵持续研磨直到混合物成浆状,将混合物均匀涂覆在经预处理的铜箔片上,经过干燥后,使用压片机将铜箔片压成电极片,从而得到工作电极。此后将电极置于充有氩气气氛的手套箱中,以金属锂片为正电极,与电解液和隔膜装成纽扣式电池,将电池在室温下静置一段时间后,对电池进行电化学测试。
2 结果与讨论
2.1 物相和形貌分析
图1 为不同铜源、硫源物质的量的比的混合物在150 ℃、10 h 的水热条件下所得样品的XRD 图谱。将样品与标准卡片(JCPDS 06-0464、JCPDS 24-0061)对照可知,在铜源、硫源物质的量的比为1∶4 的条件下制得的样品与纯相CuS 的标准卡片(JCPDS 06-0464)保持一致,样品在2θ 为10.8°、27.1°、27.7°、29.3°、31.8°、32.9°、47.9°、52.7°、58.7°、59.3°处的衍射峰分 别 对 应 六 方 靛 铜 矿 硫 化 铜 的(002)、(100)、(101)、(102)、(103)、(006)、(110)、(108)、(203)及(116)晶面,衍射峰明显,强度高,说明在此条件下制得的样品晶体结晶度高,发育良好。当减少硫源的用量,在铜源、硫源物质的量的比分别为1∶2 和1∶3 时,所得产物为CuS 与Cu7.2S4的混合物,在2θ 为27.7°、32.1°、46.1°、54.6°存在的衍射峰分别对应Cu7.2S4的(111)、(200)、(220)和(311)晶面,这可能是因为硫源的添加量不足,在反应过程中生成的产物CuS 逐渐分解,生成Cu7.2S4[17],相比而言,铜源、硫源物质的量的比为1∶2 条件下制得的样品Cu7.2S4相衍射峰更明显,结晶度更高。

图1 不同铜源、硫源物质的量的比的样品的XRD 图谱
图2 为不同铜源、硫源物质的量的比的混合物在150 ℃、10 h 的水热条件下所得样品的SEM 图谱。由图2(a)可知,在铜源、硫源物质的量的比为1∶2 时,CuS 与Cu7.2S4的混合物的形貌为大小不一的不规则颗粒,其大小约为100~900 nm。随着硫源的增加,样品形貌变为由纳米片组成的微米花,所形成的微米花大小约为3~5 μm,如图2(b)~(c)所示。在铜源、硫源物质的量的比为1∶4 时形成的微米花形貌较完整均匀,组成微米花花瓣的片层结构明显,厚度较薄,约为50 nm,如图2(d)所示。

图2 不同铜源、硫源物质的量的比下样品的SEM图谱
为了进一步观察CuS 微米花的晶体结构,使用透射电镜对铜源、硫源物质的量的比为1∶4 的样品进行了分析,如图3所示。图3(a)为CuS 微米花样品的TEM 图,可以观察到CuS样品大体为花形,大小为3~5 μm;图3(b)为CuS 微米花的HRTEM 图像,可以清楚地看到晶体内部的晶格条纹,这说明CuS 微米花具有良好的结晶度,晶体结构完整,经过测量发现,HRTEM 图像中晶面间距为0.32 nm,对应着六方CuS 的(101)晶面;图3(c)为CuS 微米花的SAED 图,经分析可知,样品的衍射花样分别对应立方CuS 的(201)、(110)以及(100)晶面,所得分析结果与XRD 分析结果一致。
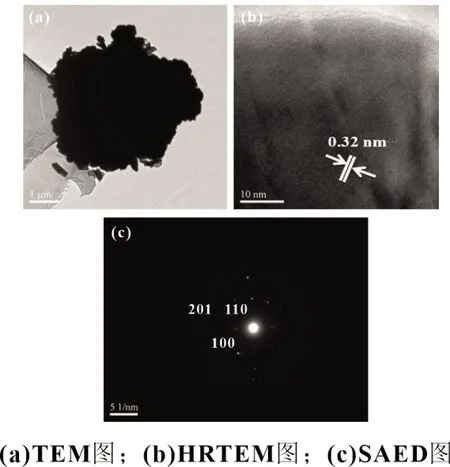
图3 铜源、硫源物质的量的比为1∶4的样品的TEM、HRTEM和SAED图
2.2 电化学性能分析
图4 为微米花状CuS 电极材料在电压为0.01~3.0 V、扫描速率0.1 mV/s 下的循环伏安曲线(CV)。在第一次扫描过程中,在1.55 和1.9 V 存在两个还原峰,在1.89 和2.42 V 存在两个氧化峰。其中在1.9 V 附近的还原峰主要归因于从CuS 到LixCuS 的可逆过程;在1.55 V 的还原峰主要归因于LixCuS 分解为金属Cu 和Li2S[18-19]。在随后的循环中,氧化峰有轻微的移动,还原峰转移到更高电势,在1.9 V 的还原峰减小并逐渐消失,这主要是因为SEI 膜和Li2S 的形成以及电解质的分解。三次扫描的形状大部分重叠,这表明锂离子的嵌入/脱出过程具有高度可逆性。CuS 电极的电化学反应过程如下:
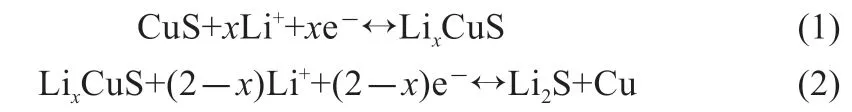

图4 CuS 微米花在扫描速率为0.1 mV/s时的循环伏安曲线

图5 CuS 和CuS/Cu7.2S4电极材料在0.1 C时的充放电曲线
图5 为CuS 和CuS/Cu7.2S4电极材料在0.1C、0.01~3.0 V电压下前三次充放电曲线。在放电过程中,两电极均在1.6和2.0 V 附近存在两个放电平台,这主要是LixCuS 相的形成导致的。在第一次充电过程中,两电极均在1.9 和2.4 V 附近存在两个充电平台,随着循环的继续进行,2.4 V 附近的平台变短,并在放电过程中逐渐消失。CuS/Cu7.2S4材料的首次充放电比容量及库仑效率分别为477.2、817 mAh/g 和58.41%,略高于纯相CuS 的首次充放电比容量及库仑效率(318.9、765.2 mAh/g 和41.68%),电解液的分解和SEI 层的形成是电池容量不可逆损失的主要原因。相比而言,CuS/Cu7.2S4电极材料性能略高于纯相CuS 电极材料。
图6 为CuS 和CuS/Cu7.2S4电极材料在0.1C~2.0C下的倍率性能曲线。随着测试倍率的不断增加,样品的比容量呈现阶梯状减少趋势,这是由于测试倍率的增加减短了电极材料充放电时间,从而导致锂离子发生不完全迁移。在0.1C~2.0C下,CuS 电极材料的放电比容量分别为98.7、73.8、58.6、49.3、41.9 mAh/g;CuS/Cu7.2S4电极材料的放电比容量分别为86.7、65.8、50.3、41.9、31.1 mAh/g。两种材料的放电比容量经前十次循环均有较大的衰减,这可能是因为在第一次充放电时形成了SEI 膜以及活性物质存在损耗所致。
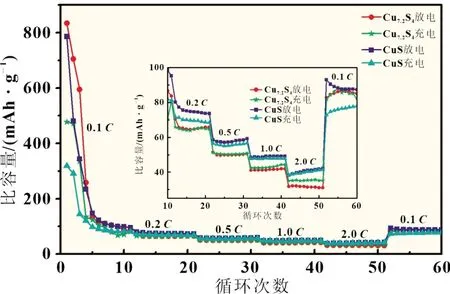
图6 CuS 和CuS/Cu7.2S4电极材料的倍率性能曲线
图7 为CuS 和CuS/Cu7.2S4电极材料在0.1C下、电压为0.01~3.0 V 时的循环性能曲线与库仑效率图。CuS 和CuS/Cu7.2S4电极材料比容量均有较大的衰减,经100 次循环后,两种电极材料的放电比容量分别为54.7 和67.6 mAh/g,这可能是由于电极材料在放电/充电过程中粉化和体积膨胀等原因造成的。相对而言,CuS/Cu7.2S4电极材料经100 次循环后放电比容量略高于纯相CuS,这可能是因为CuS/Cu7.2S4电极材料在循环过程中的体积变化比纯相CuS 低。

图7 CuS和CuS/Cu7.2S4电极材料在0.1 C 时的循环性能曲线
图8 为CuS 和CuS/Cu7.2S4电极材料的电化学交流阻抗曲线。曲线由一个凹陷的半圆与一条直线组成,凹陷的半圆表示电极和电解质之间的电荷转移电阻。直线表示锂离子的扩散过程。CuS/Cu7.2S4电极材料的半圆要小于纯相CuS 电极,这说明CuS/Cu7.2S4电极材料的电子导电性更好。

图8 CuS 和CuS/Cu7.2S4电极材料电化学交流阻抗曲线
3 结论
实验采用水热法以简单、低成本的方法合成了CuS 和CuS/Cu7.2S4材料,并对材料的物相组成、形貌以及电化学性能进行了研究。电化学结果表明,CuS/Cu7.2S4材料的首次充放电比容量及库仑效率分别为477.2、817 mAh/g 和58.41%,略高于纯相CuS 的首次充放电比容量及库仑效率(318.9、765.2 mAh/g 和41.68%),且CuS/Cu7.2S4材料的循环稳定性能比纯相CuS 好,经100 次循环后,其放电比容量比纯相CuS 略高,这说明该材料具有较好的研究前景。

