锂电池MoNxO3-x/C复合材料的制备及其储锂性能的研究
马 胜,任 军,唐旭东
(1.河北华北石油工程建设有限公司,河北沧州 062552;2.中国石油管道局工程有限公司,河北廊坊 065000;3.天津科技大学化工与材料学院,天津 300457)
目前已经商业化的动力锂离子电池主要采用LiNixCoyMn1-x-yO2和LiFePO4作为正极。虽然LiNixCoyMn1-x-y比能量高且倍率性能好,但是其制备需要大量镍钴元素,生产成本较高。另一方面,三元材料在充放电过程中结构劣化会引发严重的热失效问题,安全性较差[1-2]。LiFePO4价格相对较低,安全性更好,但是需要借助包覆和掺杂来提升电子导电性[3-4],同时其能量密度明显低于三元材料。因此,研究人员一直在探索具有可应用前景的锂离子电池正极材料。
正交相MoO3具有独特的二维层状结构,结构中包含的四面体和八面体空穴适合为Li+传输提供开放通道,表现出Li+脱/嵌性质。同时,MoO3电压平台在2.5 V 左右,能够可逆脱/嵌1.5 个单元锂(1.5 Li/Mo),电化学比容量可达280 mAh/g,具有较高能量密度,很适合作为二次电池电极材料[5]。Ramírez等[6]将MoO3用作电池正极材料,以0.02 mA/cm2电流充放电,材料的首次比容量为370 mAh/g,第2次循环后,其放电容量保持率仅为75%。Reddy等[7]制备了纳米结构MoO3,其在0.4 mA/cm2电流条件下,20 次循环后放电比容量达到280 mAh/g。但是,在随后的充放电过程中其容量开始快速衰减,衰减率为33%。研究表明,电极性能劣化一方面与MoO3体相离子迁移速率较慢和电子电导率较低有关,另一方面在于Li+脱/嵌过程所生成的LixMoO3改变Mo-O 晶格结构,最终造成电极极化程度增大,性能随之衰减[8]。
针对上述问题,本文采用乙二胺与三氧化钼的杂化前驱体作为反应模板,经过高温碳热还原反应,制备纳米形貌MoNxO3-x/C 复合材料。在此原位反应过程中,乙二胺分解生成氮化碳并释放含氮小分子,从而实现了碳包覆层与活性材料表面的紧密复合。所形成的碳包覆层可以提高材料的电导率,抑制电解液与材料界面的副反应。此外,N 元素可以原位进入Mo-O 晶格形成掺杂位。相关研究[9-10]已经表明在Mo-O晶格中掺杂N 元素能够增加晶体结构的稳定性。制备的纳米形貌MoNxO3-x能够缩短Li+在材料内部的迁移路径,降低极化阻力,利于循环寿命和倍率性能提升。
1 实验
1.1 实验试剂与合成方法
实验试剂:三氧化钼MoO3(分析级);乙二胺C2H8N2(分析级);聚丙烯微孔隔离膜PE-PP(2 400 目,Celgard);乙醇C2H5OH(分析级);金属锂片(工业级);铝箔(工业级)。合成方法:取15 mL 乙二胺溶于120 mL 无水乙醇,磁力搅拌。待乙二胺溶解,将0.93 g α-MoO3加入上述混合溶液中,60 ℃水浴加热反应15 h。反应完成,对产物进行抽滤,无水乙醇洗涤3~6 次。最后将滤饼置于干燥箱中60 ℃真空干燥24 h。所得白色粉体即为乙二胺/多钼酸盐化合物MoO3-y/EDA。取适量乙二胺/多钼酸盐化合物倒入刚玉舟,通入N2保护气氛,在管式炉中以3 ℃/min 升温速率加热至600 ℃,恒温3 h。待炉温冷却至室温后,即可得MoNxO3-x/C 复合产物。常规MoO3在空气气氛中650 ℃煅烧12 h即可制得正交相α-MoO3。
1.2 分析与表征
分析与表征设备:X 射线衍射仪(XRD),Cu-Kα1靶,波长0.154 nm,扫速5(°)/min,扫描范围5°~50°;X 射线光电子能谱仪(XPS),射线源Al-Kα,能量1 486.6 eV;扫描电子显微镜(SEM);高分辨透射电子显微镜(HR-TEM);热重-差热分析仪(TGA-DSC),N2气氛,升温速率10 ℃/min,15~900 ℃;元素分析仪,载气氧气,炉温850 ℃。
1.3 电化学测试
以复合材料MoNxO3-x/C 作为正极活性材料。将正极材料、聚偏氟乙烯PVDF(含3.5%溶液)、炭黑导电剂Super P 按照质量比85∶10∶5 搅拌均匀,涂覆在铝箔集流体上。极片经过120 ℃鼓风干燥3 h后,压片并冲切成直径12 mm 的圆形正极。极片活性材料的负载量为0.8~0.9 mg/cm2。随后极片再次以100 ℃真空烘烤12 h。待真空烘烤完成,极片在高纯度Ar气手套箱内组装CR 2032 型扣式半电池,电解液为1.0 mol/L LiPF6/[碳酸乙烯酯(EC)+碳酸二甲酯(DMC)](体积比1∶1)。装配好的电池室温环境静置12 h后,在1.5~3.6 V 电压范围内以0.05 A/g电流进行充放电循环测试。使用多通道电化学工作站进行循环伏安测试,扫描电压为1.5~3.6 V,扫描速率为0.3 mV/s。
2 结果与讨论
2.1 XRD 分析
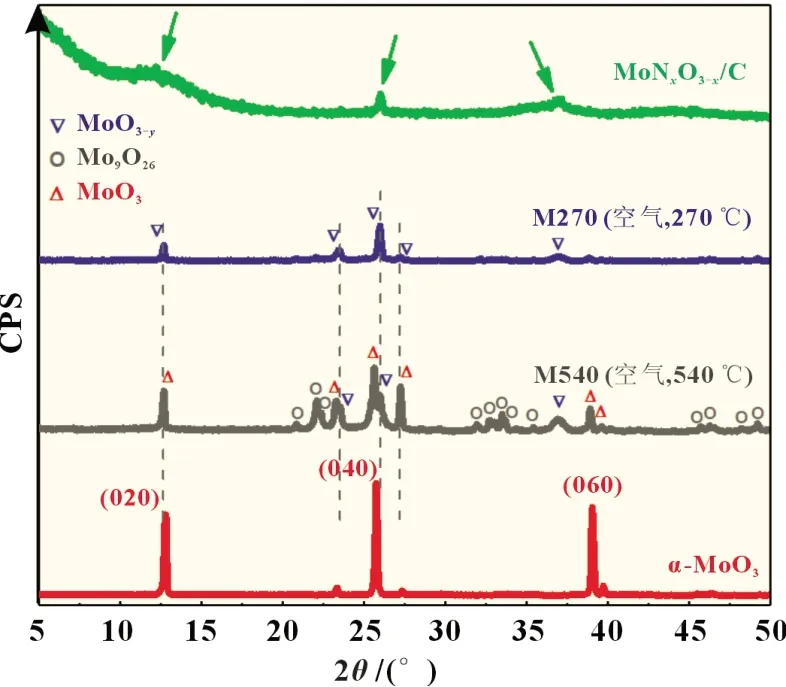
图1 α-MoO3、MoNxO3-x/C及其空气气氛中煅烧产物的XRD图
图1 为α-MoO3和MoNxO3-x/C 材料的XRD 谱图。在正交相α-MoO3晶格中,Mo-O 八面体结构单元分别在(100)和(001)晶向上,以共角和共边的连接方式形成二维层板,各层板之间又依靠范德华作用力沿(010)方向相互堆积,形成独特的层状结构。因此,在α-MoO3的XRD 图谱中(020)、(040)、(060)晶面的衍射峰呈现等间距排列。相比于α-MoO3,MoNxO3-x/C 的衍射峰强度不仅显著降低,而且衍射峰也发生不同程度偏移。在将MoNxO3-x/C 于空气中270 和540 ℃下处理2 h 后[11],发现产物衍射峰强度并不会显著提高。温度升至540 ℃,出现MoO3与Mo9O26(PDF#05-0441)[12]混合相,但衍射峰强度依然无明显提高。推测MoNxO3-x/C 的主体结构MoO3-y已经呈现出无序化特性。其原因可归结为:乙二胺热解生成的无定形碳对主体Mo-O 晶体层进行碳热还原反应,原先有序的层状结构开始无序化,衍射峰强度相应降低;无定形碳限制MoNxO3-x晶体的长程有序生长[13-14];热解过程中,含氮分子进入Mo-O 晶体层形成掺杂位,原始晶格尺寸参数改变,造成衍射峰偏移,也加重主体结构无序化程度[15]。
2.2 SEM 与TEM 分析
图2(a)~(c)分别为α-MoO3、MoO3-y/EDA 和MoNxO3-x/C的SEM 图。根据图2(a)~(b),α-MoO3为微米尺寸的块状体,但是在与乙二胺反应后,产物MoO3-y/EDA 形貌已经显著改变,呈现出纳米带状特征。这种现象的原因在于α-MoO3与乙二胺分别具有Lewis 酸和Lewis 碱的性质。借助有机胺与氧化物的酸碱反应来合成并调控复合材料微观结构的研究已被报道过[16]。在纳米带状MoO3-y/EDA 形成过程中,乙二胺起到重要的协同作用,一方面,其促进α-MoO3水解转化成多钼酸盐阴离子,另一方面,乙二铵阳离子结合在多钼酸盐阴离子表面,由于氢键效应,多钼酸阴离子在一维方向沿着乙二铵阳离子排列连接,最终形成纳米带状形貌。由图2(c)可知,经过高温煅烧后,MoNxO3-x/C 仍保留了MoO3-y/EDA 的纳米带状形貌,这种结构可以有效减少Li+在材料内部的迁移距离,降低扩散传递阻力,从而改善倍率性能。由图2(d)的TEM 图可知MoNxO3-x具有几十纳米的颗粒结构,其晶格条纹间距约为0.34 nm,对应于α-MoO3正交结构的(040)晶面[17]。不过,晶格条纹具有一定程度的无定型化特点,应该是有机胺碳热还原MoO3-y主体结构导致的,这点也与XRD 谱图分析结果一致。乙二胺热解形成的无机碳紧密包裹MoO3-y,对其晶体尺寸的有序生长起到局域限制作用。另外,能够清晰观察到材料外表面形成厚度均匀的碳包覆层。
2.3 TGA-DSC 分析
图3 为α-MoO3和MoO3-y/EDA 在N2气氛下的TGA-DSC曲线。在100~700 ℃,α-MoO3失重约为2.9%,这是由于结晶水热蒸发造成的,因此可认为几乎没有损失。而从720 ℃处开始,α-MoO3陡然失重,这是其自身在高温下升华所致。相比之下,MoO3-y/EDA 从230 ℃开始失重。在200~800 ℃,MoO3-y/EDA 的失重过程大致分为两个阶段,即200~400 ℃和400~800 ℃。第一阶段DSC 曲线上可观察到280 ℃处有一个强热吸收峰,分析认为第一阶段的失重归于乙二胺分解生成的小分子逃散以及物质表面所吸附的水分受热蒸发,失重分数共计24%。第二阶段660 ℃处存在另一个热吸收峰,此阶段的吸热反应主要对应两个过程,即无定形碳的有序转变以及N 元素和C 元素掺杂进入MoO3-x形成晶格价键。根据TGA 曲线分析,截至700 ℃,估算MoO3-y/EDA 中碳含量约为39%。对MoNxO3-x/C 材料C 元素和N 元素进行分析,测试结果为C 元素含量25.41%,N 元素含量1.14%。
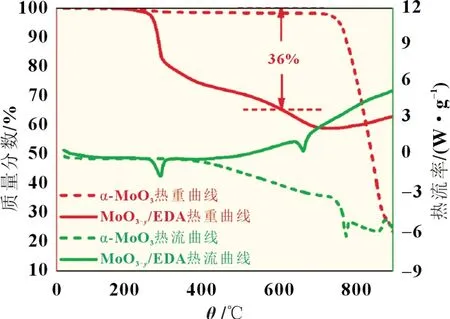
图3 α-MoO3、MoO3-y/EDA在N2气氛下的TGA-DSC曲线
2.4 XPS 分析
图4 为MoNxO3-x/C 样品的Mo3d和N1sXPS 谱图。根据相应的拟合分析,Mo 元素含有四种价态键合结构[18-19],N 元素也是以四种键合状态存在[20-21],具体结合能数据如表1 所示。其中,Mo4+和Mo5+认为是MoO3晶格中Mo6+被还原所致。图4(b)中,吡啶型-N、吡咯型-N 及石墨型-N 的出现表明有机胺已经完全转化成含氮无定形碳。上述三种N 掺杂结构对提升碳包覆层的导电性起到积极影响[22-24]。另外,无论Mo3d还是N1s拟合结果均证明活性组分形成Mo-N 键合结构,这意味着N 原子已经进入MoO3晶格中,取代了部分O 原子。据相关研究[25],当向Mo-O 晶格中掺杂进N 原子,形成的OMo-N 键合结构有助于改善钼氧化物的体相导电性能,同时对于因Li+嵌/脱而引发的晶体应力形变现象也有抑制效果。由此,上述两者的协同效应可以促进电极循环性能和倍率性能的提升。
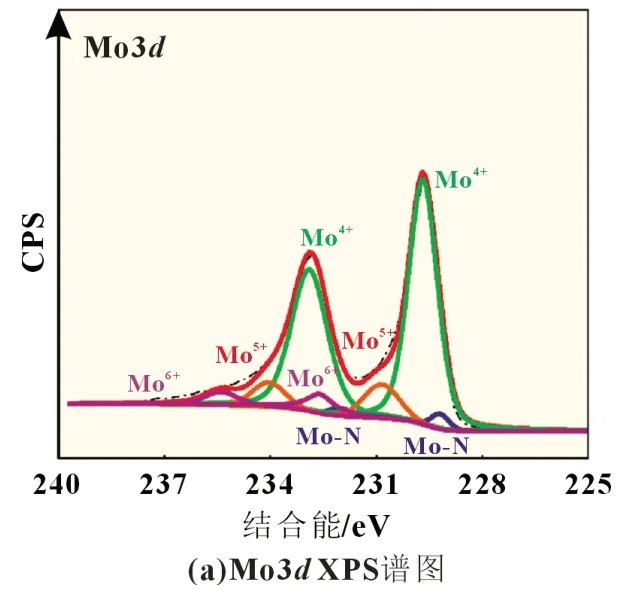
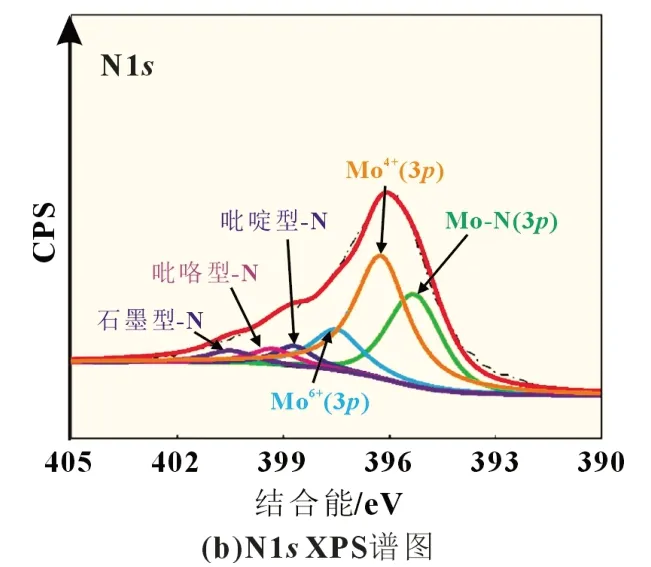
图4 样品MoNxO3-x/C的Mo3d和N1s XPS谱图
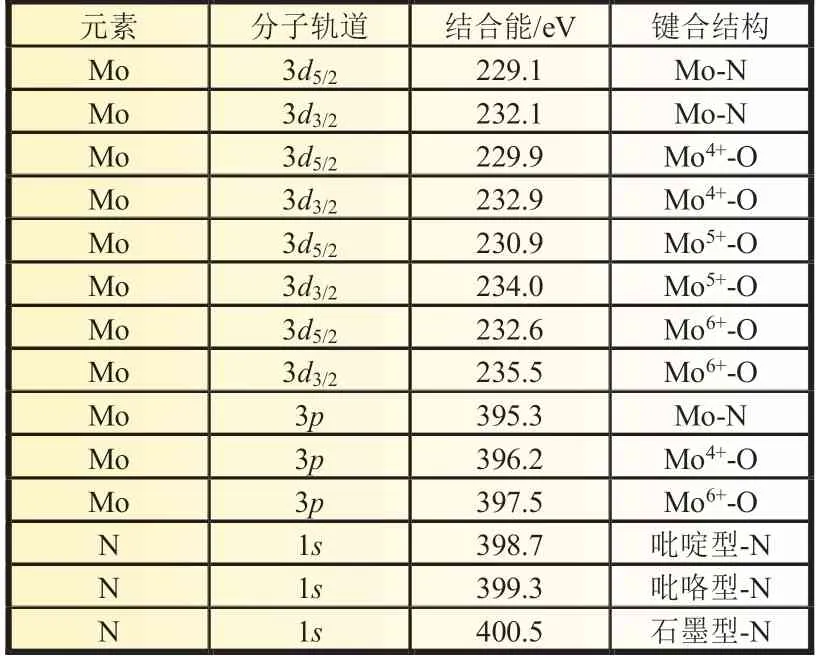
表1 样品MoNxO3-x/C 的Mo3d 和N1s 拟合结果
2.5 电化学性能测试
图5(a)~(b)为α-MoO3与MoNxO3-x/C 电极前三次的循环伏安曲线。α-MoO3电极存在一个还原峰(2.1 V)和一个氧化峰(2.8 V),分别对应嵌锂和脱锂过程。MoNxO3-x/C 电极在2.2 和2.5 V也分别出现一个还原峰和一个氧化峰。比较两者的极化压差可以发现,MoNxO3-x/C 电位差值0.3 V 明显小于α-MoO3电位差值0.7 V。这表明复合改性MoNxO3-x/C 的电化学活性高于α-MoO3。
图5(c)~(d)为α-MoO3与MoNxO3-x/C 电极前两次的充放电曲线。对于两种电极,其充电/放电的电压平台①或②与各自循环伏安曲线的峰位能够较好对应。为了评估充电/放电过程的极化程度,将首次充电的半容量所对应的电位与第二次放电的半容量所对应的电位相减,求得电位差值∆H(Q/2)。根据计算,α-MoO3的∆H(Q/2)为0.71 V,MoNxO3-x/C的∆H(Q/2)为0.29 V,这与循环伏安曲线的结果类似,再次表明复合改性MoNxO3-x/C 的电化学活性高于α-MoO3。这是因为,相较于块状形貌α-MoO3,MoNxO3-x/C 纳米带状结构有效地减少了Li+在材料内部的迁移距离,降低扩散传递极化阻力,从而显著改善充放电性能。除此以外,α-MoO3与MoNxO3-x/C 电极的首次库仑效率分别为86.1%和90.2%。MoNxO3-x/C 较高的库仑效率证明了碳包覆与晶格N 掺杂的协同作用对提高材料体相导电性,降低活性组分与电解液副反应起到积极作用。
图5(e)为α-MoO3与MoNxO3-x/C 电极在0.05 A/g 电流密度下的循环性能图。其中,α-MoO3首次放电比容量为361.5 mAh/g,MoNxO3-x/C 首次放电比容量为379.2 mAh/g。分析认为,MoNxO3-x/C 放电比容量更高的主要原因在于其表面包覆的碳阻隔电解液,避免了直接接触活性组分,利于减少副反应。循环80 次后,α-MoO3和MoNxO3-x/C 放电比容量分别为156.5 和229.2 mAh/g,容量保持率分别为43.3%和60.4%。这表明相比于α-MoO3,复合改性MoNxO3-x/C 具有更高的可逆容量和良好的稳定性。图5(f)为α-MoO3和MoNxO3-x/C 电极的倍率性能图,在0.1、0.2、0.5和1 A/g的电流条件下,MoNxO3-x/C放电比容量分别214.9、161.4、121.6 和108.9 mAh/g;在相同电流条件下,α-MoO3放电比容量分别为178.9、100.8、21.81、4.6 mAh/g。上述结果说明,纳米带状结构能够有效改善材料倍率性能。
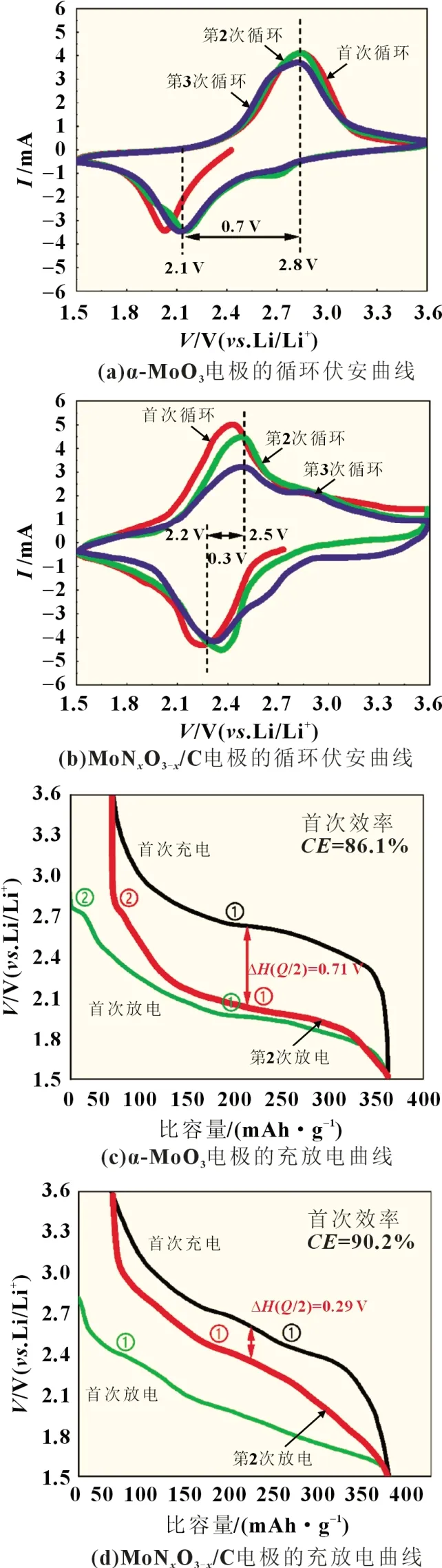
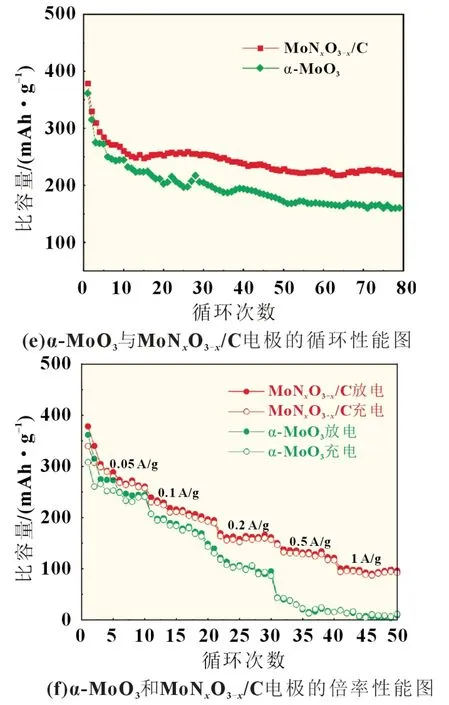
图5 α-MoO3与MoNxO3-x/C电极的循环伏安曲线、充放电曲线、循环性能图与倍率性能图
3 结论
以MoO3-y/EDA 作为模板前驱体,通过碳热还原反应,制备了带状纳米结构的MoNxO3-x/C 复合材料,并对其电化学性能进行了测试。结果表明,相比于α-MoO3,复合改性MoNxO3-x/C具有更高的可逆容量和良好的稳定性。主要原因为:乙二胺煅烧分解,原位生成的碳包覆层与活性材料紧密结合,阻隔电解液与活性组分的直接接触,从而减少副反应;碳包覆以及Mo-O 晶格N 掺杂均有利于增强活性组分的结构强度;纳米带状形貌缩短Li+在材料内部的迁移路径,降低极化阻力。综上所述,只要对其循环性能进行持续改善,MoNxO3-x/C作为一种较高容量的正极材料是可以被应用于锂离子电池中的。

