超声与磁共振成像诊断肝硬化门静脉高压症图像特征分析
赵华歌
长葛市人民医院消化内科,河南 许昌 461500
肝硬化门静脉高压常出现在肝硬化晚期,少部分见于早期[1]。肝硬化门静脉高压症会导致全身血流动力学变化。有报道发现肝硬化门静脉高压症门静脉内径增宽、流速降低。肝动脉流速增快、血流阻力增加[2]。轻度肝硬化患者各种表现尚不甚明显,但中晚期肝硬化患者各项指标表现较明显[3]。磁共振成像(MRI)能通过反映血流情况预测病情,准确鉴别图像特征有利于明确疾病,提升预后。本文以长葛市人民医院2019年1月—2020年2月收治的疑似肝硬化门静脉高压症患者作为研究对象,采用超声、MRI诊断,现将研究结果报告如下。
1 资料与方法
1.1 一般资料
随机选取长葛市人民医院2019年1月—2020年2月收治的疑似肝硬化门静脉高压症患者150例,其中男性79例,女性71例,年龄35~74岁,平均年龄(52.69±4.57)岁。肝硬化Clild-pugh分级:A级14例、B级75例、C级61例。白蛋白(g/L):>35 g/L 84例、34~51 g/L 26例、<28 g/L 40例。乙肝后肝硬化24例、丙肝后肝硬化38例、酒精性肝硬化71例、不明原因肝硬化17例。诊断标准[4]:符合中华医学会肝病分会制定的肝硬化相关诊断标准。纳入标准:知情同意、病理确诊、成年、75岁以下、肝硬化患者;排除标准:心血管疾病、胃肠道疾病、近期肝功能及腹部CT检查正常、妊娠期、哺乳期患者。
1.2 方法
超声检查:使用飞利浦公司生产设备检测,探头频率为2.0~3.5 MHZ,患者在静息状态下接受检查,选取仰卧位,对肝脏进行多切面检查获取准确数据,观察肝脏、脾腔的形态、大小、内部回声、门静脉血流情况。MRI检查:使用GE公司生产的1.5 T超导型MRI诊断仪检查,肝脏横轴位参数FSPGR120~150 ms,层厚8 mm,层间隔2 mm,矩阵256×256,1次激励,采集时间18~21 s,脂肪抑制序列TR 6000~9231 ms,层间隔2 mm,矩阵(288~320)×(160~256),3~4次,注射对比剂,开启增强扫描模式,获得完整的图像。病理检查:采用细针抽取组织,送至病理实验室进行病理检查。
1.3 观察指标
所得超声和MRI图像上传至工作站,由两名经验丰富的影像学医师采用双盲法对疑似肝硬化门静脉高压症图像特征进行分析及诊断。肝硬化门静脉高压症诊断标准参考常规影像诊断标准进行判断评分;5分,肯定为肝硬化门静脉高压症;4分,肯定为肝硬化,可能为门静脉高压症;3分,肯定肝硬化,不确定为门静脉高压症;2分,肯定为肝硬化,门静脉高压症可能性不大;1分,肯定是肝硬化,不是门静脉高压症。以5分作为超声及MRI诊断为肝硬化门静脉高压症标准。与病理诊断结果进行对照,得出阳性、阴性、假阳性、假阴性及准确率。
1.4 统计学方法
数据采用SPSS 26.0软件进行统计学分析,计量资料以均数±标准差(±s)表示,组间比较行t检验;计数资料以例数和百分比(%)表示,组间比较行χ2检验。以P<0.05表示差异有统计学意义。
2 结果
2.1 超声与MRI诊断肝硬化门静脉高压症结果比较
病理结果显示,150例患者中有123例为肝硬化门静脉高压症,比例为82%。超声检出140例肝硬化门静脉高压症,其中阳性患者91例、阴性9例、假阳性12例、假阴性28例,准确率为73.98%。MRI检出131例,其中阳性118例、阴性3例、假阳性11例、假阴性8例,准确率为95.93%。MRI诊断肝硬化门静脉高压症阳性率、准确率高于超声诊断(P<0.05),假阳性率及假阴性率低于超声诊断(P<0.05),见表1。
2.2 超声与MRI诊断肝硬化门静脉高压症图像特征分析
超声主要通过观察肝脏及脾脏的外部形态、内部结构回声等反映肝硬化程度。图像特征显示,肝硬化门静脉高压症患者脾厚度、脾长径明显增加,入肝血管的压力速度上升(图1),脾静脉内血流流入门静脉时发生阻碍。门静脉主干捷径增宽,肝功能分级差,以强回声或稍强回声为主。MRI图像发现患者门静脉片平均流速、直径、流量明显减少,减少均在30%~40%。不同肝功能患者门静脉流速明显降低,肝损伤越严重的患者门静脉流速越慢。门静脉截面积增大,门静脉阻力增大,出现肝脏功能衰竭症(图2)。
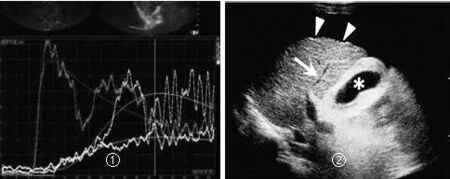
图1 超声图像特征:①门静脉血流减少;②肝脏萎缩,胆囊壁水肿

图2 MRI图像特征:①冠状面显示门静脉主干萎缩,血流减少;②横截面显示肝组织萎缩;③早期肝功能损伤症状不典型;④门静脉高信号,边缘清晰,尖锐
3 讨论
既往研究认为[5]慢性门静脉高压主要由门脉及其侧支循环血流阻力增加所致。另有研究发现[6]内脏高动力循环、门脉血流增加相互作用也会导致门静脉高压症。门静脉高压症是诊断肝硬化的重要依据,其中门静脉内径增宽是临床上判断患者是否存有门静脉高压症的重要指标[7]。本组研究也发现,肝硬化门静脉高压症患者伴有不同的门静脉血流减少,门静脉直径减少,肝组织萎缩。肝硬化属于慢性疾病,早期肝硬化处于肝脏轻度损伤阶段,临床表现为乏力、腹胀、轻度黄疸等。中度至重度肝硬化处于失代偿期,会出现肝损伤及门静脉症临床症状,严重威胁患者生命健康。超声检查发现,肝硬化患者肝脏血流动力学与正常人明显不同,其原因可能是肝小叶内纤维组织和肝细胞增生挤压肝窦使之变窄或闭塞,导致门静脉血流进入肝小叶中央静脉受阻[8],最终导致门静脉高压。如何早期、准确、无创诊断肝硬化门静脉高压症对临床治疗及预防肝硬化及其并发症显得尤为重要。超声诊断肝硬化能较好显示肝包膜、肝实质回声及胆囊壁增厚情况,可定量检测门静脉、脾静脉血流,借助这些指标判断门静脉血流[9],从而反映肝损伤程度及门静脉高压症风险。MRI现已广泛用于诊断肝脏类疾病,包括肝癌、肝硬化等肝脏类实质性疾病。MRI电影相位计数能对整个心动周期的门静脉血流进行测量,PC辅助技术下心电门能计算瞬时血流量最大峰值血流、最小血流,且操作时间较短,有利于克服呼吸伪影,清晰显示血管边缘。严茂林等[10]研究发现,MRI检查能提升肝硬化门静脉高压症胃底静脉重度曲张伴胃肾分流检出率,明确肝功能分级,指导临床手术。
肝硬化门静脉高压症以门静脉血流动力学改变为主要特点,其原因众多,不同个体间的差异较大[11]。患者所处肝硬化时期不同,其病理变化及临床特征不同,影像学图像特征也不同。国外学者通过分析肝硬化患者的门静脉血流情况判定患者肝硬化分级、是否出现门静脉高压症,措施包括超声、CT及MRI[12]。本研究结果显示,MRI诊断阳性率及准确率分别高于超声诊断,认为MRI在判断肝硬化患者是否出现门静脉高压症上价值高于超声诊断。肝硬化时患者肝小叶塌陷,弥漫性纤维隔形成及肝实质结节增生,使得门静脉血管扭曲、减少。门静脉血流受到机械性阻塞,门静脉阻力增加是门静脉高压症形成的主要因素。MRI扫描完成后通过重建4排图像显示门静脉解剖,门静脉呈高信号,信号均匀,边界清晰,主要血流减少,门静脉向心血流为低信号,离心血流则为高信号。流速分析软件结果显示,伴有门静脉高压症的肝硬化患者整个心动周期的血流速度减慢,平均血流明显减少。超声相较MRI而言功能较少,诊断肝硬化门静脉高压症主要通过血液流动力学改变,缺少必要的图像及信号处理功能,判断结果主要依靠医生自身经验,影响诊断准确性。MRI横断面能显示肝硬化患者静脉被动充血情况,若图像出现内径明显增宽、截面积明显增大,提示门静脉高压症。另有研究认为门静脉血流非常复杂,不同阶段的血流速度变化可能高于或低于正常门静脉流速,因此超声不能很好诊断门静脉高压症,而MRI能准确识别门静脉代偿期,综合横断面血管图像判断。
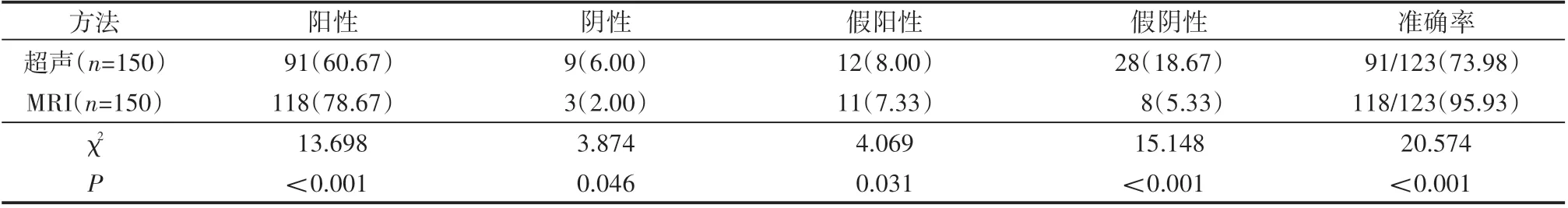
表1 超声与MRI诊断肝硬化门静脉高压症结果比较 例(%)
综上所述,超声及MRI均能反映肝硬化患者门静脉血流动力学,有利于临床判断肝硬化门静脉高压症,其中MRI诊断肝硬化门静脉高压症准确性较优,能在复杂环境下识别门静脉直径及横断面,建议使用。

