安罗替尼联合伊立替康二线治疗小细胞肺癌的临床疗效及安全性
吕艺华,赵子龙,黄革红,巴雅尔,杜伟,高辉,张美云△
小细胞肺癌(SCLC)是一种高度恶性的神经内分泌肿瘤,约占所有肺癌的15%[1]。SCLC 患者预后不佳,5年生存率低于5%,且未接受任何积极治疗的患者平均总生存期仅为2~4 个月[2]。依托泊苷联合铂类等一线化疗方案具有较高的缓解率,但易发生远处转移和获得性耐药,二线方案伊立替康联合顺铂则易出现骨髓抑制、腹泻等严重不良反应[3]。安罗替尼是一种高选择性、有效的表皮生长因子受体(EGFR)酪氨酸激酶抑制剂,常用于成人非小细胞肺癌和晚期胰腺癌的治疗[4];但目前关于安罗替尼二线治疗SCLC 的研究较少。本研究通过探讨安罗替尼联合伊立替康二线治疗SCLC 的临床疗效及对血清血管内皮生长因子(VEGF)、多效生长因子(PTN)、可溶性死亡受体5(sDR5)的影响,从而为临床治疗提供理论依据。
1 对象与方法
1.1 研究对象 采用前瞻性研究,选取2018 年3 月—2019年10 月包头市肿瘤医院诊治的一线治疗失败的82 例SCLC患者作为研究对象,按照随机数字表法分为对照组(41例)和研究组(41例)。纳入标准:(1)年龄>18岁。(2)病理明确诊断为SCLC。(3)患者经一线治疗失败,且一线治疗未应用安罗替尼和伊立替康。(4)距一线治疗结束时间>60 d。(5)预计生存时间≥3个月。(6)美国东部肿瘤协作组功能(ECOG)评分0~3分。排除标准:(1)精神障碍或拒绝配合治疗者。(2)合并其他原发肿瘤者。(3)伴有严重肝、肾、心功能损伤的基础疾病者。本研究经医院伦理委员会批准,所有研究对象或家属均知情同意。研究组和对照组年龄、性别、吸烟史、ECOG 评分、诊断分期、胸部放疗、转移灶数目、淋巴细胞计数、脑转移、一线治疗方案等资料比较差异无统计学意义(P>0.05),具有可比性,见表1。
1.2 方法
1.2.1 治疗方法 所有对象均给予止吐、保护胃黏膜等常规治疗。对照组在常规治疗的基础上给予伊立替康(江苏恒瑞医药股份有限公司,国药准字:H20040711,规格100 mg),第1 天、第8 天静脉滴注60 mg/m2;研究组在对照组基础上给予安罗替尼(正大天晴药业集团股份有限公司,国药准字:H20180004,规格12 mg),口服12 mg/次,每天1 次,连服2 周后停药1 周。21 d 为1 个周期,每治疗2 个周期进行疗效评价,计划治疗6个周期。
1.2.2 疗效评价及不良反应 治疗2 个周期后,由2 名临床医生按照实体肿瘤疗效评价标准1.1版[5]对患者的临床疗效进行评价。临床疗效分为完全缓解(CR)、部分缓解(PR)、稳定(SD)和进展(PD)。CR:肿瘤完全消失,无新病灶出现,至少维持1 个月。PR:肿瘤最大直径减少≥30%,至少维持1 个月。PD:肿瘤最大直径增加≥20%,或出现新病灶。SD:肿瘤最大直径减少未达PR,或增大未达PD。疾病控制率(DCR)=(CR+PR+SD)/总病例数×100%;客观缓解率(ORR)=(CR+PR)/总病例数×100%。根据美国国家癌症中心制定的通用不良反应分级(CTCAE)4.0[6]评价血液学和非血液学Ⅲ级以上不良反应,主要包括肝功能损伤、胃肠道反应、乏力、粒细胞减少、血小板减少、贫血等。

Tab.1 Comparison of clinical data between the two groups of patients表1 2组患者临床资料比较 (n=41,例)
1.2.3 血清指标检测 分别于治疗前、治疗4个周期后采集空腹静脉血2~3 mL,3 000 r/min 离心10 min,吸取血清,采用酶联免疫吸附测定(ELISA)法检测血清VEGF、PTN 和sDR5水平,试剂盒购自上海江莱生物科技有限公司,严格按照相应试剂盒的检测说明书进行操作。
1.2.4 随访 出院后通过电话、门诊等方式随访,从开始治疗随访12个月,终点事件为患者死亡或随访截止时间。记录患者无进展生存时间(PFS)和总生存时间(OS)。
1.3 统计学方法 采用SPSS 22.0 软件进行数据分析,符合正态分布的计量资料采用均数±标准差()表示,组间比较采用独立样本t检验;同组治疗前后的比较采用配对样本t检验。计数资料采用例(%)表示,组间比较采用χ2检验。采用Kaplan−Meier 法绘制生存曲线,比较 2 组 PFS 和 OS 的差异。检验水准α=0.05。
2 结果
2.1 2组临床疗效的比较 研究组和对照组分别治疗(5.90±0.37)和(5.78±0.61)个周期,治疗后研究组ORR(χ2=4.038)和 DCR(χ2=4.556)均高于对照组,见表2。

Tab.2 Comparison of clinical efficacy between the two groups of patients表2 2组患者临床疗效比较 例(%)
2.2 2组PFS和OS比较 研究组和对照组中位PFS分别为5 个月和3 个月,差异有统计学意义(Log−rankχ2=7.752,P<0.01);中位 OS 分别为 9 个月和 7个月,差异无统计学意义(Log−rankχ2=3.701,P>0.05),见图1。

Fig.1 Comparison of progression free survival curves between study group and control group图1 研究组和对照组SCLC患者无进展生存曲线和总生存曲线
2.3 2 组治疗前后血清 VEGF、PTN 和 sDR5 水平比较 治疗前,2 组患者血清 VEGF、PTN 和 sDR5 水平比较差异无统计学意义(P>0.05);治疗后,2组血清VEGF、PTN 和sDR5 水平较治疗前降低(P<0.01),且研究组VEGF、PTN 和sDR5 水平低于对照组(P<0.05),见表3。
Tab.3 Comparison of serum VEGF,PTN and sDR5 levels before and after treatment between the two groups表3 2组治疗前后血清VEGF、PTN和sDR5水平比较(n=41,)

Tab.3 Comparison of serum VEGF,PTN and sDR5 levels before and after treatment between the two groups表3 2组治疗前后血清VEGF、PTN和sDR5水平比较(n=41,)
*P<0.05,**P<0.01;t1为配对t检验,t2为独立样本t检验
t1组别对照组研究组t2 VEGF(ng/L)治疗前602.86±283.59 619.24±227.63 0.288治疗后499.10±266.58 377.46±197.33 2.348*9.591**11.670**t1组别对照组研究组t2 PTN(μg/L)治疗前566.03±57.92 574.72±52.99 0.708治疗后382.58±39.48 305.62±34.71 9.737**17.086**25.608**t1组别对照组研究组t2 sDR5(ng/L)治疗前20.01±5.47 19.21±6.03 0.629治疗后14.45±3.43 11.88±4.07 3.092**5.670**6.428**
2.4 2组不良反应发生率比较 2组肝功能损伤、胃肠道反应、乏力、粒细胞减少、血小板减少和贫血等不良反应发生率差异均无统计学意义(P>0.05),见表4。
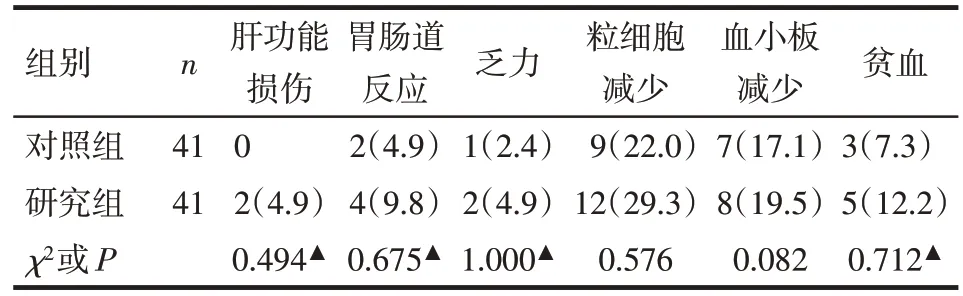
Tab.4 Comparison of grade Ⅲand above adverse reactions between the two groups表4 2组Ⅲ级及以上不良反应发生率比较 例(%)
3 讨论
SCLC 具有快速生长、早期转移、化疗耐药等特点,大多数SCLC患者在确诊时已出现肺外转移。尽管少数早期患者可以通过手术或联合放化疗治愈,但绝大多数患者预后较差,总生存率较低[7]。目前一线化疗的初始反应率较高,但多数患者短时间内出现复发或进展,因此二线治疗对于改善患者预后、延长生存时间至关重要[8]。目前临床上SCLC 患者二线治疗方案较多,但总体治疗效果较差,尚无标准的治疗方案。
肿瘤细胞的增殖、分化及迁移等过程与蛋白酪氨酸激酶(PTK)信号通路密切相关,通过干扰或阻断PTK信号通路能够抑制肿瘤细胞生长[9]。安罗替尼是我国自主研发的一种EGFR酪氨酸激酶抑制剂(TKI),不良反应小,在肝细胞色素P450(CYP)3A4和3A5 酶的作用下发生转化,通过抑制血管内皮生长因子受体(VEGFR)1~3、成纤维细胞生长因子受体(FGFR)1~4、血小板衍生生长因子受体(PDGFR)α/β 和原癌基因(c−Kit)等多个靶点,发挥抗肿瘤血管生成和抑制肿瘤生长的双重作用[10−11]。安罗替尼Ⅱ期和Ⅲ期临床试验显示其对软组织肉瘤[12]、肝内胆管细胞癌[13]和胃癌[14]患者具有良好的临床疗效。Han等[15]等通过对13个中心117例晚期非小细胞肺癌患者进行Ⅱ期临床研究,发现安罗替尼三线治疗非小细胞肺癌较安慰剂能有效延长患者中位PFS(4.8 个月vs.1.2 个月)和OS(9.3 个月vs.6.3 个月)。但是,目前安罗替尼在SCLC 患者中应用的研究尚少。伊立替康(CPT−11)是一种含有喜树碱的DNA拓扑异构酶Ⅰ抑制剂,通过干扰拓扑异构酶1β酶促进癌细胞死亡;同时还可以干扰DNA 的合成,最终导致肿瘤细胞死亡,临床上已将其作为SCLC二线治疗用药[16]。本研究发现,研究组 ORR、DCR 和 PFS均高于对照组,表明安罗替尼联合伊立替康二线治疗SCLC 患者具有较好的疗效。另外研究组Ⅲ级及以上不良反应主要表现为粒细胞减少、血小板减少、贫血和胃肠道反应,2 组不良反应发生率无明显差异,提示SCLC患者对安罗替尼联合伊立替康二线治疗的不良反应可耐受。
肿瘤的生长依赖于血管生成,VEGF 作为强效血管生成刺激因子,能够促进内皮细胞增殖和诱导血管生成,增加血管通透性,促进内皮细胞有丝分裂,影响细胞外基质;而且还可诱导纤溶酶原激活物及其抑制剂、组织因子和基质胶原酶的表达,促进血管生长[17]。另外,VEGF与血管异常增生有关,在肿瘤生长、发展和转移过程中发挥重要作用。研究发现通过抑制肺癌小鼠模型VEGF 的表达后,癌组织血管的形成明显受限,肿瘤体积缩小,生存时间延长[18−19]。PTN是一种对肝素具有高亲和力的分泌性生长因子,能够刺激神经干细胞、骨祖细胞和骨髓干细胞的分化,促进VEGF 表达,在肿瘤进展、血管生成和转移过程中起重要作用[20]。Xu等[21]发现SCLC患者血清PTN 水平显著升高,高水平PTN 患者总生存率较低,与SCLC 患者的预后不良密切相关。sDR5是一种Ⅰ型跨膜蛋白,属于肿瘤坏死因子受体超家族成员,在肿瘤细胞中高度表达,正常细胞低表达或不表达,而且可与其配体肿瘤坏死因子相关的凋亡诱导配体(TRAIL)结合,启动细胞内的信号转导,诱导细胞凋亡[22]。Wan 等[23]发现 SCLC 患者经化疗后血清sDR5水平较治疗前明显降低,可作为评价治疗效果和预后的标志物。本研究发现,SCLC患者治疗后血清VEGF、PTN 和sDR5 水平较治疗前明显降低,且研究组血清VEGF、PTN和sDR5水平明显低于对照组,提示安罗替尼联合伊立替康可有效降低 SCLC 患者血清 VEGF、PTN 和 sDR5 水平,从而抑制肿瘤细胞的转移及增殖,提高临床治疗效果。
综上所述,安罗替尼联合伊立替康二线治疗SCLC患者具有较好的疗效,可有效降低血清VEGF、PTN和sDR5水平,能够延长患者OS、PFS,安全性较好。但是,本研究样本量较小,且为单中心研究,存在一定的局限性,尚需增大样本量并进行多中心前瞻性研究安罗替尼联合伊立替康二线治疗SCLC 的临床价值及具体的作用机制。

