不同温度肠内营养液对胃癌根治术患者胃肠道并发症的影响
商文娟,曹勤洪
(江苏省中医院消化肿瘤外科,江苏 南京 210029)
胃癌是临床上常见的消化系统肿瘤之一,其常用的治疗方式为根治性手术,可有效切除肿瘤、控制病情,但术后因自身消化系统疾病及手术创伤,往往会出现不同程度的营养不良,不利于患者术后康复[1]。早期肠内营养是临床常用的营养支持方式,已逐渐被应用于胃癌根治术后,可有效改善患者营养代谢,促进其胃肠功能恢复,有利于减少胃肠道并发症,而适宜的营养液输注温度可提高营养支持效果[2-3]。但临床上关于胃癌根治术后肠内营养液的温度选择尚未统一标准且存在一定的争议,故选择合适的营养液温度是临床关注的热点。对此,本研究通过给予胃癌根治术患者不同温度肠内营养液进行肠内营养治疗,比较其对胃肠道并发症的影响,以期为临床提供参考,现报告如下。
1 资料与方法
1.1 资料来源
选取2018—2019年江苏省中医院(以下简称“我院”)收治的胃癌根治术患者180例。纳入标准:(1)均接受同一组医护人员实施的根治术且术后病理检查结果为胃癌;(2)均给予相同的肠内营养液,且营养液输入量及速度相同;(3)年龄>18岁,无精神病病史;(4)签署知情同意书。排除标准:(1)治疗前有腹胀、腹泻、呕吐及电解质紊乱等胃肠道并发症者;(2)术前有激素治疗、放化疗及免疫治疗等治疗史者;(3)有严重的心、肝、肾等疾病者;(4)有肠癌、肺癌及胰腺癌等其他恶性肿瘤者;(5)不耐受肠内营养支持者。依据随机数字表法分为低温组、体温组和高温组,每组60例。本研究经伦理委员会审批通过,低温组、体温组和高温组患者的一般资料相似,具有可比性,见表1。

表1 两组患者一般资料比较Tab 1 Comparison of general data between two groups
1.2 方法
低温组、体温组和高温组患者均参考中国抗癌协会肿瘤营养与支持治疗专业委员会发布的《胃癌患者营养治疗指南》[4],给予肠内营养治疗,即将液囊空肠导管经鼻插入胃内并经X线透视证实放置正确、固定后,术后第1日开始输注肠内营养混悬液(TPF)(规格:1 kcal/ml),第1日为250 ml/d,第2日为500 ml/d,第3日为750 ml/d,第4日为1 000 ml/d,第5~7日为1 500 ml/d,通过营养泵控制匀速泵入,速度均从20 ml/h开始逐渐递增至80 ml/h。将加温器夹持到一次性肠内营养输注器管外进行加热,其中低温组患者给予低于体温肠内营养液治疗,即将营养液加热至33.0~35.9 ℃;体温组患者给予接近体温内营养液治疗,即将营养液加热至36.0~38.0 ℃;高温组患者给予高于体温肠内营养液治疗,即将营养液加热至38.1~42.0 ℃(因临床上尚无统一标准,故依据既往研究报道及我院临床经验分组)[2]。
1.3 观察指标
观察三组患者胃肠激素水平、肠黏膜功能及胃肠道并发症发生情况。(1)胃肠激素:于治疗前及治疗3、7 d后抽取患者外周静脉血3 ml并分离血清(3 000 r/min,10 min)后,采用酶联免疫吸附法检测胃泌素(GAS)、胃动素(MTL)和胆囊收缩素(CCK)水平,试剂盒均购自广州易锦生物技术有限公司。(2)肠黏膜功能:于治疗前及治疗3、7 d后抽取患者外周静脉血3 ml并分离血清(3 000 r/min,10 min)后,采用分光光度法检测二胺氧化酶(DAO)、D-乳酸(D-LA)水平和乳果糖/甘露醇比值(L/M)。(3)胃肠道并发症:包括腹胀、腹泻、呕吐及电解质紊乱等[5]。
1.4 统计学方法

2 结果
2.1 两组患者治疗前后GAS、MTL和CCK水平比较
低温组、体温组及高温组患者治疗前的GAS、MTL和CCK水平比较,差异均无统计学意义(P>0.05);低温组、体温组及高温组患者治疗3、7 d后的GAS、MTL和CCK水平明显高于治疗前,体温组患者治疗3、7 d后的GAS、MTL和CCK水平明显高于低温组、高温组,上述差异均有统计学意义(P<0.05),见表2—4。
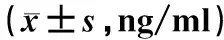
表2 两组患者治疗前后GAS水平比较Tab 2 Comparison of levels of GAS between two groups before and after treatment ng/ml)
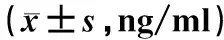
表3 两组患者治疗前后MTL水平比较Tab 3 Comparison of levels of MTL between two groups before and after treatment ng/ml)
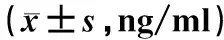
表4 两组患者治疗前后CCK水平比较Tab 4 Comparison of levels of CCK between two groups before and after treatment ng/ml)
2.2 两组患者治疗前后DAO、D-LA和L/M比较
低温组、体温组及高温组患者治疗前的DAO、D-LA和L/M水平比较,差异均无统计学意义(P>0.05);低温组、体温组及高温组患者治疗3、7 d后的DAO、D-LA和L/M水平明显低于治疗前,体温组患者治疗3、7 d后的DAO、D-LA和L/M水平明显低于低温组、高温组,上述差异均有统计学意义(P<0.05),见表5—7。
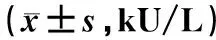
表5 两组患者治疗前后DAO水平比较Tab 5 Comparison of levels of DAO between two groups before and after treatment kU/L))

表6 两组患者治疗前后D-LA水平比较Tab 6 Comparison of levels of D-LA between two groups before and after treatment mg/L)

表7 两组患者治疗前后L/M比较Tab 7 Comparison of L/M between two groups before and after treatment
2.3 两组患者胃肠道并发症发生情况比较
体温组患者胃肠道并发症发生率为10.00%(6/60),明显低于低温组的33.33%(20/60)和高温组的26.67%(16/60),差异均有统计学意义(P<0.05),见表8。

表8 两组患者胃肠道并发症发生情况比较[例(%)]Tab 8 Comparison of gastrointestinal complications between two groups[cases(%)]
3 讨论
胃癌的病情危重、进展快,好发于中老年男性人群,受自身病情影响,患者常会出现不同程度的营养不良;根治性手术是胃癌的常用术式,因术中根治性切除胃部肿瘤及其周围病灶组织,会对胃肠组织造成严重的创伤,患者术后易因胃肠功能降低而出现胃排空延迟、肠麻痹延长等症状,不利于患者术后恢复[5-6]。
根据欧洲危重病医学会发布的《危重患者早期肠内营养指南》,肠内营养是指通过消化道使用较为全面的营养素进行营养支持治疗,早期开始肠内营养治疗可促进肠道激素合成和释放、激活肠道内分泌系统,有利于促进患者术后康复[7]。有研究结果显示,早期肠内营养已被应用于胃癌根治术后,有利于促进胃肠道蠕动及增强肠道机械和免疫屏障功能,对改善患者胃肠功能及防治胃肠道并发症具有积极的作用[8-9]。有文献报道,肠内营养的效果与营养液温度密切相关,在重型颅脑损伤患者肠内营养中,营养液温度控制在低温(22 ℃)有利于减少胃肠道应激性溃疡的发生[10]。也有研究结果显示,危重患者肠内营养温度以40~42 ℃为宜,可改善胃动力和肠屏障功能指标,有助于提高营养支持效果[11]。还有研究结果表明,肠道温度较接近机体内部温度(正常成年人温度为36.9~37.9 ℃,均值为37.5 ℃),提示将肠内营养液温度控制在适宜人体的温度可有效减少胃肠道不适[12-13]。
本研究结果显示,低温组、体温组及高温组患者治疗3、7 d后的GAS、MTL和CCK水平明显高于治疗前,体温组治疗3、7 d后的GAS、MTL和CCK水平明显高于低温组、高温组;低温组、体温组及高温组患者治疗3、7 d后的DAO、D-LA和L/M水平明显低于治疗前,体温组患者治疗3、7 d后的DAO、D-LA和L/M水平明显低于低温组、高温组,表明接近体温(36.0~38.0 ℃)的肠内营养液能够有效改善胃癌根治术患者胃肠激素及肠黏膜功能。MOT、GAS和CCK是机体主要的胃肠激素,在胃肠道动力中具有重要的作用,具有调节主细胞分泌胃蛋白酶原、胃强力收缩及小肠分节运动等作用,可反映胃癌根治术患者的胃肠功能状况[14-15]。DAO是肠黏膜上层绒毛中的细胞内酶,D-LA是肠道固有菌的代谢物,L/M是反映肠黏膜通透性的客观、准确的指标;肠道黏膜屏障功能受损时,可导致DAO、D-LA和L/M水平升高,故上述3个指标可反映胃癌根治术患者的肠黏膜功能状况[16-17]。因此,在胃癌根治术后早期肠内营养中,可能由于胃肠道对营养物质的吸收能力取决于消化酶的活性,而人体消化酶活性的最适温度相当于细胞最适生活环境的温度(36.9~37.9 ℃,均值为37.5 ℃)。低于体温(33.0~35.9 ℃)肠内营养液治疗的温度可能过低,会影响消化酶活性而使酶蛋白活性、酶反应速率降低,导致早期肠内营养支持治疗的效果降低,影响了其对胃癌根治术患者胃肠激素及肠黏膜功能的改善作用。高于体温(38.1~42.0 ℃)肠内营养液治疗的温度可能过高,会引起消化酶变性而降低了其活性,使酶反应速率降低,影响了早期肠内营养支持治疗的效果,从而降低了胃癌根治术患者胃肠激素及肠黏膜功能的改善效果。而采用接近体温(36.0~38.0 ℃)肠内营养液治疗则可能由于温度适宜,使消化酶处于适宜的催化活性温度而能够更好地协助肠道吸收营养,从而达到较为良好的早期肠内营养支持治疗效果,更好地改善患者胃肠激素及肠黏膜功能。
此外,本研究结果发现,体温组患者胃肠道并发症发生率明显低于低温组、高温组,表明接近体温(36.0~38.0 ℃)肠内营养液能够有效减少胃癌根治术患者胃肠道并发症的发生,与既往研究中控制适宜肠内营养液温度可减少患者胃肠道并发症的结论相似[18]。这可能是由于接近体温(36.0~38.0 ℃)肠内营养液能够使胃癌根治术患者肠道内消化酶处于高活性的温度,更好地促进了肠道激素合成和释放、激活肠道内分泌系统并改善了肠黏膜功能,有利于促进胃肠道蠕动及增强肠道机械和免疫屏障功能,从而促进患者胃肠功能恢复,有利于减少腹胀、腹泻、呕吐和电解质紊乱等胃肠道并发症发生[19-20]。同时,肠内营养液温度过高易损伤胃肠黏膜、影响消化功能而导致腹泻,腹泻则易引起脱水而导致电解质紊乱;肠内营养液温度过低则易引起胃肠痉挛、肠蠕动增强而致恶心呕吐、腹胀和腹泻等胃肠功能紊乱症状;肠内营养液接近体温(36.0~38.0 ℃)则能够有效减少温度过高或过低对胃癌根治术患者肠道的不良影响,从而进一步减少腹胀、腹泻、呕吐和电解质紊乱等胃肠道并发症发生。
综上所述,接近体温(36.0~38.0 ℃)肠内营养液可有效改善胃癌根治术患者胃肠激素及肠黏膜功能,有利于减少胃肠道并发症。

