α-Fe2O3与活性炭协同处理尿液废水的过程优化与吸附特性
焦赟仪,周书葵,张良长,艾为党,康赛,李晨璐,郑利兵,魏源送
(1 中国科学院生态环境研究中心环境模拟与污染控制国家重点联合实验室,北京100085;2 中国科学院生态环境研究中心水污染控制实验室,北京100085;3 南华大学土木工程学院,湖南衡阳421001;4 中国航天员训练中心人因工程重点实验室,北京100094)
废水的处理与资源回收已成为水处理领域的重要命题[1],其中,尿液作为一种富含丰富营养元素的废水资源,其处理与回收受到广泛关注[2]。一方面,尿液中含有高浓度的P,其体积比不到城市生活污水的1%,但贡献的P占生活污水的50%[3]。传统的处理方式将其汇入污水处理厂集中处理,不仅增加了污水处理厂的负荷与能耗,还复杂了P的处理与回收[4]。另一方面,尿液中含有大量有机物,包括残留药物和内分泌干扰物,且易滋生致病微生物,在作为肥料资源回用的过程中将对土壤和地下水资源带来污染[5]。特别的是,在载人航天等特殊环境中,尿液废水的循环利用与营养盐的回收对维持宇航员的生命活动与保障长期航天任务至关重要[6]。因此,开发高效的尿液处理与资源回收技术具有重要意义。
现有的尿液处理技术主要有化学沉淀法[7]、电化学法[8]、吸附法[9]、膜分离技术[10]等,其中吸附法因其操作简单、处理效率高而被广泛应用。目前,用于尿液处理的主要吸附材料包括活性炭、金属氧化物、树脂等,其中,活性炭材料经济环保、比表面积大且吸附位点丰富,能够有效去除尿液中有机物、药物类污染物及代谢产物[9,11],但是对P 没有明显的吸附效果[12]。而近年来被广泛关注的铁基吸附材料对P 具有较好的吸附作用[11,13],但是其比表面积低,对尿液中其他物质的吸附能力有限。针对以上问题,铁氧化物与活性炭协同吸附是提高尿液处理效率的简便易行的方法,本文作者课题组前期研究[11]已表明铁氧化物能够促进活性炭对P 的吸附,但铁氧化物与活性炭协同吸附P和有机物的过程及主要作用机制尚不明确,在尿液处理相关的研究中尚未报道,因此,协同吸附特性仍需进一步探讨。

1 材料与方法
1.1 实验材料
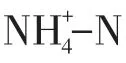
1.2 吸附实验
向新鲜尿液中投加一定量的椰壳活性炭、α-Fe2O3,放入振荡培养箱中使吸附剂与尿液充分接触,温度为25℃,转速为150r/min,吸附时间为24h 以实现吸附平衡,取上清液过0.45μm 膜并进行检测分析。每组实验进行3次平行实验。
1.2.1 铁炭质量比的影响
投加1g活性炭至25mL尿液中,分别投加不同质量的α-Fe2O3(铁炭质量比为0.2、0.4、0.6、0.8、1)进行吸附。

图1 活性炭形貌、孔径分布及尿液有机组成
1.2.2 吸附剂投加量影响
投加活性炭1g、2g、4g、5g、6g、8g,分别投加α-Fe2O3与活性炭质量比为0.6 的α-Fe2O3于100mL尿液中进行吸附。
1.2.3 吸附等温线
分别稀释尿液1 倍、1.25 倍、1.67 倍、2.5 倍、5 倍、10 倍,投加4g 活性炭和2.4g α-Fe2O3于不同浓度的100mL 尿液中进行吸附。载人航天密闭空间中为了长时间储存尿液通常对尿液进行加酸预处理,因此本研究设置尿液酸预处理组,即在尿液样品中加浓硫酸至pH为2,其余操作重复以上步骤。
1.2.4 吸附动力学
投加4g活性炭和2.4g α-Fe2O3于100mL尿液中进行吸附实验,每隔5min、15min、30min、1h、2h、3h、4h、6h、8h、10h、22h、24h 的时间进行取样。设置尿液酸预处理组重复以上实验步骤。
1.3 测试方法
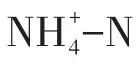
溶液中CDOM 采用三维激发-发射荧光光谱仪(3DEEM;F-7000,日本日立公司)测定。采用荧光区域积分法(FRI 方法)[14]分析尿液CDOM 的分布特征及活性炭吸附效果,将荧光图谱分为Ⅰ、Ⅱ、Ⅲ、Ⅳ、Ⅴ区5个区域,分别对应酪氨酸类芳香蛋白质、色氨酸类芳香蛋白质、富里酸类物质、可溶性微生物代谢产物、腐殖酸类物质,通过FRI法积分公式[15]对尿液中有机物质进行定量计算。同时,根据3DEEM 结果计算荧光指数(fluorescence index,FI)、生物指数(biological index,BIX)和腐殖化指数(humification index,HIX)[16]。
1.4 吸附等温线与吸附动力学
采用Langmuir 模型、 Freundlich 模型和Redlich-Peterson 模型对吸附等温线数据进行拟合并分析其吸附机理。Langmuir模型假定在吸附剂表面发生均相吸附[17],吸附质分子间不发生相互作用,该等温线用于解释在活性位点上发生单分子层吸附。Freundlich 模型假定吸附剂表面发生不同吸附质分子的作用或不同表面形貌、基团种类、数量和分布位置不同的异质吸附[18],用于解释吸附到活性位点附近的离子发生多位分子相互作用,吸附质在吸附剂表面形成多层吸附。Redlich-Peterson 模型综合了Langmuir和Freundilich模型,被广泛用于均相和非均相吸附体系,该模型假设吸附过程同时发生单层吸附和多位分子间相互作用[17]。3 种模型表达式见式(1)~式(3)。

式中,qe为吸附平衡时的吸附量,mg/g;qmax为最大吸附容量,mg/g;KL为Langmuir 吸附常数,L/mg;Ce为吸附平衡时的浓度,mg/L;Kf为与吸附容量相关的Freundlich 常数,(mg·g-1)·(L·mg-1)1/n;1/n为与表面不均匀性相关的Freundlich常数,其值越小则吸附性能越好,1/n在0.1~0.5 时容易吸附,大于2时则难以吸附;a和Kr为Redlich-Peterson 常数;g为0~1之间的值的指数。
采用准一级[式(4)]、准二级[式(5)]、Elocvich[式(6)]和颗粒内扩散模型[式(7)]对动力学数据进行拟合,并分析其吸附机理,qt和qe分别代表吸附剂在t时刻和吸附平衡时的吸附量。
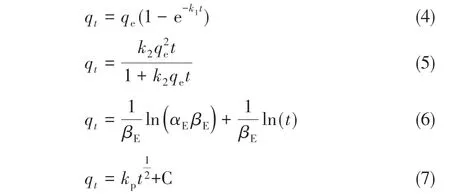
式中,qt和qe分别为吸附剂在t时刻和吸附平衡时的吸附量,mg/g;k1为准一级动力学模型的吸附平衡速率常数,min-1;k2为准二级动力学模型的吸附平衡速率常数,min-1;α为初始吸附速率,mg/(g∙min);βE为表面覆盖度和活化能相关的常数,g/min;K为颗粒内扩散速率常数;t为反应时间,min;C为与边界层厚度相关的值。
2 结果与讨论
2.1 铁炭比对吸附的影响
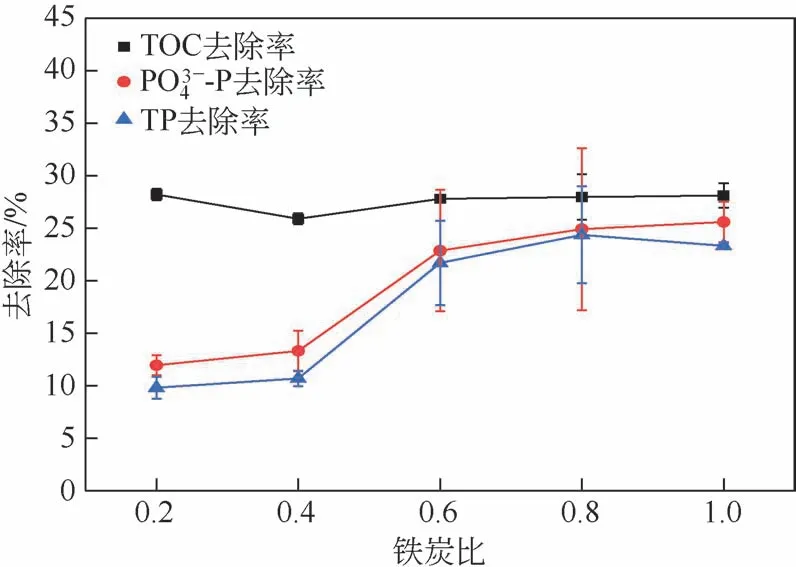
图2 铁炭比对尿液TOC、TP和PO-P去除的影响
2.2 投加量对吸附的影响
图3对比了活性炭不同投加量下,活性炭单独吸附和α-Fe2O3与活性炭协同吸附(铁炭比为0.6)对尿液的处理效果。由图3(a)可知,两组吸附实验中TOC 去除率基本一致,当活性炭投加量为1~4g时,随活性炭的增加,TOC去除率迅速上升。活性炭投加量为4g 时,活性炭对TOC 的去除率为39.22%,协同吸附对TOC 的去除率为39.51%,仅比单独活性炭吸附提高0.29%,这表明α-Fe2O3对TOC去除效果影响较小,TOC去除的主要机制为活性炭的吸附作用,与2.1 节结论一致。当活性炭投加量大于4g 时,TOC 去除率增加速率降低,投加量为8g 时,单独吸附与协同吸附对TOC 去除率为47.31% 和46.99%,去除率分别增加8.09% 和7.45%。这是由于当污染物初始浓度和体积恒定时,随吸附剂投加量的增加,单位质量的吸附剂对污染物的吸附量将减少。
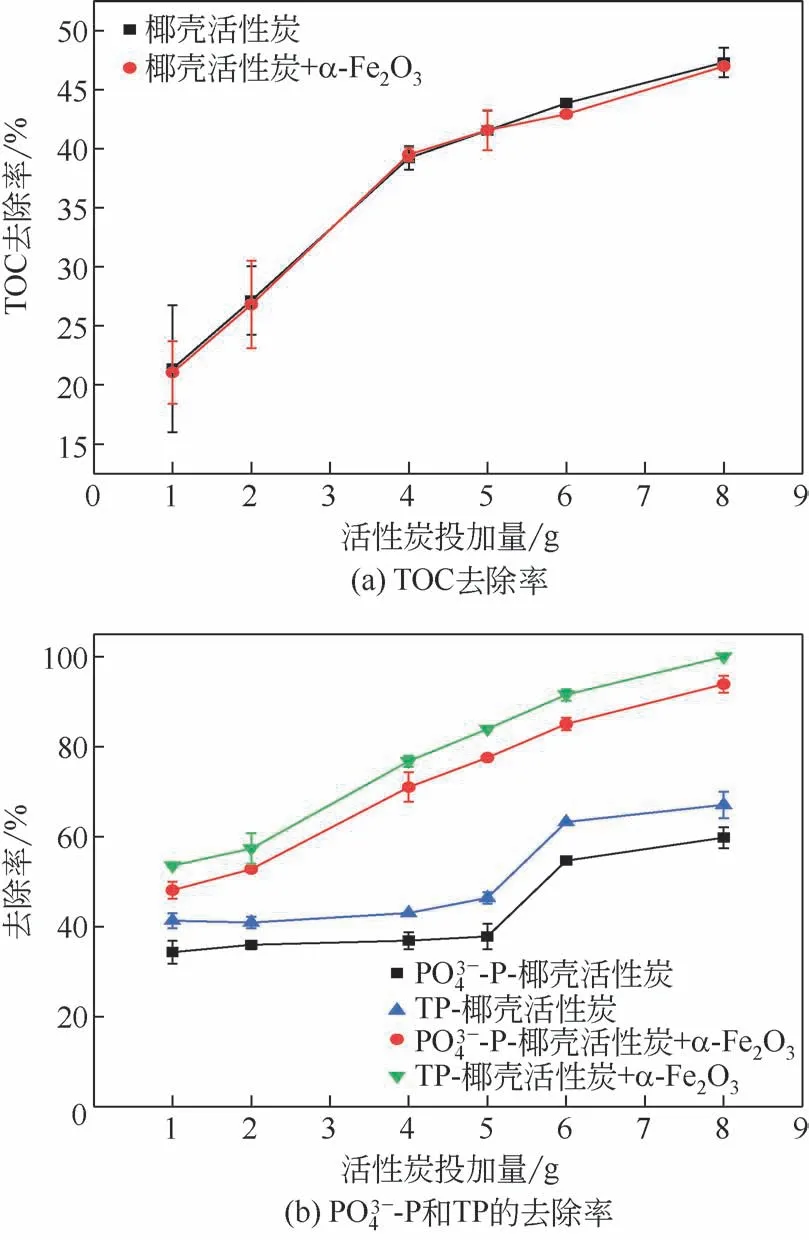
图3 投加量对TOC、TP和PO-P去除的影响
2.3 吸附等温线
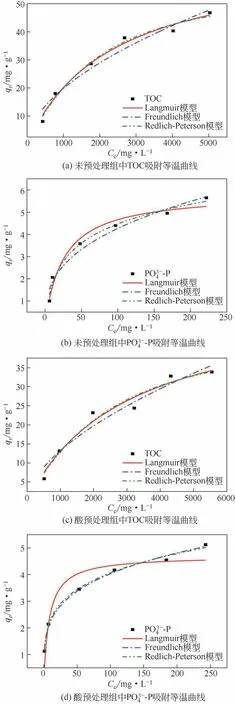
图4 吸附剂对TOC和PO-P 的吸附等温线拟合
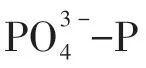
表1 TOC和PO-P吸附等温线模型吸附参数及相关系数
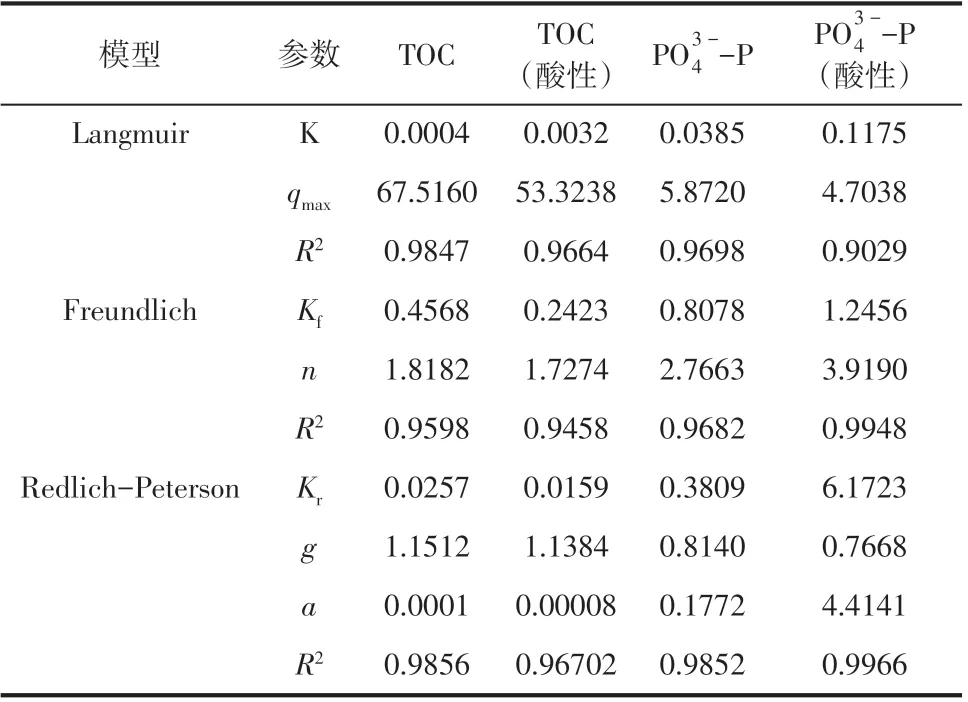
表1 TOC和PO-P吸附等温线模型吸附参数及相关系数
模型Langmuir参数PO3-4 -P PO3-4 -P K qm ax Freundlich Redlich-Peterson R2 Kf n R2 Kr g a R2 TOC 0.0004 67.5160 0.9847 0.4568 1.8182 0.9598 0.0257 1.1512 0.0001 0.9856 TOC(酸性)0.0032 53.3238 0.9664 0.2423 1.7274 0.9458 0.0159 1.1384 0.00008 0.96702 0.0385 5.8720 0.9698 0.8078 2.7663 0.9682 0.3809 0.8140 0.1772 0.9852(酸性)0.1175 4.7038 0.9029 1.2456 3.9190 0.9948 6.1723 0.7668 4.4141 0.9966
2.4 吸附动力学
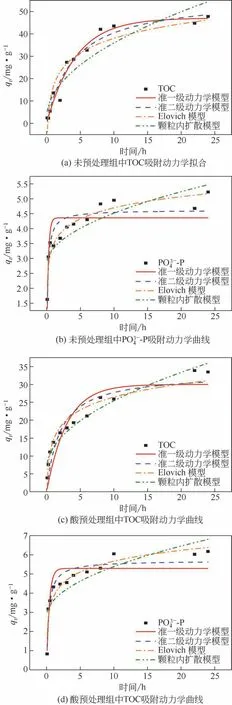
图5 吸附剂对TOC和PO-P的吸附动力学拟合
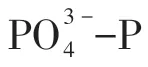
表2 TOC和PO-P的吸附动力学模型吸附参数及相关系数
表2 TOC和PO-P的吸附动力学模型吸附参数及相关系数
模型准一级动力学模型参数PO3-4 -P PO3-4 -P k1 qe R2准二级动力学模型Elovich模型k2 qeR2αβR2颗粒内扩散模型kp C R2 TOC 0.2315 47.0908 0.9697 0.0044 56.7022 0.9608 54.2731 0.1068 0.8968 10.6292 2.3401 0.8685 TOC(酸性)0.3341 29.9960 0.8167 0.0153 33.1784 0.9004 82.2303 0.1910 0.9546 6.0469 6.3054 0.9569 4.3485 4.3600 0.7207 1.2542 4.6190 0.8513 342.1035 1.8654 0.9147 0.5487 2.7825 0.7199(酸性)2.5223 5.2882 0.8357 0.5601 5.6938 0.9134 85.9608 1.2283 0.9220 0.8195 2.7906 0.7018
2.5 CDOM的去除效果
原尿液三维荧光图谱如图1(c)所示,在Ⅰ、Ⅱ、Ⅲ、Ⅳ区分别主要存在4 个较强烈的特征荧光峰A(Ex/Em=205/300)、B(Ex/Em=220/360)、C(Ex/Em=220/380)、D(Ex/Em=275/370),表明尿液中酪氨酸类芳香蛋白质、色氨酸类芳香蛋白质、富里酸类物质、可溶性微生物代谢产物的含量较高,同时区域Ⅴ还存在面域较广的腐殖酸类物质。由于尿液中含有尿酸、肌酐等蛋白质类有机物,且易滋生细菌[23],因此呈现出较明显的蛋白类有机物和可溶性微生物代谢产物的荧光。由图6可看出,吸附后的尿液中有机物污染物荧光强度随吸附时间的增加而降低,前1h 阶段荧光强度快速下降,即有机污染物的去除主要发生在初期吸附阶段,6h 后吸附剂吸附量逐渐达到饱和,因此后期荧光强度变化差异较小,这与TOC吸附动力学过程相一致。表3为不同时间段尿液的荧光区域积分标准体积,荧光区域标准体积越高代表污染物含量越高,从表3可知经24h吸附处理,未预处理尿液Ⅰ、Ⅱ、Ⅲ、Ⅳ、Ⅴ区域标准体积分别下降46.90%、65.69%、73.26%、74.60%、77.03%,总积分标准体积下降72.16%,表明经过α-Fe2O3协同活性炭吸附对五类有机物均有较好的吸附效果,对Ⅴ区域中腐殖酸类物质的吸附效果最佳。
经过24h的吸附平衡,酸预处理尿液吸附实验组中总荧光区域积分标准体积为2115119au∙nm2,高于未预处理尿液总荧光区域积分标准体积1938751au∙nm2,有机物质的去除率减少2.37%,同样验证了酸预处理不利于α-Fe2O3协同活性炭对有机物的吸附,这与前期结论一致。酸预处理尿液经过吸附后相对于原尿液Ⅰ、Ⅱ、Ⅲ、Ⅳ、Ⅴ区域标准体积分别下降36.71%、60.95%、72.04%、69.87%、77.96%、71.64%。相对于未预处理组,酸性条件下Ⅰ区、Ⅱ区和Ⅳ区的污染物去除率分别下降10.19%、4.74%和4.73%,表明酸预处理不利于α-Fe2O3协同活性炭对酪氨酸类芳香蛋白质、色氨酸类芳香蛋白质和可溶性微生物代谢产物的吸附。荧光指数FI 通常表征物质的来源,从表3 可知,尿液中FI 均大于1.8,表明溶解性荧光有机物主要以自生源为主。原尿液和吸附处理后的尿液BIX 均大于1,并随时间的增长而增大,表明收集的尿液存在微生物生长,同时微生物活性随着吸附时间的增长而增加。HIX反应了尿液中腐殖质的含量及腐殖化程度,原尿液HIX为0.36,表明尿液中存在部分芳香性物质[24]。经过活性炭吸附和酸预处理后的吸附平衡,原尿液HIX均呈现下降趋势,表明活性炭吸附能够减少腐殖质类物质,与总荧光区域积分标准体积计算结果一致。
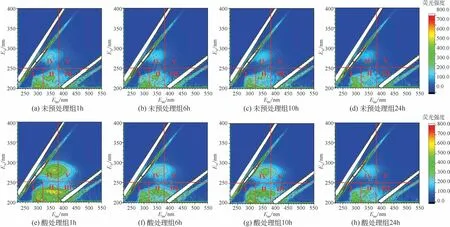
图6 吸附后尿液中有机物组成
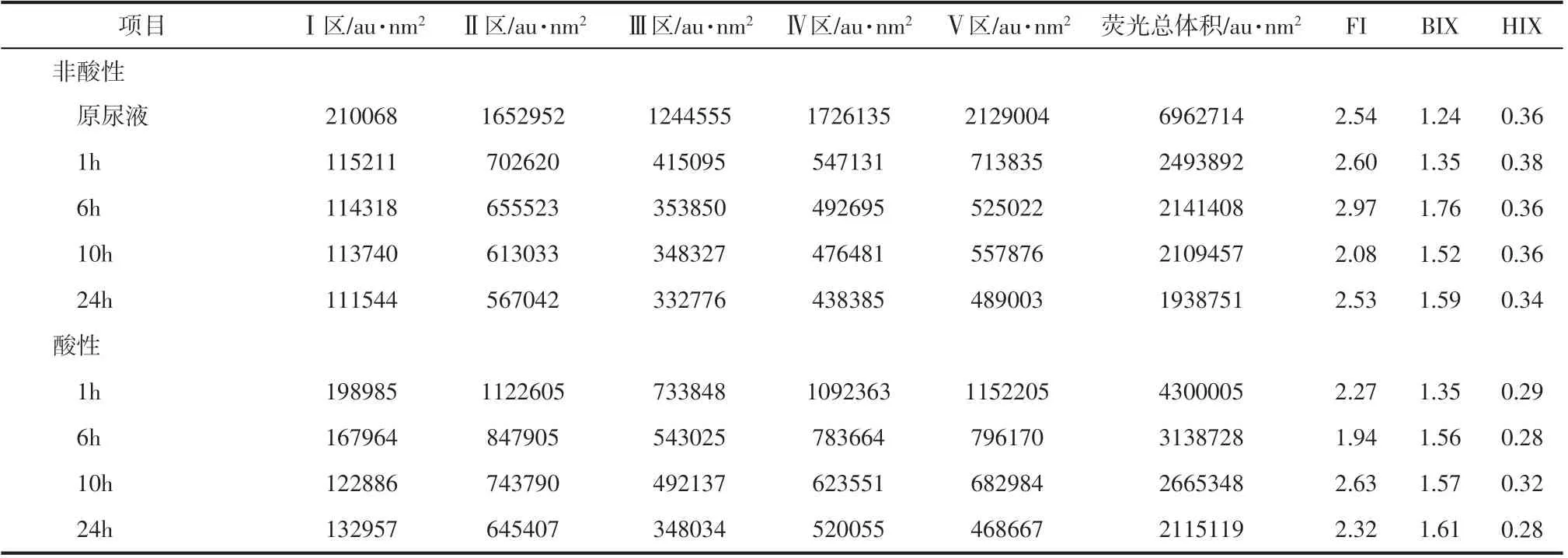
表3 尿液荧光区域积分标准体积及荧光指数
2.6 SEM-EDS
原活性炭表面疏松,具有多条并列的孔道结构,孔道内壁有丰富的微孔[图1(a)],经BET 测定其表面积为566.52m2/g,总孔体积为0.294cm3/g,从图1(b)的活性炭孔径分布图可知,活性炭孔径以微孔为主,微孔容积占总孔容积的82.81%,表明活性炭本身具有良好的吸附性能。从图7 可看出,α-Fe2O3与活性炭协同吸附尿液后,在活性炭表面及孔道内附着多种颗粒状固体,采用EDS-Mapping扫描分析其表面元素组成可知,表面物质主要有N、P、K、Ca、Mg、S、Fe 和O,表明吸附过程存在多种物质被同时吸附。由图7可知活性炭表面的N、P、Mg分布一致,推测表面沉积了大量磷酸铵镁(MgNH4PO4∙6H2O)晶体[20],表面还附着含量分别2%、3%和4%的Ca、K、S,沉积的物质可能为羟磷灰石[Ca10(PO4)6(OH)2]、方解石(CaCO3)以及钾盐和硫酸盐等晶体[25],表明无机盐沉积是去除P、Ca、Mg 等盐离子的主要机制之一。此外,图中Fe、O、P 的分布表现出高度的一致性,且重叠部分具有更高的荧光强度,推测生成了磷酸铁盐[13],表明P 与α-Fe2O3表面的羟基结合形成磷酸铁盐沉积可能是去除P的另一个重要机制[11]。因此,结合α-Fe2O3对P吸附的强化及P的吸附动力学特征,可以推断α-Fe2O3与P 反应后产生的盐类共沉淀是P吸附的机制之一。

图7 α-Fe2O3与活性炭协同吸附尿液后的形貌及元素分布图
3 结论
本研究采用α-Fe2O3与活性炭协同吸附处理尿液,开展过程优化与吸附机理研究,主要结论如下。
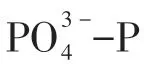
(4)协同吸附对尿液中CDOM类有机物有较好的去除效果,去除率可达72.16%。其中酪氨酸类芳香蛋白质、色氨酸类芳香蛋白质、富里酸类物质、可溶性微生物代谢产物和腐殖酸类有机物质分别 减 少 46.90%、 65.69%、 73.26%、 74.60%、77.03%。酸预处理降低了酪氨酸类芳香蛋白质、色氨酸类芳香蛋白质和可溶性微生物代谢产物的吸附,同时降低吸附速率。
(5)P 的去除主要依靠于其与α-Fe2O3和尿液中无机盐的共沉淀作用,并以无机盐沉积的形式附着于活性炭孔道内。

