PVA/KHA/GG多孔水凝胶的制备及吸附性能研究
宋洁,韩星星,黄良仙,牛育华
(1.陕西科技大学 化学与化工学院,陕西 西安 710021;2.陕西农产品加工技术研究院,陕西 西安 710021)
染料与重金属离子不仅对水体、土壤的污染日益严重,而且对动植物及人类的生存造成巨大的威胁。亚甲基蓝是一种结构稳定又难以降解的阳离子染料,是染料废水污染的主要来源之一[1-2]。铅离子的毒性是重金属离子中毒性较大的一种,对人体的各系统和器官都有伤害[3-4]。吸附法因其操作简单、处理效率高、成本低廉,同时又不会产生二次污染而被广泛使用[5]。
水凝胶是一类具有轻交联度的三维网状聚合物材料。水凝胶良好的网络结构使其在水中溶胀却不溶解,吸附后的水凝胶与液相极易分离,能极大简化后续的分离工作,因此特别适合用于对染料和重金属离子废水的处理[6]。
1 实验部分
1.1 试剂与仪器
聚乙烯醇(PVA)、瓜尔胶(GG)、丙烯酸(AA)、氢氧化钠、过硫酸钾(KPS)、N,N′-二亚甲基双丙烯酰胺(MBA)、硝酸铅(Pb(NO3)2)均为分析纯;腐植酸钾(KHA),化学纯;亚甲基蓝(MB),指示剂。
UV-752型紫外可见分光光度计;AA-6880型原子吸收分光光度计;VECTOR-22型傅里叶红外光谱仪;S-4800型扫描电子显微镜。
1.2 PVA/KHA/GG水凝胶的制备
在装有冷凝管、搅拌器的250 mL 三口瓶中分别加入一定量10%(质量分数)的PVA溶液和3%(质量分数)的GG溶液,持续搅拌。然后,将适量的MBA、KPS和KHA分别溶于10 g蒸馏水中制得溶液,并将MBA溶液与10 g AA(中和度为60%)混合均匀。于一定温度下,将MBA与AA混合溶液和KPS溶液同时滴加入三口瓶中,控制在30 min滴加完。其中,在引发15 min时,将KHA溶液加入三口瓶中,反应3 h。待反应完全后倒出,用乙醇浸泡以除去未反应的单体和水,于60 ℃鼓风干燥箱中烘干,粉碎备用。
1.3 PVA/KHA/GG水凝胶的表征和测试
使用FTIR、XRD对合成原料和吸附前后的水凝胶的官能团和结晶形态变化进行测定,使用SEM对吸附前后的水凝胶的微观形貌进行观察。
1.4 吸附实验
1.4.1 MB吸附测试 向250 mL三口瓶中分别加入0.1 g吸附剂和50 mL初始浓度为500 mg/L的MB溶液,置于水浴温度为30 ℃的恒温振荡箱中。在反应一定时间后,离心取上层清液,用紫外可见分光光度计,在最大波长为664 nm处测定吸光度。根据式(1)计算吸附容量(Qt)。
(1)
式中C0——初始浓度,mg/L;
Ct——t时刻的浓度,mg/L;
V——溶液的体积,mL;
m——初始吸附剂的用量,mg。
1.4.2 Pb(Ⅱ)吸附测试 向250 mL三口瓶中分别加入0.1 g吸附剂和50 mL初始浓度为100 mg/L的MB溶液,置于水浴温度为30 ℃的恒温振荡箱中。在反应一定时间后,离心取上层清液,用原子吸收分光光度计测定吸光度,根据式(1)得出吸附容量(Qt)。
2 结果与讨论
2.1 聚合条件对PVA/KHA/GG水凝胶吸附MB、Pb(Ⅱ)性能的影响
2.1.1 PVA用量对吸附量的影响 在KHA为0.2 g,GG为10 g,KPS为0.08 g,MBA为0.04 g,聚合温度为65 ℃条件下,考察PVA用量对MB和 Pb(Ⅱ)吸附量的影响,结果见图1。
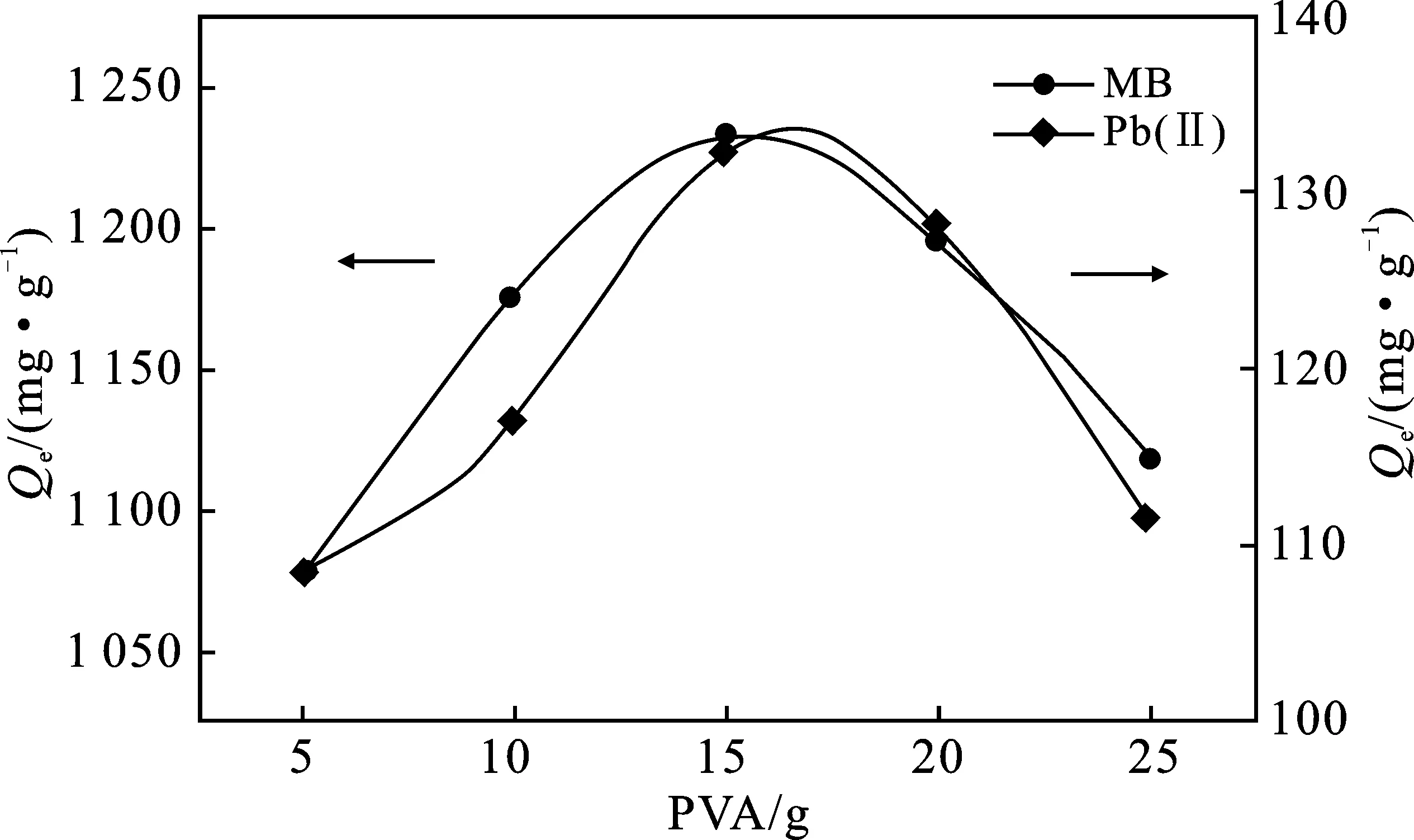
图1 PVA用量对吸附量的影响Fig.1 Effect of PVA dosage on adsorption capacity
由图1可知,随着PVA用量的增加,PVA/KHA/GG水凝胶对MB和Pb(Ⅱ)的吸附量均呈现先增加后降低的趋势,当PVA用量为15 g时,有最大吸附量。随着PVA用量的增加,引入大量的亲水性羟基,有利于水分子进入和对MB和Pb(Ⅱ)的吸附,直至达到最大吸附量。当PVA用量继续增加时,水凝胶中过多的羟基形成分子内氢键,不利于水分子的进入及对MB和Pb(Ⅱ)的吸附,进而吸附量降低[7]。因此,PVA用量15 g较合适。
2.1.2 GG用量对吸附量的影响 在PVA为15 g,KPS为0.08 g,MBA为0.04 g,聚合温度为65 ℃条件下,考察GG用量对MB和 Pb(Ⅱ)吸附量的影响,结果见图2。
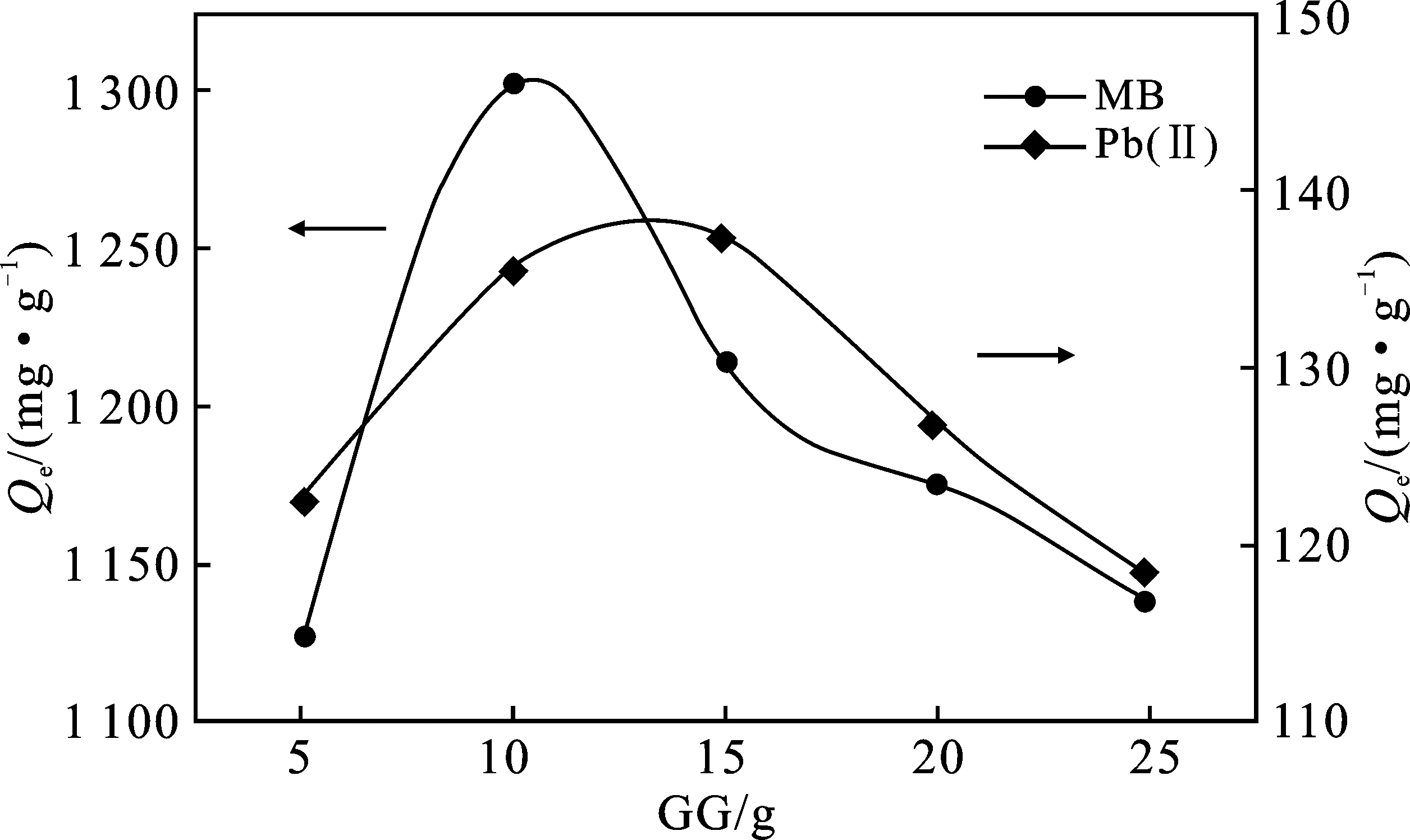
图2 GG用量对吸附量的影响Fig.2 Effect of GG dosage on adsorption capacity
由图2可知,随着GG用量的增加,PVA/KHA/GG水凝胶对MB和Pb(Ⅱ)的吸附量均呈现先增加后降低的趋势,当GG用量分别为10 g和15 g时,对MB和Pb(Ⅱ)有最大吸附量。随着GG用量的增加,引入大量的亲水性羟基,有利于水分子进入和对MB和Pb(Ⅱ)的吸附,直至达到最大吸附量。当GG用量过高时,体系黏度过大,引发效率降低,聚合物分子链中GG的接枝率降低,水凝胶对MB和Pb(Ⅱ)的吸附量降低。因此,GG用量分别为10 g和15 g较合适。
2.1.3 KHA用量对吸附量的影响 在PVA为15 g,GG为10 g,KPS为0.08 g,MBA为0.04 g,聚合温度为65 ℃条件下,考察KHA用量对MB和 Pb(Ⅱ)吸附量的影响,结果见图3。
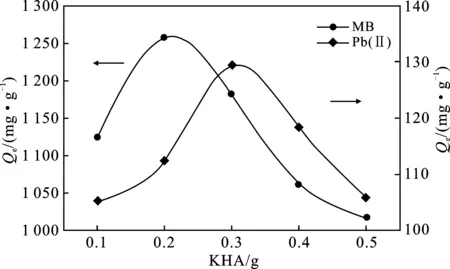
图3 KHA用量对吸附量的影响Fig.3 Effect of KHA dosage on adsorption capacity
由图3可知,随着KHA用量的增加,PVA/KHA/GG水凝胶对MB和Pb(Ⅱ)的吸附量均呈现先增加后降低的趋势,当KHA用量分别为0.2 g和0.3 g时,对MB和Pb(Ⅱ)有最大吸附量。随着KHA用量的增加,引入大量的羟基、氨基、羧基和苄基等活性基团,增加了对MB和Pb(Ⅱ)的吸附能力[8]。当KHA用量过高时,分子间位阻较大,不利于进一步的聚合,形成三维多孔结构,故对MB和Pb(Ⅱ)的吸附量降低。因此,KHA用量分别为 0.2 g 和0.3 g较合适。
2.1.4 KPS用量对吸附量的影响 在PVA为 15 g,GG为10 g,KHA分别为0.2 g和0.3 g,MBA为0.04 g,聚合温度为65 ℃条件下,考察KPS用量对MB和 Pb(Ⅱ)吸附量的影响,结果见图4。
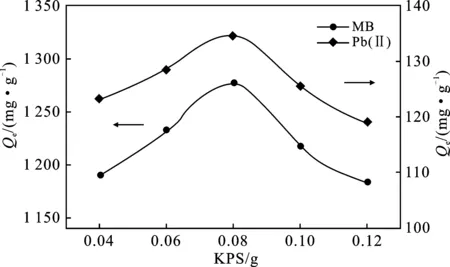
图4 KPS用量对吸附量的影响Fig.4 Effect of KPS dosage on adsorption capacity
由图4可知,随着KPS用量的增加,水凝胶对MB和Pb(Ⅱ)的吸附量逐渐增加,但当KPS用量超过0.08 g后,其对MB和Pb(Ⅱ)的吸附量逐渐降低。这是由于KPS用量较少时,引发产生的自由基较少,不利于聚合和交联反应的进行。随着KPS用量的增多,引发速率加快,反应速率增加,利于三维网络的形成,使得水凝胶的吸附性能增强。然而,当KPS用量过多时,在反应体系中自由基过多,致使聚合物的平均动力学链长降低,聚合物交联点间的分子质量过小,所得水凝胶的吸附性能变差。因此,KPS用量为0.08 g较合适。
2.1.5 MBA用量对吸附量的影响 在PVA为 15 g,GG为10 g,KHA分别为0.2 g和0.3 g,KPS为0.08 g,聚合温度为65 ℃条件下,考察MBA用量对MB和 Pb(Ⅱ)吸附量的影响,结果见图5。
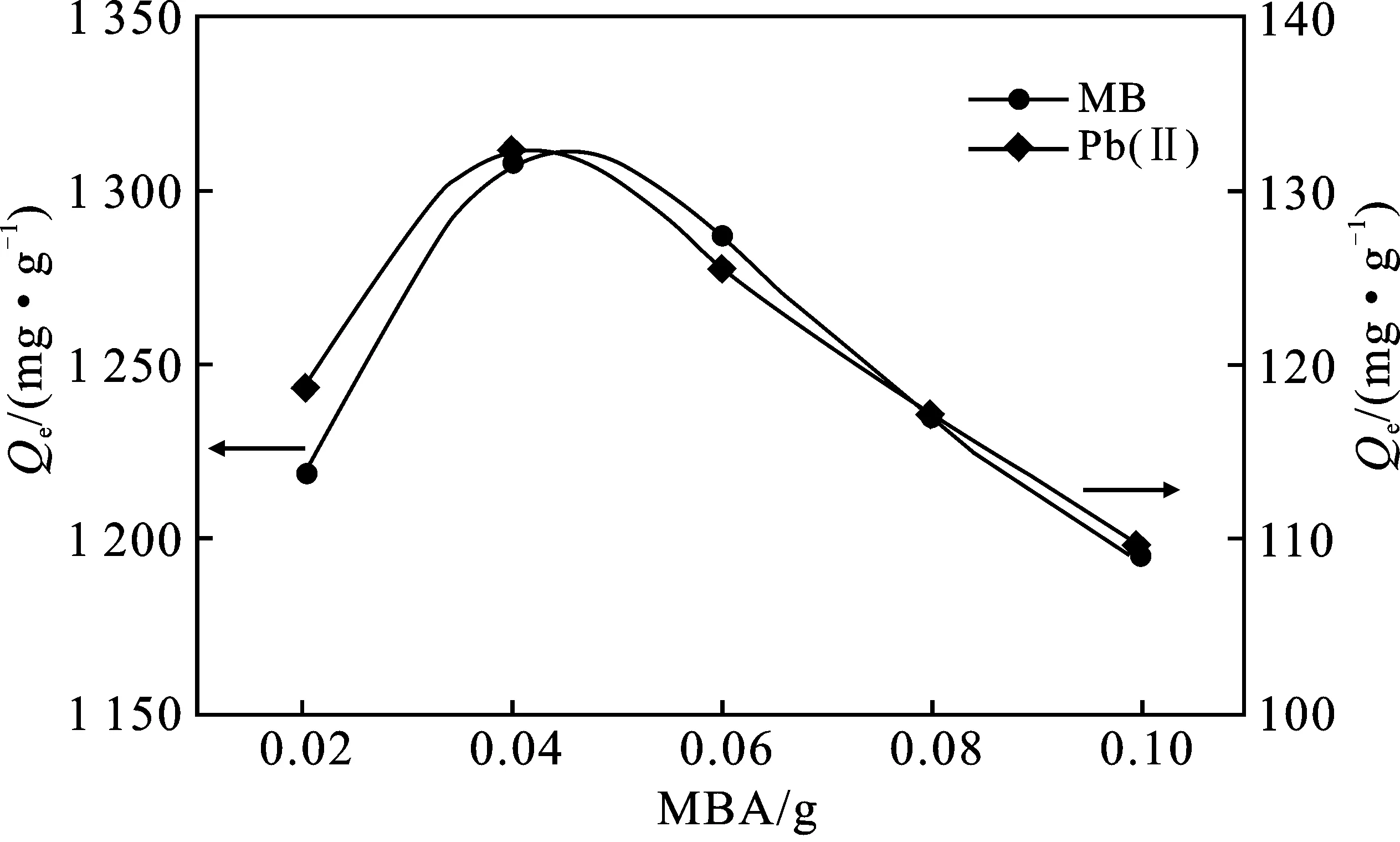
图5 MBA用量对吸附量的影响Fig.5 Effect of MBA dosage on adsorption capacity
由图5可知,随着MBA用量的增加,水凝胶对MB和Pb(Ⅱ)的吸附量均呈现先增加后降低,在MBA用量为0.04 g时达最大。这是因为MBA用量较少时,水凝胶的交联度小,凝胶有部分水溶性。随着MBA用量的增加,水凝胶三维网状结构逐渐形成,其吸附性能增强。而当MBA用量过高时,水凝胶交联密度过大,凝胶内部三维网络结构过于致密,不利于MB和 Pb(Ⅱ)的进入,水凝胶的溶胀度变小,吸附性能变差。因而,MBA用量为0.04 g较合适。
2.1.6 聚合温度对吸附量的影响 在PVA为 15 g,GG为10 g,KHA分别为0.2 g和0.3 g,KPS为0.08 g,MBA为0.04 g条件下,考察聚合温度对MB和 Pb(Ⅱ)吸附量的影响,结果见图6。
由图6可知,随着聚合温度的升高,水凝胶对MB和Pb(Ⅱ)的吸附量,均呈现先增加后降低的趋势。当聚合温度为65 ℃时,有最大吸附量。这是因为当聚合温度较低时,不能产生有效的自由基,聚合速度较慢。随着聚合温度的逐渐升高,聚合速度加快,水凝胶的三维网络结构逐渐形成,其吸附性能增强。而当聚合温度过高时,KPS分解速度加快,聚合过程的链转移与链终止速率增加,使聚合物的聚合速度加快,不利于水凝胶三维网络结构的形成,致使吸附量的逐渐降低。因此,聚合温度为65 ℃较合适。
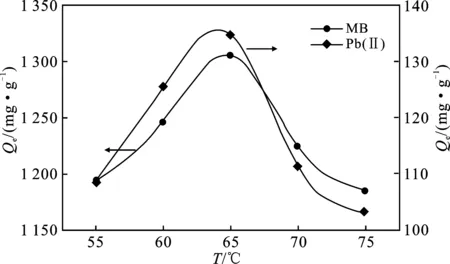
图6 聚合温度对吸附量的影响Fig.6 Effect of polymerization temperature on adsorption capacity
2.2 PVA/KHA/GG水凝胶的表征
2.2.1 FTIR分析 图7是水凝胶合成原料PVA、KHA、GG和PVA/KHA/GG水凝胶及其吸附前后的红外光谱图。
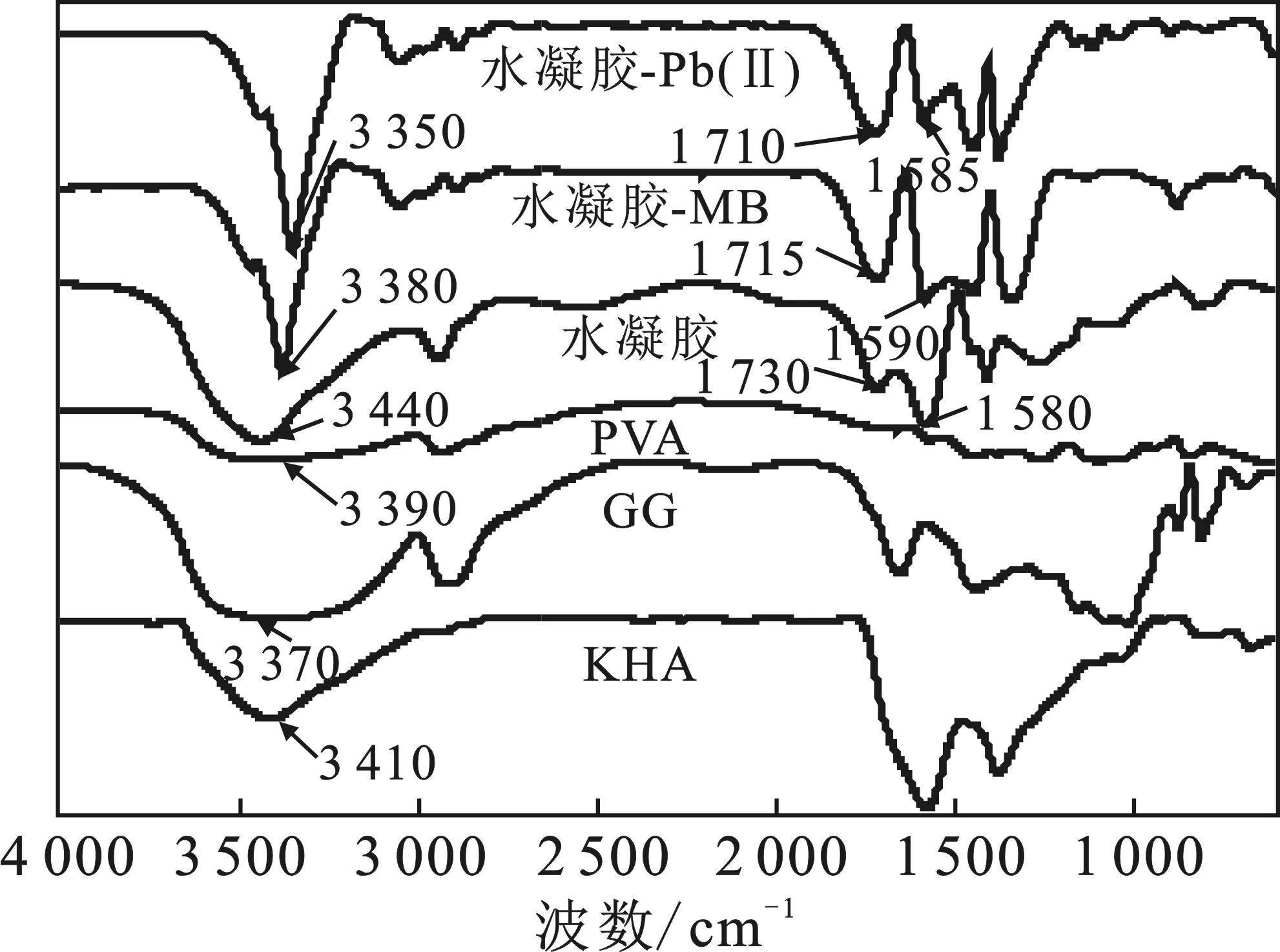
图7 水凝胶合成原料及其吸附前后的红外光谱图Fig.7 FTIR spectra of raw materials for hydrogel synthesisand before and after adsorption

2.2.2 XRD分析 图8分别为合成原料PVA、KHA、GG和PVA/KHA/GG水凝胶及其吸附前后的XRD谱图。
图8的XRD光谱图提供了关于合成原料和水凝胶吸附MB和Pb(Ⅱ)后的结构信息。在水凝胶的曲线上,2θ为19.55°存在一个宽峰,并未观察到与合成原料(GG(19.73,38.45°)、KHA(26.75°) 和PVA(19.55,40.86°))相关的特征衍射峰,这就表明PVA、KHA和GG已经成功地反应。此外,在水凝胶吸附MB后的曲线中,在2θ为10~30°出现一宽峰,这是分子内氢键作用的结果。在水凝胶吸附Pb(Ⅱ)的曲线中,在2θ=19.63,22.65,25.35°等处,存在众多特征衍射峰,这归因于典型的 Pb(NO3)2晶体结构[11]。这些结果表明,MB和 Pb(Ⅱ)已被吸附到水凝胶上。
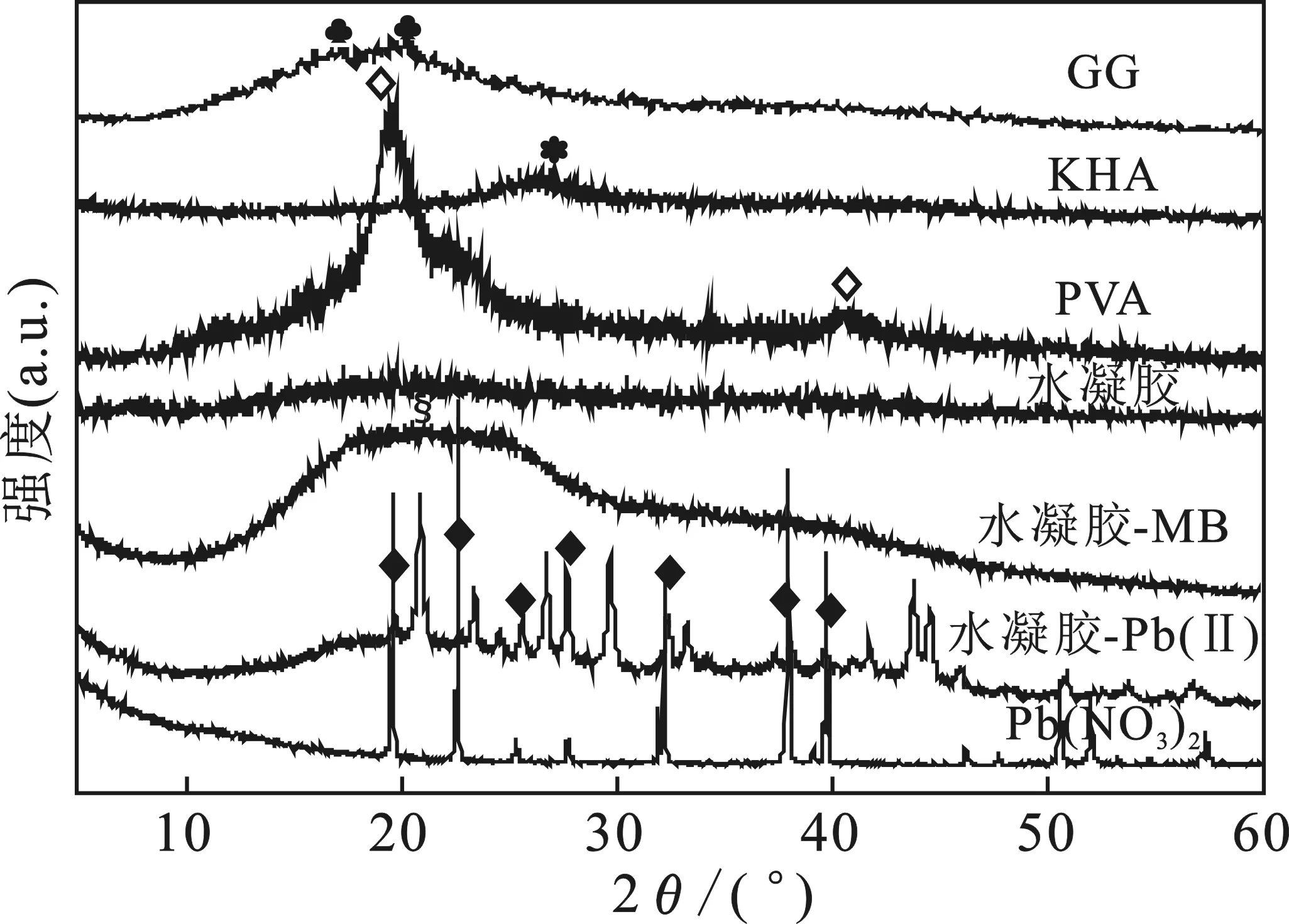
图8 水凝胶合成原料及其吸附前后的XRD光谱图Fig.8 XRD spectra of raw materials for hydrogel synthesisand before and after adsorption
2.2.3 SEM分析 PVA/KHA/GG水凝胶吸附MB和Pb(Ⅱ)前后的扫描电镜图见图9。



图9 水凝胶的SEM照片Fig.9 SEM image of hydrogela.吸附前;b.吸附MB后;c.吸附Pb(Ⅱ)后
由图9a原水凝胶的微观照片可观察到纵横交错的孔状结构,有效增大水凝胶与MB和Pb(Ⅱ)的接触面积,从而提高了水凝胶对MB和Pb(Ⅱ)的吸附速率和吸附容量。图9b是水凝胶吸附MB染料后的微观图像,可清楚观察到水凝胶表面附着有大量形状不同的颗粒,并有部分颗粒已进入到水凝胶孔隙中。图9c是水凝胶吸附Pb(Ⅱ)后的微观图像,可清楚观察到水凝胶表面粗糙并有大量片状的颗粒沉积在水凝胶表面。与未吸附水凝胶相比,水凝胶的孔隙结构已被完全覆盖,这就表明水凝胶对MB和Pb(Ⅱ)具有较强的吸附作用。
2.3 吸附动力学研究
为对水凝胶的吸附过程和吸附机理做进一步的研究,利用准一级动力学反应方程(2)和准二级动力学反应方程(3)对吸附数据进行拟合分析[12]。
ln(Qe-Qt)=lnQe-k1t
(2)
(3)
式中Qe和Qt——分别平衡时刻和t时刻的吸附量,mg/g;
t——吸附时间,min;
k1——准一级反应速率常数,min-1;
k2——准二级反应速率常数,g/(mg·min)。
图10是PVA/KHA/GG水凝胶吸附MB和Pb(Ⅱ)的吸附量与吸附时间变化关系图。
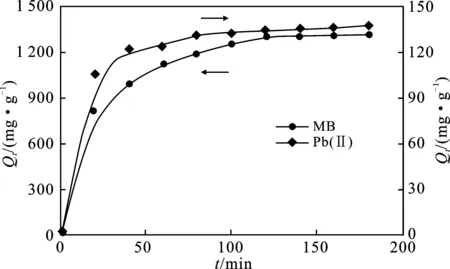
图10 吸附时间对吸附量的影响Fig.10 Effect of adsorption time on adsorption capacity
由图10可知,在起始60 min内吸附速率最高,随着时间的增加吸附速率逐渐减小,在吸附120 min左右基本达到平衡。
根据水凝胶对MB 和Pb(Ⅱ)吸附量随时间变化的数据进行拟合,动力学方程的拟合结果见图11和图12。
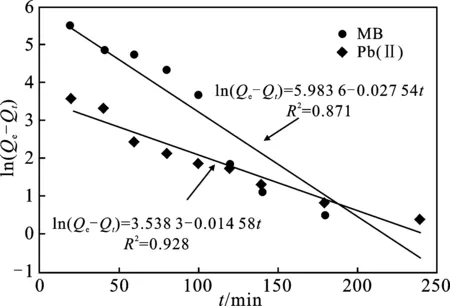
图11 准一级动力学方程拟合曲线Fig.11 Fitting curves of pseudo-first-order kinetic equation
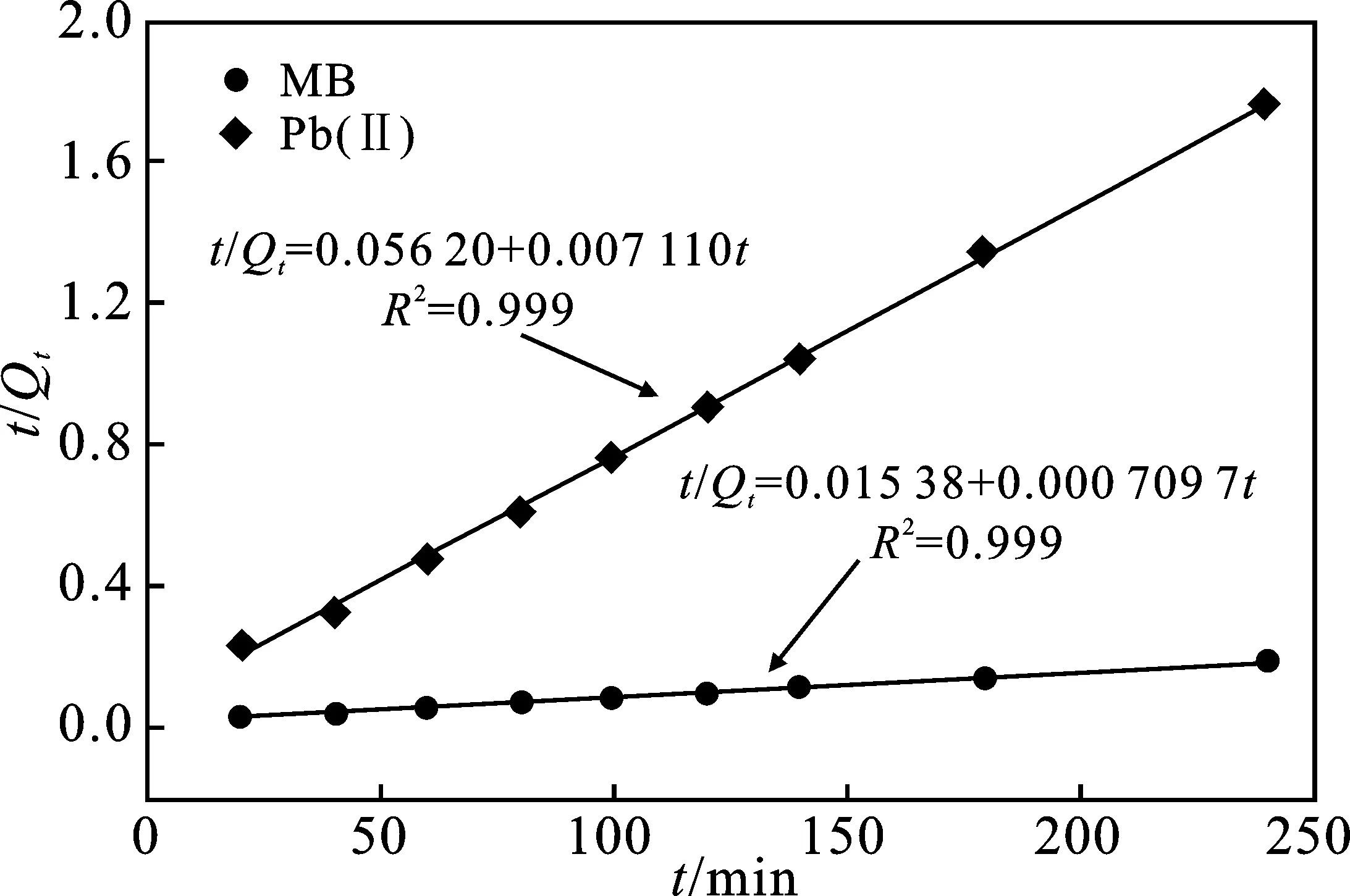
图12 准二级动力学方程拟合曲线Fig.12 Fitting curves of pseudo-second-orderkinetic equation
由表1可知,从实验中测得的MB和Pb(Ⅱ)平衡吸附量分别为1 387.2 mg/g和138.5 mg/g,其与准二级动力学方程计算得到的平衡吸附量 1 409.046 mg/g 和140.647 mg/g更为接近。同时,对准二级动力学方程的拟合相关系数(R2)更接近于1。由此可知,水凝胶对MB和Pb(Ⅱ)的吸附过程可以用准二级动力方程来描述和解释,该水凝胶对MB和Pb(Ⅱ) 的吸附属于化学吸附过程。

表1 水凝胶对MB和Pb(Ⅱ)吸附动力学参数Table 1 Kinetic equation parameters of MB and Pb(Ⅱ) adsorption onto hydrogel
3 结论
(1)采用水溶液聚合法成功制备出一种具有多孔结构的PVA/KHA/GG水凝胶。当PVA为15 g,KHA分别为0.2 g和0.3 g,GG分别为10 g和15 g,KPS为0.08 g,MBA为0.04 g,聚合温度为65 ℃时,水凝胶对MB和Pb(Ⅱ)吸附量达最大。
(2)FTIR和XRD分析表明,PVA、KHA和GG成功反应并制得PVA/KHA/GG水凝胶。SEM图片分析表明,PVA/KHA/GG水凝胶为多孔结构材料,且对MB和Pb(Ⅱ)具有较强的吸附作用。
(3)PVA/KHA/GG水凝胶对MB和Pb(Ⅱ)的吸附动力学较符合准二级动力学方程,对MB和 Pb(Ⅱ)的最大吸附量分别为1 387.2 mg/g和 138.5 mg/g。

