多维突破元素知识 原创试题提升复习效率
湖南
1 高考背景
2019年6月19日国务院办公厅发布的《国务院办公厅关于新时代推进普通高中育人方式改革的指导意见》中关于深化考试命题改革中明确要求“创新试题形式,加强情境设计,注重联系社会生活实际,增加综合性、开放性、探究性试题”,2020年1月份教育部考试中心发布的《中国高考评价体系》和《中国高考评价体系说明》成为“后考纲”时代高考复习教学的重要参考文件。
元素化合物知识是高考题中较关键的部分,通常会渗透于理论与实验,生活与生产等具体问题中,重点考查知识的应用能力。近五年全国卷工艺流程题与实验题中主要载体元素见表1及表2。
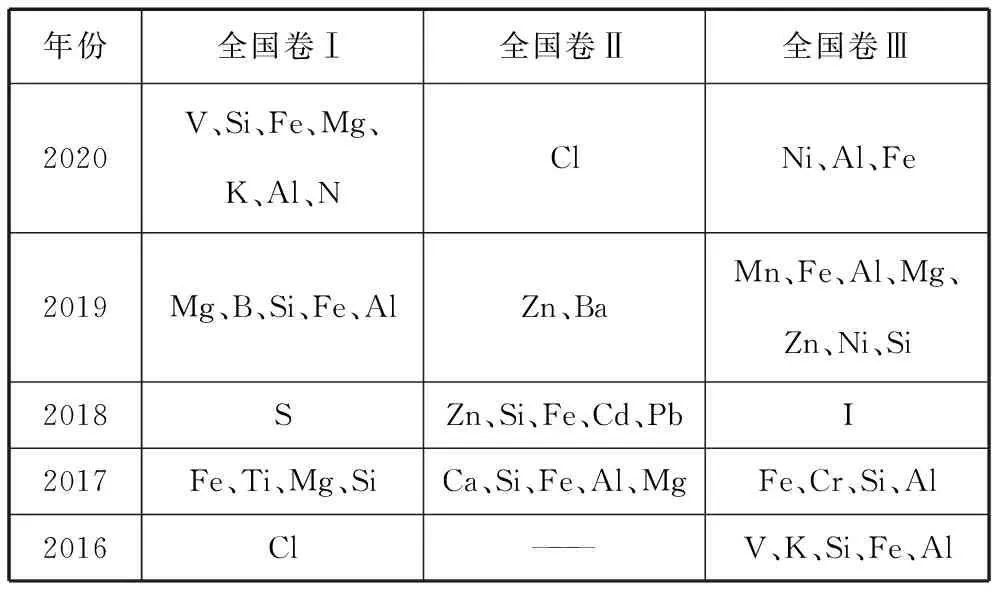
表1 近五年全国卷工艺流程题元素考查情况汇总
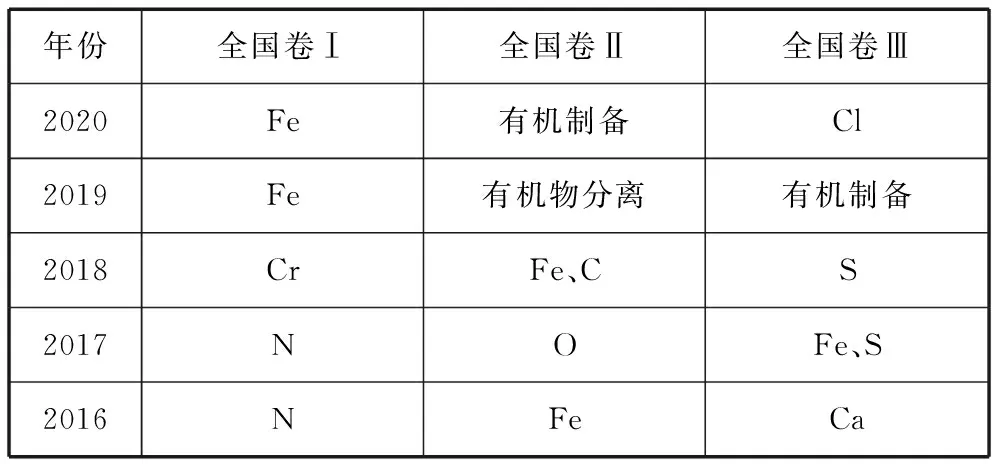
表2 近五年全国卷实验题主要载体元素
2 利用原创试题突破元素化合物知识的复习
《普通高中化学课程标准(2017年版2020年修订)》提出高中主要掌握的元素有Na、Fe、Cl、N、S,共5种。在复习过程中一般分为金属及其化合物、非金属及其化合物两个模块。在2020年新冠肺炎的影响下,全国卷化学非常注重难度调控,关注学生切身感受。故复习中进行试题命制时,需在保证试卷总体区分度的前提下,提高学生的感受度和学生答题的积极性,因此,笔者认为可从2个方面科学合理地调控试题难度,第一,试题选取的元素应贴近学生学习实际;第二,改变某类试题的考查方式,例如2020年全国卷Ⅱ36题对同分异构体的考查,由原来的写出同分异构体数目改为以选择题的形式呈现;再比如,计算题可只要求给出计算式。
2.1 创“填空题”夯实元素基础
教材是学生突破高考试题的基础,是思维的来源,如今高考题越发新颖的原因就是希望改变“靠刷题就能得高分”的现状,故教师们需要采用“授之以渔”的方式通过创设新颖的试题夯实基础,同时为进阶学习提供契机。
笔者以硫及其化合物为例,以提高学生能力为目的,创设了如下题目。
【硫及其重要化合物】填空题
1.硫元素在周期表中的位置:________。用硫粉和亚硫酸钠反应制Na2S2O3时,一般会在溶液中加入乙醇的目的是:。
2.写出硫单质分别与Fe、Cu单质反应方程式:
______________;____________________。
3.向硫代硫酸钠溶液滴入稀硫酸,有淡黄色沉淀产生,请写出相关离子方程式:________________________。硫代硫酸钠可用于吸收Cl2,写出相应的离子方程式:____________________。已知:NaHSO3过饱和溶液脱水结晶得到焦亚硫酸钠(Na2S2O5)固体,写出相应的化学方程式:____________________,葡萄酒中常需要加入适量的焦亚硫酸钠(Na2S2O5),目的是____________________,可用碘标准溶液滴定,确定是否超标,滴定原理的离子方程式为____________________。
4.碳单质与浓硫酸加热反应的化学方程式:
________________,硫单质与浓硫酸加热反应的化学方程式:____________________,体现了浓硫酸具有________性。浓硫酸能否干燥H2S、SO2气体________,若不能,请用化学方程式解释原因。
铜单质与浓硫酸加热反应的化学方程式:
,
体现了浓硫酸具有________性。能否使用pH试纸测浓硫酸的pH________。
5.在水溶液中,Ag2SO4与单质S作用,沉淀变为Ag2S,分离后,向所得溶液中加碘水不褪色。则Ag2SO4与单质S作用的离子方程式为________________。在酸化的KI溶液中通入SO2,观察到溶液出现淡黄色沉淀且溶液显棕黄色,写出相应反应的离子方程式:________________,继续通SO2,溶液变为无色,写出相应反应的离子方程式:________________。总反应方程式为________________,说明KI在反应中的作用________。
6.已知I2易溶于KI溶液是由于能够反应生成一定量的KI3,写出该反应的离子方程式:____________________;单质S可溶于Na2S溶液,黄色固体消失得到Na2S2溶液。向所得溶液中加入稀盐酸,溶液中产生淡黄色沉淀,写出整个过程发生反应的离子方程式:____________________。
通过这样的练习,学生既能夯实基础,同时也提升了学习能力,比如其中一些陌生情境的创设就凸显了对学生学习能力的考查。
那么,该如何创编这样的填空题呢?
1.基于教材和教辅材料梳理命制题目的主干部分,并有所涉及部分相关的化学反应理论,可侧重实验和工艺流程的基础知识。
2.合理设空,注重前后的逻辑关系,不可“一空到底”,例如在考查物质性质时,可先要求学生书写方程式,然后再对其性质设问,这样可提高学生感受度,起到循序渐进的作用。
3.多关注拓展性的元素知识,巧妙设置已知信息,例如以上填空题中的5题,从而提高学生获取信息并解决问题的能力。
在创设过程中,应摒弃“死记硬背”的方式,注重发展学生的思维方式。
2.2 创“流程题”助力元素应用
2.2.1 探索高考命题规律 确定试题命制方向
表3为近五年全国卷工艺流程题的考查内容及频次。
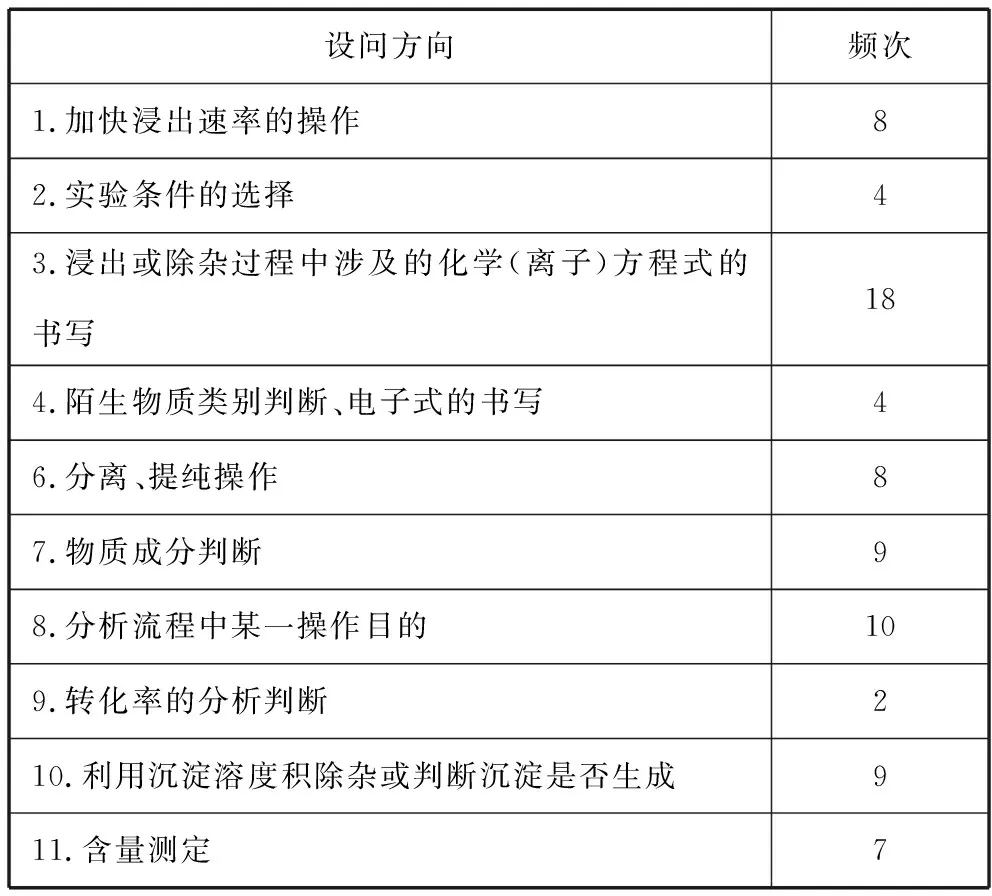
表3 近五年全国卷高考试题工艺流程题的设问方向及频次
2.2.2 以科技论文或专利为工艺流程题的主体素材
笔者在命制工艺流程题时,首先预设了该题需要考查的考点,选取素材方向。此类试题主要有两种形式,即“产品包含的元素是陌生的,杂质包含的元素是熟悉的”和“产品、杂质包含的元素均是熟悉的”,大多数题中涉及的原料为固体矿物质,由于地壳中含量最多的前四位元素为O、Si、Al、Fe,故常见杂质含有的非氧元素为Si、Al、Fe,因此在命制过程中“产品元素陌生,杂质元素熟悉”是该题的主流形式。
1.选择锂离子电池的正极材料为素材。锂离子电池在新能源发展中具有较大的潜力,因而对所用材料的合成研究也非常之多,故笔者初步确定从正极材料角度进行文献筛选。
2.选择科研论文,在百度学术或知网上进行查找,笔者最终确定以钟燕萍的《以废弃二次电池为原料制备α-Ni(OH)2正极材料的研究》为参考资料进行试题设计。
3.预设考查角度为化合价的计算、反应方程式的书写、原理的分析和反应条件的控制等,通过化合价、方程式书写等基础内容考查学生的必备知识,通过原理的分析、反应条件的控制等来考查学生的信息处理、分析、整合等关键能力,同时设问均取材于真实的科技论文,具有较强的科学依据。
4.由于该文献篇幅较大,笔者选择了文中主要的研究方式——湿法处理工艺流程,该过程较其他方式而言降低了复杂性,原料的选取也突出了绿色化学的要求,符合高考命题的特点。在具体命制过程中需要注重文献的科学性及设问的简单化,如由于废旧二次电池原料过于复杂,酸浸后的成分采用了直接给出离子种类的方式,同时对稀土复盐进行了有效“屏蔽”,减少了学生的困惑。
根据以上过程最终命题成文如下:
LiNiO2是一种前景极好的锂离子电池正极材料。回答下列问题:
已知:LiNiO2在850℃左右开始分解
(1)LiNiO2中Ni的化合价为________,利用电池级的Ni(OH)2与LiOH,在空气气氛中,700~800℃煅烧可制得LiNiO2。写出该过程的化学方程式
,
加热温度不宜过高的原因是
,
可用LiNO3代替LiOH,存在的缺点是。
(2)以废弃二次电池为原料回收利用合成电池级Ni(OH)2的工艺如图1所示:
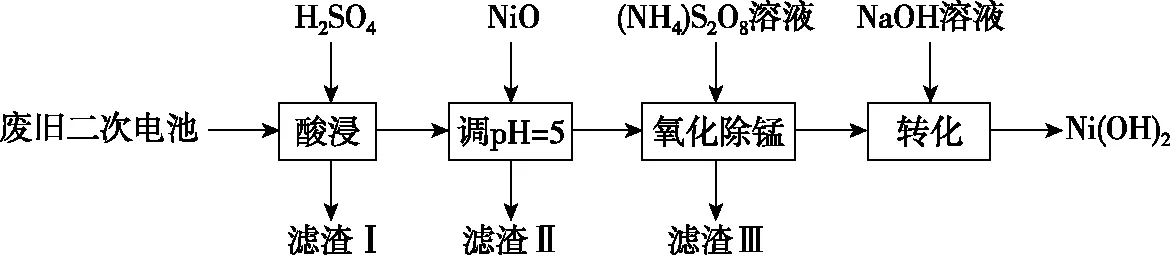
图1
已知:酸浸后滤液中含有Ni2+、Al3+、Fe3+、Mn2+;
Ksp[Fe(OH)3]=4.0×10-38,Ksp[Al(OH)3]=1.0×10-33,Ksp[Ni(OH)2]=1.6×10-14;
①“滤渣Ⅱ”为________。
②“氧化除锰”即将锰元素最终转化为MnO2而除去,反应历程如下:

ⅱ.
(用离子方程式表示)。
③“转化”后,产品需经过洗涤、烘干,则检验Ni(OH)2是否洗涤干净的实验操作是。
④“调pH=5”时,已知溶液中Ni2+浓度为2 mol·L-1,则“滤渣Ⅱ”中是否存在Ni(OH)2沉淀?
(列式计算)。

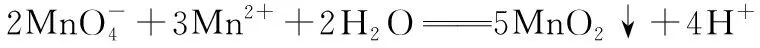
③取最后一次洗涤液,先加稀盐酸酸化,再滴加BaCl2溶液,若无白色沉淀产生,则洗涤干净
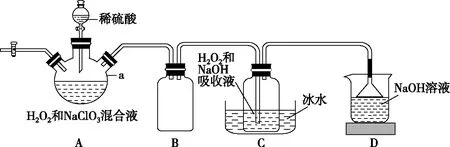
④pH=5,滤液中c(OH-)=10-9mol·L-1,Qc=c2(OH-)·c(Ni2+)=(10-9)2×2=2×10-18 【说明】笔者认为原创工艺题时要注意以下几点: 1.明确该题的产物及原料; 2.多方查找文献,以最新研究为主,深入研究其中素材,将其简化、试题化,同时可以综合多篇文献,对除杂、分离提纯等阶段进行基于学生学情的综合替换或拼接; 3.反复核实,保证不出现科学性或知识性差错; 4.注重对学生信息处理、整合、应用能力的考查设问。 2.3.1 明晰实验主体——气体或溶液 近年高考试题逐步呈现出以溶液实验为主的趋势,这比较符合教材的真实情况。教材实验大多以试管实验为主,有气体参与的综合性实验较少,在创新大赛中,实验往往以“微、精、简”为主流。故在考查过程中,溶液类实验更能全面体现高中化学必备知识与关键能力。 2.3.2 基于真实情境命制实验试题 实验题与工艺流程题实际上均有实验操作,前者侧重元素化合物知识在实验中的应用,以实验基本操作、原理、实验现象、实验条件等为主要考查方向,后者更侧重元素化合物知识本身,如方程式书写、成分分析等。二者有较多相似点,这两种题型是元素化合物知识复习的重要载体。前文已经对工艺流程题的命制作了分析,下面来讲讲实验题。 首先要确定命制实验题的类型:制备类、性质探究类、定量计算类、原理探究类,其次是素材的选取,通过搜索多个科研论文确定目标,最后再根据考查内容设问。 笔者确定题目类型为制备类,以NaClO2的合成为目标,筛选文献,最终选择专利——《亚氯酸钠的制备方法》为主要参考资料。 最终命制试题如下: 亚氯酸钠(NaClO2)是一种高效含氯消毒剂和漂白剂,主要用于自来水、污水等水环境的杀菌消毒,也常用作纸浆、砂糖、油脂的漂白剂。图2为目前生产亚氯酸钠的流程之一(夹持装置省略),所得NaClO2具有纯度高的优点。 图2 已知:NaClO2饱和溶液在低于38℃时会析出NaClO2·3H2O,高于38℃时析出NaClO2,高于60℃时NaClO2分解成NaClO3和 NaCl。 试回答下列问题: (1)仪器a的名称为________。 (2)装置A用来制取ClO2,发生反应的离子方程式为____________________。 图3 (4)C装置采用“冰水浴”的目的是。 (5)充分反应后,从产品溶液中获取NaClO2晶体的操作是:55℃恒温减压蒸发结晶、趁热过滤、________℃水洗涤、干燥。 (本题部分内容已应用于教学考试优师计划研发项目) 【说明】本题为笔者命制的2020年常德市高考模拟试题中的一道实验题。为了给试题创设亮点,命制过程中对NaClO2的生成条件进行了文献查询,最终设计了(3),原文献包含两个图像,但笔者有意图创设双纵坐标图像,效仿了与 2020年全国卷Ⅰ13题。在图像设置中要注意降低学生形成错误思维可能性,本题的设问是选择合适的实验条件,对于学生来讲有一定的难度,原因在于不少学生没有考虑生产成本,故此问可帮助学生加深绿色化学的理念。因而还有一种设问方式即为何选用c(NaOH)=0.8 mol·L-1最为合适?笔者又在第(6)问涉及了文献中含量测定时常出现的角色——滴定度,设计了相关问题,较好的考查了学生分析、解决问题和整合信息的能力。因此,本题具备了良好的区分度。 通过关注与学科相关的新闻,关注与学科相关网站,查找教材、杂志、报刊等角度挖掘新材料,具体可以有两种形式,第一,以现有习题的目标物质为目标,搜索相关科技文献,重新组织题干与设问;第二,以目前少见的物质合成为目标编制新题,但要确保试题的严谨性与真实性。 注重试题设问角度,通过拼接、模仿、套用、反转、变形等手段进行再创造,但要注意保证试题不偏、不怪。命题应以“改编为主,创新为辅”的形式,逐步向“创新为主、改编为辅”的形式转变。2.3 创“实验题”助力元素探究
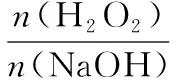


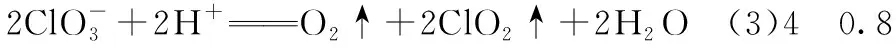
3 命制优秀试题的方向
3.1 保证试题命制的材料新
3.2 注重试题设问角度的再创造
4 结语


