PTCBA联合DCB扩张术治疗冠状动脉分叉病变的疗效及对患者血流TIMI分级的影响
李雪锋,廖春华,邹云新,徐璧江,杨浩祺
丰顺县人民医院心血管内科,广东梅州514300
冠状动脉分叉病变主要指冠脉主支、分支部位同时或分别有严重的狭窄病变,在所有冠状动脉病变中比例为15%~16%[1-2]。经皮冠状动脉介入术(PCI)是治疗冠状动脉病变的常用术式,但和单纯的冠状动脉病变相比,分叉病变存在着较高的剪切力和涡流,可造成不稳定斑块移位、分支闭塞等不良现象,增加分支再狭窄的发生风险,极易影响到应有的治疗效果[3]。经皮冠状动脉腔内切割球囊成形术(PTCBA)可均匀性的扩开血管壁,有助于增加分支开口面积,避免血管弹性回缩的现象[4]。药物涂层球囊(DCB)是种新型的介入治疗技术,主要是将球囊作为抗细胞增殖的药物载体,并采用球囊扩张技术,将抗增殖药物释放于冠脉血管壁,从而对血管内膜增生产生抑制作用[5]。因此,本研究将PTCBA联合DCB扩张术用于冠状动脉分叉病变患者的治疗,旨在探讨其疗效及对心肌梗死溶栓试验(TIMI)分级的影响。
1 资料与方法
1.1 一般资料选择2019年1月至2020年3月丰顺县人民医院心血管内科收治的80例冠状动脉分叉病变患者进行研究。本研究获得本院伦理委员会批准实施,相关患者均知情并签署知情同意书。纳入标准:①符合冠状动脉分叉病变诊断标准[6],并通过冠状动脉造影检查确诊真分叉病变(Medina分型1,1,1;0,1,1;1,0,1),主支和分支血管狭窄程度>75%;②主支或分支血管病变无严重钙化、迂回、冠状动脉肌桥等情况;③具有PCI适应证;④年龄40~80岁。排除标准:①分支靶血管直径<2 mm;②病变部位是由于冠状动脉支架植入术所致的术后再狭窄;③合并心源性休克、急性心肌梗死;④合并严重肝肾功能障碍、严重甲状腺功能亢进;⑤合并出血性疾病、凝血功能障碍,或者无法耐受双联抗血小板治疗者;⑥合并恶性肿瘤或其余重大躯体疾病,预计寿命<1年;⑦对碘造影剂过敏;⑧精神障碍及异常。按照随机数表法将患者分为观察组和对照组各40例,两组患者的一般资料比较差异均无统计学意义(P>0.05),具有可比性,见表1。
表1 两组患者的一般资料比较[±s,例(%)]
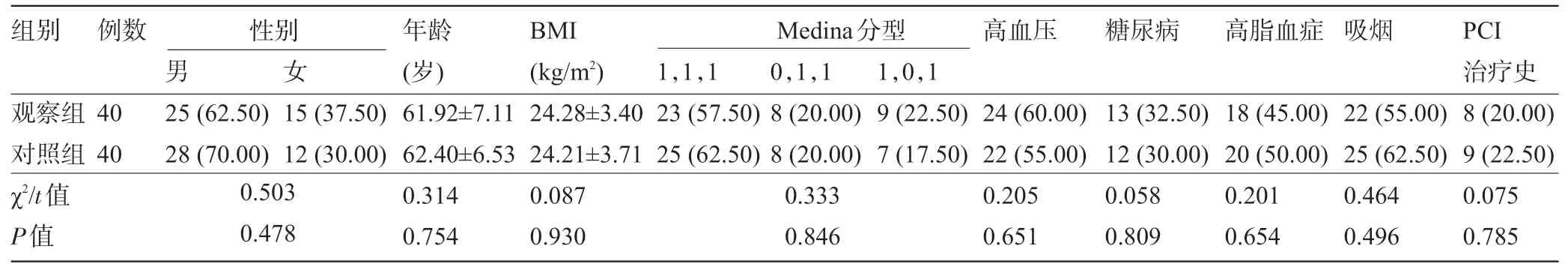
表1 两组患者的一般资料比较[±s,例(%)]
?
1.2 治疗方法所有患者入院后均给予常规阿司匹林、氯吡格雷的双联抗血小板治疗,术前12 h使用负荷剂量的氯吡格雷治疗。两组患者均接受PCI手术治疗,方法如下:①两组均选择桡动脉穿刺进行手术,选择2根导丝分别置入主支、分支血管,主支血管均采用普通球囊进行预扩张,分支血管首先采用PTCBA预扩张,切割球囊和分支血管直径比为1:1,切割球囊在对分支开口病变进行扩张时,选择缓慢加压模式,每隔3~5 s,进行1 atm的加压,最高压力低于10 atm,到达最大压力之后,维持5~10 s,确保球囊获得充分的扩张,并保证分支开口的残余狭窄程度<30%。②切割球囊预扩张后,观察组采用DCB预埋,DCB直径和血管直径比为0.8~1.0,两端长度需覆盖分支开口和远端预先处理范围2~3 mm之外,释放压力7~8 atm,持续时间>30 s,若患者可耐受,则持续60 s,DCB进入后2 min内释放完毕,扩张后将药物球囊暂时保留于分支;对照组则采用普通版顺应性球囊进行,暂时保留球囊于分支开口处。③球囊扩张满意后,两组均于主支血管置入药物洗脱支架,再对先前留于分支的药物球囊和普通球囊进行对吻扩张,释放完毕后,将分支的药物球囊和普通球囊、主支的普通球囊退出,进行支架内后扩张,完成手术。
1.3 观察指标与评价方法①血流TIMI分级:记录术后即刻两组主支、分支血流TIMI达到3级的患者,TIMI3级标准:完全灌注,造影剂在冠状动脉内可获得迅速的充盈和清除;②主支、分支病变血管最小内径(MLD)、狭窄程度及晚期管腔丢失情况:分别于术前、术后即刻以及6个月时接受冠状动脉造影检查,采用SIE-ADSV3.1图像处理软件对冠状动脉造影图像进行分析,记录上述时间点主支和分支病变血管MLD以及病变狭窄程度的变化,并计算主支和分支病变晚期管腔丢失情况,晚期管腔丢失情况计算方法为:术后即刻MLD-术后6个月时MLD;③不良心血管事件:主要观察内容包括术后6个月期间靶血管再狭窄(主支及分支)、再发心绞痛、靶血管心肌梗死、靶血管血运重建以及心源性死亡的发生情况。
1.4 统计学方法应用SPSS18.0软件进行数据统计学分析,计量资料以均数±标准差(x-±s)表示,组间比较采用t检验,计数资料以例数或率表示,组间比较采用χ2检验,以P<0.05表示差异具有统计学意义。
2 结果
2.1 两组患者术后即刻主支和分支病变血流TIMI3级情况比较两组患者术后即刻主支、分支病变血流TIMI3级患者比较差异均无统计学意义(P>0.05),见表2。
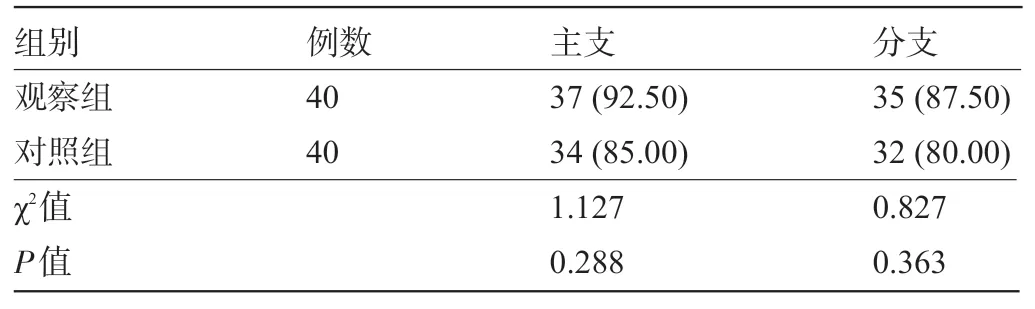
表2 两组患者术后即刻主支和分支病变血流TIMI3级情况比较[例(%)]
2.2 两组患者主支和分支病变MLD、狭窄程度比较两组患者在术前、术后即刻时主支、分支病变MLD、狭窄程度比较差异均无统计学意义(P>0.05);术后6个月时,两组患者的主支病变MLD、狭窄程度比较差异均无统计学意义(P>0.05),但观察组患者的分支病变MLD明显高于对照组,狭窄程度明显低于对照组,差异均有统计学意义(P<0.05),见表3。
表3 两组患者主支和分支病变MLD、狭窄程度比较(±s)
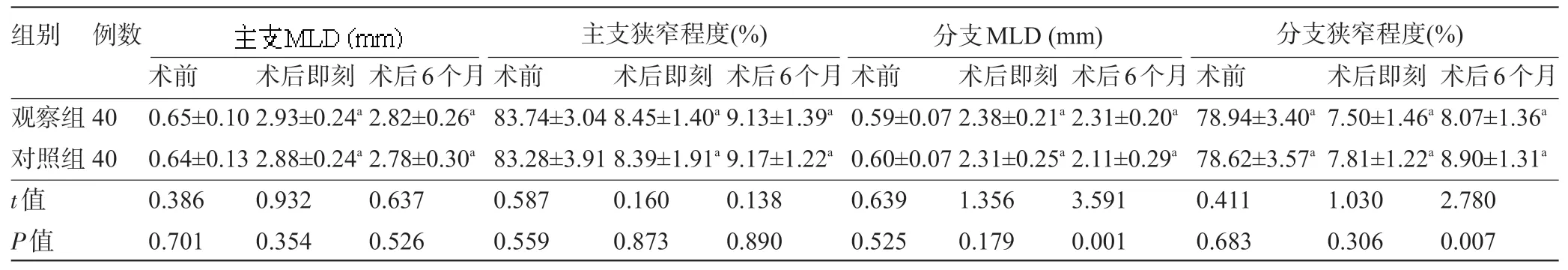
表3 两组患者主支和分支病变MLD、狭窄程度比较(±s)
注:与本组术前比较,aP<0.05。
?
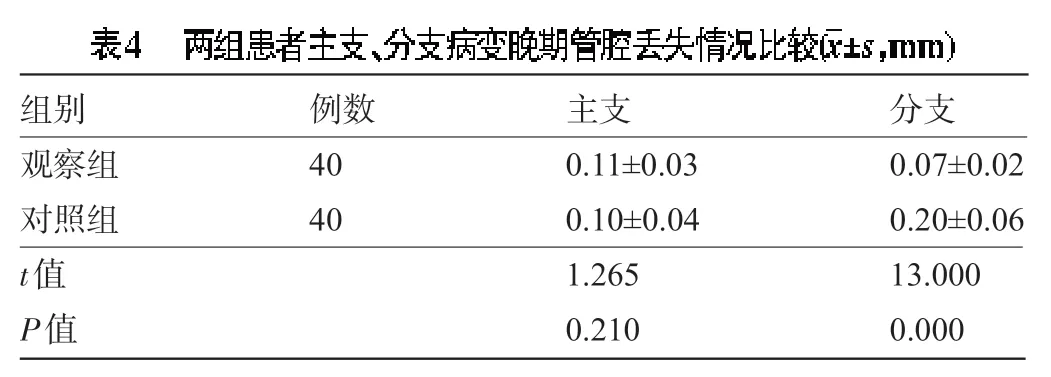
2.3 两组患者主支和分支病变晚期管腔丢失情况比较两组患者术后6个月时,主支病变晚期管腔丢失比较差异无统计学意义(P>0.05),但观察组患者的分支病变晚期管腔丢失明显少于对照组,差异有统计学意义(P<0.05),见表4。
2.4 两组患者的主要不良心血管事件发生情况比较两组患者均获得随访,随访期间无失访患者。随访6个月期间,两组患者均无心源性死亡患者,通过对靶血管再狭窄(主支及分支)、再发心绞痛、靶血管心肌梗死、靶血管血运重建的记录显示,观察组患者的并发症总发生率明显低于对照组,差异有统计学意义(χ2=4.114,P=0.043<0.05),见表5。
?

表5 两组患者的主要不良心血管事件发生率比较(例)
3 讨论
冠状动脉分叉病变一直临床治疗的难点问题,该病的解剖结构复杂,主支血管、分支血管两者之间呈倒“Y”字形表现,且分支病变的血管直径很小,分叉开口处的血液存在着湍流、高剪切力的情况,容易形成动脉粥样硬化斑块、血管分叉嵴移位等情况,加上分叉病变的部位通常有较重的斑块负荷,一旦术中处理不当,术后的再狭窄风险也会明显增加[7-8]。因此,在对于冠状动脉分叉病变的治疗中,不仅需确保主支血管通畅,积极的促进分支血管通畅并减少分支血管再狭窄的发生率也显得极为重要。
目前对于冠状动脉分叉病变的治疗中,主支病变多倾向于选择支架置入治疗,但临床上对于分支病变的处理仍无统一定论。较为常用的分支保护策略则是采用球囊扩张技术,但普通的球囊进行预扩张也容易增加开口斑块移位、分支血流限制、丢失等不良情况,临床获益欠佳[9]。PTCBA主要是采用切割球囊,将血管内、中膜缓慢均匀的切开,让斑块撕裂,可最大程度的避免斑块移位以及内膜夹层,且有助于令血管壁的环匝应力得以解除,防止球囊扩张或所发生的弹性回缩现象[10-11]。但也有研究指出,虽然PTCBA的即刻效果良好,但切割球囊在切割斑块的时候可能会导致内膜破裂,容易增加内膜增生、血栓等发生风险,继而影响到远期疗效[12]。DCB是一种新型的治疗技术,近年来在国外已得到广泛的开展,主要推荐应用于支架内再狭窄、小血管病变、分叉病变等患者的治疗[13]。DCB的表面负载着紫杉醇涂层,当球囊靠近血管壁后,紫杉醇可迅速被血管内膜所吸收,发挥抑制内膜增生、炎症反应等效果,且和药物洗脱支架相比,不存在金属网络和聚合物基质等物质的残留,在应用中也具有较高的安全性[14]。李蒙等[15]实验将DCB应用于冠状动脉左主干分叉病变患者的治疗,结果显示该方式可明显减少左回旋支开口的管腔丢失,具有较高的临床应用价值。
本研究结果显示,术后即刻时两组TIMI分级达到3级的患者以及主支和分支MLD、病变狭窄程度比较差异均无统计学意义(P>0.05),且术后6个月时主支病变的MLD、病变狭窄程度、晚期管腔丢失的结果也相近。但术后6个月时,使用PTCBA联合DCB治疗的患者分支病变MLD明显更高,狭窄程度和晚期管腔丢失结果明显更低。分析其原因可能为:①PTCBA进行预处理时,切割球囊可解除血管壁的环匝应力,减少内膜不规则撕裂现象,并降低之后球囊扩张分支病变所带来的夹层风险;②DCB通过球囊扩张后可于分支病变血管壁释放抗增殖药物紫杉醇,并可持续在术后短时间发挥抑制血管内膜炎症反应、内膜增生等作用,对分支病变起到保护作用,有助于避免仅使用PTCBA所导致的内膜破裂风险;③PTCBA以及DCB两组方式结合各自不同的优势特点,取长补短,进一步提高了治疗效果,并能减少分支病变再狭窄风险及不良心血管事件的发生率。但由于时间限制,本研究仅观察了术后6个月时各患者的情况,针对更远期的效果及安全性方面此后也将进一步持续探讨。
综上所述,PTCBA联合DCB扩张术治疗冠状动脉分叉病变的效果显著,术后血流TIMI分级满意,且能降低分支病变再狭窄情况及不良心血管事件的发生率,值得应用推广。

