肺部超声评估ARDS患者病情严重程度及预后的应用价值
张磊 郭丽芬 俞万钧
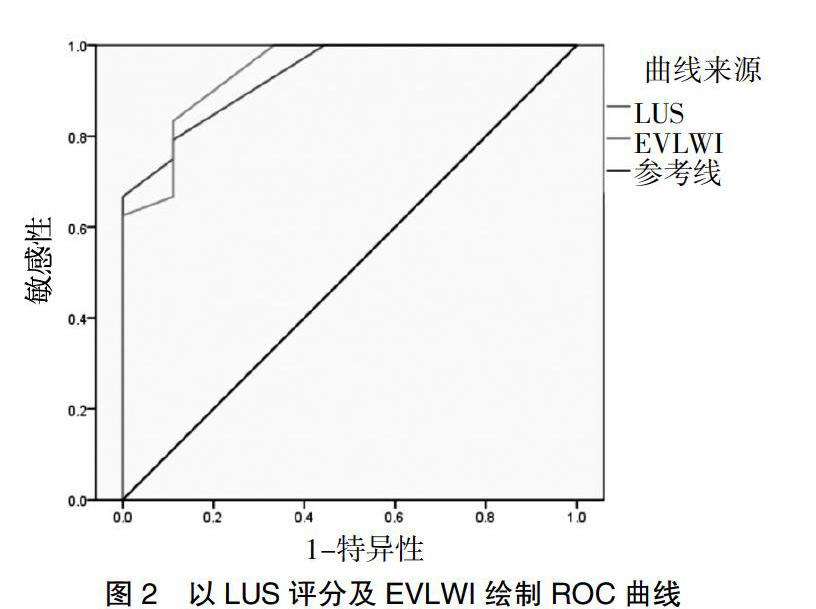
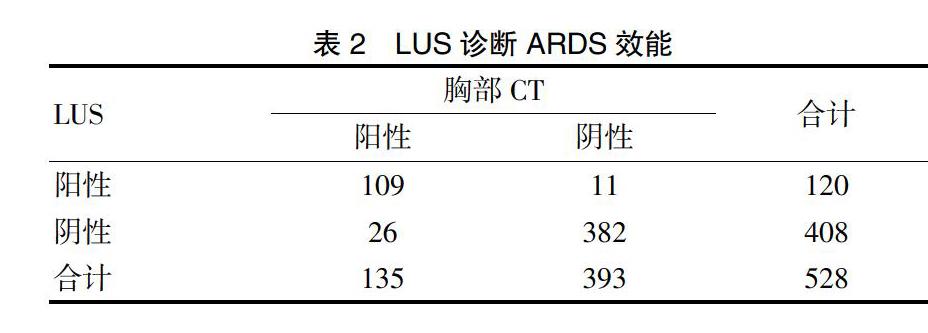
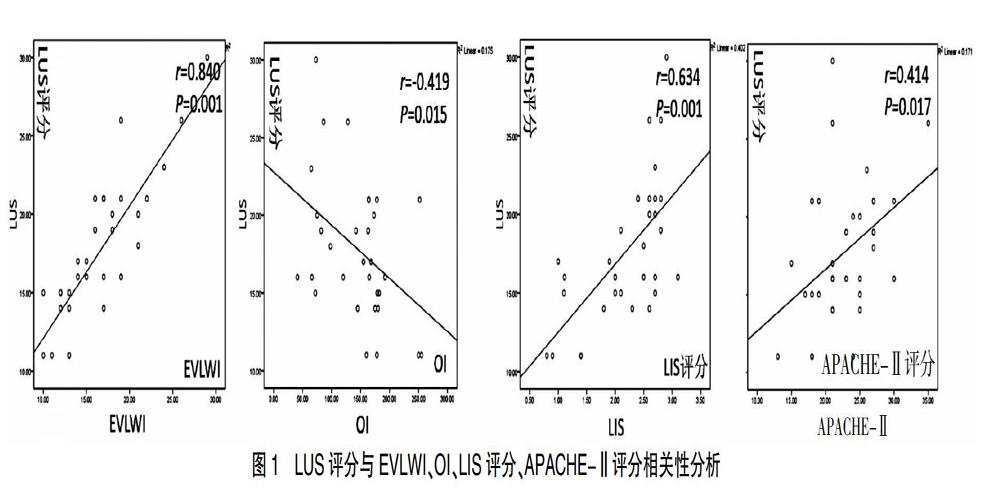
[摘要] 目的 探討肺部超声(LUS)在急性呼吸窘迫综合征(ARDS)患者中的病情评估及预后价值。 方法 采用前瞻性双盲队列研究,选取2016年7月至2018年1月宁波大学附属人民医院重症监护病房(ICU)符合柏林标准定义的ARDS患者33例,根据氧合指数(OI)将患者分为轻中度组(100 mmHg [关键词] 超声检查;肺;急性呼吸窘迫综合征;氧合指数 [Abstract] Objective To investigate the value of lung utrasonography (LUS) in evaluating the severity and prognosis of the patients with acute respiratory distress syndrome(ARDS). Methods A prospective double-blind cohort study was conducted. 33 patients with ARDS in the intensive care unit(ICU) of Ningbo Yingzhou People's Hospital from July 2016 to January 2018 conforming to Berlin standard definition were selected. The patients were divided into the mild-moderate group (n=24) (100 mmHg [Key words] Ultrasonography; Lung; Acute respiratory distress syndrome; Oxygenation index ARDS(Acute respiratory distress syndrome)是临床常见的各种肺内、肺外因素导致的弥漫性肺泡损伤及肺部炎症,进而发展为急性进行性、缺氧性呼吸衰竭为主要表现的临床综合征。近年来随着诊疗技术的提高,病死率较前有所下降,但仍居高不下,总体病死率在30%以上[1-2],其预后与早期原发病治疗和疾病严重程度明显相关。目前ARDS诊断仍无特异性生物学标志物,主要依靠临床及影像学表现,胸部CT仍被认为是诊断“金标准”[3],但由于其费用高、辐射损伤、可重复性差、重症患者存在转运风险等诸多因素限制了其在危重症患者中的临床应用。肺部超声在急性呼吸窘迫综合征应用中具有明显优势[4-6],表现为肺泡间质综合征,其ARDS诊断敏感性和特异性与胸部CT相似[7-9],还可以通过LUS根据氧合指数(OI)评分半定量评估ARDS患者血管外肺水含量[10-11]。本研究采用LUS(Lung utrasonography)评分技术评估ARDS患者病情及预后价值。现报道如下。 1 资料与方法 1.1 一般资料 选取2016年7月至2018年1月我院ICU收治符合柏林标准定义33例ARDS患者临床资料,根据氧合指数(OI)分为轻中度组(100 mmHg 1.2 方法 所有入组患者检查前给予纯氧吸入30 min并完成动脉血气检查(计算OI)、胸部CT和LUS检查,股动脉穿刺置管行经肺热稀释技术(Transpulmonary thermodilution,TPTD)监测获取 EVLWI;患者取仰卧位,以腋前线、腋后线及两侧乳头连线将半侧胸廓分为6个分区,整个胸部分为12个分区,指定同一名超声医师扫查整个胸部12个分区,记录每个分区最高分值,12个分区分值总和即为LUS评分,分值越高代表肺水含量越多,病情越重,预后越差。LUS评分标准[12-13]:正常肺组织通气区计0分,轻中度肺组织失气化计1分,重度肺组织失气化计2分,肺实变计3分。 1.3观察指标及评价标准 ①LUS量表评分标准[12-13]:正常肺组织通气区计0分,轻中度肺组织失气化计1分,重度肺组织失气化计2分,肺实变计3分;②通过TPTD监测获取EVLWI;③OI为PaO2/FiO2,临床上常用于评估ARDS病情严重程度的指标;④APACHE-Ⅱ评分包括体温、血压、血肌酐水平等17项急性生理学评分、年龄评分、慢性健康状况评分,三项评分总值即为APACHE-Ⅱ评分值,最高分值71分,分值越高,表示病情越严重,预后越差,病死率越高;⑤LIS评分是临床上常用的评价肺损伤严重程度的指标,包括肺部X线、低氧血症、呼吸末正压和呼吸系统顺应性评分,但呼吸系统顺应性评分受条件限制并非肺损伤评分必须项目,根据分值无肺损伤0分、轻中度肺损伤为0.1-2.5分、重度>2.5分,分值越高说明病情越重。 1.4 统计学分析 采用SPSS 18.0统计学软件进行分析,计量资料以均数±标准差(x±s)表示,组间比较采用两独立样本t检验。计数资料以[n(%)]表示,采用χ2检验。双变量采用Pearson相关分析变量之间的相关性,绘制ROC曲线LUS评分及EVLWI曲线下面积,计算出LUS评分预测患者严重程度界值。P<0.05为差异有统计学意义。 2 结果 2.1 LUS诊断ARDS效能 本研究共扫查了528个肺区,CT诊断肺实变135区,超声诊断肺叶实变120区,LUS诊断准确率、敏感性、特异性、阳性预测值及阴性预测值分别为93.00%、80.70%、97.20%、90.80%、93.60%。见表2。 2.2 LUS评分与EVLWI、OI、LIS评分、APACHE-Ⅱ评分相关性 Pearson相关性结果显示,LUS评分与EVLWI、LIS评分、APACHE-Ⅱ评分呈正相关(P<0.05),与OI呈负相关(P<0.05),且与EVLWI及LIS评分呈高度正相关(r=0.840,P<0.05;r=0.634,P<0.05)。见图1。 2.3 LUS评分评估ARDS病情严重程度价值 采用LUS评分ROC曲线下面积(AUC)及通过TPTD获取EVLWI曲线下面积分别为0.933(P<0.05)、0.942(P<0.05),以LUS评分20.50分作为阈值预测重度ARDS敏感性及特异性分别为88.90%、79.20%。见图2;當LUS评分界值≥20.50分时,说明患者病情危重,ICU住院时间延长,死亡风险显著增高。 3 讨论 目前ARDS诊断仍存在困难,胸部CT仍认为是诊断“金标准”,但对于重症患者来说存在转运风险、可重复性差、有辐射损伤,实际运用中临床医师及患者家属存在较多顾虑。床边胸部X线片检查优点在于可避免转运风险,但影像较复杂、分辨率差、缺乏客观性,且病情反映滞后。LUS已成为成熟的诊断技术,其在ARDS应用中具有明显优势[4,14],其无创、可反复床边检查等优势特别适用于ARDS患者。 ARDS的特点是肺毛细血管通透性增加,致血管外肺水(EVLW)增多,是一种典型的非心源性肺水肿,EVLW的积累会损害肺泡气体交换,导致严重的呼吸窘迫。ICU可以通过 TPTD技术客观地获取ARDS患者血管外肺水含量指数(EVLWI),在床边定量评价肺水肿[15]。Sakka等[16]研究发现,ICU患者初始EVLW程度与死亡率相关,最近的大规模研究也明确证实EVLW与ARDS患者预后之间呈明显相关[17-18]。虽然 TPTD 监测技术测定 EVLWI准确性高,但该项技术属于有创检查,且费用昂贵,不能常规开展,极大限制了其在临床中的应用。近年来国内外研究者均发现,LUS评分与通过TPTD监测技术监测客观数据EVLWI呈极明显的正相关[10-11,19];Bataille等[10]研究表明,LUS评分以半定量方式评估ARDS患者毛细血管外肺水含量,与经肺热稀释技术相比具有明显优势;胸部CT被认为是ARDS诊断的“金标准”,Ma等[9]研究报道,ARDS患者LUS评分与胸部CT影像具有很强的相关性。本研究结果显示,LUS评分与通过TPTD监测技术获得的客观数据EVLWI呈正相关,与Zhao等[11]的研究结果相符。 APACHE-Ⅱ评分系统[20]是世界范围内信度较高的危重病病情评价系统,可预测患者病情危重程度和病死率,APACHE-Ⅱ分值与病死率之间呈明显正相关,即分值越高,病情越危重,病死率越高,其预测病死率高达86%。LIS评分[21]是对肺损伤程度的临床评价,对ARDS的肺损伤程度作量化分析,评分内容包括胸片受累象限数、OI、PEEP水平及肺顺应性变化的评分,评分越高,肺脏受累范围越广,病情越重,并与肺血管通透性密切相关。有研究表明,LIS评分能准确评价肺损伤程度,目前在临床应用中最为广泛。本研究中LUS评分与目前临床广泛使用信度较高的APACHE-Ⅱ、LIS评分进行相关性分析,结果发现LUS评分与APACHE-Ⅱ评分、LIS评分呈正相关,与之前的研究者[11,22-23]研究结论相一致。与金标准胸部CT相比,LUS诊断ARDS准确率、敏感性、特异性、阳性预测值及阴性预测值分别为93.00%、80.70%、97.20%、90.80%、93.60%,表明LUS具有较高的诊断效能,值得临床推广应用。此外,LUS评分及EVLWI的ROC曲线下面积分别为0.933、0.942,LUS评分为20.50分作为界值预测重度ARDS敏感性为88.90%,特异性为79.20%;当LUS评分值≥20.50分时,提示患者病情极严重,ICU住院时间延长,死亡风险明显增加,与Zhao等[11]、Li等[23]研究结果相符。 [参考文献] [1] Afshari A,Brok J,Moller AM,et al. Inhaled nitric oxide for acute respiratory distress syndrome and acute lung injury in adults and children:A systematic review with meta-analysis and trial sequential analysis[J]. Anesth Analg,2011,112(6):1411-1421. [2] Bellani G,Laffey JG,Pham T,et al. Epidemiology,patterns of care,and mortality for patients with acute respiratory distress syndrome in intensive care units in 50 countries[J]. JAMA,2016,315(8):788-800. [3] Mazzei MA,Guerrini S,Cioffi Squitieri N,et al. Role of computed tomography in the diagnosis of acute lung injury/acute respiratory distress syndrome[J]. Recenti Prog Med,2012,103(11):459-464. [4] Volpicelli G,Elbarbary M,Blaivas M,et al. International evidence-based recommendations for point-of-care lung ultrasound[J]. Intensive Care Med,2012,38(4):577-591. [5] 張磊,俞万钧,马坚. 超声在肺部疾病中的临床应用[J]. 中国医学影像技术,2017,33(4):608-611. [6] Huang H,Cui Y,Tian Z,et al. Value of lung ultrasonography in the diagnosis of acute respiratory distress syndrome[J]. Zhonghua Wei Zhong Bing Ji Jiu Yi Xue,2014, 26(8):606-608. [7] Wang Y,Shen Z,Lu X,et al. Sensitivity and specificity of ultrasound for the diagnosis of acute pulmonary edema:A systematic review and meta-analysis[J]. Med Ultrasound,2018,1(1):32-36. [8] Corradi F,Brusasco C,Pelosi P. Chest ultrasound in acute respiratory distress syndrome[J]. Curr Opin Crit Care,2014,20(1):98-103. [9] Ma H,Huang D,Guo L,et al. Strong correlation between lung ultrasound and chest computerized tomography imaging for the detection of acute lung injury/acute respiratory distress syndrome in rats[J]. J Thorac Dis,2016, 8(7):1443-1448. [10] Bataille B,Rao G,Cocquet P,et al. Accuracy of ultrasound B-lines score and E/Ea ratio to estimate extravascular lung water and its variations in patients with acute respiratory distress syndrome[J]. J Clin Monit Comput,2015,29(1):169-176. [11] Zhao Z,Jiang L,Xi X,et al. Prognostic value of extravascular lung water assessed with lung ultrasound score by chest sonography in patients with acute respiratory distress syndrome[J]. BMC Pulm Med,2015,15(9):98-105. [12] Soummer A,Perbet S,Brisson H,et al. Ultrasound assessment of lung aeration loss during a successful weaning trial predicts postextubation distress[J]. Crit Care Med,2012,40(7):2064-2072. [13] Monastesse A,Girard F,Massicotte N,et al. Lung ultrasonography for the assessment of perioperative atelectasis:A pilot feasibility study[J]. Anesth Analg,2017,124(2):494-504. [14] Volpicelli G. Point of care lung ultrasound[J]. Praxis,2014,103(12):711-716. [15] Tagami T,Ong MEH. Extravascular lung water measurements in acute respiratory distress syndrome:Why,how,and when?[J]. Curr Opin Crit Care,2018,24(3):209-215. [16] Sakka SG,Klein M,Reinhart K,et al. Prognostic value of extravascular lung water in critically ill patients[J]. Chest,2002,122(6):2080-2086. [17] Jozwiak M,Silva S,Persichini R,et al. Extravascular lung water is an independent prognostic factor in patients with acute respiratory distress syndrome[J]. Crit Care Med,2013,41(2):472-480. [18] Dong Y,Liang X,Yu X. Prognostic value of the dynamic changes in extra vascular lung water index and angiopoietin-2 in severe multiple trauma patients with acute respiratory distress syndrome[J]. Zhonghua Wei Zhong Bing Ji Jiu Yi Xue,2019,31(5):571-576. [19] 王敏佳,龔仕金,严静,等. 肺部超声B线数目与血管外肺水的相关性分析[J]. 浙江医学,2016,38(2):109-111. [20] Mach K. Staphylococcus epidermidis infection. Results of three groups evaluated according to APACHE Ⅱ-severity of disease classification system-with reference to risk,mortality and prognosis[J]. Wien Klin Wochenschr,1992, 104(17):540-542. [21] Murray JF,Matthay MA,Luce JM,et al. An expanded definition of the adult respiratory distress syndrome[J]. Am Rev Respir Dis,1988,138(3):720-723. [22] Santos TM,Franci D,Coutinho CM,et al. A simplified ultrasound-based edema score to assess lung injury and clinical severity in septic patients[J]. Am J Emerg Med,2013,31(12):1656-1660. [23] Li L,Yang Q,Li L,et al. The value of lung ultrasound score on evaluating clinical severity and prognosis in patients with acute respiratory distress syndrome[J]. Zhonghua Wei Zhong Bing Ji Jiu Yi Xue,2015,27(7):579-584. (收稿日期:2020-03-12)

