富马酸依美斯汀治疗慢性荨麻疹的疗效研究
孙蔚凌,吴国勤,王 军
(1.南京医科大学第一附属医院/江苏省人民医院皮肤科,南京 210029;2.复旦大学附属中山医院皮肤科,上海 200032;3.皖南医学院弋矶山医院皮肤性病科,安徽芜湖 241001)
富马酸依美斯汀的化学名为1-(2-乙氧基乙基)-2-(4-甲基-1-高哌嗪基)苯并咪唑双富马酸盐,属于组胺H1受体拮抗剂。该药物还可抑制钙离子内流进入嗜碱性粒细胞细胞膜,抑制细胞内的钙离子释放[1]。富马酸依美斯汀在化学结构上与传统的苯并咪唑类H1受体拮抗剂不同,将苯并咪唑2-位哌啶环变为7元杂环,具有较强的选择性和竞争性拮抗H1受体活性,抗胆碱和抗5-HT等中枢神经不良反应较弱。富马酸依美斯汀缓释胶囊为缓释剂型,经口服给药后起效迅速,能够较长时间平稳地维持有效血药浓度[2]。为了评估富马酸依美斯汀治疗慢性荨麻疹的有效性和安全性,本研究在多家医院开展富马酸依美斯汀治疗慢性荨麻疹的临床试验,现报道如下。
1 资料与方法
1.1 一般资料
选取2019年7—12月于南京医科大学第一附属医院、复旦大学附属中山医院、皖南医学院弋矶山医院就诊的119例慢性荨麻疹患者为研究对象。纳入标准:(1)年龄18~65岁,男女不限;(2)符合慢性荨麻疹的临床诊断标准;(3)病程大于6周;(4)1周内没有服用抗组胺药物;(5)3个月内没有服用皮质类固醇激素或参加其他药物的临床研究者;(6)患者在入组时有荨麻疹的症状和体征;(7)同意参加研究并签署知情同意书。排除标准:(1)妊娠或哺乳期妇女;(2)有严重心、肝脏、肾脏、血液系统和精神疾病者;(3)对研究药品的同类药物过敏者;(4)物理性荨麻疹。剔除标准:(1)依从性差,严重违背研究方案者;(2)试验期间泄盲者;(3)失访者;(4)因严重不良反应终止用药者不列入疗效统计,但列入不良反应统计;(5)因其他原因不能或不愿参加研究者。所有患者根据治疗方式分试验组和对照组,试验组59例,对照组60例。两组一般资料比较,差异无统计学意义(P>0.05),具有可比性。
1.2 方法
1.2.1试验方法
本临床试验采用随机、双盲、阳性药平行对照、多中心临床研究。随机数字表由南京医科大学统计学专业人员提供,利用SAS软件模拟产生。由本次临床研究无关人员完成药品编盲。若所选病例符合纳入标准,则按入组顺序得到相应经随机编号后的药品。研究者分次提供每位患者同一编号、足够1个访视期的研究药品。
试验组于早餐后口服富马酸依美斯汀缓释胶囊(四川德峰药业有限公司提供,批号190601,2毫克/粒)1粒+氯雷他定模拟片1片,晚餐后口服富马酸依美斯汀缓释胶囊1粒。对照组于早餐后口服氯雷他定片(常州四药制药有限公司生产,批号20180811,10毫克/片)1片+富马酸依美斯汀模拟胶囊1粒,晚餐后口服富马酸依美斯汀模拟胶囊1粒。所有患者用药2周,分别于用药前、用药后第(7±1)、(14±2)天随访检查,评价疗效并进行安全性评估。
1.2.2疗效评价
(1)症状和体征评分总分。由患者在“患者日记”上每日详细记录服药前后风团的数目、大小、皮肤瘙痒和每日发作次数的情况,并记录症状和体征评分总分,比较治疗前、用药后1、2周总分变化,见表1。(2)总分改善率。总分改善率=(治疗前总分-治疗后总分)/治疗前总分×100%。(3)疗效。疗效分临床控制、显效、进步、无效4级评定,总分改善率大于或等于90%为临床控制,60%~<90%为显效,20%~<60%为进步,<20%为无效,总有效=临床控制+显效。

表1 慢性荨麻疹症状和体征评分标准
1.2.3安全性评估 通过一般体格检查、实验室检查的异常表现和心电图Q-T间期的变化来发现不良事件,进而评估药物的安全性。
1.3 统计学处理
2 结 果
2.1 两组总分下降值及总分改善率比较
用药后1、2周两组总分下降值和总分改善率比较,差异无统计学意义(P>0.05)。用药前及用药后1、2周两组组内前后比较,差异有统计学意义(P<0.05),见表2。
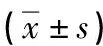
表2 两组总分下降值及总分改善率比较
2.2 疗效比较
用药后2周同一中心两组间及不同中心相同组间临床控制率和总有效率比较,差异均无统计学意义(P>0.05),见表3。
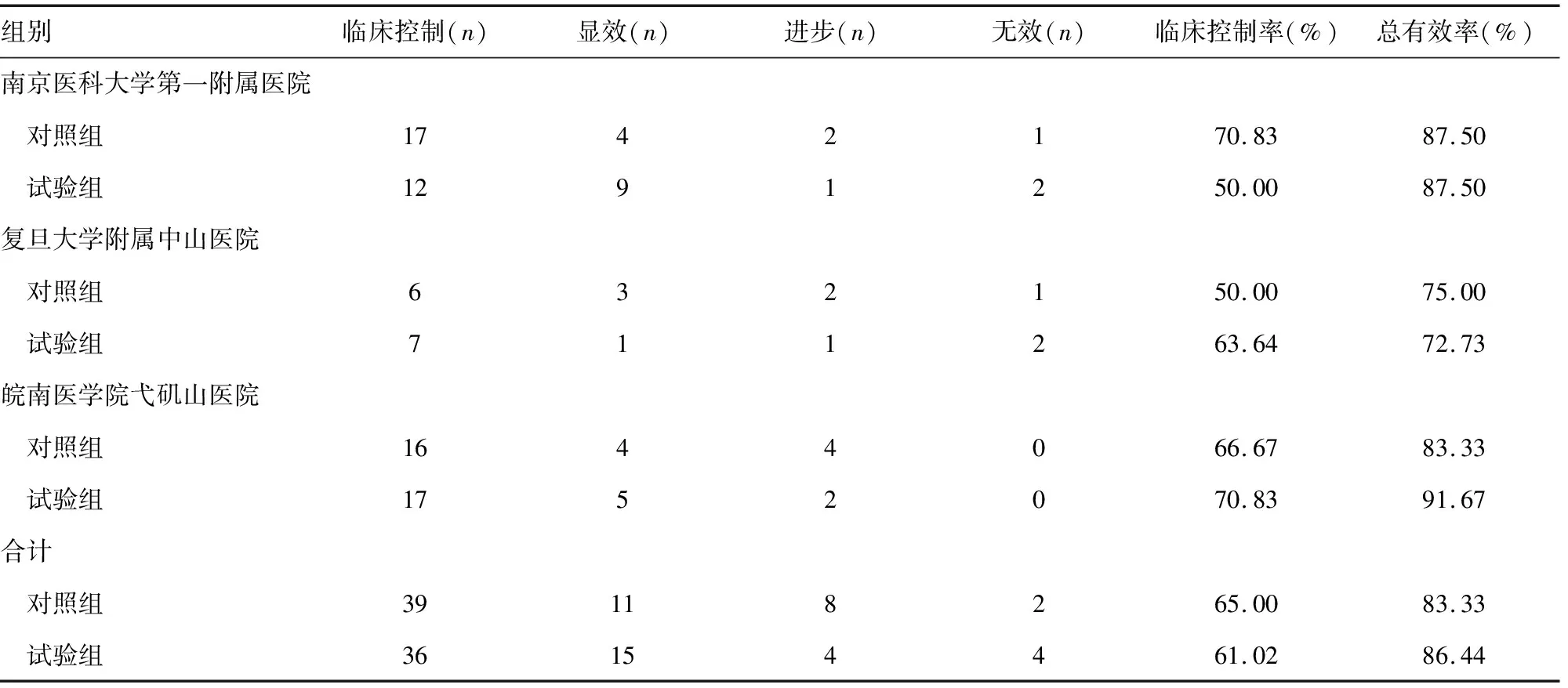
表3 疗效比较
2.3 两组安全性比较
试验组7例(11.86%)和对照组5例(8.33%)发生不良反应,主要表现在中枢神经系统(困乏、嗜睡)、心血管系统(胸闷、心悸)、消化系统(上腹不适、腹痛)及口干、腰酸,经统计学分析,结果显示两组不良反应发生率比较,差异无统计学意义(P>0.05)。试验组1例患者用药后出现丙氨酸氨基转移酶(ALT)升高(已随访至正常),1例出现室性早搏(此不良事件为频发室性早搏,经治疗患者仍有偶发室性早搏,经组长单位伦理委员会专家鉴定为“与试验药可能无关”)。
3 讨 论
荨麻疹是由于皮肤、黏膜小血管扩张及渗透性增加出现的一种局限性水肿反应。荨麻疹在临床上主要表现为风团和(或)血管性水肿[3],在10%~20%的病例中,血管性水肿可以是最早出现且唯一出现的临床表现[4]。慢性荨麻疹是指风团每天发作或间歇发作,持续时间大于6周[3]。荨麻疹发病机制复杂,肥大细胞是关键的效应细胞,通过免疫和非免疫机制被诱导活化[5-7]。肥大细胞脱颗粒后,导致组胺及多种炎性因子产生,影响荨麻疹发生、发展、预后和治疗反应。
富马酸依美斯汀是一种高度选择性的新型抗组胺H1受体拮抗剂,能选择性和竞争性拮抗H1受体活性[8-9]。体外试验显示富马酸依美斯汀能浓度相关性地抑制组胺和白三烯C4(LTC4)的释放。富马酸依美斯汀具有很强的Ⅰ型变态反应抑制作用,对Ⅱ、Ⅲ、Ⅳ型变态反应抑制作用较弱。研究显示,除了拮抗组胺受体,依美斯汀还具有一定的抗炎作用[10]。在体外结膜成纤维细胞模型,富马酸依美斯汀能抑制激动剂诱导的组胺和白细胞介素(IL)-1、IL-6、IL-8的释放,抑制细胞间黏附分子-1(ICAM-1)的表达[11]。根据富马酸依美斯汀的作用机制,临床上常用于过敏性结膜炎、过敏性鼻炎及荨麻疹等过敏性疾病的治疗[12],已在西欧、拉丁美洲、土耳其、以色列、埃及、韩国等地上市销售[13]。此外,富马酸依美斯汀抑制磷脂酰肌醇水解效果显著,同时对嗜酸性粒细胞的趋化作用和上皮细胞分泌IL-6、IL-8 等均具有抑制作用,从而有效抑制炎性反应的加剧[14]。最新的一项研究显示,每日口服2 mg富马酸依美斯汀,孕期从母体血液转移给胎儿的药物浓度对胎儿没有造成有害影响,哺乳期从母亲血液转移到乳汁中的药物浓度也没有对婴儿造成不利影响[15],提示依美斯汀具有较高的安全性。
本研究显示,富马酸依美斯汀治疗慢性荨麻疹的总有效率为86.44%,氯雷他定为83.33%,差异无统计学意义(P>0.05)。不良反应的症状和体征主要表现在中枢神经系统(困乏、嗜睡)、心血管系统(胸闷、心悸)、消化系统(上腹不适、腹痛)及口干、腰酸,但两组不良反应发生率比较,差异无统计学意义(P>0.05)。富马酸依美斯汀主要通过肝脏CYP450酶代谢,可能引起个别患者ALT轻度升高,一般停药后不久可恢复正常。
综上所述,富马酸依美斯汀可有效缓解慢性荨麻疹患者的临床症状,治疗效果和氯雷他定相似,安全性较好,值得推广应用。

