芪连结肠宁方治疗腹泻型肠易激综合征脾虚湿热证临床研究
谭华梁,徐寅,肖麟,蒋士生
临床研究
芪连结肠宁方治疗腹泻型肠易激综合征脾虚湿热证临床研究
谭华梁1,徐寅2,肖麟2,蒋士生3
1.湖南中医药大学,湖南 长沙 410036; 2.湖南中医药大学第一附属医院,湖南 长沙 410007; 3.湖南中医药研究院,湖南 长沙 410006
观察芪连结肠宁方治疗腹泻型肠易激综合征(IBS-D)脾虚湿热证的临床疗效、安全性,以及对脑肠肽、肠黏膜屏障功能的影响。采用随机数字表法将96例患者分为观察组和对照组各48例,治疗期间观察组脱落3例,对照组脱落2例、失访1例。观察组予芪连结肠宁方,每日1剂,每日2次,口服。对照组予马来酸曲美布汀胶囊,0.2 g/次,3次/d,口服;双歧杆菌四联活菌片,0.5 g/次,3次/d,口服。2组均连续治疗4周。观察2组临床疗效,比较2组治疗前后中医症状评分、肠易激综合征症状严重程度量表(IBS-SSS)积分、肠易激综合征生活质量量表(IBS-QOL)评分及血清5-羟色胺(5-HT)、血管活性肠肽(VIP)、P物质、二胺氧化酶(DAO)、D-乳酸、内毒素(ET)水平,并进行安全性评价。观察组总有效率为91.11%(41/45),对照组为82.22%(37/45),2组比较差异有统计学意义(<0.05)。与本组治疗前比较,2组治疗后腹痛、大便稀溏、神疲倦怠、大便频次、纳呆评分及IBS-BSS积分降低,IBS-QOL积分升高(<0.05);2组治疗后比较,观察组腹痛、大便稀溏、神疲倦怠、大便频次、纳呆评分明显低于对照组(<0.05),IBS-BSS评分低于对照组(<0.01),IBS-QOL评分高于对照组(<0.01)。与本组治疗前比较,2组治疗后5-HT、VIP、P物质、DAO、D-乳酸及ET水平降低(<0.05);2组治疗后比较,观察组5-HT、VIP、P物质、DAO、D-乳酸及ET水平低于对照组(<0.01)。2组均未见不良反应。芪连结肠宁方治疗IBS-D脾虚湿热证疗效较好,可改善患者中医症状评分,提高生活质量,调节脑肠肽水平,改善肠黏膜屏障功能,安全性较好。
腹泻型肠易激综合征;脾虚湿热证;芪连结肠宁方;脑肠肽;肠黏膜屏障功能
肠易激综合征(irritable bowel syndrome,IBS)主要表现为伴随大便性状或习惯改变的反复发作性的腹痛,该病患病率高,明显降低患者生活质量。临床上,IBS可分为腹泻型(diarrhea-predominant irritable bowel syndrome,IBS-D)、便秘型和混合型,以IBS-D最为常见[1]。目前,IBS的治疗包括调整生活方式、抗焦虑或抑郁、调节肠道菌群、解痉止痛、缓解内脏高敏、调节肠道蠕动等[2],单纯西药治疗效果个体差异较大,中医辨证论治疗效显著[3]。芪连结肠宁方是国家级名老中医蒋士生教授治疗慢性溃疡型结肠炎脾虚湿热证的经验方,实验研究显示具有促进肠黏膜修复、健脾止泻之功[4]。根据“异病同治”原则,笔者采用芪连结肠宁方治疗IBS-D脾虚湿热证,观察临床疗效,现报道如下。
1 资料与方法
1.1 一般资料
选择2017年12月-2019年8月湖南中医药大学第一附属医院脾胃病科门诊患者96例,按随机数字表法分为观察组和对照组各48例,治疗期间观察组脱落3例(治疗后拒绝复查),对照组脱落2例(治疗期间自行停药)、失访1例,最终2组各完成45例。观察组男性24例,女性21例;年龄19~65岁,平均(40.60±12.27)岁;病程2.0~6.5年,平均(4.09±1.27)年;对照组男性28例,女性17例;年龄20~65岁,平均(37.24±8.89)岁;病程2.1~6.4年,平均(4.13±1.16)年。2组一般资料比较差异无统计学意义(>0.05),具有可比性。本研究经湖南中医药大学第一附属医院伦理委员会审查,符合伦理审查相关要求。
1.2 西医诊断标准
参照罗马Ⅳ诊断标准[1]制定西医诊断标准。近3个月平均每周至少1 d出现反复发作的腹痛,并与以下≥2项相关:①与排便相关;②伴大便次数变化;③伴大便性状改变。在诊断前症状至少出现6个月,且近3个月必须符合以上诊断标准,即可诊断为IBS。IBS-D诊断标准:1/4以上排出大便为糊状粪或水样粪(Bristol粪便性状量表6或7型),硬粪或干球粪(Bristol粪便性状量表1或2型)少于1/4。
1.3 中医辨证标准
参照《肠易激综合征中医诊疗专家共识意见(2017)》[5]制定脾虚湿热证辨证标准。主症:大便稀溏、泻下不爽、腹痛隐隐、神疲倦怠;次症:劳累后发作或加重、纳呆、脘闷不舒、口干不欲饮,或口苦口臭;舌脉:舌红边有齿痕、苔黄腻或白腻,脉沉或滑数。具备主症加次症2项,参考舌脉即可明确辨证。
1.4 纳入标准
①符合上述西医诊断标准及中医辨证标准;②病程>1年;③年龄18~65岁;④患者对本研究知情,并签署知情同意书。
1.5 排除标准
①因器质性消化系统疾病或其他系统疾病导致腹泻者;②合并严重的肝肾功能不全、心脑血管疾病者;③妊娠及哺乳期妇女;④精神障碍不能表达及不能配合治疗者;⑤服用影响疗效观察的药物者。
1.6 治疗方法
对照组予马来酸曲美布汀胶囊(杭州民生药业集团有限公司,批号20180130,0.1 g/粒),2粒/次,3次/d,口服;双歧杆菌四联活菌片(杭州远大生物制药有限公司,批号20150817,0.5 g/片),1片/次,3次/d,口服。观察组予芪连结肠宁方,药物组成:黄芪20 g,白术15 g,茯苓15 g,黄连5 g,黄柏10 g,仙鹤草20 g,升麻3 g,泽泻10 g,白芷9 g。每日1剂,湖南中医药大学第一附属医院煎药室制备,用无菌真空袋包装为2袋(200 mL/袋),早晚餐后30 min各1袋,口服。2组均连续治疗4周。
1.7 观察指标
1.7.1 中医症状评分
参照《胃肠疾病中医症状评分表》[6]进行中医症状评分。根据症状的无、轻、中、重,腹痛、大便稀溏、神疲倦怠分别计0、2、4、6分,大便频次、纳呆分别计0、1、2、3分。舌脉不计分。各项中医症状评分之和为中医症状积分。
1.7.2 肠易激综合征症状严重程度量表评分
采用IBS症状严重程度量表(IBS-BSS)[7]评估患者症状严重程度。包括腹痛程度、腹痛时间、腹胀程度、排便满意度、生活受影响程度5个方面,每项100分,共计500分。该量表具有较高的信效度和敏感度,分值越高提示病情越重。
1.7.3 肠易激综合征生活质量量表评分
采用IBS生活质量量表(IBS-QOL)[8]评价患者近4周的生活质量,包括情绪、精神状态、睡眠、精力、躯体功能、饮食、社会角色、躯体角色、性生活共9个维度30个条目,评分越高表明患者生活质量越好。
1.7.4 血清脑肠肽
分别于治疗前后抽取患者空腹外周静脉血5 mL,静置于含有柠檬酸钠试管中20 min,3000 r/min离心20 min,取上清液,置-20 ℃冰箱保存备用。ELISA检测血清5-羟色胺(5-HT)、血管活性肠肽(VIP)、P物质,严格按照试剂盒(深圳市绘云生物科技有限公司,批号20180603)说明书操作。
1.7.5 肠黏膜屏障功能标志物
分别于治疗前后用绿色肝素管抽取患者空腹外周静脉血3 mL,3000 r/min离心10 min。采用JY-DLT全自动快速肠道屏蔽功能分析仪(北京金霞十色生物科技有限公司)与二胺氧化酶/乳酸/细菌内毒素三联试剂盒(安徽安昌生物技术有限公司,批号2401208)检测血浆二胺氧化酶(DAO)、D-乳酸和内毒素(ET)水平。
1.7.6 安全性评价
记录2组治疗过程中可能出现的不良反应,如头晕头痛、胸闷心悸、恶心呕吐、发热皮疹等,监测2组治疗前后血、尿、粪常规,肝、肾功能及心电图。
1.8 疗效标准
参照《中药新药临床研究指导原则(试行)》[9]制定疗效标准。临床痊愈:腹痛缓解,大便性状恢复正常,伴随症状及体征消失;显效:大便次数每日2~3次,近似成形,或便溏而每日仅1次,中医症状积分减少率>70%;有效:腹痛和大便次数、性状有好转,35%<中医症状积分减少率≤70%;无效:未达到上述标准者。积分减少率(%)=(治疗前症状积分-治疗后症状积分)÷治疗前症状积分×100%。总有效率(%)=(临床痊愈例数+显效例数+有效例数)÷总例数×100%。
1.9 统计学方法
2 结果
2.1 2组临床疗效比较
观察组总有效率为91.11%(41/45),对照组为82.22%(37/45),观察组优于对照组(<0.05)。见表1。

表1 2组IBS-D脾虚湿热证患者临床疗效比较(例)
2.2 2组治疗前后中医症状评分比较
与本组治疗前比较,2组治疗后腹痛、大便稀溏、神疲倦怠、大便频次、纳呆评分明显降低(<0.05);2组治疗后比较,观察组上述中医症状评分明显低于对照组(<0.05)。见表2。
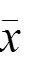
表2 2组IBS-D脾虚湿热证患者治疗前后中医症状评分比较(±s,分)
注:与本组治疗前比较,*<0.05;与对照组治疗后比较,#<0.05
2.3 2组治疗前后肠易激综合征症状严重程度量表评分比较
与本组治疗前比较,2组治疗后IBS-BSS评分明显降低(<0.05);2组治疗后比较,观察组IBS-BSS评分明显低于对照组(<0.01)。见表3。
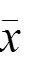
表3 2组IBS-D脾虚湿热证患者治疗前后IBS-BSS评分比较(±s,分)
注:与本组治疗前比较,*<0.05;与对照组治疗后比较,##<0.01
2.4 2组治疗前后肠易激综合征生活质量量表评分比较
与本组治疗前比较,2组治疗后IBS-QOL评分明显升高(<0.05);2组治疗后比较,观察组IBS-QOL评分明显高于对照组(<0.01)。见表4。
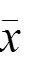
表4 2组IBS-D脾虚湿热证患者治疗前后IBS-QOL评分比较(±s,分)
注:与本组治疗前比较,*<0.05;与对照组治疗后比较,##<0.01
2.5 2组治疗前后血清脑肠肽水平比较
与本组治疗前比较,2组治疗后5-HT、VIP、P物质水平明显降低(<0.05);2组治疗后比较,观察组5-HT、VIP、P物质水平明显低于对照组(<0.01)。见表5。
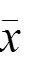
表5 2组IBS-D脾虚湿热证患者治疗前后血清脑肠肽水平比较(±s)
注:与本组治疗前比较,*<0.05;与对照组治疗后比较,##<0.01
2.6 2组治疗前后肠黏膜屏障功能标志物比较
与本组治疗前比较,2组治疗后DAO、D-乳酸、ET水平明显降低(<0.05);2组治疗后比较,观察组DAO、D-乳酸、ET水平明显低于对照组(<0.01)。见表6。
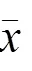
表6 2组IBS-D脾虚湿热证患者治疗前后血清肠黏膜屏障功能标志物水平比较(±s)
注:与本组治疗前比较,*<0.05;与对照组治疗后比较,##<0.01
2.7 2组不良反应
2组治疗期间未见不良反应。
3 讨论
IBS-D属中医学“腹痛”“泄泻”“腹胀”等范畴。该病病位在肠,与脾胃密切相关。《脾胃论》曰:“形体劳役则脾病,脾病则怠惰嗜卧,四肢不收,大便泄泻。”说明劳役过度,导致脾胃亏虚,运化不及,清阳不升而浊气下注,成泄泻之候。然脾虚失运,湿浊停滞,蕴结肠道,可形成湿热之邪,即《临证指南医案•卷六•泄泻》所谓“脾胃久困,湿热滞浊”。蒋士生教授认为IBS-D临床多见此类脾虚湿热之证。脾虚之因有先天不足,更多是后天失养,部分患者因工作压力大,未规律进餐,日久暗耗脾气,致运化失司,故可有神疲倦怠、纳呆等症;水湿停滞,蕴久化热,湿热下迫肠道,腑中气机不畅而有泄泻、腹痛等症。《景岳全书•泄泻》有“泄泻之本,无不由于脾胃”,故治当在清热祛湿同时,要健脾益气。
芪连结肠宁方中黄芪益气健脾,茯苓健脾渗湿,白术健脾燥湿,三药协同益气补中,同时祛除水湿,使脾不为水湿所困;黄连、黄柏清热燥湿,去除脾胃大肠湿热之邪;小剂量升麻与泽泻合用,以升清降浊,恢复胃肠气机;仙鹤草可收敛止泻治其标,还可补虚健脾治其本;白芷辛香温散,能疗风邪久泻,取其风能胜湿也。诸药合用,益气健脾、清热祛湿,使脾胃健,湿热除,泄泻止。本研究显示,芪连结肠宁方可改善患者神疲倦怠和纳呆症状,缓解患者腹痛,改善大便性状,减少大便频次,各项中医症状评分均明显低于对照组(<0.05)。
IBS严重影响患者的生活质量,症状程度越重,生活质量越差。本研究采用IBS-BSS、IBS-QOL分别评估IBS-D患者的症状程度和生活质量。结果显示,观察组治疗后IBS-BSS评分低于对照组(<0.01),IBS-QOL评分高于对照组(<0.01),提示观察组可减轻患者腹痛腹胀程度,改善排便性状和次数,减少生活受影响程度,以提高患者生活质量。
马来酸曲美布汀胶囊是一种胃肠动力调节剂,能双向调节消化道平滑肌运动,具有胃肠兴奋和抑制双向作用,平衡调节患者肠动力状态,缓解患者腹痛不适。IBS-D患者常有肠道菌群失调,由肠球菌、乳酸杆菌、酪酸菌及双歧杆菌组成的双歧杆菌四联活菌能在肠道中形成一层生物性保护屏障,促进肠道菌群平衡恢复,改善患者大便性状。本研究中对照组临床疗效与既往报道基本一致[10]。
脑肠肽是一类分布于脑和胃肠道的小分子物质,具有激素和神经递质双重作用,在调节胃肠蠕动、内脏感觉及精神心理方面有重要作用,常见影响IBS发病的脑肠肽为5-HT、P物质、VIP等。外周或中枢的5-HT、P物质异常增加可引起IBS患者的腹痛、腹泻等症状[11],VIP可刺激胃肠黏膜分泌细胞增加水、电解质的分泌,导致肠液增多,引起IBS患者腹泻和黏液便。肠道黏膜的慢性炎症常可诱发加重IBS,也是IBS临床症状反复出现的病理因素。肠黏膜炎症常导致其屏障功能障碍。目前,血清DAO、D-乳酸、ET是检测肠黏膜屏障功能常用的标志物[12]。脑肠肽和肠黏膜屏障功能标志物的变化能在一定程度上反映IBS的严重程度及治疗效果。本研究显示,2组治疗后5-HT、P物质、VIP、DAO、D-乳酸、ET均下降,提示2组可通过调节IBS-D患者脑肠肽,改善肠黏膜屏障功能,缓解患者腹痛、腹泻等症状。观察组调节脑肠肽、改善肠黏膜屏障功能效果更明显(<0.01)。2组治疗期间未发现不良反应。
综上所述,芪连结肠宁方治疗IBS-D脾虚湿热证患者疗效显著,可改善中医症状,提高患者生活质量,调节脑肠肽水平,促进肠黏膜屏障功能修复,且不良反应少。但本研究缺少随访研究,样本量偏小,有一定局限性,今后将继续深入研究。
[1] MEARIN F, LACY B E, CHANG L, et al. Bowel disorders[J]. Gastroenterology,2016,150:1393-1407.
[2] FORD A C, LACY B E, TALLEY N J. Irritable bowel syndrome[J]. N Engl J Med,2017,376(26):2566-2578.
[3] 万凌峰.中医药治疗腹泻型肠易激综合征的临床研究进展[J].中国中医急症,2020,29(1):171-173.
[4] 蒋士生,李勇敏,朱克俭,等.芪连结肠宁片对大鼠慢性非特异性溃疡性结肠炎的影响[J].中国实验方剂学杂志,2011,17(23):217-219.
[5] 中华中医药学会脾胃病分会.肠易激综合征中医诊疗专家共识意见(2017)[J].中医杂志,2017,58(18):1614-1620.
[6] 中国中西医结合学会消化系统疾病专业委员会.胃肠疾病中医症状评分表[J].中国中西医结合消化杂志,2011,19(1):66-68.
[7] FRANCIS C Y, MORRIS J, WHORWELL P J. The irritable bowel severity scoring system:A simple method of monitoring irritable bowel syndrome and its progress[J]. Aliment Pharmacol Ther,1997,11(2):395-402.
[8] HAHN B A, KIRCHDOERFER L J, FULLERTON S, et al. Evaluation of a new quality of life questionnaire for patients with irritable bowel syndrome[J]. Aliment Pharmacol Ther,1997,11(3):547-552.
[9] 郑筱萸.中药新药临床研究指导原则(试行)[M].北京:中国医药科技出版社,2002:139-142.
[10] 张霞,蒋欢欢,赵汉清,等.双歧杆菌四联活菌胶囊治疗肠易激综合征的临床效果[J].中国医药导报,2016,13(15):154-157.
[11] 王思玉,彭美哲,李享,等.健脾安肠汤联合匹维溴胺治疗肠易激综合征的临床疗效及对血清5-HT、CGRP、SP、VIP水平的影响[J].现代生物医学进展,2019,19(13):2476-2480.
[12] 陈军亮,樊志敏.肠屏障功能常用血清学检测现状及进展[J].结直肠肛门外科,2009,15(3):207-209.
Clinical Study onDecoction for Treatment of Diarrhea-predominant Irritable Bowel Syndrome with Spleen Deficiency and Damp Heat Syndrome
TAN Hualiang1, XU Yin2, XIAO Lin2, JIANG Shisheng3
To observe the clinical efficacy and safety ofDecoction for the treatment of diarrhea-predominant irritable bowel syndrome (IBS-D) with spleen deficiency and damp heat syndrome and its effects on brain-gut peptide and intestinal mucosal barrier function.Totally 96 patients were divided into the observation group and the control group (48 cases in each group) by random number table method. 45 patients in observation group completed the therapy (3 patients were falling off), and 45 patients in control group completed the therapy (2 patients were falling off and 1 patient was missing). The observation group was givenDecoction, 1 dosage a day, twice a day, orally. The control group was given trimebutine maleate capsules, 0.2 g per time, three time a day, orally; and Bifidobacterium quadruple viable tablets, 0.5 g per time, three time a day, orally. The course of treatment in both groups was 4 weeks. The clinical efficacy of the two groups was observed. TCM symptom scores, IBS-SSS score, IBS-QOL score, serum 5-HT, VIP, SP, DAO, D-lactic acid, endotoxin (ET), levels were compared between the two groups before and after treatment. Clinical safety was evaluated.The total effective rate of the observation group was 91.11% (41/45) and that of the control group was 82.22% (37/45), with statistical significance (<0.05). Compared with before treatment, the scores of abdominal pain, loose stool, mental fatigue, stool frequency and anorexia, and IBS-BSS score of the two groups decreased after treatment, IBS-QOL score increased (<0.05). After treatment, the scores of abdominal pain, loose stool, mental fatigue, stool frequency and anorexia in the observation group were lower than those in the control group (<0.05), the IBS-BSS score was lower than that in the control group (<0.01), the IBS-QOL score was higher than that of the control group (<0.01). Compared with before treatment, the levels of 5-HT, VIP, SP, DAO, D-lactic acid and ET in the two groups decreased (<0.05). After treatment, the levels of 5-HT, VIP, SP, DAO, D-lactic acid and ET in the observation group were lower than those in the control group (<0.01). There were no adverse reactions in the two groups.Decoction for IBS-D patients with spleen deficiency and dampness heat syndrome can improve TCM symptom scores, promote quality of life, regulate brain gut peptide, and improve intestinal mucosal barrier function, which has good clinical efficacy and safety.
diarrhea-predominant irritable bowel syndrome; spleen deficiency and damp heat syndrome;Decoction; brain gut peptide; intestinal mucosal barrier function
R259.746.2
A
1005-5304(2021)02-0092-05
10.19879/j.cnki.1005-5304.202008007

全国名老中医药专家传承工作室建设项目(2013年);湖南中医药大学国内一流学科建设资助项目(2018-2020年)
蒋士生,E-mail:282112763@qq.com
(收稿日期:2020-08-01)
(修回日期:2020-09-02;编辑:季巍巍)

