CartoSound指导下肥厚型梗阻性心肌病射频消融治疗
白瑾 刘书旺 冯新恒 冯杰莉 徐昕晔 徐维 陈少敏 李蕾 高炜
肥厚型心肌病(hypertrophic cardiomyopathy,HCM)是以心肌肥厚为特征的心肌疾病,2/3的HCM患者存在左室流出道(left ventricular outflow tract,LVOT)梗阻,即肥厚型梗阻性心肌病(hypertrophic obstructive cardiomyopathy,HOCM)[1-3]。减轻LVOT 压力阶差可改善患者症状和预后。部分患者经过β受体阻滞剂和/或非二氢吡啶类钙离子拮抗剂治疗仍然不能控制LVOT 梗阻引起的症状,需要接受侵入性治疗以减轻LVOT 梗阻。近年来,国内外相继报道射频导管消融术(radiofrequency cat heter ablation,RFCA)可作为一种有效治疗HOCM 的方法[4-9]。本中心在心腔内超声CartoSound三维标测指导下,完成5例HOCM 经皮射频消融室间隔治疗,并随访至术后6个月,笔者评估该手术效果及安全性。
1 资料与方法
1.1 一般资料 分析2018年12月至2019年11月于北京大学第三医院心内科住院,在心腔内超声CartoSound三维标测指导下,经皮射频消融室间隔治疗的5例HOCM 患者资料。患者术前均行经胸心脏超声检查,测量室间隔厚度、收缩期二尖瓣瓣叶前向运动(systolic anterior motion,SAM)现象、LVOT 压力阶差。入选标准:经胸心脏超声诊断为HOCM 伴有LVOT梗阻(SAM 征阳性),静息状态下或活动后LVOT压力阶差>50 mmHg(1 mmHg=0.133 k Pa),经充分药物治疗症状改善不明显或不能耐受或不良反应,有严重临床症状,尤其伴有黑矇、晕厥者。排除标准:肥厚型非梗阻性心肌病、主动脉瓣严重狭窄、终末期心力衰竭、二度以上房室传导阻滞、严重肝肾功能衰竭者。本研究符合2013年修订的《赫尔辛基宣言》对伦理学的要求。
5例患者中,男2例,女3例;平均年龄55.2(45~62)岁;病史4~20 年;室间隔厚度(16.1±2.9)mm;LVOT 压力阶差(105±93.6)mmHg;5例患者均出现心绞痛症状,合并黑矇、晕厥症状者2例,心力衰竭NYHA 心功能Ⅲ级者1例。HCM-SCD 评分平均2.13分(表1)。1例患者在4年前曾在院外接受过乙醇室间隔化学消融术(alcohd septal ablation,ASA)。
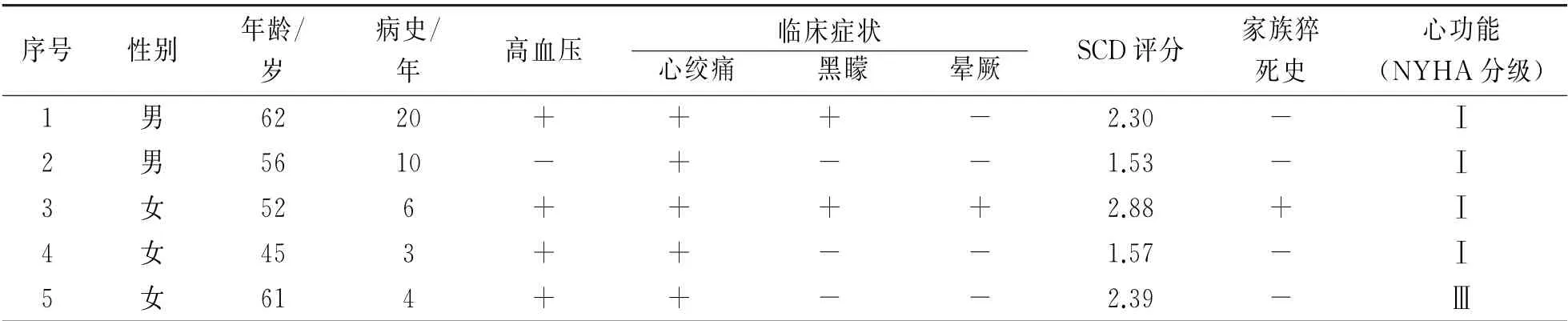
表1 临床资料
1.2 经皮室间隔射频消融术 ①左室测压:右侧股动脉途径置入6F 猪尾导管,跨越主动脉瓣逆行进入左室心腔,分别在左室中部、主动脉瓣下、主动脉瓣上测压,计算LVOT 压力阶差。并静脉输注多巴酚丁胺(Dobutamine,Dob)2.5μg·kg-1·min-1,心率上升10次/分以上,复测LVOT 压力阶差。②左室解剖建模:左侧股静脉途径置入三维诊断超声导管 (Sound Star 3 D,Biosense-Webster,CA,美国),在三维标测系统指导下行左室腔建模,实时观察SA M 现象,并对SA M 对应的室间隔部位进行标记,测量SA M 区面积(图1A)。③左室传导束标测:右侧股动脉途径途径置入Smartouch盐水灌注消融电极(Biosense-Webster,Diamond Bar,CA,美国)进入左室心腔,在三维标测系统指导下,标测心脏正常传达束分布区域,标记His 束及左前分支、左后分支传导束电位(图1B)。④靶部位的选择及消融:以SA M 对应的室间隔部位作为消融首选靶点,消融需避开His束及近端传导束的分布区域(图1C)。
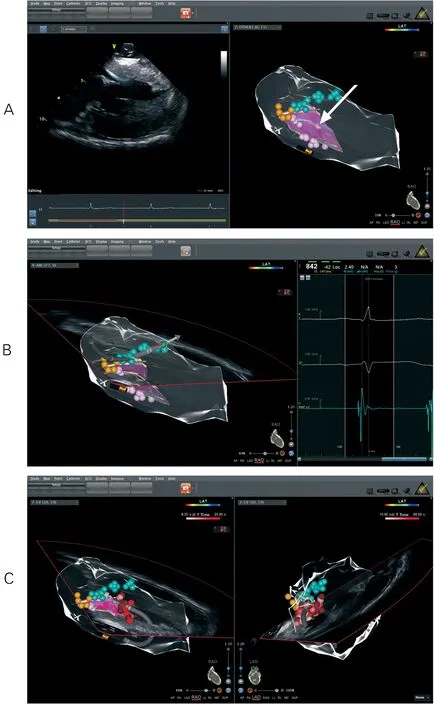
图1 CartoSound界面标测SAM 区、正常传导系统分布区域
手术选择消融能量35~40 W,冷盐水灌注流速20 mL/min,温度43℃,贴靠压力5~10 g,每次放电时间60 s,观察放电后心率、心律、QRS波形态及房室传导情况。消融至SA M 征消失或局部室间隔心肌活动减弱,重复测定LVOT压力阶差及Dob药物负荷后LVOT 压差,以消融后LVOT 压力阶差下降≥50%为消融有效标准。如消融后LVOT 压力阶差无下降或出现左束支传导阻滞、持续性房室传导阻滞等,则放弃进一步消融。术中持续监测患者血压、心率、指脉氧参数,并经左股静脉置入临时起搏电极,设定起搏频率50次/分。在心腔内超声CartoSound界面,实时监测有无心脏瓣膜损伤及心包积液。
2 结果
术前完成LVOT 测压,静息状态LVOT 压力阶差(32±26.3)mm Hg,1例因静息LVOT 压力阶差>70 mmHg,未进行药物负荷,余4例均进行Dob药物输注,药物负荷后LVOT 压力阶差明显升高至(101±37.5)mm Hg,给药后5例均出现心悸、胸闷症状,1例患者出现血压下降,上述临床表现,停药后均恢复正常。5例均完成CartoSound指导下左室心腔三维建模。5例均采用经主动脉逆行途径标测、消融。累计消融放电15~42次,单次消融时间30~60 s。消融范围占SA M 区域比值22.9%~76.6%(表2)。消融后再次Dob药物输注,复测LVOT压力阶差下降至(40.6±37.2)mm Hg。消融后即刻压差明显变化者4例,1例术后即刻LVOT 压力阶差下降不明显,但消融SA M 区域局部心肌活动明显减弱,考虑消融范围满意(达SA M 区域的76.6%),终止手术(图2,表3)。术中一过性左束支传导阻滞1例;5例均未发生手术相关并发症。
5例均完成术后7 天、1 个月、6 个月的随访。随访至术后6个月,5例心绞痛症状均消失,无晕厥、黑矇发作,心功能恢复正常,NY HA 分级I级。术后6个月,超声心动图数据提示仍存在SA M 现象阳性1 例;室间隔厚度由术前(16.1±2.9)mm 下降至(13.3±2.4)mm(术 后6 个 月)(P =0.115);LVOT 压力阶差由术前(105±93.6)mm Hg逐步下降至(94.7±71.9)mmHg(术后7日,P=0.146)、(30.72±12.9)mm Hg(术后1个月,P<0.01)、(19.4±17.8)mm Hg(术后6个月,P<0.01)(图3)。
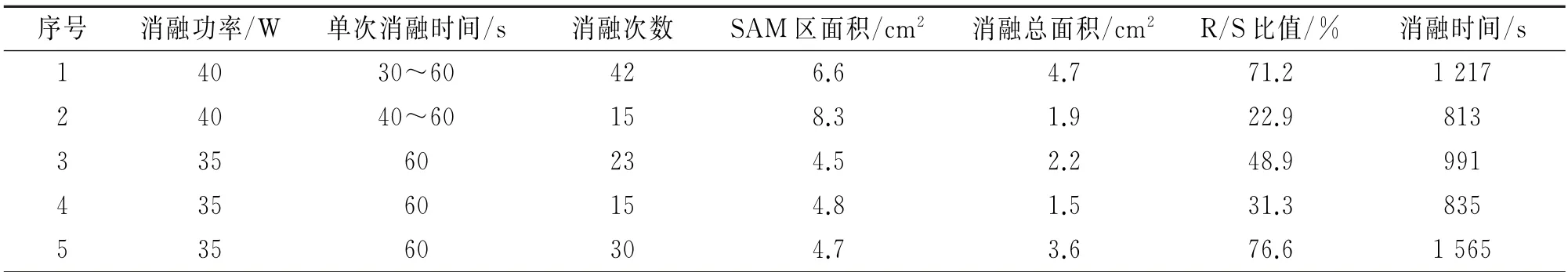
表2 手术参数
3 讨论

图2 术中CartoSound界面,显示术前(A)、术后(B)SAM区超声图像改变(如箭头所示)
HOCM 的临床症状与LVOT 压力阶差有密切关系,目前临床上有效改善LVOT 压力阶差的方法有室间隔心肌切除术(Morr ow 手术)和乙醇室间隔化学消融术(alcohol septal ablation,ASA)。但室间隔心肌切除术创伤较大,技术操作要求较高;而ASA治疗效果依赖于间隔支的解剖走形以及与肥厚间隔心肌的对应关系,而且围术期房室传导阻滞及心肌梗死的发生率高,远期再次梗阻、LVOT 压力阶差升高的现象不容忽视[10-12]。同时,HOCM的患者中,一部分为静息状态即存在LVOT 梗阻,而有一部分患者只有在激发状态下(包括运动、Valsal va动作)才会出现梗阻。我中心治疗的5例患者中第一例患者即为第二种情况,此患者曾在4年前接受过外院ASA 治疗,术后心脏病情好转,但入院前3个月开始出现活动时黑矇,超声心动图检查证实其静息状态下无明显LVOT 压力阶差,但运动负荷后LVOT 存在严重梗阻,同时超声心动图影像提示该患者主动脉瓣下存在室间隔局限性增厚。该患者临床症状显著,但现有病情不宜行再次ASA 治疗。新近国内外研究报道,心腔内超声指导下经皮室间隔射频消融治疗是改善HOCM 患者LVOT压力阶差,尤其是不宜实施Morr ow 手术及ASA 治疗患者的一项有效治疗方法。
2016年Cooper等[5]在心腔内超声指导下射频消融治疗5例HOCM,具体消融参数设置如下:消融功率50~60 W,冷盐水灌注流速30 mL/min,每次放电2 min,放电时间28~42 min。术后6月随访:静息LVOT 压力阶差从(64.2±50.6)下降至(12.3±2.5)mm Hg,活动后LVOT 压力阶差从(93.5±30.9)下降至(23.3±8.3)mm Hg。Shel ke等[6]同样在心腔内超声指导下对7例HOCM 患者行射频消融治疗,并随访12个月,LVOT 压力阶差由术前(81±14.8)mm Hg逐步下降至(48.5±22.6)mm-Hg(术后1个月,P=0.0004);(49.8±19.3)mm Hg(术后6个月,P=0.0004)和(42.8±26.1)mm Hg(术后12个月,P=0.05)。2019年我国陶海龙等[8]总结了该中心的20例HOCM 患者经心腔内超声三维标测指导下射频消融治疗,随访6个月,LVOT压力阶差由术前(106.0±36.5)mm Hg下降至(28.4±12.9)mm Hg(P<0.01)。上述研究结果提示心腔内超声指导下的射频消融治疗有望成为一种有效治疗HCOM 的手段。
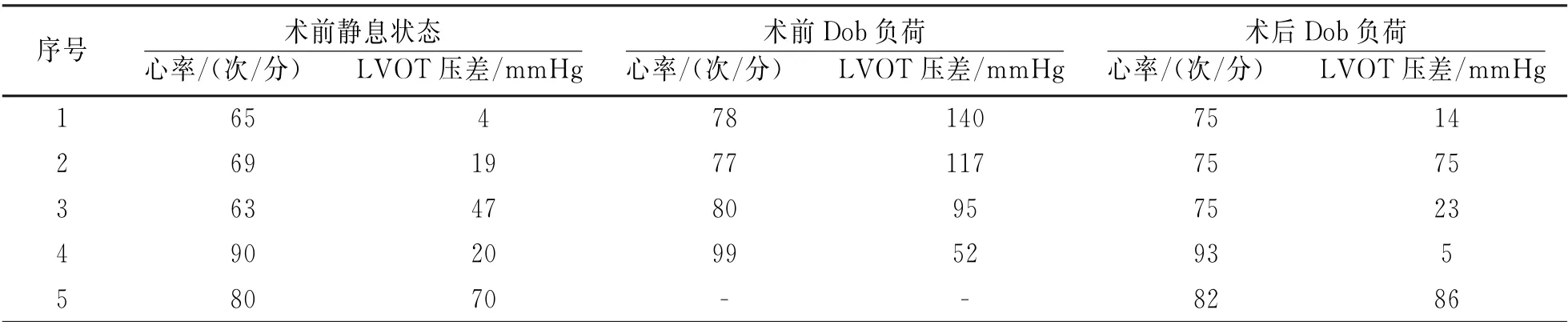
表3 射频消融术中LVOT 压差变化

图3 5例LVOT 压差变化
本中心在心腔内超声CartoSound三维标测指导下对5例HCOM 患者行射频消融治疗,术后随访均取得较满意治疗效果。随访至术后6个月,5例患者心绞痛症状均消失,无晕厥、黑矇发作,心功能恢复正常,NYHA分级I级;超声心动图提示LVOT压力阶差由术前(105±93.6)mmHg下降至(19.4±17.8)mmHg,较消融术前有显著改善(P<0.01)。
5例患者的术后随访证实,该项治疗在取得较好临床效果的同时,“零”手术并发症。但是,回顾Cooper等[5]研究结果发现,该项研究的5例手术患者中出现1例左束支传导阻滞、1例完全性房室传导阻滞、1例腹膜后出血死亡的并发症。其研究中并发症发生较高,进一步分析,考虑与该研究术中采用了较高的消融功率(50~60 W),同时手术消融范围较大有关。5例患者术中射频消融面积为标测SAM 区域的4.7~7.5倍。SAM 征所在室间隔区域理论上均应进行消融,本中心在术中三维标测时发现,SAM 征区域同时包含正常传导系统,为消融“禁区”,故理论上消融范围仅为SAM 区域一部分。故建议消融前应明确标记正常传导束分布,避免消融中伤及正常传导系统。本中心采用较适宜的消融能量35~40 W,术中消融面积仅占SAM 区域面积的22.9%~76.6%;术后5例患者均未出现严重房室传导阻滞及束支阻滞等并发症。故不建议在术中过大范围、过高功率的消融治疗,避免增加手术并发症的风险。
现有的研究报道均建议以射频消融术后测定LVOT 压力阶差显著下降达50%作为手术即刻成功终点。本中心4例患者均在消融后测定LVOT压力阶差显著下降达50%,终止手术;其中一例患者未达到消融后LVOT 压力阶差下降达50%,但在CartoSound界面观察到该SA M 区域局部心肌活动明显减弱,消融范围达SA M 区域的76.6%,考虑消融范围满意,终止手术。术后随访数据显示,该患者术后1个月超声心动图证实LVOT 压力阶差显著下降,由术前257 mm Hg下降至34 mm Hg,患者临床症状缓解,心脏功能显著改善。因此,结合现有研究结果和本中心数据,HOCM 经心内膜面的射频消融靶点应以SA M 区域为主,手术终点主要为LVOT 压力阶差下降达50%以上,但仍要结合患者消融范围,及消融后SA M 征区域心腔内超声直视下影像进行综合判断,考虑到消融局部水肿等可能导致LVOT 压力阶差下降延迟。此外,本中心随访中同样发现射频消融对室间隔局部心肌的损伤存在延迟治疗作用。多数患者临床症状、心功能明显改善,及LVOT 压力阶差明显下降在1~6个月时出现,且多数患者的室间隔厚度较术前并无显著变化。因此,术中盲目扩大消融范围并不能明显消除心肌肥厚,并有增加手术风险的可能。
经皮室间隔射频消融作为治疗HCOM 的一项新技术,对心肌细胞的损伤小,不受间隔支动脉解剖变异的影响,操作风险相对较低,易被患者接受。在心腔内超声CartoSound指导下,明确标测SA M 征区及正常传导束分布区域,并可在术中时时监测心脏状态,辅助射频消融治疗安全、有效。本次总结病例较少,有关消融参数设定、消融终点确定、长期预后及治疗机制等均需要进一步深入研究。

