紫花前胡的提取工艺优化研究
马思楠, 李 欠*,陈玉莹,冯彦梅,余 萍
(1.甘肃省干旱生境作物学重点实验室,甘肃 兰州730070; 2.甘肃农业大学 农学院,甘肃 兰州730070; 3.甘肃省中药材规范化生产技术创新重点实验室,甘肃 兰州730070)
中药紫花前胡是伞形科当归属植物紫花前胡Peucedanumdecursivum(Miq.) Maxim 的干燥根[1]。紫花前胡为常用中药,具有降气化痰,疏散风热的功效,用于治疗风热咳嗽痰多等症[1-2]。现代药理学研究表明,紫花前胡中主要活性成分是香豆素类化合物,其具有抗神经衰弱、抗凝血、抗氧化、抗菌、抗癌等多方面的药理活性[3-4],在药物研发和临床应用中具有广泛应用价值。
中药成分复杂,采用单一指标成分来控制单味药材的质量,具有一定的片面和局限性[5]。因此多指标定量分析受到人们广泛的关注,而中药多指标分析的前提是中药多组分的提取,所以优选适合中药多指标成分的提取工艺参数是关键所在。近年来,响应面法已广泛应用于优化中药提取工艺的研究[6-9],具有试验次数相对较少、检测精确度高、预测的函数模型精准的优点[10-11]。目前对紫花前胡药材研究多集中在单指标成分含量测定,多指标成分含量研究较少[12]。为此,以紫花前胡为研究对象,以香豆素类成分紫花前胡苷、伞形花内酯、花椒毒素、补骨脂素和佛手柑内酯为考察指标进行综合评分,结合响应面法,优化紫花前胡的提取工艺,对进一步提升紫花前胡资源的开发和利用具有重大意义。
1 仪器与试剂
1.1 试验仪器
Waters 高效液相色谱仪(上海市沃特世科技有限公司);KQ-500B超声波清洗仪(深圳市得康科技有限公司);JFSD-100粉碎机(浙江省永康市金穗机械制造厂);AL-104电子分析天平(慈溪市天东衡器厂);T6 新世纪紫外可见分光光度计(北京普析通用仪器有限责任公司)。
1.2 试验材料
对照品伞形花内酯(批号18010202)、紫花前胡苷(批号18030702)、补骨脂素(批号19101703)、花椒毒素(批号17111503)、佛手柑内酯(批号17120501)均购于成都普菲德生物技术有限公司,纯度≥98%;乙腈、甲醇(色谱纯,均购于国药集团化学试剂有限公司);紫花前胡药材采购于甘肃黄河药材市场经甘肃农业大学中药学教研室陈垣教授鉴定为中药紫花前胡。
2 方法
2.1 溶液的制备
2.1.1 对照品溶液的制备
取伞形花内酯、紫花前胡苷、补骨脂素、花椒毒素和佛手柑内酯对照品适量,精密称定,分别置于5 mL容量瓶内,加甲醇溶解并稀释即得对照品储备液。分别精密吸取对照品储备液0.5 mL置于10 mL容量瓶内,加甲醇定容至刻度,摇匀,制成浓度分别为42、41、41、86、56 μg·mL-1的混合对照品溶液,用时加甲醇溶液稀释,得到含有不同质量浓度的混合对照品溶液,备用。
2.1.2 供试品溶液的制备
取紫花前胡药材粉末(过三号筛)1 g,精密称定,置于锥形瓶中,加甲醇25 mL,浸渍1 h后超声(功率250 W、频率50 KHz)提取20 min,取出,冷却补重,摇匀,滤过,取续滤液,即得供试品溶液。进样前用0.45 μL微孔滤膜滤过。
2.2 色谱条件
色谱柱:C18柱(150 mm×4.6 mm,5 μm);流动相:水(A)-乙腈(B),梯度洗脱(0~2 min,20%~25% B;2~18 min,25%~40%B;18~28 min,40%~50%B;28~31 min,50%~65%B;31~45 min,20%B);检测波长:259 nm,325 nm;柱温:30℃;流速:1.0 mL·min-1;进样量:10 μL。在上述条件下伞形花内酯、紫花前胡苷、补骨脂素、花椒毒素、佛手柑内酯的分离度良好,混合对照品及紫花前胡样品HPLC色谱图见图1。
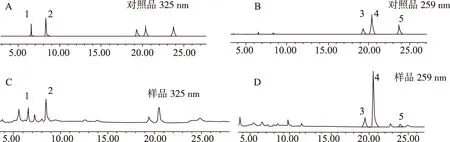
图1 混合对照品(A),(B)和紫花前胡样品(C),(D)的HPLC色谱图Fig.1 HPLC chromatograms of mixed references(A),(B)and sample (C),(D) 注:1-伞形花内酯;2-紫花前胡苷;3-补骨脂素;4-花椒毒素;5-佛手柑内酯
2.3 高效液相色谱法方法学考察
2.3.1 线性关系考察
将上述不同质量浓度的混合对照品按照“2.2”项依次进样,测定并记录各色谱峰峰面积。以溶液质量浓度为横坐标(X),对应峰面积为纵坐标(Y),绘制标准曲线。
2.3.2 精密度试验
取“2.1.1”项下对照品溶液,在“2.2”项色谱条件下,连续进样6次,记录峰面积,分别计算5种香豆素类物质的Relative standard deviation(RSD)值。
2.3.3 稳定性试验
取紫花前胡样品6份,按照“2.1.2”项方法制备供试品溶液,分别于0、2、4、8、12 h进样测定,记录峰面积,分别计算5种香豆素类物质的RSD值。
2.3.4 重复性试验
平行制备6份供试品溶液,在同一试验条件下测定,记录峰面积,分别计算5种香豆素类物质的RSD值。
2.3.5 加样回收率试验
精密称取已知含量的紫花前胡样品1 g,平行6份,分别加入一定量的各对照品储备液,按照“2.1.2”项方法制备供试品溶液,进样,测定峰面积,计算平均加样回收率。
2.4 样品含量测定
精密称量单因素及响应曲面试验样品,按“2.1.2”项方法制备溶液,“2.2”项色谱条件进样测定,平行制备3份,得到样品含量平均值。
2.5 数据标准化处理
将单因素试验和响应面试验的结果进行Z-score 标准化处理[9,13-14],得到5种指标成分的综合评分。
2.6 单因素试验设计
以5种香豆素类成分含量的综合评分值为考察指标,分别考察液料比、甲醇浓度和超声时间对提取率的影响。试验设计方案见表1。
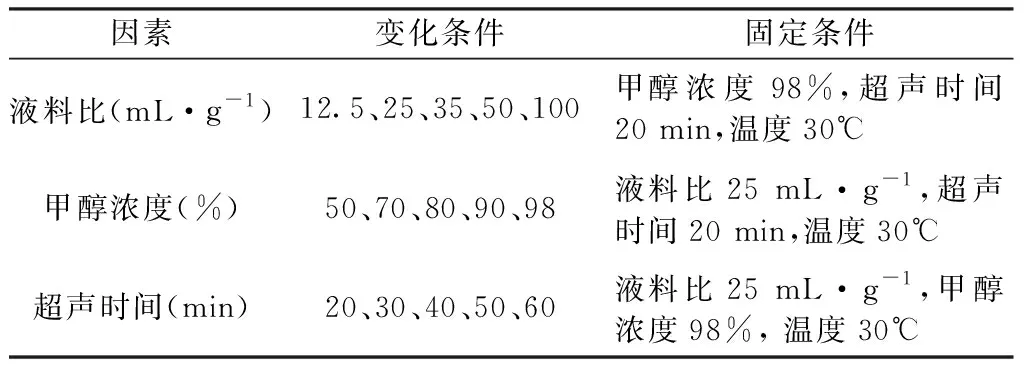
表1 单因素试验条件Table 1 Design of single factor tests
2.7 响应面试验设计方案
以上述优化后的各单因素值为基础,通过Design-Expert 8.0.6 Trial软件Box-Behnken响应面设计,对液料比、甲醇浓度、超声时间3个因素结果进一步优化,重复试验,并进行分析。
3 结果与分析
3.1 方法学考察结果
3.1.1 线性关系考察
分别以对照品的峰面积(X)与对照品溶液浓度(Y)做线性回归,得到伞形花内酯、紫花前胡苷、补骨脂素、花椒毒素和佛手柑内酯的回归方程及线性范围分别为:
Y=19285X+6074.9,R2=0.999 8,线性范围0.07~42.00 μg·mL-1;
Y=38779X+10295,R2=0.999 8,线性范围0.06~41.00 μg·mL-1;
Y=25689X+6779.5,R2=0.999 8,线性范围0.07~41.00 μg·mL-1L;
Y=41421X+28717,R2=0.999 8,线性范围0.14~86.00 μg·mL-1;
Y=24865X-559.34,R2=0.999 9,线性范围0.09~56.00 μg·mL-1。
3.1.2 精密度试验
以峰面积计算得到伞形花内酯、紫花前胡苷、补骨脂素、花椒毒素、佛手柑内酯的RSD分别为0.96%、0.62%、1.08%、0.86%、0.84%,表明该条件下仪器的精密度良好。
3.1.3 稳定性试验
以峰面积计算得到伞形花内酯、紫花前胡苷、补骨脂素、花椒毒素、佛手柑内酯的RSD分别为0.82%、0.15%、0.86%、0.45%、0.86%,表明该供试品溶液在12 h内稳定性良好。
3.1.4 重复性试验
以峰面积计算得到伞形花内酯、紫花前胡苷、补骨脂素、花椒毒素、佛手柑内酯的RSD分别为0.28%、0.61%、1.56%、0.45%、0.86%,表明该方法重复性良好。
3.1.5 加样回收率试验
伞形花内酯,紫花前胡苷,补骨脂素,花椒毒素和佛手柑内酯平均回收率分别为101.31%、105.27%、90.85%、106.42%、90.19% ,RSD分别为2.07%、3.17%、1.62%、2.53%、4.54%,结果显示加样回收率良好。
3.2 单因素试验结果
3.2.1 料液比对综合评分的影响
根据单因素试验设计(表1)进行实验,考察结果采用Z-score标准化处理数据(表2)。当液料比增加时,有利于有效成分扩散,从而增大提取极限[15]。随着液料比增加,有效成分获得足够的扩散空间,提取率达到最佳且基本稳定。考虑到液料比会对溶液的酸碱度产生影响,使紫花前胡中某些香豆素苷类成分结构发生变化,因此液料比35 mL·g-1作为最优选择。
3.2.2 甲醇浓度对综合评分的影响
根据单因素试验设计(表1)进行,考察结果采用Z-score标准化处理数据(表2)。随着甲醇浓度的增加,有利于有效成分脱离固体表面溶解到溶剂主体中,增大溶出率[16],当甲醇浓度达到80%时,五种香豆素类成分总的提取率达到最高,甲醇浓度高于80%,提取率缓慢降低。由于甲醇是中性溶剂且药材成分复杂,对于有效成分的溶解有一定的限制,若甲醇和水按照一定比例溶解,会加速药材中亲脂和亲水性成分的溶出,所以选择甲醇浓度80%为最佳提取浓度。
3.2.3 超声时间对综合评分的影响
根据单因素实验设计(表1)进行实验,考察结果采用Z-score标准化处理数据(表2)。利用超声提取的机械作用、空化作用和热效应,增大溶剂的扩散、浸透和溶解[16],当超声时间在20~40 min时,综合评分逐渐增大,在40~50 min时,综合评分缓慢减小。推测出有效成分随着超声时间的增加,紫花前胡中有效成分逐渐溶出,当到达一定时间后,提取时间的增加会破坏有效成分的析出,因此,选择40 min作为最佳超声时间。

表2 单因素试验结果Table 2 Results of single factor tests
3.3 响应面试验结果
3.3.1 响应面试验设计方案
在单因素试验基础上,根据Box-Behnken响应面法设计原理,设计17个试验点(5个零点)的三因素三水平的响应面分析试验,以料液比(A)、甲醇浓度(B)、超声时间(C)为自变量,5种香豆素类成分含量的综合评分作为响应值,进行Box-Behnken试验设计(表3)。
3.3.2 模型显著性分析
利用Design-Expert 8.0.6 Trial软件对二次多项式回归方程进行拟合,得二次多元回归方程:
R=7.72+1.66A+0.36 B+1.32 C+0.17 AB+0.94AC-0.17BC-7.59A2-5.07 B2-2.16 C2
由表4的方差分析结果可知,该拟合模型具有极显著(P<0.001)失拟项不显著(P=0.2605)。由F值可以看出,所选的各因素水平范围内,对成分提取的影响大小为液料比(A)>超声时间(C)>甲醇浓度(B)。
3.3.3 最佳提取工艺优化与参数预测结果
以5种香豆素类成分含量最大值为目标,运用Design-Expert 8.0.6 Trial软件绘制三维响应面图(图2)并进行预测分析。以各组分综合评分值为评价指标优选紫花前胡最佳提取工艺参数为液料比33.69 mL·g-1,甲醇浓度80.32%,超声时间46.64 min。在此条件下,5种香豆素类成分提取综合评分为5.940 1。

表3 响应面实验设计与结果Table 3 Design and results of Box-Behnken test
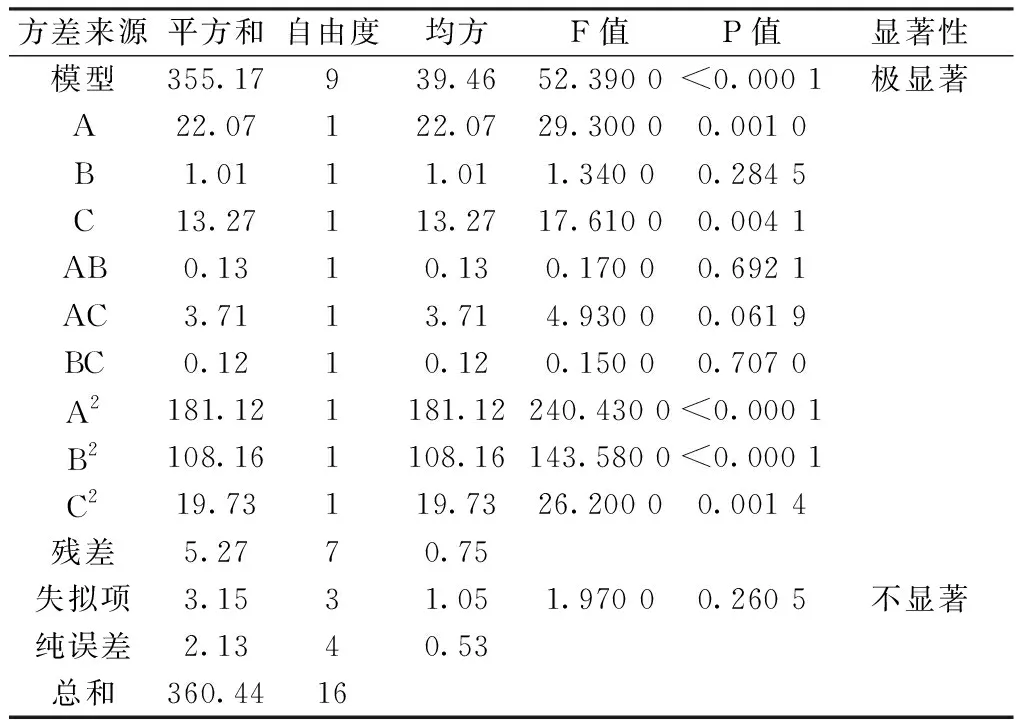
表4 回归模型方差分析Table 6 ANOVA for regression model
3.4 验证试验结果分析
根据最佳提取工艺条件进行验证试验,同时考虑到实际操作的可行性,将工艺参数调整为,液料比34 mL·g-1,甲醇浓度80%,超声时间47 min,重复3次,结果见表5。对结果的均值进行标准化处理后,得综合评分为6.073 4,与预测值5.940 1相比,验证值与预测值偏差为2.28%,模型预测性好,说明优化后的提取工艺可靠,稳定,具有实际应用价值。将《中国药典》2015年版中所使用的含量测定方法制备供试品溶液,与验证试验结果进行比较。根据药典中规定的紫花前胡苷含量为单一评价指标,优化的提取工艺比药典法高;伞形花内酯含量也明显高于药典法,而其它3种香豆素类成分含量无明显变化。因此,基于多指标综合评分法建立的提取工艺参数,其重复性好,操作性强,具有实际应用价值。

图2 紫花前胡提取工艺优化响应面图Fig.2 Optimized response surface map of extraction process of P. decursivum
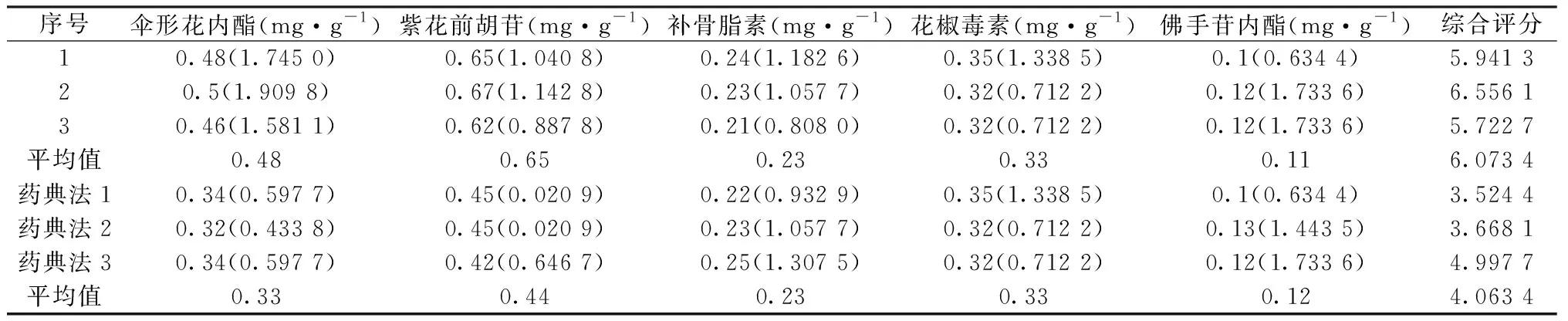
表5 工艺验证结果
4 讨论
中药紫花前胡的研究主要集中在化学成分分离分析和单一成分的药理作用,对于多指标成分含量研究还相对较少。香豆素类是紫花前胡中含量相对较多且生物活性较强的一类化合物[17-19],具有多种药理活性,是广泛分布于植物界中的次生代谢产物[3]。因此,研究紫花前胡中香豆素类化合物具有重大意义。
目前药典中紫花前胡药材质量控制仅以紫花前胡苷单指标性成分作为评价指标[1],而中药成分复杂,单一成分难以综合评价药材质量,无法保证中药临床药效。因此,为了更好的发挥其药用价值,对其化学成分的提取工艺进行优化。提取工艺主要以提取含量作为评价指标,而高效液相色谱法测定药材成分的含量会更加准确和可靠,故本实验选择HPLC法检测5种香豆素类成分即伞形花内酯、紫花前胡苷、补骨脂素、花椒毒素和佛手柑内酯的含量,以这5种香豆素类成分的总提取量为指标进行单因素考察,通过单因素试验选择合适的3因素3水平,以料液比、甲醇浓度和超声时间进行考察,为避免5种成分质量分数差异太大造成低含量成分的影响被掩盖的问题而影响实验结果的准确性,将5种香豆素类成分的含量用Z-score标准化处理得到综合评分作为响应值,再通过Box-Behnken响应面法进行拟合,得到最佳的提取工艺条件,为进一步研究紫花前胡有效成分开发利用提供参考价值。

