CT 血管成像检测血透患者自体动静脉内瘘成形术后血流动力学参数的临床意义
贾秀芬 刘瑾瑾 郑尘非
1.温州医科大学附属第一医院放射科,浙江温州 325000;2.温州医科大学附属第一医院肾内科,浙江温州 325000
血液透析(以下简称“血透”)患者进行自体动静脉内瘘成形术(AVF)治疗现已逐渐成为血透重要的辅助治疗手段之一[1]。但是,由于受反复穿刺操作影响,实施AVF 治疗的血透患者容易出现内瘘闭塞、狭窄、流量不足等情况,造成AVF 功能不良[2]。研究表明[3],AVF 功能不良会增加狭窄风险,而狭窄的形成是AVF 血管通路功能丢失的重要原因,其发生率高达30%。影像学技术是评估血管通路重建是否理想的有效手段,其中,彩超的应用受到限制,如无法提供直观的血管图像而影响诊断结果判断[4-5]。CT 血管成像(CTA)检查则可提供血管图像,而且可通过利用计算机流体力学(computational fluid dynamics,CFD)建立数值模型得到血流速度、剪切力等参数来反映血流动力学情况[6]。有研究发现[7],AVF 血流动力学的变化对尿毒症患者血管通路的成熟与预后均有一定影响。基于此,本研究观察血透患者AVF 术后CTA 检测数据下建立的CFD 中的血流动力学参数,以指导后续AVF功能的评估,改善血透患者预后。
1 资料与方法
1.1 一般资料
回顾性分析2019 年4 月—2020 年4 月温州医科大学附属第一医院80 例血透患者临床资料,其中男43 例,女37 例;年龄42~75 岁,平均(65.31±3.57)岁;原发病:糖尿病肾病46 例,慢性肾小球肾炎25 例,高血压肾病4 例,慢性肾盂肾炎4 例,尿酸性肾病1 例。
纳入标准:①符合《中国血液透析充分性临床实践指南》[8]中血透标准;②血透时间≥3 个月;③自体动静脉内瘘使用时间≥1 个月。排除标准:①存在代谢功能异常、自身免疫系统疾病;②临床资料不完整。根据患者的血透结果将其分为功能不良组(21 例)与对照组(59 例)。功能不良组男12 例,女9 例;年龄42~74 岁,平均(65.27±3.76)岁;原发病:糖尿病肾病12 例,慢性肾小球肾炎7 例,高血压肾病1 例,慢性肾盂肾炎1 例。对照组男31 例,女28 例;年龄44~75 岁,平均(65.25±3.79)岁;原发病:糖尿病肾病34 例,慢性肾小球肾炎18 例,高血压肾病3 例,慢性肾盂肾炎3 例,尿酸性肾病1 例。两组一般资料比较,差异无统计学意义(P >0.05)。本研究经医院医学伦理委员会批准。
1.2 方法
1.2.1 检查方法 使用64 排螺旋CT 机(GE 公司,Optima CT660 型),先行CT 平扫,再行造影剂增强扫描,即高压注射器将100 mL 非离子型造影剂碘海醇(GE Healthcare AS)以3~4 mL/s 的速度注入对侧肢体。CT扫描参数:层厚1.2 mm,层间隔1.0 mm。
1.2.2 AVF 功能不良评估方法 血透时患者的血流量<200 m/min 或静脉压>200 mmHg(1 mmHg=0.133 kPa)则评估为AVF 功能不良[9]。
1.3 观察指标
1.3.1 AVF 功能状况 统计AVF 功能不良例数,计算发生率。
1.3.2 AVF 后血流动力学参数 结合CT 检查数据,汇总两组吻合口静脉端血流速度与桡动脉剪切力并进行比较。
1.3.3 血流动力学对AVF 功能的影响 采用logistic 回归分析吻合口静脉端血流速度、桡动脉剪切力对AVF功能不良的影响。
1.3.4 预测价值 绘制受试者工作曲线(ROC)得到曲线下面积(AUC),检验CTA 检测数据下建立的CFD中血流动力学参数预测AVF 功能不良的价值。
1.4 统计学方法
采用SPSS 24.0 统计学软件进行数据分析,计量资料用均数±标准差()表示,两组间比较采用t 检验;计数资料用例数或百分率表示,组间比较采用χ2检验;CTA 检查血流动力学参数与AVF 功能不良的关系采用logistic 回归分析;绘制ROC 得到AUC,检验CTA 检查血流动力学参数预测AVF 功能不良的价值,AUC 值>0.90 表示预测性能较高,>0.70~0.90表示有一定的预测性能,0.50~0.70 表示预测性能较差。以P <0.05 为差异有统计学意义。
2 结果
2.1 两组AVF 后血流动力学参数比较
功能不良组AVF 后吻合口静脉端血流速度低于对照组,桡动脉剪切力高于对照组,差异有统计学意义(P <0.05)。见表1。
表1 两组AVF 后血流动力学参数比较()
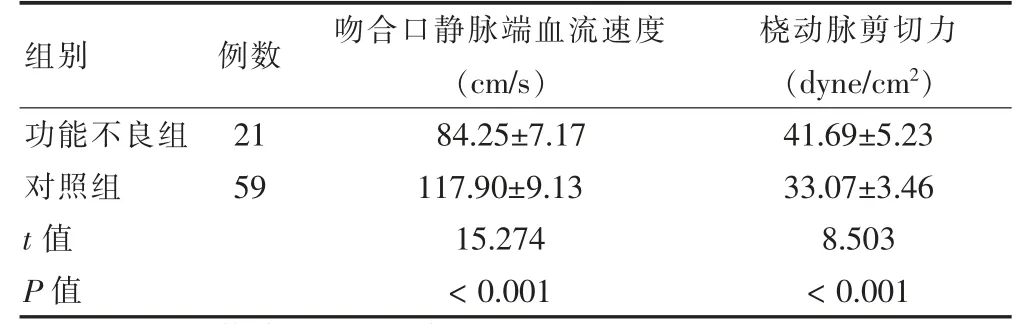
表1 两组AVF 后血流动力学参数比较()
注:AVF:动静脉内瘘成形术
2.2 血流动力学对AVF 功能的影响
将AVF 后吻合口静脉端血流速度、桡动脉剪切力作为协变量,AVF 后功能不良作为因变量(1=功能不良,0=正常),logistic 回归分析结果显示,吻合口静脉端血流速度缓慢、桡动脉剪切力高是AVF 后功能不良的影响因素(OR >1,P <0.05)。见表2。
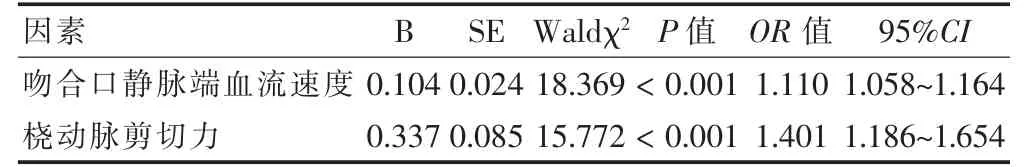
表2 血流动力学对AVF 功能的影响
2.3 血流动力学参数预测AVF 功能不良的价值
ROC 曲线发现,吻合口静脉端血流速度、桡动脉剪切力单项检测用于AVF 功能不良预测的AUC 分别为:0.847、0.843,联合检测为0.943。见表3、图1。
3 讨论
AVF 功能不良发展严重可造成AVF 狭窄,严重影响患者预后。故早期评估AVF 功能和诊断AVF 狭窄对血透患者具有重要意义。
研究表明[10],行AVF 治疗的血透患者发生AVF功能不良风险较高。本研究结果显示,80 例患者AVF后功能不良发生率为26.25%,提示AVF 功能不良的发生率较高,与上述结果一致。目前血管检查的金标准是“数字减影血管造影(DSA)”,但DSA 检查具有创伤性,应用受限[11-13]。超声检查则避免了该局限,但超声检查又因易受含气肺组织、肋骨等影响,继而影响结果的准确判读,降低准确性[14-15]。研究表明[16-18],CTA 对脑血流动力学有一定评估价值,可反映狭窄的发生和程度,提示CTA 也可评估血管情况。

表3 血流动力学参数预测AVF 功能不良价值

图1 ROC 曲线图
本研究经结果显示,功能不良组吻合口静脉端血流速度低于对照组,桡动脉剪切力高于对照组(P <0.05),且ROC 曲线结果显示吻合口静脉端血流速度缓慢、桡动脉剪切力高是AVF 后功能不良的影响因素,二者单项和联合用于AVF 后功能不良预测的AUC>0.80,有一定预测价值,上述结果均提示经CTA检测数据下建立的CFD 血流动力学参数中,吻合口静脉端血流速度、桡动脉剪切力是导致AVF 后功能不良的因子,可作为AVF 后早期功能不良风险的预测指标。分析可能原因为:血流对机体血管壁产生的机械力主要包括血液流动产生的剪切力和牵张力、压力[19]。其中,剪切力对内皮细胞和静脉内膜均具有较大的影响,剪切力的稳定较为重要[20]。剪切力与血流量、血流速度呈正相关,当患者未得到有效的动静脉扩张,将造成AVF 血流量减少,延缓血流速度,此时剪切力降低,造成振荡剪切力[21]。本研究吻合口桡动脉端血流速度增大,故桡动脉剪切力增高,吻合口静脉端血流速度降低,剪切力下降,从而产生不稳定的剪切力,而不稳定的剪切力会造成血管内皮功能紊乱,对血管内皮细胞功能产生破坏,增加内皮增生,从而诱导或加重血栓形成,导致AVF 后功能不良发生甚至狭窄[22]。同时,血流量、血流速度降低,低剪切力也会损伤内皮细胞,诱发氧化应激,导致静脉内膜增生和血栓,影响AVF 功能[23]。AVF 建立后,吻合口局部血流动力学的变化可能会损伤细胞,激活下游信号传导通路,介导各种细胞因子的合成与分泌,对邻近细胞产生影响[24]。尤其是发生内皮细胞损伤,将造成各种生长因子分泌的增加而导致平滑肌细胞迁移与增殖加快,引起静脉内膜异常增生,进一步减慢血流速度,同时增加AVF功能不良的发生风险[25]。因此,吻合口静脉端血流速度、桡动脉剪切力是AVF 功能不良的影响因素。此外,研究表明,AVF 功能不良的主要原因是静脉内膜增生加速[26]。静脉内膜异常增生会造成静脉狭窄,一方面对AVF 功能产生负面影响,一方面造成血流量的减少和血流速度的降低[27-28]。进一步证实本研究结果。
综上所述,血透患者自体AVF 术后AVF 功能不良发生率高,可能与术后吻合口静脉端血流速度缓慢、桡动脉剪切力高有关,CTA 检测数据下建立的CFD模型所体现的吻合口静脉端血流速度、桡动脉剪切力可预测AVF 术后功能不良风险。

