GeneXpert实时荧光定量PCR在诊断艰难梭菌感染中的临床应用*
程敬伟,刘畅,肖盟,孙宏莉,王瑶,杨启文,徐英春
(1.首都医科大学附属北京友谊医院检验科,北京 100050;2.清华大学附属华信医院检验科,北京 100016;3.中国医学科学院北京协和医院检验科,北京100730)
艰难梭菌(Clostridiumdifficile)是一种产芽胞革兰阳性厌氧菌。大量应用广谱抗生素、免疫抑制剂或化疗药物可导致肠道菌群失调,艰难梭菌优势繁殖并分泌毒素而引发艰难梭菌感染(Clostridiumdifficileinfection, CDI)[1]。临床上,约10%~25%的抗生素相关性腹泻及90%以上的伪膜性肠炎由CDI引起[2]。近年来,一种高毒力核糖体型别027型(RT027)艰难梭菌在欧美等国家大规模暴发流行,该菌株感染引起的发病率、复发率及死亡率更高[3]。目前,RT027型菌株已在我国的北京、广州、武汉、香港和台湾等地区分离报道[4-6]。CDI主要的诊断方法包括传统的厌氧培养法、基于酶免疫反应的谷氨酸脱氢酶(GDH)和毒素A/B检测,以及核酸扩增技术(nucleic acid amplification tests, NAATs)检测毒素基因等,各方法的敏感性、特异性存在一定差异。GeneXpert艰难梭菌核酸检测试剂盒基于实时荧光多重PCR技术,可同时检测毒素B基因、二元毒素基因以及tcdC基因117位的缺失(报告是否为RT027型菌株)。本研究旨在评价GeneXpert试验诊断CDI的临床应用价值。
1 材料和方法
1.1标本来源 收集2016年1月至2017年6月北京协和医院住院腹泻患者非重复粪便标本296份。患者年龄2~95岁,中位年龄58岁;男性患者占51%;内科患者占58%,外科患者占15%,其他科室患者占27%。
1.2主要仪器和试剂 GeneXpert系统及配套的艰难梭菌检测试剂盒(美国Cepheid公司),S100 Thermal Cycle PCR扩增仪(美国伯乐公司),毛细管电泳用ABI 3730测序仪(美国应用生物系统公司),艰难梭菌鉴定培养基(CDIF)、哥伦比亚血琼脂培养基、厌氧产气袋(法国生物梅里埃公司),基质辅助激光解吸电离飞行时间质谱(matrix-assisted laser desorption/ionization time of flight mass spectrometry,MALDI-TOF MS)仪(德国Bruker Doltanics公司)。
1.3GeneXpert试验 用拭子取少量不成形粪便,拭子在样本处理试剂中混悬,将样品管中所有液体移入检测盒的样品室,将检测盒载入GeneXpert全自动医用PCR分析系统中,根据产品说明书进行操作和结果判读。报告:仅有内参基因阳性为产毒艰难梭菌阴性;内参基因阳性及tcdB基因阳性为产毒素B艰难梭菌;内参基因阳性、tcdB基因阳性、tcdC基因阳性且二元毒素基因阳性,报告为核糖体型别027型菌株。
1.4产毒素培养(toxigenic culture, TC) TC指粪便培养分离艰难梭菌,再用PCR方法检测菌株是否含有毒素基因。TC阳性:培养分离出艰难梭菌,且检测到毒素基因;TC阴性:未分离出艰难梭菌,或分离到艰难梭菌但未检测到毒素基因。
1.4.1艰难梭菌培养及鉴定 取不成形粪便标本直接接种于CDIF培养基,置于厌氧产气袋37 ℃培养48 h,将具有黑色菌落特征的菌株转种至哥伦比亚血琼脂培养基,厌氧培养48 h后取单菌落进行MALDI-TOF MS质谱鉴定。将单菌落均匀涂布于质谱靶板上,滴加1 μL HCCA肉桂酸基质,待干燥后参照仪器说明书上机检测。
1.4.2艰难梭菌毒素基因检测 使用五重PCR的方法扩增艰难梭菌的16S rDNA、毒素A、B编码基因tcdA、tcdB以及二元毒素基因cdtA、cdtB,并对tcdA基因是否存在1.8 kb片段缺失进行确证[7-8]。引物见表1。
1.5PCR-核糖体分型 PCR扩增艰难梭菌核糖体DNA基因间隔区(rDNA intergenic spacer region, ISR),其中16S-USA端引物使用5′-FAM进行荧光标记,在ABI 3730测序仪上用毛细管电泳的方法对扩增产物进行检测,将数据提交至数据库http://webribo.ages.at并确定菌株核糖体型别[9],引物见表1。

表1 艰难梭菌毒素基因扩增及分型引物
1.6统计学分析 采用SPSS 22.0软件,以TC结果为参考,计算GeneXpert试验的敏感性、特异性、阳性预测值、阴性预测值,用Kappa检验评价结果一致性。
2 结果
2.1TC结果 296份粪便标本中,共培养出艰难梭菌152株,其中tcdA+tcdB+cdtA/cdtB+(A+B+CDT+)型3株、tcdA+tcdB+cdtA/cdtB-(A+B+CDT-)型113株、tcdA-tcdB+cdtA/cdtB-(A-B+CDT-)型18株、不产毒菌株tcdA-tcdB-cdtA/cdtB-(A-B-CDT-)18株。共检出毒素基因阳性菌株134例。部分菌株五重PCR扩增产物电泳及tcdA基因扩增产物电泳结果见图1、图2。
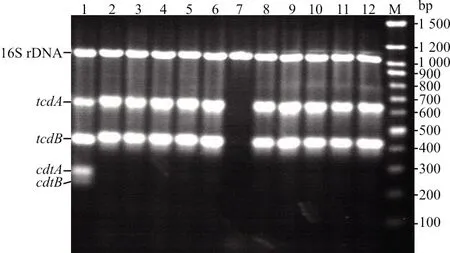
注:1号菌株,tcdA、tcdB、cdtA、cdtB基因阳性;2—6、8—12号菌株,tcdA、tcdB基因阳性;7号菌株,阴性;M,100 bp ladder marker。

注:M,2 000 bp marker;a、b、c、d、e、h、i、j、k,菌株无tcdA缺失;f、g,菌株tcdA缺失。
2.2GeneXpert试验结果 296份标本中,GeneXpert报告阳性标本144份,阴性标本152份,阳性标本中包括142份产毒素B艰难梭菌,2份RT027型艰难梭菌。
2.3GeneXpert与TC检测结果的比较 以TC为参考,GeneXpert试验的敏感性为98.5%,95%置信区间为94.7%~99.8%;特异性为92.6%,95%置信区间为87.4%~96.1%;阳性预测值为91.7%,95%置信区间为85.9%~95.6%;阴性预测值为98.7%,95%置信区间为95.3%~99.8%。2种方法总一致率为95.3%,一致性检验Kappa值为0.905,GeneXpert与TC一致性好,见表2。GeneXpert与TC检测结果不一致的标本有14份,其中GeneXpert阳性、TC阴性标本12份,包括未培养出菌株标本9份,培养出的菌株但不产毒素标本3份;另外2份标本为GeneXpert阴性、TC阳性,菌株分别为A-B+CDT-型和A+B+CDT-型。
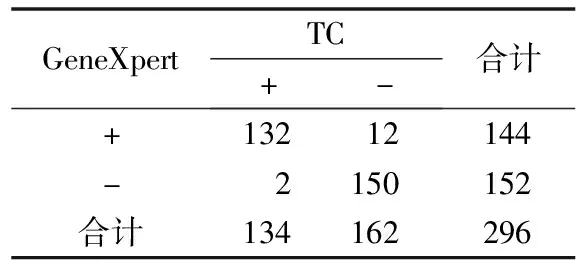
表2 GeneXpert试验与TC检测结果的比较
2.4GeneXpert与PCR-核糖体分型 GeneXpert试验报告2株RT027型艰难梭菌;PCR-核糖体分型结果显示,与RT027型标准菌株条带一致,确证为RT027型艰难梭菌。RT027型艰难梭菌与标准菌株的毛细管电泳图谱见图3。

注:A、B,临床菌株图谱;C,CA2标准菌株图谱;横轴为ISR片段长度;纵轴为峰强度。
3 讨论
CDI的诊断主要包括腹泻患者粪便标本中检测到艰难梭菌毒素或者产毒素的艰难梭菌,或者内镜检查为伪膜性肠炎[10]。艰难梭菌培养以及GDH检测具有较高的敏感性,不能区分菌株是否产毒素,而直接从粪便标本中检测毒素A/B的酶免疫方法敏感性较低,不推荐单独用于诊断CDI[11-12]。CDI诊断的金标准包括细胞毒性中和试验和TC,但2种方法操作繁琐,不适应于临床常规使用。GeneXpert试验可直接从粪便标本中快速检测毒素基因,在国外已得到广泛应用。
本研究结果表明,GeneXpert试验的敏感性、特异性、阳性预测值、阴性预测值均在90%以上。这与上海华山医院黄海辉教授牵头的多中心研究结果较为接近[13],文献综述表明GeneXpert试验的敏感性为94%~100%、特异性为93%~99%[12]。GeneXpert试验操作简便,且可在1 h内发出报告,具有良好的临床应用价值。此外,GeneXpert可准确报告高毒力RT027型艰难梭菌,对流行病学调查和院内感染防控均有重要意义。RT027型高毒力艰难梭菌在欧美等地区引起大规模暴发流行。近年来,我国多个城市报道了散发的RT027型菌株,与欧美等不同的是,我国ST37和ST81型A-B+型艰难梭菌流行率较高,该型菌株同样可以引起临床患者重症感染。GeneXpert检测的靶标为tcdB基因、二元毒素基因以及tcdC基因,本研究结果表明A-B+型菌株同样可被GeneXpert准确报告为阳性标本,目前国内尚未发现A+B-型艰难梭菌。
本研究中所用五重PCR检测艰难梭菌毒素基因为传统的PCR方法,之后使用电泳技术检测是否扩增出毒素基因,该方法操作复杂,在常规临床实验室不易开展。PCR-核糖体分型技术常用于艰难梭菌的流行病学调查,PCR扩增后使用毛细管电泳技术检测艰难梭菌ISR多态性,然后与标准菌株比对确定其核糖体型别。该技术因缺乏标准化而难以推广和应用,目前更常用的分型方法为多位点序列分型技术。NAATs直接检测艰难梭菌毒素基因,具有较高的敏感性,被美国胃肠病学会和美国感染病学会推荐可作为唯一的独立测试技术诊断CDI[11,14]。欧洲临床微生物与感染病学会和中国艰难梭菌感染诊断和治疗专家共识推荐使用两步法或者三步法联合诊断CDI,NAATs则作为其中的重要一个步骤[10,15]。一些研究者担忧NAATs方法过于敏感而导致过度诊断和治疗[16]。临床应结合患者是否具有高危因素及其他实验室检查综合判断CDI或定植。
综上所述,GeneXpert 实时荧光定量PCR方法具有较高的敏感性和特异性,可为CDI的诊治提供可靠的科学依据。

